Введение
В последнее время достигнут значительный прогресс в понимании этиологии и патогенеза ПЭ. Утратили свою актуальность утверждения о сугубо психогенной этиологии ПЭ, сложилось определенное понимание механизмов развития ПЭ и возможной роли нейробиологических факторов в данном процессе. Одновременно появились новые подходы к лечению данного вида патологии.
Следует, однако, отметить, что далеко не все вопросы, связанные с диагностикой и лечением ПЭ, до конца раскрыты, что требует проведения дальнейших исследований. Отсутствие четких данных о нормативных показателях длительности полового акта также создает серьезные трудности в диагностике и лечении ПЭ.
Подробный анализ литературных данных позволяет выделить четыре основных компонента, характерных для определения ПЭ:
- отсутствие контроля над процессом эякуляции;
- короткий промежуток времени до наступления эякуляции или эякуляция до интроекции;
- отсутствие сексуального удовлетворения;
- нарушение межличностных взаимоотношений между партнерами.
Для объективизации нормальной продолжительности полового акта в определение введен термин “интравагинальное время до наступления эякуляции” (ИВНЭ) [1], которое, по данным Международного общества сексуальной медицины, должно в норме превышать одну минуту [2]. С учетом вышеприведенных данных сформулировано следующее определение ПЭ: изначальное или приобретенное сексуальное нарушение, постоянно или периодически проявляющееся сочетанием отсутствия контроля над эякуляцией с нарушением психологической гармонии в паре ввиду недостижения удовлетворения мужчиной и/или его партнершей, а также c ускоренным развитием семяизвержения менее чем через минуту после начала коитуса или до введения полового члена во влагалище.
Большинство авторов по периоду возникновения выделяют две формы ПЭ: первичную (ППЭ), или изначальную, возникшую с начала половой жизни, и вторичную (ВПЭ), или приобретенную, появившуюся после ранее нормальной продолжительности полового акта [3].
Очень часто ПЭ сочетается с ЭД, но важно отметить, что время возникновения этих двух патологических состояний может различаться. Вначале может возникнуть ПЭ, а в дальнейшем, если пациент длительно страдает этим заболеванием, к ней может присоединиться психогенная ЭД. То есть пациент испытывает определенный психологический дискомфорт, связанный со страхом ожидания неудачи, что впоследствии может привести к ЭД [4, 5]. В некоторых случаях, напротив, к ПЭ приводит ЭД, т. к. нестойкая эрекция не позволяет проводить полноценный половой акт, и это ассоциируется с невольным желанием пациентов ускорить его завершение [6]. В конечном итоге сочетание этих двух заболеваний приводит к возникновению порочного круга, в котором они способны усиливать и маскировать друг друга, затрудняя диагностику и лечение. Поэтому необходим четкий алгоритм обследования и дальнейшего назначения специфической терапии в зависимости от периода возникновения данных заболеваний и присоединившихся осложнений. Причем предпочтительным представляется такое лечение, положительный эффект которого будет сохраняться длительное время после его отмены.
В настоящее время выделяют четыре основных подхода к лечению ПЭ:
- психотерапия;
- местное лечение;
- фармакотерапия;
- хирургическое лечение.
Психотерапевтический подход еще в недавнем прошлом был доминирующим, однако, как показывает практика, этот метод не всегда эффективен в качестве монотерапии. Он требует больших затрат времени и непременного участия партнерши, что утраивает далеко не всех мужчин [7].
Использование местных анестетиков, таких как лидокаин и/или прилокаин, в качестве крема, геля или спрея обладает при ПЭ умеренной эффективностью и сопряжено с возможной трансвагинальной абсорбцией. Это в свою очередь ведет к снижению влагалищной чувствительности и аноргазмии у женщины, если не используется презерватив. Местные анестетики могут также значительно снижать чувствительность полового члена, что может приводить к ухудшению эрекции [8].
В настоящее время селективные ингибиторы обратного захвата серотонина (СИОЗС), к числу которых относятся сертралин, флуоксетин, пароксетин, циталопрам, считаются наиболее эффективными и патогенетически обоснованными средствами лечения ПЭ [9]. Многочисленные клинические исследования подтвердили достоверное увеличение ИВНЭ на фоне приема данных препаратов у пациентов с ПЭ [10]. Однако, по некоторым данным, имеются группы больных, у которых прием СИОЗС не вызывает улучшения. Кроме того, прием этих препаратов нередко сопровождается определенными побочными эффектами, в частности снижением эректильной функции и либидо, что создает дополнительные проблемы при сочетании ПЭ и ЭД [11]. Кроме того, остается открытым вопрос о длительности регулярного приема этих препаратов. Все это свидетельствует о необходимости поиска новых медикаментозных подходов к лечению ПЭ, особенно при ее сочетании с ЭД. В этом плане большой интерес представляют препараты из группы ингибиторов фосфодиэстеразы типа 5 (ФДЭ-5).
В литературе имеется достаточно много данных о возможности использования ингибиторов ФДЭ-5 при лечении больных ПЭ [9]. В большинстве из них демонстрируется увеличение ИВНЭ. Авторы связывают данный факт со снижением чувствительности головки полового члена за счет сдавления нервных волокон кавернозными телами при усилении эрекции [12]. Улучшение эрекции придает также больше психологической уверенности и улучшает контроль половой акт. Кроме того, на фоне приема ингибиторов ФДЭ-5 у больных появляется возможность проведения повторных половых актов, при которых обычно увеличивается длительность коитуса. Однако эффективность ингибиторов ФДЭ-5 в лечении ПЭ показана не во всех работах и некоторые авторы считают их использование у данной категории больных нецелесообразным [12, 13].
При неэффективности психо-, фармакотерапии и местного лечения иногда применяется хирургический метод. Суть его состоит в пересечении дорсальных нервных стволов, иннервирующих головку члена, после чего с помощью микрохирургического инструмента нервы восстанавливаются путем наложения интрафасцикулярного шва. Недостатки данной методики состоят в возможном длительном резком снижении чувствительности полового члена, что может негативно влиять на эректильную функцию; затяжном течении реабилитационного периода, а также в вероятности рецидивов, требующих повторной операции [14].
Таким образом, на сегодня отсутствует четкий алгоритм лечения пациентов с ПЭ в сочетании с ЭД. В связи с этим мы сочли необходимым провести собственное исследование, целями которого были оптимизация методов лечения ПЭ в сочетании с ЭД и без нее, а также оценка отдаленных результатов различных схем лечения.
Материал и методы
В исследование был включен 151 мужчина с ПЭ, в т. ч. 87 пациентов сППЭ и 64 – с ВПЭ, которые в зависимости от наличия или отсутствия ЭД были разделены на 4 группы. В первую группу вошли 58 мужчин с ППЭ без ЭД (средний возраст – 26,2 ± 5,9 года), во вторую – 29 пациентов с ППЭ, в дальнейшем осложненной ЭД (средний возраст – 36,4 ± 7,9 года). Третью группу составили 37 больных с ВПЭ без ЭД (средний возраст – 27,2 ± 8,3 года) и четвертую – 27 пациентов с ЭД и присоединившейся ВПЭ (средний возраст – 42,2 ± 8,7 года). В последующем все пациенты четырех групп были разделены в случайном порядке на три подгруппы (рис. 1). В первой из них в регулярном режиме был назначен препарат группы СИОЗС – пароксетин в дозе 20 мг 1 раз в день; во второй – ингибитор ФДЭ-5 – тадалафил в дозе 20 мг 3 раза в неделю; в третьей – комбинация этих препаратов в указанных дозировках и режимах приема в течение 3 месяцев.

Всем больным было проведено комплексное андрологическое обследование, включившее подробную беседу с пациентом и его половой партнершей, общеклинические лабораторные тесты, ультразвуковое исследование предстательной железы, бактериологическое и микроскопическое исследование секрета предстательной железы, оценку гормонального статуса. Применялся также комплекс нейрофизиологических методов исследования, включавший оценку латентного периода бульбокавернозного рефлекса, соматосенсорные вызванные потенциалы, а также вибрационную чувствительность головки полового члена. По антропометрическим показателям все группы были сопоставимыми (р > 0,05; табл. 1).
Таблица 1. Антропометрические показатели больных в группах.
Для определения длительности полового акта пациенты или их партнерши оценивали ИВНЭ с помощью секундомера, данные которого регистрировались при каждом визите пациента. С целью оценки эректильной функции использовалась анкета Международного индекса эректильной функции (МИЭФ). В исследование были включены пациенты с умеренно легкой ЭД. В дальнейшем на повторных визитах через 3 месяца лечения и через месяц после отмены препаратов оценивались отдаленные результаты ИВНЭ и эректильная функция МИЭФ.
Результаты
Исходное обследование показало, что до лечения ИВНЭ у больных всех групп достоверно не различалось и составляло в среднем от 0,9 ± 0,3 до 1,4 ± 0,3 минуты.
При контрольном обследовании через 3 месяца динамика изменений ИВНЭ в группах оказалась различной. При сопоставлении исходных результатов и после трех месяцев лечения пароксетином мы получили достаточно интересные и клинически значимые факты. Так, у пациентов 1-й группы с ППЭ без ЭД и второй с ППЭ + ЭД отмечено значительное увеличение ИВНЭ (до 7,5 ± 1,3 и 4,2 ± 1,2 минуты), которое было достоверно большим, чем в третьей и в четвертой группах (2,6 ± 1,2 и 2,0 ± 0,8 минуты соответственно). При этом, как мы видим, лучшие результаты были достигнуты в 1-й группе. По окончании 1-месячного наблюдения после лечения у больных 1-й группы средние показатели также ИВНЭ были достоверно выше, чем у пациентов 2-й, 3-й и 4-й групп.
Анализируя полученные результаты через 3 месяца после приема тадалафила, можно отметить, что достоверное увеличение ИВНЭ было зафиксировано у пациентов 4-й группы (до 7,5 ± 1,9 минуты), которые изначально страдали ЭД с присоединившейся к ней ВПЭ. Положительная динамика в 4-й группе отмечена и после отмены тадалафила (6,5 ± 1,5 минуты), достоверно превосходя результаты, достигнутые в других группах. Оценивая результаты комбинированной терапии пароксетином и тадалафилом, можно отметить достоверное увеличение ИВНЭ во всех группах. Наиболее значимые результаты были зафиксированы во 2-й и 4-й группах (8,2 ± 2,1 и 8,4 ± 2,3 минуты соответственно). При контрольном обследовании через месяц показатели ИВНЭ в 1-й, 2-й и 4-й группах остались на высоком уровне, а в 3-й ИВНЭ снизилось практически до начального значения и составило 1,7 ± 0,5 минуты (табл. 2).
Таблица 2. Динамика ИВНЭ на фоне приема различных препаратов у пациентов с ПЭ в сочетании с ЭД и без ЭД.
Проанализировав исходные показатели эректильной функции по МИЭФ и зарегистрированные после трехмесячного курса пароксетином, можно отметить, что у пациентов с изначально нормальной эректильной функцией после лечения измененийне отмечено. Напротив, мужчины, страдающие ЭД, после лечения отметили снижение эректильной функции, которая в среднем уменьшилась на 2 балла от исходных показателей. В 4-й группе, в которой ЭД была изначальной, показатели МИЭФ снизились до 16,6 ± 0,3 балла. При контрольном обследовании через месяц положительной или отрицательной динамики отмечено не было. Совсем иные результаты были получены после терапии тадалафилом – отмечалось значительное достоверное увеличение эректильной функции, особенно во 2-й и 4-й группах (до 26,2 ± 0,5 и 25,7 ± 0,6 балла соответственно). Средние значения эректильной функции по МИЭФ в группах через месяц после окончания лечения достоверно не изменялись. Но наилучшие результаты были получены при комбинированной терапии. Через месяц после лечения показатели эректильной функции были выше и более стабильными, чем после монотерапии тадалафилом. На фоне комбинированной терапии у пациентов увеличились либидо и частота половых актов в отличие от пациентов, которые принимали только пароксетин (табл. 3).
Таблица 3. Динамика МИЭФ на фоне приема различных препаратов у пациентов с ПЭ в сочетании с ЭД и без ЭД.
Переносимость препаратов была хорошей, однако при комбинированной терапии частота нежелательных явлений увеличивалась. Побочные эффекты были невыраженными и носили временный характер. Ни один из пациентов не выбыл из исследования.
Обсуждение
Этиопатогенез ПЭ связан с гиперчувствительностью серотониновых рецепторов 5-HT2c и пониженной активностью 5-HT1а рецепторного аппарата головного мозга. Серотонинергический контроль эякуляции формируется за счет регуляции содержания серотонина (5-гидрокситриптамина или 5-HT) в синаптической щели определенных типов церебральных нейронов. При избытке данного нейротрансмиттера происходит подавление эякуляторной функции, а недостаток приводит к ускорению семяизвержения. 5-HT2cи 5-HT1а-рецепторы являются частью системы саморегуляции уровня серотонина в синаптических щелях некоторых нейронов по механизму отрицательно обратной связи. Нейробиологическая концепция ПЭ сформировалась после эффективного применения СИОЗС при лечении данного расстройства. Указанные препараты снижают чувствительность 5-HT2c-рецепторов и повышают ее в 5-HT1а-рецепторах, формируя определенный баланс между их активностью, что приводит к повышению содержания 5-гидрокситриптамина внутри синаптических щелей серотонинергических нейронов [15]. Поэтому наиболее эффективной была терапия пароксетином у пациентов, изначально страдающих ПЭ, т. е. имеющих дисфункцию серотонинергической регуляции эякуляторного центра.
Существуют работы, свидетельствующие, что ингибиторы ФДЭ-5 достоверно увеличивают как ИВНЭ, так и показатели эректильной функции у больных с ПЭ и ЭД [16, 17]. Более подробный анализ показывает, что 3-месячный прием тадалафила наиболее эффективен в группе больных, изначально страдающих ЭД. Эти факты позволяют говорить о том, что патогенез как ЭД, так и ПЭ у разных групп пациентов не идентичен и возникновение этих расстройств может быть обусловленным как психогенными, так и органическими причинами. ЭД, возникшая после ПЭ, чаще всего имеет психогенный характер. Однако у пациентов, у которых нарушение эрекции первично по отношению к ПЭ, в основном встречается органическая ЭД. В связи с тем что ПЭ у данной категории больных является осложнением ЭД, использование ингибиторов ФДЭ-5 дает хороший клинический эффект за счет улучшения качества эрекций. Эффективность тадалафила у больных, изначально имеющих ПЭ, можно также объяснить улучшением качества эрекции, которое позволяет пациентам более уверенно контролировать свой половой акт. Однако эффективность тадалафила в данной группе была достоверно ниже, чем у больных, изначально страдающих ЭД.
Подводя итоги полученных нами результатов лечения ПЭ, в т. ч. после отмены препаратов, с учетом клинической эффективности, стоимости, а также побочных эффектов применявшихся лекарственных средств можно сформулировать наиболее оптимальный алгоритм терапии для больных с различными формами ПЭ в сочетании ЭД и без нее (рис. 2).
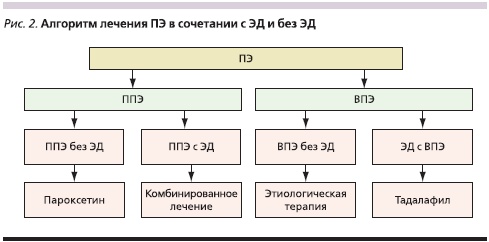
Так, у пациентов первой группы с ППЭ и хорошей эректильной функцией наилучшие результаты были получены при монотерапии пароксетином, не отличаясь достоверно от результатов комбинированного лечения. Эректильная функция у этих больных не различалась достоверно до и после лечения. Поэтому с медицинской и экономической точек зрения монотерапия пароксетином для указанной категории пациентов наиболее обоснованна.
Для группы больных с ППЭ и нарушенной эректильной функцией как наиболее эффективной оптимальной является комбинированная терапия пароксетином и ингибитором ФДЭ-5.
Лечение пациентов третьей группы с ВПЭ без ЭД обеспечивало терапевтический эффект только в период приема препаратов, но после их отмены показатели ИВНЭ и МИЭФ достоверно не отличались от начальных значений.
В четвертой группе, в которую были включены пациенты с ЭД и присоединившейся в последующем ВПЭ, с учетом всех медицинских и экономических аспектов наиболее обоснованной является монотерапия тадалафилом.
Заключение
Под перспективными средствами терапии ПЭ подразумеваются эффективные и безопасные препараты, обеспечивающие контроль над процессом эякуляции в течение непродолжительного курса лечения у большинства больных. К сожалению, на данный момент ни один из существующих препаратов не отвечает этим требованиям. Имеющиеся сегодня лекарственные средства для достижения оптимального эффекта приходится принимать длительно, применение же их по требованию демонстрирует слабую эффективность. Эффективная терапия по требованию должна быть действенной в течение периода времени, удобного для пациента, т. е. с момента начала сексуальной прелюдии до удовлетворительного завершения полового акта. Разработанный нами алгоритм лечения больных с ПЭ в сочетании с ЭД и без нее поможет практикующим врачам подобрать наиболее оптимальное возможное лечение, удовлетворяющее пациента и его партнершу.
Информация об авторах:
Гамидов Сафаил Исраил оглы – доктор медицинских наук, профессор кафедры урологии ГОУ ВПО РГМУ
Росздрава, профессор кафедры акушерства, гинекологии, перинатологии и репродуктологии
с курсом клинической андрологии ГОУ ВПО ММА им. И.М. Сеченова Росздрава.
Тел. 8 (495) 777-30-28, e-mail: docand@rambler.ru;
Попова Алина Юрьевна – кандидат медицинских наук, научный сотрудник ФГУ НЦАГиП
им. В.И. Кулакова Росмедтехнологий.
E-mail: alina-dock@yandex.ru;
Павловичев Алексей Александрович – аспирант кафедры урологии ГОУ ВПО РГМУ Росздрава.
E-mail: alexxei4@rambler.ru;
Тажетдинов Олег Халитович – аспирант кафедры урологии ГОУ ВПО РГМУ Росздрава.
E-mail: gelotazh2007@rambler.ru;
Тхагапсоева Регина Амирбековна – аспирант кафедры урологии ГОУ ВПО РГМУ Росздрава.
E-mail: reginamed2@mail.ru;
Щербаков Дмитрий Викторович – аспирант кафедры урологии ГОУ ВПО РГМУ Росздрава.
E-mail: sherb-dm@yandex.ru


