Допплерографическое исследование кавернозных артерий полового члена основано на анатомических данных и современных представлениях о физиологии эрекции [1, 2]. Половой член состоит из двух кавернозных тел и вентрально расположенного губчатого тела, окружающего уретру. Кавернозные тела заключены в белочную оболочку. Фасция Бака покрывает оба кавернозных и губчатое тела, формируя половой член как единое целое. Через кавернозное тело проходит кавернозная артерия. Артерии полового члена образуются из внутренней срамной артерии. Артерия полового члена делится на дорсальную артерию и кавернозную артерию. Кавернозная артерия входит в пещеристое тело на верхнемедиальной поверхности полового члена. Ветви этой артерии называются завитковыми артериями и в свою очередь делятся на более мелкие ветви, сообщающиеся с лакунами пещеристого тела. Венозный отток осуществляется в венозное сплетение, расположенное под белочной оболочкой. Венозные выпускники перфорируют белочную оболочку, и кровь через огибающие вены оттекает в глубокую дорсальную вену. Венозный отток осуществляется также по подкожной дорсальной вене.
В покое гладкая мускулатура кавернозных тел полового члена находится в состоянии полного сокращения, периферическое сопротивление высокое, в результате чего отмечается умеренный артериальный кровоток. В начале эрекции гладкая мускулатура пещеристых тел расслабляется вследствие нейромедиаторного ответа, сопротивление кавернозных тел снижается, питающие артерии расширяются. Это приводит к повышению артериального кровотока и увеличению объема полового члена (фаза набухания). Поскольку плотная белочная оболочка малорастяжима, при увеличении объема крови венулы между наполненными синусоидами и оболочкой сдавливаются, венозный отток прекращается, половой член становится твердым.
Эрекция – это сложный нейрососудистый феномен, который зависит от общего состояния здоровья, психологического состояния и социального благополучия.
Материал и методы
В клинике урологии Первого МГМУ им. М.М. Сеченова обследованы 396 пациентов с жалобами на эректильную дисфункцию (ЭД). Возраст исследуемых составил 43 (23–61) года. Из всех обратившихся у 41 (10,3 %) пациента сексуальная активность отсутствовала в течение минимум четырех недель перед обращением. Перед обследованием 357 (89,7 %) пациентов с сохраненной эректильной функцией ответили на вопросы шкалы МИЭФ-5 (Международный индекс эректильной функции). Результаты анкетирования представлены в табл. 1.
Результаты исследования
Данные анкетирования подтверждают общеизвестный факт, согласно которому основным фактором, влияющим на снижение эректильной функции, является возраст (р = 0,005).
В процессе сбора анамнеза факторов риска ЭД для 281 (70,6 %) пациента не выявлено. У 62 (15,6 %) пациентов выявлены васкулогенные факторы риска (атеросклероз), у 30 (7,5 %) – нейрогенные (диабетическая, алкогольная полиневропатия), у 25 (6,3 %) – другие (прием блокаторов кальциевых каналов, ингибиторов ангиотензин-превращающего фермента, употребление наркотических средств). Распределение пациентов с наличием или отсутствием сексуальной активности в зависимости от наличия и вида факторов риска не было значимым (р = 0,062).
Степень тяжести ЭД была статистически связана с васкулогенными и нейрогенными факторами риска (р = 0,001).
Дифференциальная диагностика психогенной, нейрогенной и васкулогенной ЭД часто затруднена даже после детального сбора анамнеза, физикального обследования и изучения эндокринного статуса. Инъекция сосудорасширяющего препарата в кавернозное тело – полезный, недорогой и минимально инвазивный диагностический метод для пациентов с подозрением на васкулогенную ЭД [11].
С целью фармакодопплерографии кавернозных артерий мы применяли алпростадил, который является формой простагландина Е1 (PGE1), встречающейся в естественных условиях, и обладает широким спектром фармакологического действия. Среди наиболее значимых эффектов алпростадила отмечают расширение сосудов и подавление агрегации тромбоцитов. При интракавернозном введении алпростадил ингибирует α1-адренорецепторы в тканях, расслабляет мускулатуру кавернозных тел, увеличивает кровоток и улучшает микроциркуляцию. Алпростадил вызывает эрекцию путем релаксации трабекулярной гладкой мускулатуры пещеристых тел и дилатацию кавернозных артерий, что ведет к расширению лакунарных пространств и перекрытию кровотока за счет прижатия венул к белочной оболочке (окклюзия вен полового члена).
Для исследования кровотока применяют линейный датчик частотой 7 Мгц. С его помощью оценивают состояние кавернозных артерий до и после интракавернозного введения PGE1 при помощи иглы размером 27–30G. Доза алпростадила составила 5 мкг.
В России первый опыт применения PGE1 в диагностике и лечении ЭД был доложен в 1995 г. [7]. Тогда прозвучало предложение в диагностических целях применять и даже выпускать PGE1 в дозировке 5 мкг. В большинстве источников описана дозировка PG от 10 до 20 мкг [2, 4–6, 10]. Однако имеются указания, что количество препарата необходимо дифференцировать. Пациентам младше 50 лет вводить 5 мкг препарата, а в возрасте более 50 лет – 10 мкг [11].
Результат пробы был оценен через 15 минут после интракавернозного введения препарата. Степень эрекции определена в соответствии со степенью набухания и ригидности полового члена (табл. 1) [6, 8]. Клинический результат пробы с алпростадилом представлен в табл. 2.
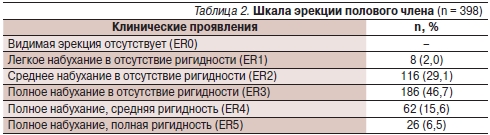
Через 15 минут после введения 5 мкг алпростадила получены различные комбинации набухания и ригидности полового члена. Следует отметить, что никакой сексуальной стимуляции при выполнении исследования не было.
Было отмечено, что клинический результат интракавернозного введения алпростадила значимо зависел от возраста (р = 0,008). Степень набухания и ригидности у более молодых пациентов была выше, чем у лиц старшего возраста. При этом наличие или отсутствие выявленных факторов риска не имели статистически значимого влияния на клинический результат интракавернозной пробы (р = 0,29). Кроме того, результат пробы не зависел от вида факторов риска ЭД (р = 0,064).
Выявлено статистически значимое распределение пациентов в зависимости от степени набухания и ригидности полового члена после интракавернозного введения алпростадила и результатов анкетирования по шкале МИЭФ-5 (р = 0,011). У пациентов с сохраненной сексуальной активностью клинический результат интракавернозного введения препарата был значимо лучше (р = 0,002).
Таким образом, клиническая оценка интракавернозной пробы в сочетании с данными анамнеза и результатами анкетирования позволит уточнить причину и вид ЭД с достаточной степенью вероятности.
Одновременно с оценкой эффективности введения алпростадила анализировали спектральные характеристики кровотока кавернозных артерий. Максимальную систолическую скорость измеряли в области проксимальной трети полового члена, т. к. на этом уровне скорости имеются наибольшие значения. Если измерение скорости кровотока проводится в дистальном отделе, результаты оказываются заниженными.
Спектральную допплерографию кавернозных артерий начинали с 5-й минуты после инъекции, а затем повторяли каждые 5 минут до 25-й минуты. После введения препаратов, содержащих PG, скорость кровотока должна быть не менее 35–40 см/с [2, 3].
В качестве дополнительных критериев учтена способность кавернозных тел к расширению и асимметрии скоростей кровотока в кавернозных артериях более 10 %.
Венозный отток подозревали в том случае, если имелся адекватный артериальный приток, развивалась эрекция, но ее продолжительность была невелика, а также определялся постоянный антеградный диастолический кровоток на всем протяжении исследования. Постоянный диастолический кровоток – это сохранение скорости диастолического кровотока на протяжении всех стадий эрекции. Значение скорости проводится после коррекции на величину угла.
Еще одним признаком венозного оттока является индекс резистентности (ИР), который является надежным методом диагностики кавернозного венозного оттока: ИР менее 0,75 сопровождается венозным оттоком для 90 % пациентов, ИР более 0,9 отмечен для 90 % здоровых субъектов.
При оценке результатов мы руководствовались рекомендациями Европейского общества урологов (пик систолического тока крови выше 30 см/с, ИР – выше 0,8) [9].
Прежде всего мы уточнили симметричность показателей кровотока в правой и левой кавернозных артериях после введения PGE1. Скорость кровотока (р = 0,662) и индекс резистентности (р = 0,297) не имели значимых различий. Поэтому для дальнейшей оценки приведены показатели одной артерии. Результаты фармакодопплерографии кавернозных артерий представлены в табл. 3.
Из табл. 3 видно, что клинический результат фармакодопплерографии кавернозных артерий зависит от максимальной скорости кровотока и блокирования венозного оттока после интракавернозного введения 5 мкг PGE1. Максимальная скорость кровотока в каверной артерии при контрольном измерении была выше у больных молодого возраста по сравнению со старшими группами (р = 0,001). Индекс резистентности также был выше у пациентов молодого возраста (р = 0,001). Таким образом, возраст оказывает влияние не только на клинические признаки и степень выраженности ЭД, но и на объективные параметры кровотока в кавернозных артериях.
Наличие или отсутствие интимной активности в течение минимум четырех недель перед исследованием не имело значимого влияния на максимальную скорость кровотока (р = 0,291) и ИР (р = 0,187).
Максимальная скорость кровотока была значимо ниже (р = 0,002) для лиц с выявленными факторами риска ЭД (васкулогенными, нейрогенными и др.). При этом ИР не зависел от факторов риска (р = 0,255). Максимальная скорость кровотока в кавернозных артериях не зависела от степени нарушения эрекции, установленной по данным анкетирования по шкале МИЭФ-5 (р = 0,901). Не выявлено и зависимости ИР (р = 0,226).
Если предположить, что отсутствие ригидности полового члена (ER1–3) после интракавернозного введения вазоактивного препарата можно рассматривать как отрицательный результат пробы, а наличие ригидности (ER4–5) как положительный, то чувствительность и специфичность пробы с 5 мкг PGE1 выглядят следующим образом (см. рисунок).
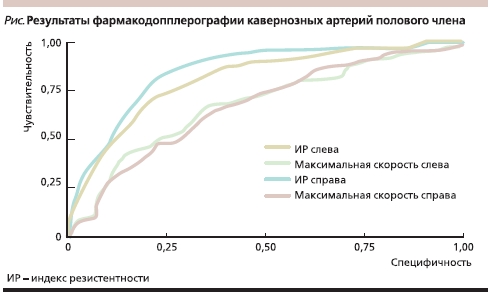
Максимальная скорость кровотока и ИР обладают достаточной чувствительностью и специфичностью. Это доказывает эффективность применения 5 мкг PGE1 с диагностической целью. Также очевидно, что параметры кровотока в правой и левой кавернозных артериях значимо не различаются.
Клинический результат интракавернозного введения алпростадила (степень наполнения и жесткость полового члена) был наиболее выражен среди пациентов молодого возраста. Наличие и вид факторов риска не оказывали значимого влияния на клинический результат пробы. Для пациентов с сохраненной сексуальной активностью клинический результат интракавернозного введения препарата был значимо лучше. Данный аспект исследования позволяет представить влияние психологических или органических причин ЭР.
Максимальная скорость кровотока и ИР в каверной артерии после введения алпростадила были выше у больных молодого возраста. Наличие или отсутствие интимной активности не имело значимого влияния на спектральные характеристики кровотока. Отмечено влияние установленных факторов риска на максимальную скорость кровотока в кавернозных артериях. Спектральные характеристики кровотока не зависели от степени нарушения эрекции, по данным анкетирования по шкале МИЭФ-5.
Таким образом, применение 5 мкг алпростадила является эффективным и безопасным методом обследования пациентов с ЭД различного генеза и степени тяжести.


