Введение
По данным 10-го издания Атласа диабета Международной диабетической федерации (IDF), за 2021 г. 537 млн взрослых лиц (20–79 лет) живут с диабетом, что составляет 1 из 10. По прогнозам, это число возрастет до 643 млн к 2030 г. и 783 млн к 2045 г. Более 3 из 4 взрослых, страдающих диабетом, живут в странах с низким и средним уровнем дохода. Диабет стал причиной 6,7 млн смертей в 2021 г. – одной каждые 5 секунд. Расходы на здравоохранение из-за диабета составили по меньшей мере 966 млрд долл. США – рост на 316% за последние 15 лет.
У 541 млн взрослых лиц нарушена толерантность к глюкозе, что подвергает их высокому риску развития сахарного диабета 2 типа (СД2) [1]. В данной статье будут рассматриваться современные возможности оценки гликемии у пациентов с СД1 и СД2, что является важной составляющей в управлении этим заболеванием.
В основном речь пойдет о самоконтроле уровня глюкозы крови. Мы обсудим необходимость и оптимальную частоту самоконтроля в различных группах больных СД, опираясь на клинические исследования.
Самоконтроль уровня гликемии (СГ)
СГ был принят в качестве важного инструмента, который позволяет людям с СД достигать и поддерживать терапевтические цели. Частый и точный мониторинг уровня глюкозы в крови и сопутствующая оптимальная корректировка инсулина в зависимости от потребления углеводов и физических нагрузок являются основой лечения пациентов с СД1 и СД2, получающих инсулин [4], а также пациентов с СД2, его не получающих.
Частота СГ связана с улучшением уровня гликированного гемоглобина (HbA1c) у пациентов с СД1. Считается, что это коррелирует как с лучшей адаптацией дозировки вводимого инсулина к потребляемой пище, так и с возможностью быстро корректировать уровень глюкозы, выходящий за целевые показатели. Кроме того, раннее выявление низких значений уровня глюкозы до симптоматической гипогликемии может позволить проводить коррекцию с уменьшенным риском чрезмерной коррекции и последующей гипергликемии. Использование СГ во время физических нагрузок также помогает корректировать дозировку инсулина и снижать риск гипогликемии во время и после физических нагрузок [4].
Глюкозу в крови лучше всего измерять в разное время суток, чтобы показать уровни гликемии на следующих фазах: после ночного голодания, в течение ночи (для выявления незаметной гипогликемии и гипергликемии), в ответ на инъекции инсулина (при ожидаемых пиках и минимумах его действия); после приема пищи (через 1,5–2,0 часа после еды) и при интенсивной физической активности (во время и через несколько часов после), чтобы можно было вносить изменения в лечение для улучшения профилей глюкозы в крови, подтверждения и коррекции гипогликемии, а также во время интеркуррентного заболевания для предотвращения гипергликемических кризов [4].
Частоту СГ нужно подбирать индивидуально в зависимости от типа и режима введения инсулина и способности пациента выявлять гипогликемию. Успешное лечение СД с помощью многократной инъекционной или помповой терапии инсулином требует частого СГ (4–6 раз в сутки) и регулярного анализа результатов для выявления закономерностей, требующих корректировки плана лечения диабета. Оптимальная частота и время СГ во многом зависят от индивидуальной ситуации и будут меняться изо дня в день в зависимости от активности, общего состояния здоровья или недавних изменений в терапии. Целевые показатели гликемии натощак, перед приемом пищи и после приема пищи для СГ описаны в клинических рекомендациях [2]. Однако пациентам следует индивидуально определять свои целевые показатели с целью достижения значения, максимально близкого к норме, избегая при этом тяжелой гипогликемии, а также частой гипогликемии легкой и умеренной степеней [4].
Оценка гликемии у пациентов с СД2
Мониторинг уровня глюкозы в крови для контроля гликемии является фундаментальной частью лечения СД2 [3].
В ноябре 2022 г. китайскими учеными был опубликован систематический обзор и мета-анализ исследований «Эффективность и частота самоконтроля уровня глюкозы в крови у пациентов с СД2, не получающих инсулина» [5].
В обзоре использовались публикации с января 2000 по апрель 2022 г. из баз данных PubMed, Embase, Cochrane Library и ClinicalTrials.gov. Были включены рандомизированные контролируемые исследования, сравнивавшие СГ с отсутствием СГ или структурированным СГ (С-СГ, СГ с определенным временем и частотой измерения уровня глюкозы). Мета-анализ был проведен для оценки эффективности, оптимальной частоты и наиболее подходящей популяции для СГ. Было обработано 22 исследования с участием 6204 человек, в т.ч. 17, сравнивавших СГ с отсутствием СГ, и 4, сравнивавших СГ с С-СГ.
В этой статье СГ упоминался как самоконтроль уровня глюкозы в крови не реже 1 раза в неделю, С-СГ упоминался как мониторинг в определенное время и с определенной частотой. Суть СГ заключается в контроле уровня глюкозы в крови посредством реакции пациента на показания уровня глюкозы в крови. Пациентам рекомендуется корректировать свой образ жизни, например, заниматься физическими упражнениями или диетой, а также обращаться к врачам за корректировкой лечения.
СГ был связан со значительным снижением HbA1c по сравнению с отсутствием СГ по итогам исследования (табл. 1). С-СГ снижал уровень HbA1c более существенно, чем СГ.
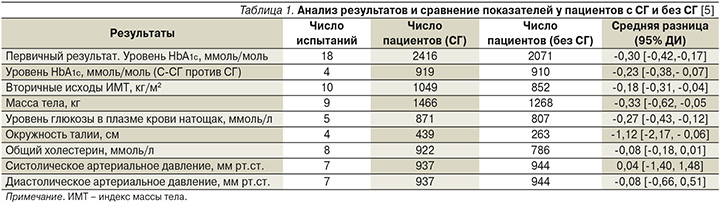
Была значительная разница в эффекте СГ между двумя группами, классифицированными по частоте мониторинга. Контроль HbA1c был лучше среди пациентов с СГ>7 раз в неделю по сравнению с пациентами с СГ≤7 раз в неделю. Однако не было обнаружено существенной разницы в контроле уровня HbA1c между СГ 8–11 раз в неделю и СГ ≥12 раз в неделю.
В свете преимуществ С-СГ ученые дополнительно изучили оптимальную частоту мониторинга уровня глюкозы в крови. Была рекомендована частота 8–11 раз в неделю. Частота 8–14 раз в неделю была указана в исследовании Y. Xu et al. [6], но в данный обзор было включено больше исследований с частотой СГ выше 11 раз в неделю и никаких дополнительных преимуществ более частого измерения не наблюдалось. Между тем в некоторых исследованиях анализировалось время мониторинга. По данным V. Mohan et al. [7], в отличие от групп с СГ натощак и до приема пищи постпрандиальный мониторинг был связан со значительным снижением уровня HbA1c. Использование данных СГ после приема пищи для корректировки терапии привело к значительному регрессу утолщения комплекса интимы-медиа сонной артерии и снижению уровня HbA1c при СД2, в то время как у пациентов, которые использовали данные СГ натощак/перед приемом пищи для корректировки терапии, не наблюдалось существенного улучшения этих параметров.
Корректировка образа жизни на основе СГ более существенно снизила уровень HbA1c (РС -0,37%, 95% ДИ от -0,50 до -0,23) по сравнению с группой без корректировки (РС -0,09%, 95% ДИ от -0,18 до -0,01; P <0,01). Это исследование также подтвердило, что СГ имел ограниченное действие на снижение уровня HbA1c даже без корректировки образа жизни.
По сравнению с отсутствием СГ снижение ИМТ, массы тела, уровня глюкозы в плазме натощак и окружности талии в группе СГ составило -0,18 кг/м2 (95% ДИ от -0,31 до -0,04), -0,33 кг (95% ДИ от -0,62 до -0,05), -0,27 ммоль/л (95% ДИ от -0,43 до -0,12) и -1,12 см (95% ДИ от -2,17 до -0,06) соответственно.
Значительное снижение уровня HbA1c наблюдалось у пациентов с СГ по сравнению с отсутствием СГ (-0,30% аналогично предыдущим мета-анализам [3, 13]), что имеет клиническое значение для долгосрочного контроля гликемии и уменьшения частоты осложнений, согласно рекомендациям ADA (American Diabetes Association – Американская диабетическая ассоциация [16]). Проспективное исследование диабета в Великобритании (UKPDS) показало, что каждый 1% снижения уровня HbA1c соответствует 37%-ному снижению риска микрососудистых осложнений [14].
Появилось множество новых технологий мониторинга глюкозы, в т.ч. непрерывный мониторинг глюкозы в реальном времени и флэш-мониторинг глюкозы, который также называется непрерывным мониторингом уровня глюкозы (НМГ) с периодическим сканированием. Они компенсируют некоторые недостатки СГ. Тем не менее пациенты, использующие НМГ, должны иметь доступ к СГ, как рекомендовано ADA [16].
Этот систематический обзор подтвердил эффективность СГ у пациентов с СД2, не получавших инсулина. Более того, было обнаружено, что С-СГ превосходит СГ, а СГ при частоте 8–11 раз в неделю демонстрирует преимущества по сравнению с другими режимами измерений. Корректировка образа жизни в соответствии с данными СГ была связана со снижением уровня HbA1c, а корректировка планов лечения, основанная на СГ, может иметь долгосрочные преимущества.
Таким образом, СГ является необходимым условием для реализации стратегий оптимального лечения пациентов с СД2.
Оценка гликемии у пациентов с СД1 и СД2
В октябре 2017 г. было опубликовано открытое многоцентровое обсервационное исследование «Улучшенный контроль гликемии в группе пациентов, выполняющих 7-точечный профиль самоконтроля уровня глюкозы в крови и интенсивное документирование данных» [8]. В 12-недельном открытом многоцентровом обсервационном исследовании 51 пациенту (26 с СД1 и 25 с СД2) было поручено выполнять СГ не менее 7 раз в день. Пациенты самостоятельно анализировали и обрабатывали свои данные. В целом среднее изменение уровня HbA1c на 12-й неделе по сравнению с исходным уровнем составило -0,46% (p<0,0001). Изменение уровня HbA1c наблюдалось у пациентов с СД1: -0,27% (р=0,0063) и СД2: -0,65 % (р<0,0001) (рис. 1). Изменение уровня HbA1c не коррелировало с увеличением числа случаев гипогликемии (уровень глюкозы в крови менее 55 мг/дл (3,1 ммоль/л) (рис. 2). Большинство побочных эффектов были симптоматическими гипогликемическими явлениями (42 события; 9 пациентов).
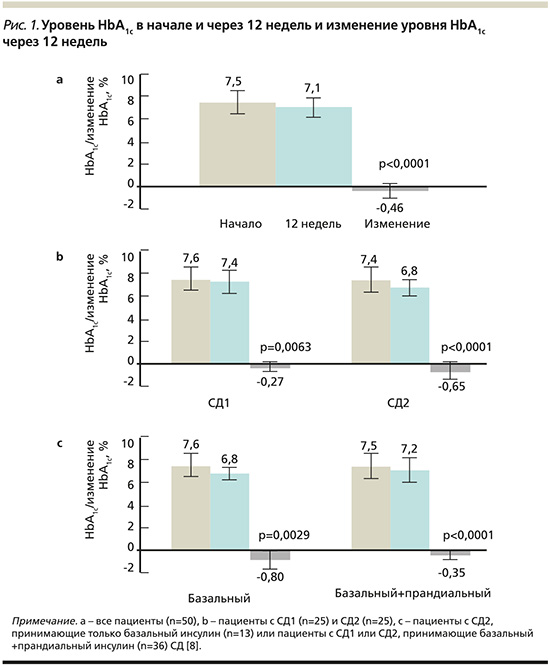
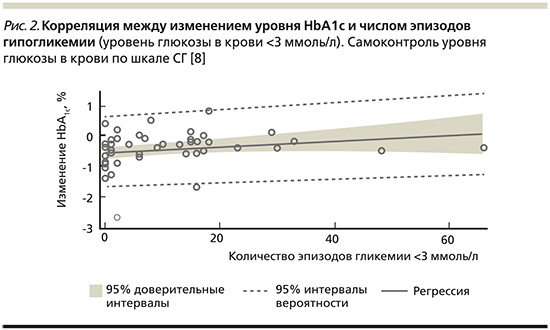
Выводом данного исследования стало то, что контроль гликемии можно улучшать, выполняя ежедневный 7-точечный профиль СГ и используя приложение для записи результатов.
Сравнение СГ крови с данными НМГ
В декабре 2021 г. было проведено исследование «Рандомизированное сравнение самоконтроля уровня глюкозы в крови (СГ) с данными НМГ для оптимизации контроля уровня глюкозы при диабете 2 типа» [9]. Целью исследования было оценить, приводят ли С-СГ или НМГ в реальном времени к улучшению контроля уровня глюкозы (HbA1c). Было проведено параллельное исследование трех методов лечения CД2 ±метформин (комбинация): 1) сульфонилмочевина (СМ), 2) инкретин (ингибитор ДПП-4 или агонист ГПП-1), 3) инсулин. После базового НМГ 114 взрослых пациентов были рандомизированы и проводили СГ (4 раза в сутки) или НМГ (24/7) в течение 16 недель с корректировкой терапии каждые 4 недели.
Среднее значение HbA1c снизилось с 8,19 до 7,07 (- 1,12%) при НМГ (n=59) и с 7,85 до 7,03 (- 0,82%) при СГ (n=55), p<0,001. Группы СГ и НМГ показали значительное улучшение в диапазоне и вариабельности уровня глюкозы без существенной разницы между двумя группами. Клинически значимая гипогликемия (<50 мг/дл) была значительно ниже в группе НМГ по сравнению с СГ (p<0,01), особенно у субъектов, принимающих инсулин или получающих терапию с более высоким риском гипогликемии (СМ).
По итогам исследования был сделан вывод, что при СД2 структурированное, последовательное использование данных глюкозы крови независимо от устройства (С-СГ или НМГ) приводит к улучшению контроля HbA1c. НМГ более эффективен, чем СГ, в минимизации гипогликемии, особенно у тех, кто использует терапию с более высоким гипогликемическим риском.
Способы анализа данных СГ и НМГ: структурный анализ и время в целевом диапазоне
Структурный анализ СГ – это систематический подход к выявлению гликемических закономерностей в данных СГ и последующему принятию соответствующих мер на основе этих результатов. Использование структурного анализа включает установление целевых уровней глюкозы до и после приема пищи, получение данных об уровнях глюкозы, потреблении углеводов, приеме лекарств, уровнях активности и физическом/эмоциональном стрессе; выявление закономерностей колебаний гликемии, оценка любых влияющих факторов и осуществление соответствующих действий и выполнение СГ для оценки воздействия любых внесенных терапевтических изменений [10].
НМГ предоставляет такие показатели, как процент времени в пределах целевого диапазона (TIR–ВЦД). В исследованиях было показано, что существует хорошая корреляция между уровнем HbA1c и ВЦД, что может позволить переходить на ВЦД в качестве предпочтительного показателя для определения результатов клинических исследований, прогнозирования риска осложнений диабета и оценки контроля гликемии у конкретного пациента [11].
Фактические данные подтверждают связь между осложнениями СД и показателями вариабельности гликемии в течение дня, получаемыми на основе НМГ. ВЦД стал наиболее последовательным показателем, подтверждающим его растущую роль в клинической практике [12].
Изучение современных подходов к СГ у пациентов с СД1 и СД2 в отделении ЦКБ ГА
В отделении эндокринологии ЦКБ ГА проводилось изучение современных подходов к СГ у пациентов с СД. Так, за 14 дней наблюдения проводились оценка и сравнение показателей гликемического контроля у пациентов c CД1 и СД2, использовавших глюкометр Контур Плюс Уан с мобильным приложением Контур Диабитис по сравнению с пациентами с СД1 и СД2, использовавшими глюкометры без мобильных приложений. Глюкометр напрямую подключается к приложению Контур Диабитис, что позволяет автоматически синхронизировать результаты и вести электронный дневник самоконтроля. Также приложение позволяет получать уведомления о критически низком или критически высоком уровне глюкозы в крови, анализировать показатели, выявлять тенденции гликемии, формировать отчеты и отправлять их лечащему врачу. В табл. 2 и 3 приведены основные характеристики пациентов, принявших участие в исследовании.
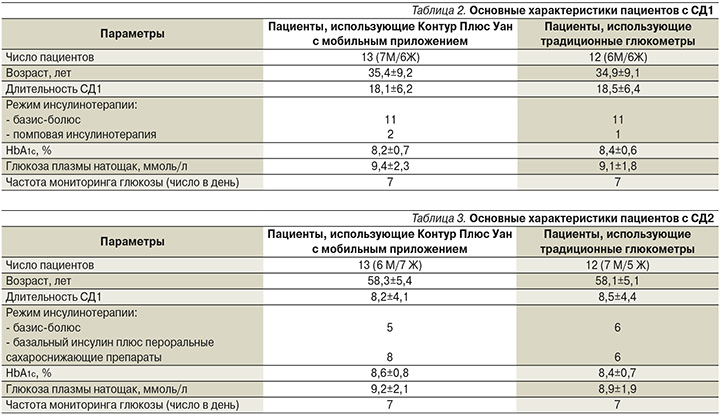
У всех участников исследования оценивались показатели гликемического контроля, описанные в табл. 4.
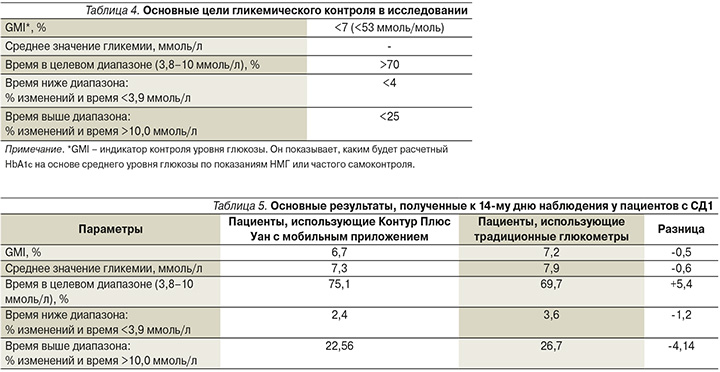
Через 14 дней наблюдения были получены следующие результаты, представленные в табл. 5 и 6, на рис. 3–6, отражающие преимущества использования глюкометра с мобильным приложением, как у пациентов с СД1, так и с СД2.
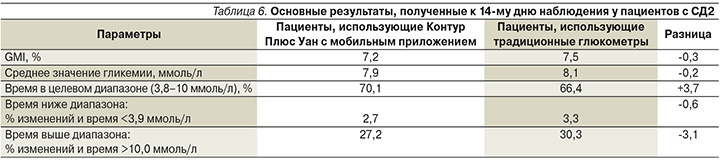
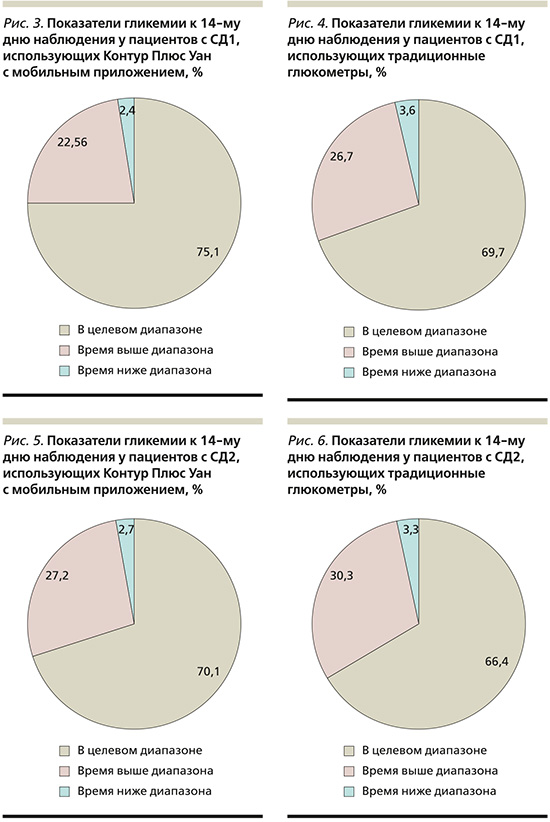
Таким образом, используя современные возможности СГ по 7 точкам на протяжении 14 дней с глюкометром Контур Плюс Уан и цифровым приложением Контур Диабитис пациенты с СД1 и СД2 достигли основных целей в показателях гликемии, таких как время в целевом диапазоне, процент времени ниже целевого диапазона и процент времени выше целевого диапазона, в отличие от пациентов, использовавших традиционные приборы.
Заключение
Современные методы оценки гликемии у пациентов с СД предоставляют им значительное преимущество в контроле и управлении своим заболеванием. Самоконтроль позволяет пациентам более точно контролировать свой уровень глюкозы крови и принимать необходимые меры для поддержания его в целевом диапазоне. Это способствует предотвращению острых осложнений и снижению риска хронических осложнений СД. Ежедневный 7-точечный профиль глюкозы крови как минимум на протяжении 14 дней позволяет улучшать основные показатели гликемии у пациентов с СД1, а также у пациентов с СД2. Существуют современные методы НМГ, но СГ остается по-прежнему актуальным. Данные, полученные с помощью СГ, могут быть использованы медицинскими специалистами для оптимизации лечения и индивидуального подхода к каждому пациенту. Это значительно повышает качество жизни пациентов с СД и снижает риск развития поздних осложнений СД.



