Введение
Несмотря на многолетнее изучение эпилепсии и коморбидных заболеваний, лечение пациентов, сочетающих такие состояния, представляет проблему в реальной клинической практике. Коморбидные заболевания продолжают недооцениваться клиницистами, а пациенты не получают должного комплексного лечения [1]. Между тем известно, что у пациентов молодого возраста имеется в среднем два хронических заболевания, у людей старше 65 лет - шесть. В нескольких крупных наблюдательных исследованиях продемонстрировано, что от 26 до 50% взрослых с эпилепсией имеют как минимум одно из коморбидных заболеваний, которые до 8 раз чаще встречаются у пациентов с эпилепсией по сравнению с общей популяцией, при этом негативно влияют на прогноз эпилепсии и качество жизни - КЖ [2-4]. Преобладающими являются нарушения деятельности нервной системы и перинатальные поражения, психиатрические заболевания, заболевания сердечно-сосудистой системы, эндокринные заболевания и метаболические расстройства [4]. Существуют различные типы коморбидных заболеваний и их связь с эпилепсией [2, 3]. При одних заболеваниях эпилепсия развивается как следствие структурного повреждения центральной нервной системы (ЦНС) при инсульте, опухолях головного мозга и т.п. [5-8]. Другие заболевания и состояния развиваются на фоне имеющейся эпилепсии и применения антиэпилептических препаратов (АЭП): когнитивные расстройства, тревога, депрессия, снижение концентрации внимания, нарушения сердечного ритма и т.п. [3, 9-11]. Причинно-следственные связи между эпилепсией и коморбидными заболеваниями могут быть прямыми, непрямыми, одно- или двунаправленными (взаимовлияющими друг на друга), а также иметь общие факторы риска и генетические факторы [2].
Так, одним из ключевых процессов в развитии патологии мозга при травмах, нейродегенеративных заболеваниях и сосудистых катастрофах является нейровоспаление. Происходит активация астроцитов и микроглии, сопровождающаяся синтезом провоспалительных цитокинов, запускается патологический каскад, включающий изменение возбудимости нейронов, долгосрочные пластические изменения, дисфункцию астроцитов, нарушение проницаемости гематоэнцефалического барьера и программируемую гибель нейронов. Это может в конечном итоге способствовать развитию судорожных приступов. С другой стороны, нейровоспаление является звеном патогенеза ряда нервно-психических расстройств. Следовательно, нейровоспаление может быть связующим звеном между эпилепсией и коморбидными заболеваниями и состояниями, включая расстройства настроения, тревогу, а также нарушения памяти [11].
Важной составляющей эффективного лечения эпилепсии является приверженность пациентов терапии, соблюдение схемы лечения, назначенной доктором [12, 13]. И здесь немаловажны переносимость АЭП, их безопасность, риски развития побочных эффектов, поскольку у пациентов с эпилепсией может быть сопутствующая соматическая и неврологическая патология и удержание на терапии будет напрямую зависеть от того, насколько оказывают влияние на коморбидность принимаемые препараты.
Цель исследования: оценить течение различных форм эпилепсии у взрослых пациентов при добавлении к терапии перампанела и оценить его влияние на коморбидную соматическую патологию.
Методы
Клиническое наблюдение проведено на базе неврологического отделения консультативно-диагностической поликлиники ГАУЗ СО «СОКБ № 1» Екатеринбурга. Набор пациентов проводился случайным методом при их плановом обращении на прием.
Критерии включения: возраст 18 лет и старше, наличие показаний к приему перампанела, отсутствие противопоказаний к приему перампанела, согласие на прием перампанела в качестве препарата дополнительной терапии, готовность регулярно посещать врача и выполнять лечебные рекомендации.
Критерии исключения: медикаментозная ремиссия в настоящее время, соматические противопоказания, нерегулярное обращение в клинику, пропуски в терапии АЭП.
Анализировались жалобы, анамнез, социальный статус, данные нейровизуализации и электроэнцефалографии (ЭЭГ). Диагноз эпилепсии выставлялся согласно классификации Международной противоэпилептической лиги (2017), основываясь на семиологии приступов [14-16].
Оценку ЭЭГ проводил сертифицированный врач функциональной диагностики на аппарате «Энцефалан» (Медиком МТД, Россия).
Всем пациентам была ранее проведена МРТ головного мозга на аппаратах 1,5 или 3 Тл с целью выявления структурной патологии как этиологического фактора эпилепсии.
За всеми пациентами вели длительное динамическое наблюдение. На каждом визите к врачу (1 раз в 3 месяца) проводили оценку жалоб, соматического и неврологического статуса, дневника приступов, показателей ЭЭГ, схемы лечения, включая дозы и переносимость АЭП.
Эффективность дополнительной терапии перампанелом оценивали через 12 месяцев наблюдения в зависимости от уменьшения числа приступов: ремиссия - отсутствие приступов в течение всего периода наблюдения (не менее 12 месяцев от начала лечения), улучшение/ответ на терапию — уменьшение числа приступов на 50% и более от исходного уровня, нет эффекта - уменьшение числа приступов менее чем на 50% от исходного уровня.
Для оценки КЖ пациентов до начала терапии и в процессе лечения с использованием перампанела применяли опросник QOLIE-31 (Quality of Life in Epilepsy), версия 1.0, адапированный для пациентов с эпилепсией [17].
Статистический анализ проведен с использованием статистического пакета MedCalc версия 13.3.1 (MedCalc Software, Бельгия). Для качественных показателей представлены абсолютные и относительные величины (%), рассчитывался доверительный интервал (ДИ). Статистически значимыми считали различия при p<0,05.
Результаты
Перампанел был назначен 51 пациенту (5 пациентов отказались принимать препарат из-за боязни очередной неудачи в лечении, 6 пациентов не явились на очередной осмотр). Таким образом, результат лечения оценили у 40 пациентов: 22 (55%) женщин и 18 (45%) мужчин.
Средний возраст пациентов с разными формами эпилепсии составил 35,5 лет (95% ДИ: 18-55). Средний возраст пациентов со структурной эпилепсией (СЭ) составил 34,5 года, с фокальной эпилепсией неизвестной этиологии (ФЭНЭ) - 37, с идиопатической генетической эпилепсией (ИГЭ) - 33,5 года. Пациентов молодого (до 44 лет) возраста было 34 (85%), среднего (до 59 лет) - 5 (12,5%), пожилого возраста - 1 (2,5%) пациент. Анализ форм эпилепсий у пациентов различного возраста не выявил статистически значимых различий.
Пациентов с СЭ было 22 (55%), с ФЭНЭ - 16 (40%), с ИГЭ - 2 (5%) человека. Средний возраст начала заболевания СЭ составил 7,5 лет, ФЭНЭ - 12, ИГЭ - 8,5. Различий по половой принадлежности выявлено не было: у женщин средний возраст начала заболевания составил 11 лет, у мужчин - 8 лет (95% ДИ).
Средний стаж заболевания на момент включения в клиническое наблюдение был достаточно большим и составил 26 лет для всех пациентов (СЭ - 27,5; ФЭНЭ - 18,5; ИГЭ - 27 лет соответственно).
Большинство пациентов имели 3-ю, 2-ю или 1-ю группу инвалидности (36 человек - 90%), что было связано с тяжестью течения заболевания, из них 3-я группа была у 15 (37,5%) человек, 2-я - у 17 (42,5%), 1-я - у 3 (7,5%). Пять (12,5%) человек не имели группы инвалидности.
В основном пациенты смогли получить средне-специальное образование (18 человек - 45%). Коррекционную школу окончили 12 (30%), 9 классов - 4 (10%) человека. Высшее образование получили только 4 (10%) человека. Два (5%) человека с СЭ вследствие когнитивного дефицита не получили никакого образования. Достоверных различий по форме эпилепсии и уровню образования выявлено не было (р=0,155).
Большинство пациентов не работали (30 человек - 75%), что связано как с тяжестью течения заболевания, так и со стигматизацией в связи с болезнью. Семь (17,5%) пациентов работали, 2 (5%) учились, еще 1 (2,5%) человек достиг пенсионного возраста.
Оценка семейного положения выявила, что более половины (23 человека; 57,5%) пациентов были одинокими, что, вероятно, связано с тяжестью течения заболевания, бременем забот, к которым приводили частые приступы, и стигматизацией таких пациентов в обществе в целом. Чуть больше среди одиноких пациентов встречались лица мужского пола - одинокими были 13 мужчин и 10 женщин. В браке состояли 14 (35%) человек, разведены 3 (7,5%), 23 (57,5%) человека не имели детей. По 1 ребенку было у 6 (15%), по 2 - у 7 (20%), по 3 и более детей было у 3 (7,5%) человек соответственно.
У 21 (52,5%) человека неврологический статус был в пределах нормы. Очаговая симптоматика в виде геми- и парапареза имела место у 11 (27,5%) человек, рассеянная симптоматика - у 8 (20%). Когнитивные нарушения выявлены более чем у половины пациентов. В основном встречалось малое нейрокогнитивное расстройство (у 18 человек - 45%). Большое нейрокогнитивное расстройство имело место у 5 (12,5%) пациентов, 17 (42,5%) человек не имели когнитивных расстройств.
У 23 (57,5%) больных преобладала височная, у 13 (32,5%) - лобная локализация эпилептиформной активности, 2 (5%) человека имели затылочную локализацию, еще у 2 (5%) имела место идиопатическая генерализованная эпилепсия (рис. 1).
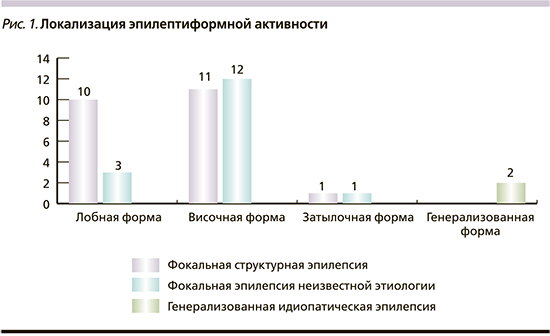
Среди типов приступов чаще всего имело место сочетание фокальных и билатеральных тонико-клонических приступов. Данное сочетание верифицировали у 32 (80%) вошедших в наблюдение больных. Только фокальные приступы наблюдались у 6 (15%), миоклонии и генерализованные приступы - у 2 (5%) пациентов соответственно (рис. 2).
Практически у всех пациентов до начала терапии перампанелом течение заболевания было резистентным: диагноз «резистентная эпилепсия» был поставлен 36 (90%) больным, в т.ч. 19 - СЭ, 15 - ФЭНЭ, 2 - ИГЭ. Среди пациентов без диагноза резистентная эпилепсия СЭ имела место у 3, ФЭНЭ у 1 больного (рис. 3).

У большинства (34 больных; 85%) пациентов преобладало серийное течение приступов, из них 8 с СЭ, 15 с ФЭНЭ и 1 пациент с ИГЭ соответственно. У 5 (12,5%) пациентов в анамнезе был эпистатус (билатеральные тонико-клонические приступы) (рис. 4).
Анализ причин, вызвавших развитие эпилепсии, показал, что в группе ФЭНЭ у 16 (40%) больных на МРТ головного мозга патологии выявлено не было. В случае СЭ основной причиной развития эпилепсии были перинатальное поражение ЦНС (22,5% случаев), послеоперационные изменения после радикального удаления опухоли (10%), последствия черепно-мозговой травмы (7,5%), мезиальный височный склероз (7,5%), фокальная корковая дисплазия (7,5%). Другие причины, среди которых последствия воспалительных заболеваний ЦНС и отравление угарным газом, носили единичный характер.
До назначения терапии перампанелом 13 (32,5%) пациентов находились на монотерапии, из них 6 с СЭ, 6 с ФЭНЭ, 1 с ИГЭ. Большинство участвовавших в данном клиническом наблюдении (27 больных; 67,5%) находились на политерапии, в т.ч. 16 с СЭ, 10 с ФЭНЭ, 1 с ИГЭ. Соответственно, перампанел был добавлен вторым препаратом 13 (32,5%) пациентам и третьим - 27 (67,5%). Использовавшиеся в политерапии АЭП приведены в табл. 1.
Длительность терапии препаратом перампанел на момент статистической обработки составила до 2 лет включительно у 16 (40%), от 3 до 4 лет - у 11 (27,5%), 4 года и более - у 13 (32,5%) человек.

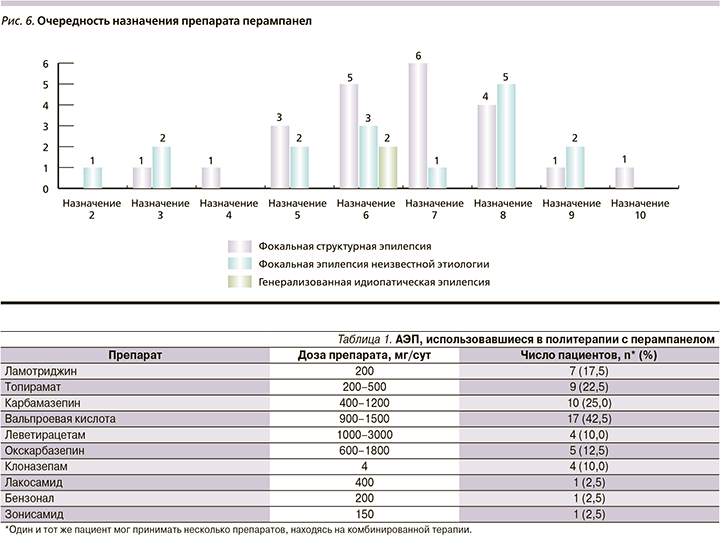
Перампанел назначали в дозе 2 мг, шаг титрации был 1 раз в 2-3 недели. Изначально 2 мг принимали 5 (12,5%), 4 - 11 (27,5%), 6 - 8 (20%), 8 - 10 (25%), 10 - 5 (12,5%), 12 - 1 (2,5%) пациент. Чаще всего больные находились на терапии перампанелом в дозах 4 (27,5%), 6 (20%) и 8 мг (25%) (рис. 5). Перампанел назначали достаточно поздно, в основном в 5-й (12,5%), 6-й (25%), 7-й (17,5%) и даже 8-й (22,5%) схемах лечения (рис. 6).
Несмотря на преобладание пациентов молодого возраста среди участников наблюдательной программы, более чем у половины (у 21 пациента; 52,5%) имелась сопутствовавшая соматическая патология, требововшая периодического или постоянного дополнительного лечения помимо приема АЭП. Соматически здоровы были 19 (47,5%) больных эпилепсией.
Среди 21 пациента с коморбидной патологией чаще встречались пациенты с одним сопутствовавшим заболеванием (13 пациентов; 62%). Остальные имели 2 (4 пациента; 19%) или 3 коморбидных заболевания (4 пациента — 19%) соответственно.
На первом месте среди коморбидных заболеваний была патология желудочно-кишечного тракта (ЖКТ): она имела место у 8 (38%) пациентов. При этом патология одного органа была у 3 пациентов, двух — у 2 пациентов. У 3 пациентов было сочетание патологии ЖКТ с анемией, гипотиреозом и ожирением.
На втором месте было алиментарно-конституциональное ожирение, наблюдавшееся у 6 (28,6%) пациентов. Изолированное ожирение имело место у 4 больных эпилепсией. У одной пациентки оно сочеталось с дисменореей. Еще у одного пациента ожирение сочеталость с патологией ЖКТ.
Равное распределение было между пациентами с патологией сердечно-сосудистой системы (артериальная гипертензия), опорно-двигательного аппарата и глаз: эти коморбидные патологии имели по 2 (9,5%) больных эпилепсией. У 1 (4,8%) человека было сочетание гипотиреоза с дисменореей.
В постоянном приеме сопутствовавших препаратов в связи с коморбидностью нуждались 5 (23,8%) человек: 2 с гипотиреозом (принимали L-тироксин), 2 с артериальной гипертензией (принимали антигипертензивные средства), 1 с ревматоидным артритом (пациентка принимала метатрексат, нестероидные противо-воспалительные средства в таблетках). Остальные 9 (42,9%) пациентов с патологией ЖКТ и дисменореей проводили лечение периодически. Семь (33,4%) пациентов с коморбидной патологией в связи с ее стабильным хроническим течением не использовали дополнительную лекарственную терапию.
Из-за отсутствия эффекта 8 (20%) пациентам перампанел был отменен, 27 (67,5%) больных продолжили терапию в дозах 4 мг (3 пациента), 6 мг (8 пациентов), 8 мг (10 пациентов), 10 мг (5 пациентов), 12 мг (1 пациент), причем эффективность перампанела была хорошей как для молодых больных, так и для пациентов среднего и пожилого возраста.
Несмотря на исходно тяжелое течение заболевания и число резистентных пациентов, ремиссия на политерапии с перампанелом была достигнута 5 (12,5%) пациентами. Число респондеров (пациентов, у которых частота приступов снизилась на 50% и более) составило 55% (22 человек). Эффект на терапию отсутствовал у 13 (32,5%) больных (р=0,016) (рис. 7).
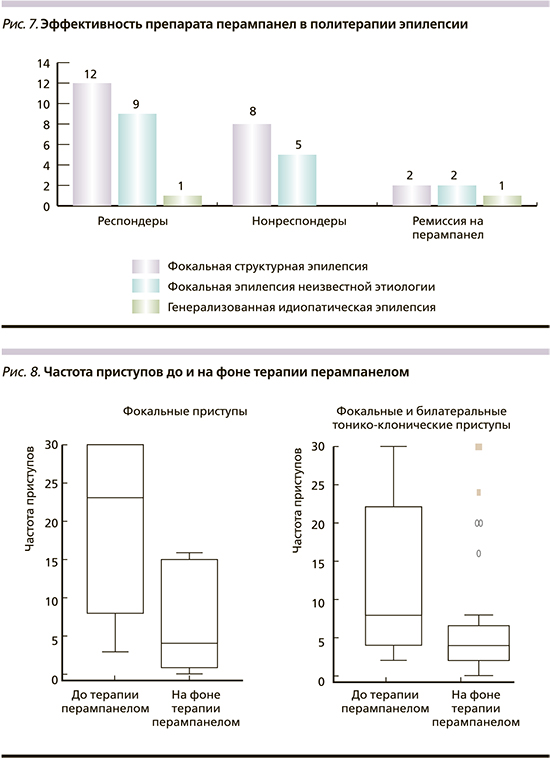
На фоне проводимой терапии препаратом перампанел зарегистрировано достоверно значимое снижение частоты всех типов приступов как фокальных, так и билатеральных тонико-клонических, генерализованных приступов, миоклоний. Процент снижения средней частоты фокальных приступов к окончанию периода наблюдения составил 82%, средняя частота фокальных и билатеральных тонико-клонических сократилась на 50%, процент снижения средней частоты генерализованных приступов (в сочетании с миоклониями или без) к окончанию периода наблюдения составил 88%, (р=0,006) (рис. 8).
Полученные данные подтвержают эффективность препарата перампанел при разных формах эпилепсии.
Средний балл КЖ был выше на 5 баллов у пациентов на терапии препаратом перампанел и составил 54±6,92, в то время как до начала терапии он составлял 49±7,3. Различия имеют статистическую достоверность: р<0,01 (табл. 2).
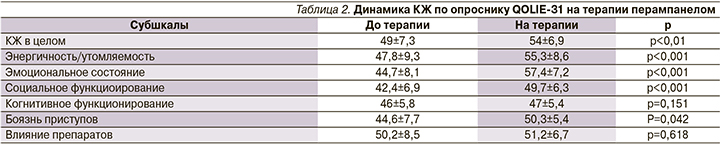
По субшкале энергичность/утомляемость в группах сравнения данные были выше у пациентов на лечении с перампанелом (55,3±8,6 по сравнению с 47,8±9,3 до терапии перампанелом; р<0,001). На фоне терапии перампанелом пациенты отметили, что стали более энергичными, реже испытывали усталость, что не могло не сказаться на улучшении КЖ в целом.
Субшкала эмоционального состояния выявила достоверно более низкий показатель до начала лечения перампанелом по сравнению с таковым на лечении (44,7±8,1 и 57,4±7,2 соответственно; р=0,03), что может свидетельствовать о более высокой степени тревожности у пациентов, не получавших перампанел.
Показатели субшкалы социального функционирования среди пациентов на терапии препаратом перампанел также были достоверно выше, чем до начала терапии (49,7±6,3 по сравнению с 42,4±6,9). Хотя процент безработных был достаточно высоким среди всех пациентов, на фоне снижения числа приступов пациенты стали более самостоятельными в своей повседневной активности и отметили снижение опеки со стороны родственников.
Умственная деятельность и субшкала когнитивной функции показали сопоставимый результат в группах наблюдения без статистических различий (р=0,151), что свидетельствовало об отсутствии влияния препарата на когнитивные функции.
Беспокойство по поводу приступов достоверно чаще проявляли пациенты до терапии с препаратом перампанел: 44,6±7,7 балла по сравнению с 50,3±5,4 (р=0,042). Этот фактор способствовал выполнению рекомендаций врача по лечению с целью дополнительного контроля болезни. Более чем половиной пациентов на терапии перампанелом достигнуто сокращение частоты приступов, четверть пациентов вышли в ремиссию, что не могло не сказаться на снижении обеспокоенности в связи с заболеванием.
Субшкала по влиянию лекарственных средств выявила схожие показатели у пациентов до и на фоне терапии перампанелом: 50,2±8,5 и 51,2±6,7 балла соответственно (р=0,618). Это связано как с продолжительностью заболевания, так и большим числом принимаемых до старта терапии перампанелом схем лечения.
В целом у пациентов была хорошая переносимость препарата перампанел. Процент удержания пациентов на терапии составил 67,5%, длительность удержания на терапии соответствовала всему периоду наблюдения: 12 месяцев. Побочные эффекты отсутствовали у 32 (80%) пациентов на перампанеле. У 8 больных (6 молодых и 2 пациента среднего возраста) были зарегистрированы побочные эффекты. Чаще встречались сонливость, головокружение и слабость, которые имели место у 3 (7,5%) 3 (7,5%) и 2 (5%) пациентов соответственно. Изменение массы тела имело место у 2 (5%) человек, при этом у 1 больного была прибавка, у другого - снижение массы тела. Реже встречались головные боли, агрессия, трудности в подборе слов, сердцебиение: каждый из побочных эффектов был зарегистрирован у 1 пациента из числа принявших участие в наблюдении. Сочетание побочных эффектов имело место у 4 (10%) больных. У 5 (12,5%) пациентов с побочными эффектами имела место сопутствовавшая соматическая патология, у 3 (7,5%) больных с побочными эффектами таковой не было.
Среди пациентов с коморбидной патологией побочные эффекты, приведшие к отмене лечения, отмечены у 4 человек из 5. У первой пациентки с патологией ЖКТ зарегистрированы такие побочные эффекты, как сердцебиение и сонливость; у второй с гипотиреозом и дисменореей - сонливость и агрессия; у третьей пациентки с ожирением - заторможенность; у четвертой пациентки с ревматоидным артритом, остеопорозом, дисменореей - слабость, сонливость и головокружение. Следует отметить, что у всех четырех коморбидных пациентов, прервавших терапию перампанелом, побочные эффекты затронули нервную систему и ни у одного не было выявлено влияния перампанела на имевшуюся соматическую патологию.
Пятый пациент остался на терапии перампанелом, несмотря на развившийся побочный эффект: снижение массы тела на 15 кг от исходного уровня, поскольку изначально имел ожирение, т.е. препарат оказал «положительное действие» на массу тела. Также перампанел у данного пациента оказал отчетливое действие на урежение тонико-клонических приступов более чем на 50% и позволил оптимизировать терапию - вывести из схемы вальпроевую кислоту, которая привела к развитию лекарственного гепатита, и остаться на комбинации леветирацетам+перампанел.
Из трех соматически здоровых пациентов с побочными эффектами двое (1 пациент с прибавкой массы тела и 1 пациент с преходящей сонливостью) продолжили терапию перампанелом, одна пациентка завершила терапию в связи с жалобами на головные боли и головокружение.
Не было выявлено различий по характеру развития побочных эффектов в группе соматически здоровых и коморбидных пациентов. В обоих случаях преобладали побочные эффекты, связанные с негативным влиянием на ЦНС, которые переносились хуже всего, что в итоге привело к отмене лечения 5 пациентов из 8 с побочными эффектами на фоне терапии перампанелом. В то же время побочные эффекты, связанные с изменением массы тела, не привели к прекращению лечения: оба пациента остались на терапии препаратом перампанел, поскольку отметили хороший эффект от лечения и были готовы мириться с побочными эффектами.
У всех 5 пациентов, которые вынуждены были завершить терапию перампанелом на первом месяце лечения вследствие побочных эффектов, степень их выраженности была легкой и не требовала дополнительного лечения и/или диагностических процедур. Все побочные эффекты полностью регрессировали после отмены препарата.
Также не было отмечено влияния доз на частоту появления и выраженность побочных эффектов. Как на 2, 4 мг, так и на более высокой дозе распространенность побочных эффектов была одинаковой. Вместе с тем, чем больше сопутствовавших АЭП получал пациент, тем чаще развивались побочные эффекты. Так, если перампанел назначался 3-м и последующим препаратом, риск развития побочных эффектов был в 3 раза выше: у 6 (15%) пациентов с побочными эффектами перампанел был назначен 3-м и последующим препаратом, и только у 2 (5%) пациентов - вторым препаратом. В группе коморбидных пациентов у 4 человек, завершивших терапию вследствие развития побочных эффектов, перампанел был 3-м добавленным к лечению препаратом, у 1 пациентки - 4-м, тогда как у соматически здоровых пациентов 2 человека из 3 получали монотерапию и 1 человек находился на дуотерапии.
Наличие побочных эффектов не зависело от числа сопутствовавших заболеваний (р=0,269), что позволяет считать перампанел достаточно безопасным в плане лечения комобидных пациентов.
Анализируя комбинации препаратов и возникшие побочные эффект, следует отметить, что в группе пациентов с коморбидными заболеваниями и развившимися побочными эффектами в период наблюдения 1 человек получал вальпоевую кислоту и топирамат, 1 - вальпроевую кислоту и зонисамид, 1 - леветирацетам и вальпроат, 1 - леветирцетам и трилептал, 1 - леветирацетам, ламотриджин и клоназепам.
Среди соматически здоровых один человек принимал вальпроат, один - вальпроат и топирамат, один - топирамат.
Самые распространенные побочные эффекты были со стороны ЦНС и чаще возникали на различных комбинациях с топираматом (3 человека). Соответственно, пациентов, находившихся на терапии топираматом, можно отнести к группе риска, поскольку топирамат сам по себе достаточно часто приводит к развитию побочных эффектов с вовлечением ЦНС.
Обсуждение
В данном наблюдении, выполненном в условиях реальной клинической практики, продемонстрирована эффективность использования препарата перампанел в политерапии в отношении разных видов приступов у пациентов с резистентной эпилепсией. На фоне проводимой терапии перампанелом зарегистрировано достоверно значимое снижение числа всех типов приступов: фокальных, сочетание фокальных и тонико-клонических, генерализованных приступов и миоклоний. Процент снижения средней частоты фокальных приступов к окончанию периода наблюдения составил 82%, средняя частота фокальных и билатеральных тонико-клонических сократилась на 50%, процент снижения средней частоты генерализованных приступов (в сочетании с миоклониями или без) к окончанию периода наблюдения составил 88% (р=0,006). Это подтверждает эффективность препарата при разных формах эпилепсии. Достигнуть медикаментозной ремиссии и удержать ее удалось 12,5% пациентов. Более половины (55%) пациентов были респондерами и только трети не удалось достигнуть желаемого эффекта.
Позднее назначение препарата было связано как с длительным стажем болезни пациентов и отсутствием современных АЭП в начале заболевания, так и с их ограниченными финансовыми возможностями, что мешало назначать терапию перампанелом раньше. Включение перампанела с октября 2017 г. в Перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения (ЖНВЛП) [18] расширяет возможности применения этого препарата в повседневной клинической практике, в т.ч. и в ранней дополнительной терапии. Недавно опубликованный международный опыт применения перампанела в повседневной клинической практике свидетельствует: препарат демонстрирует хорошую переносимость вне зависимости от сопутствующего АЭП [19], при этом лучшая эффективность наблюдается при применениии перампанела в ранней дополнительной терапии [20].
В клиническое наблюдение включены пациенты с коморбидной патологией, причем спектр соматических заболеваний был достаточно широк: патология со стороны ЖКТ, метаболические нарушения, сердечно-сосудистая коморбидность (артериальная гипертензия), хронические нейроэндокринные заболевания. Несмотря на имевшуюся полиморбидность выборки пациентов, у 80% из них на фоне лечения перампанелом побочных эффектов не отмечалось. Терапия перампанелом отменена только лишь четверым коморбидным пациентам по причине развития побочных эффектов со стороны ЦНС (сонливость, вялость и т.д.), а не из-за ухудшения статуса коморбидного заболевания. Перампанел показал хорошую переносимость в разных возрастных группах как пациентов молодого, так и среднего возраста. Не было выявлено влияния перампанела на сопутствовавшую патологию, в т.ч. требовавшего модификации дополнительной терапии. Риск побочных эффектов увеличивался, если перампанел назначали в схеме терапии 3-м и последующим препаратом. Таким образом, для снижения риска побочных эффектов необходима оптимизация схемы лечения. Побочные эффекты чаще затрагивали ЦНС и по характеру проявлений совпадали с таковыми по данным многоцентровых зарубежных исследований [2125]. Однако частота побочных эффектов со стороны ЦНС была выше при добавлении перампанела к топирамату [26].
Хорошая переносимость перампанела коморбидными пациентами в сочетании с эффективным контролем приступов коррелирует и с показателями КЖ (QOLIE) [17]. Исходный уровень КЖ у пациентов исследуемой группы был достаточно низким, что связано как с длительным стажем заболевания, так и с его тяжестью, что неизбежно осложняло социальную активность пациентов и влияло на их эмоциональное состояние. Большинство пациентов отмечали потребность в дополнительной опеке со стороны родственников. На фоне дополнительной терапии препаратом перампанел КЖ значимо улучшилось. Также удалось добиться повышения показателей по субшкалам социального функционирования, энергичности/утомляемости, эмоционального состояния.
Заключение
Лечение пациентов с эпилепсией — длительный процесс, целью которого является контроль приступов с сохранением КЖ. Когда принимается решение о назначении АЭП, особенно в схемах, в которых используется несколько препаратов, необходимо учитывать не только особенности основного заболевания — эпилепсии (тип приступов, тип эпилепсии, эпилептический синдром), но и сопутствующую коморбидную патологию. Современная парадигма терапии хронических заболеваний предполагает фокус внимания не на заболевании, а на пациенте.
В связи с этим переносимость и безопасность принимаемых препаратов, их влияние на КЖ становятся в один ряд с эффективностью терапии. Профиль безопасности и хорошая переносимость АЭП пациентами с сопутствовавшими соматическими заболеваниями — это краеугольный камень при подборе терапии. Коморбидные состояния со стороны ЦНС, сердечно-сосудистой, нейроэндокринной систем, ЖКТ и др. при эпилепсии утяжеляют состояние больного и ухудшают прогноз. Кроме того, коморбидность снижает приверженность приему АЭП. Пытаясь устранить побочные эффекты от приема АЭП, удержать привычный уровень КЖ, пациенты могут самостоятельно снижать дозы АЭП, а порой и прекращать их прием, тем самым утяжеляя течение эпилепсии, в конечном итоге ухудшая прогноз заболевания и прогноз жизни в целом. В этом контексте с учетом полученных в ходе данного наблюдения результатов можно рассматривать перампанел как препарат выбора в дополнительной терапии пациентов с коморбидными состояниями с точки зрения эффективности и безопасности.
Поскольку пациент с отягощенным соматическим статусом зачастую не привержен АЭП из-за рисков прогрессирования соматического заболевания, необходимо выбирать такую противоэпилептическую терапию, которая бы не усугубляла коморбидный фон, не ухудшала КЖ пациента, при этом надежно контролировала бы приступы. Как показала клиническая практика, перампанел является одним из таких вариантов дополнительной терапии.



