Болезнь Паркинсона (БП) – медленнопрогрессирующее нейродегенеративное заболевание, характеризующееся накоплением альфа-синуклеина и формированием интранейрональных телец Леви, которое проявляется главным образом двигательными расстройствами в виде гипокинезии, ригидности мышц, тремора покоя и постуральных нарушений, вызванных преимущественным поражением дофаминергических нейронов черной субстанции. Кроме того, БП сопровождается широким спектром немоторных расстройств, значительно ухудшающих повседневную активность и качество жизни пациентов. Немоторные симптомы представлены при БП вегетативными нарушениями (гастроинтестинальные, мочеполовые, кардиоваскулярные, сексуальные, терморегуляционные расстройства); нарушениями сна (сонливость в дневное время, бессонница в ночное время, нарушения поведения в фазе быстрого сна); нейропсихиатрическими симптомами (когнитивные нарушения, депрессия, тревога, апатия, зрительные галлюцинации и бредовые расстройства), болью [1].
Как правило, критериями эффективности лечения в клинических исследованиях являются физикальные данные и лабораторные показатели, но они не отражают самочувствия больного и его функционирование в повседневной жизни. Исследование качества жизни (КЖ) позволяет изучить влияние заболевания и лечения на показатели КЖ больного человека, оценивая все составляющие здоровья – физическое, психологическое и социальное функционирование [2].
В современных клинических исследованиях показатели КЖ больного являются в ряде случаев основными критериями определения эффективности лечения. В течение последнего десятилетия практически все многоцентровые рандомизированные исследования, посвященные сравнению эффективности различных методов лечения, наряду с традиционными клиническими критериями изучения их эффективности включают оценку КЖ. В зависимости от результатов исследования КЖ рассматривают как дополнительный или как основной критерий при определении преимуществ той или иной схемы лечения. Доказано, что параметры КЖ больного обладают независимой прогностической значимостью и являются более точным фактором прогнозирования течения заболевания на фоне терапии, чем соматический статус [3, 4].
Экспертами Межнационального центра исследования качества жизни была разработана концепция исследования КЖ в медицине [1]. Основные элементы этой концепции:
- определение понятия «качество жизни»;
- составляющие концепции КЖ;
- методология исследования КЖ;
- основные направления применения исследования КЖ в медицине.
Существуют различные определения КЖ. Тем не менее общепризнанно, что КЖ служит многомерным понятием и отражает степень соответствия между реальным и желаемым состояниями индивидуума; на него влияют состояние его здоровья, положение в обществе, его цели, планы и возможности [5]. Под КЖ обычно понимают степень жизненного благополучия, которая определяется соответствием между реальным и желаемым состояниями индивидуума, на которое влияют как объективные факторы (прежде всего степень функционального дефекта), так и субъективные – эмоциональные, социально-психологические и др. [6]. КЖ – интегральная характеристика физического, психологического, эмоционального и социального функционирования больного, основанная на его субъективном восприятии [7].
В современной медицине широкое распространение получил термин «качество жизни, связанное со здоровьем» (КЖСЗ), при этом под этим термином подразумевается субъективное восприятие пациентом влияния проявлений болезни и ее последствий на жизнь пациента [8]. К составляющим КЖСЗ относятся психологическое, социальное, физическое и духовное благополучие пациента (табл. 1) [9].
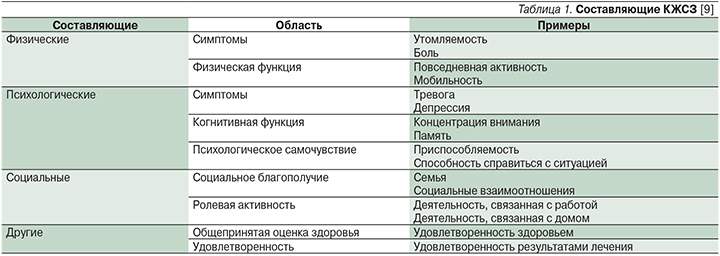
КЖСЗ оценивает компоненты, не связанные и связанные с заболеванием, а также позволяет дифференцированно определить влияние болезни и лечения на состояние больного. БП – хроническое заболевание, при котором оценка пациентом своего состояния является самым важным показателем КЖ. В табл. 2 представлены факторы, влияющие на КЖСЗ пациентов БП. Некоторые из них изучены исчерпывающе и значительно ухудшают КЖСЗ (например, депрессия, нарушения сна), тогда как другие факторы требуют дальнейшего изучения с целью повышения эффективности оказания медицинской помощи и социальной адаптации больных [8].
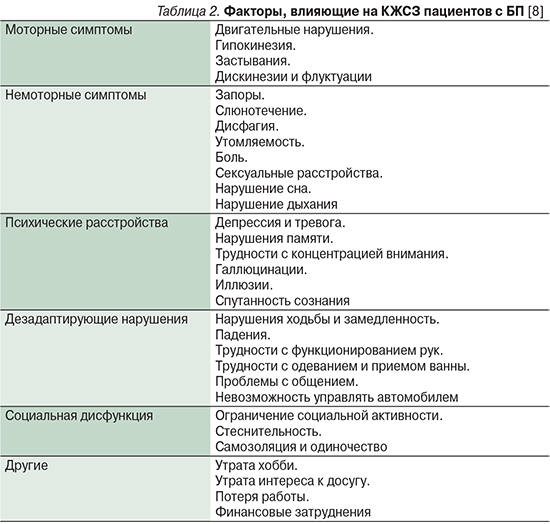
Выделяют три основные составляющие концепции КЖ:
- многомерность (термин КЖ включает информацию об основных сферах жизнедеятельности человека: физической, психологической, социальной, духовной и экономической);
- изменяемость во времени (показатели КЖ меняются во времени в зависимости от состояния больного, обусловленного рядом экзогенных и эндогенных факторов);
- участие больного в оценке его состояния (оценка КЖ должна проводиться пациентом, т.к., по результатам многочисленных исследований, она часто не совпадает с оценкой КЖ, выполненной врачом).
Сферы применения исследования КЖ в практическом здравоохранении достаточно обширны, к наиболее важным относятся стандартизация методов и экспертиза новых методов лечения; обеспечение индивидуального мониторинга состояния больного с оценкой ранних и отдаленных результатов лечения; разработка прогностических моделей течения и исхода заболевания, проведение социально-медицинских популяционных исследований с выделением групп риска; разработка фундаментальных принципов паллиативной медицины; обеспечение динамического наблюдения и оценка эффективности профилактических программ; повышение качества экспертизы новых лекарственных препаратов, а также экономическое обоснование методов лечения с учетом фармакоэкономических критериев [8, 10].
Правильный выбор инструмента исследования – основа методологии исследования КЖ. В зависимости от области применения выделяют общие и специальные опросники. Общие опросники предназначены для оценки КЖ как здоровых, так и больных независимо от заболевания. Отдельные инструменты оценки КЖ разработаны и внедрены в клиническую практику специально для пациентов с БП, включающие оценку тяжести двигательных симптомов, двигательной и социальной активности, эмоционального состояния и когнитивного статуса пациентов. Шкалы, позволяющие наиболее полно оценить различные аспекты КЖ пациентов с БП: шкала оценки качества жизни при БП, состоящая из 39 пунктов (PDQ-39) и ее краткая форма, состоящая из 8 пунктов (PDQ-8); шкала КЖ БП (PD-QUALIF) и опросник для оценки КЖ БП (PDQL) [11–14]. Кроме того, для оценки пациентов с БП широко используются общие шкалы, такие как EuroQol-5D (EQ-5D), краткий вариант опросника для оценки состояния здоровья, состоящий из 36 пунктов (SF-36), и профиль влияния заболевания (SIP) [15–17]. При использовании этих шкал в клинических исследованиях оценивались отдельные показатели КЖ больных БП. Однако ряд потенциальных проблем, представленных в табл. 3, препятствует объективному исследованию показателей КЖСЗ [8].
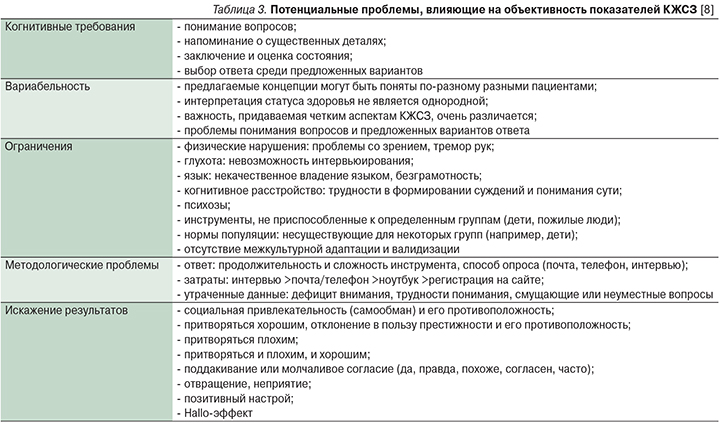
Одно из ведущих направлений исследований при БП – выявление факторов, ухудшающих КЖ пациентов. Перспективной задачей служит разработка индивидуализированной терапии с учетом ведущих дезадаптирующих проявлений заболевания. В связи с этим активно изучаются эмоциональные, когнитивные, поведенческие расстройства, утомляемость, нарушения сна и бодрствования, что обусловлено их высокой частотой при БП, а также значимым негативным влиянием на КЖ пациентов и их близких [18, 19].
Влияние моторных флуктуаций (феномен истощения окончания действия дозы, непредсказуемые периоды выключения, утренняя и ночная акинезия), двуфазных дискинезий, утренней дистонии, дискинезии пика дозы, постуральной неустойчивости, падений, застываний при ходьбе, брадикинезии, ригидности, нарушений речи и глотания на КЖ пациентов с БП не вызывает сомнений. Однако расстройства сна, снижение массы тела, аффективные нарушения (депрессия, апатия, ангедония), когнитивные расстройства и нарушения мочеиспускания также в значительной степени снижают показатели КЖСЗ. Наряду с этим такие особенности пациента, как психологический настрой по отношению к болезни, низкий уровень образования, субъективная оценка в отношении диагноза, играют важную роль в самооценке КЖСЗ.
К настоящему времени получено недостаточно данных о влиянии на КЖ пациентов БП нефармакологических методов лечения, таких как лечебная физкультура, танцевальная терапия, питание, поддержка со стороны родственников; не изучена роль информационной поддержки, обучающих программ и психотерапевтических занятий. В некоторых экспериментальных исследованиях показано, что ежедневная физическая активность на ранних этапах болезни способна увеличить выработку собственного дофамина и снизить потребность в противопаркинсонических препаратах большинства пациентов [20]. Возможно, физическая реабилитация обладает нейропротективным потенциалом, способствуя продукции нейротрофических факторов головного мозга и замедлению нейродегенеративного процесса. Однако данный эффект утрачивается, как только регулярная физическая активность прекращается [21]. Кроме того, проблемы с ходьбой на развернутых стадиях болезни в виде застываний становятся самостоятельным дезадаптирующим фактором [22].
В клинических исследованиях, определяющих влияние различных факторов на КЖ больных БП, было убедительно показано, что депрессия и нарушения сна являются главными немоторными нарушениями, определяющими КЖСЗ. Поэтому оценка эффективности на основании только двигательных нарушений в клинических исследованиях не позволит определить влияние противопаркинсонических препаратов на КЖ, особенно у тех пациентов, у которых преобладают немоторные нарушения.
Нарушения сна и бодрствования в значительной части случаев оказывают крайне неблагоприятное влияние на общее состояние больных, в то время как активная терапия этих расстройств существенно улучшает повседневную активность и КЖ пациентов с БП [23, 24]. Выделяют первичные и вторичные нарушения сна при БП. Первичные нарушения сна представлены трудностями засыпания, фрагментацией сна, частыми пробуждениями, трудностями засыпания после пробуждения, поверхностным сном, а также повышенной дневной сонливостью, нарушением поведения во сне с быстрыми движениями глазных яблок. Они могут задолго предшествовать манифестации двигательной стадии БП и нарастают по мере прогрессирования заболевания. Вторичные нарушения сна служат следствием моторных ночных симптомов (акинезия, ригидность, тремор, акатизия, синдром беспокойных ног, периодические движения конечностей во сне) и немоторных проявлений заболевания (никтурия, болезненные крампи, панические атаки, тревога, галлюцинации, ночные кошмары, сноговорение, возбуждение) [25]. Некоторые ночные симптомы, ухудшающие сон при БП, связаны с приемом противопаркинсонических препаратов (холинолитики, амантадины, агонисты дофаминовых рецепторов, ингибиторы моноаминооксидазы типа В, ингибиторы катехол-О-метилтрансферазы). Существенное влияние на регуляцию сна и бодрствования оказывают противопаркинсонические средства и ряд других препаратов: амантадины, леводопа, селективные ингибиторы обратного захвата серотонина [26].
Дофаминергические препараты могут улучшать или ухудшать сон пациентов с БП. Низкие дозы дофаминергических препаратов оказывают седативное действие, а более высокие дозы затрудняют засыпание, могут вызывать ночные кошмары, галлюцинации, фрагментацию сна, дневную сонливость, а также некоторые парасомнии. В то же время, уменьшая ночную акатизию, ригидность и периодические движения конечностями во сне, они могут улучшать сон. Выраженность и частота первичных нарушений сна и бодрствования при БП обычно коррелирует с продолжительностью заболевания и нарастает по мере увеличения тяжести его симптомов.
Распространенность нарушения сна при БП трудно установить, данные различных авторов варьируются от 42 до 98% [27]. Нарушения сна и бодрствования могут быть представлены расстройством засыпания и поддержания сна (инсомнией), повышенной дневной сонливостью (гиперсомнией) и парасомниями.
Нарушение засыпания возникает у двух третей больных БП и может быть связано с усилением симптомов паркинсонизма в вечернее и ночное время (особенно у больных с моторными флуктуациями), приемом противопаркинсонических средств, синдромом беспокойных ног и тревогой. Нарушение поддержания сна и преждевременное утреннее пробуждение чаще всего обусловлены усилением паркинсонической симптоматики на фоне ослабления действия вечерней дозы леводопы и депрессии. Повышенная дневная сонливость может иметь постоянный или пароксизмальный характер (в виде приступов непреодолимого засыпания). Причиной дневной сонливости могут быть нарушения ночного сна, синдром центральных или обструктивных апноэ во сне, прием седативных препаратов и дофаминергических средств, в т.ч. леводопы и агонистов дофаминовых рецепторов.
К наиболее частым парасомниям, наблюдающимся при БП, относятся двигательная активность во сне с быстрыми движениями глаз, периодические движения конечностями, ночная миоклония, ночные кошмары, сноговорение и ночные галлюцинации. Среди многочисленных немоторных симптомов БП депрессия играет важную роль из-за высокой частоты и значительного влияния на КЖ больных и их родственников. Выраженная депрессия ухудшает повседневную активность, отягощает течение основного заболевания, часто является фактором риска развития деменции при БП. Кроме того, она уменьшает комплаентность больного. Аффективные нарушения часто не диагностируются при БП, и больные не получают адекватной терапии.
Депрессия встречается на любой стадии БП и ассоциируется с низким КЖ пациентов и их родственников. По данным различных авторов, частота депрессии в популяции составляет 3–10%, при БП она встречается в среднем среди 40–50% больных. У одних больных депрессия предшествует развитию двигательных расстройств, у других совпадает с началом моторных проявлений, у третьих – развивается на фоне моторных флуктуаций [28].
В структуре депрессии часто возникает апатия – одно из самых частых аффективных расстройств у пациентов с БП, характеризующееся утратой мотивации, интереса к окружающему, снижением инициативы, эмоциональной тупостью, индифферентностью [29]. Чаще всего депрессию сопровождает тревога, но может встречаться и отдельно от нее. Как и депрессия, тревога может иметь реактивный характер или быть связанной с дегенерацией дофаминергических, серотонинергических или норадренергических нейронов ствола мозга и вторичной дисфункцией подкорково-корковых кругов [30].
Нарушение когнитивных функций (памяти, внимания, ориентации, мышления и др.) с помощью нейропсихологических тестов выявляется у 95% больных. В начале заболевания у большинства пациентов с БП когнитивные нарушения бывают легкими и умеренными. При первичном обследовании деменция выявляется примерно у 30–40% больных БП. Однако при длительном наблюдении за отобранной группой больных деменция рано или поздно развивается у 50–80% больных.
Деменция характеризуется множественным нарушением когнитивных функций, приводящим к социальной дезадаптации, т.е. к утрате трудоспособности или бытовой независимости, которую невозможно объяснить чисто двигательными дефектами.
Медикаментозная терапия, направленная на коррекцию двигательных нарушений, в т.н. медовый месяц наиболее эффективна и значительно улучшает повседневную активность и КЖ пациентов. Однако с прогрессированием заболевания, нарастанием моторных осложнений и немоторных симптомов коррекция только моторных нарушений не улучшает показателей КЖ пациентов.
За последнее десятилетие во всем мире существенно возросла исследовательская активность в области изу-чения КЖ больных как одного из важнейших показателей эффективности оказания медицинской помощи. Несмотря на большую распространенность немоторных симптомов БП и их влияние на уровень функциональной активности и КЖ, клинические исследования, оценивающие эффективность и безопасность лечения этих симптомов, особенно у больных БП, малочисленны.
Таким образом, исследование КЖ является важным компонентом современных клинических исследований и клинической практики. Необходимо различать понятия «качество жизни» и «качество жизни, связанное со здоровьем». КЖ отражает степень соответствия между реальным и желаемым состоянием индивидуума, на которое влияют состояние его здоровья, положение в обществе, его цели, планы и возможности. А КЖСЗ – это субъективное восприятие пациентом влияния проявлений болезни и ее последствий на жизнь пациента.
Информация о субъективных переживаниях больного, изложенная врачом, недостаточна для принятия ряда важных клинических решений. Субъективные переживания больного должен выражать сам больной. Таким образом, оценка КЖСЗ самим пациентом предпочтительна и дополняет общую клиническую картину.
Исследования КЖСЗ – принципиально новый метод, позволяющий изучать многоплановую картину субъективных переживаний больного, вызванных болезнью. Методология исследования КЖ позволяет определять показатели ключевых составляющих здоровья человека: физического, психического и социального функционирования. Правильный выбор инструмента исследования – основа методологии исследования КЖ.
В зависимости от области применения выделяют как общие (EuroQol-5D, SF-36, SIP), так и специальные опросники (PDQ-39, PDQ-8, PD-QUALIF, PDQL).
Оценка показателей КЖСЗ позволяет объективно оценить состояние пациента, определить основные факторы, ухудшающие КЖСЗ, и расставить приоритеты, согласно им. Интегрированная информация о физическом, психологическом, духовном и социальном аспектах заболевания способствует получению представления об общих закономерностях реакции больного на патологический процесс, выявлению индивидуальных особенностей реакции на заболевание, а также оценке эффективности лечения конкретного больного по данным индивидуального мониторинга и использованию этих данных для определения персонифицированной программы лечения.



