Внутрипеченочный холестаз беременных (ВХБ) является наиболее частой патологией печени у беременных [1]. По современным данным, частота развития ВХБ достигает 15,6% [1–3]. Анализ клинических проявлений ВХБ и тактики лечения представляется актуальным не только для акушеров и гинекологов, но и для врачей общей практики, терапевтов и гастроэнтерологов [3]. ВХБ – это относительно доброкачественное холестатическое заболевание печени, развивающееся во II или III триместре беременности, характеризующееся зудом и повышением концентрации желчных кислот в сыворотке крови [1]. Несвоевременность диагностики ВХБ приводит к неадекватной медикаментозной коррекции данного состояния у матери и как следствие – возможного развития перинатальных осложнений (преждевременные роды, дистресс плода, его внутриутробная гибель).
Причина развития ВХБ неизвестна, но, по-видимому, оно обусловлено мультифакториальным фоном, включающим генетические, гормональные, средовые и диетические факторы [1, 3, 4]. Семейные случаи заболевания и повышенная заболеваемость в определенных этнических группах могут быть объяснены генетическим компонентом. К настоящему времени известно, что до 16% случаев ВХБ ассоциированы с мутациями гена ABCB4 [5].
Основываясь на современных данных, можно сделать следующий вывод: генетический базис ВХБ не ограничивается лишь вариациями гена ABCB4, а носит комплексный характер, т.к. в генезе данного заболевания могут принимать участие и другие гены, кодирующие канальцевые транспортеры или их регуляторы, в частности гены FXR и ABCC2 [6, 7]. В экспериментальных и клинических исследованиях доказано, что эстрогены могут индуцировать холестаз и, по-видимому, ВХБ [8]. В большинстве описанных случаев ВХБ развивается в течение III триместра, когда концентрация эстрогенов в сыворотке крови достигает максимума. Кроме того, ВХБ часто развивается при многоплодной беременности, при которой уровень циркулирующих эстрогенов выше, чем при одноплодной беременности [9]. Развитие ВХБ также может быть связано с изменениями метаболизма прогестерона, т.к. прием препаратов, содержащих прогестерон, служит установленным фактором риска ВХБ [10, 11].
Дебют заболевания приходится на 28–30-ю неделю беременности.
У пациенток развивается кожный зуд, интенсивность которого часто изменчива [1, 2]. Достаточно характерно усиление кожного зуда по ночам. Локализация зуда вариабельна от всей поверхности тела, до локального зуда ладоней и ступней. Зуд может развиваться до появления лабораторных признаков заболевания [12]. Диспепсические явления (тошнота, рвота, анорексия) и боль в животе возникают относительно редко. Развитие фульминантного течения с нарастанием признаков печеночной недостаточности не характерно для ВХБ и требует поиска других причин заболевания печени [1].
При объективном осмотре пациентки оценивается выраженность желтухи, которая может варьироваться от легкой иктеричности склер до интенсивного окрашивания кожных покровов. Частота возникновения желтухи варьируется от 17 до 75% случаев ВХБ [13–15]. Этот симптом обычно развивается через 1–4 недели от появления кожного зуда [1, 3, 13]. Необходимо обращать внимание на наличие гематом, а также прицельно расспрашивать пациентку о наличии кровоточивости десен, носовых и геморроидальных кровотечений, что может свидетельствовать о дефиците витамина К [16]. Значительная гепато- и спленомегалия при объективном обследовании выявляется чрезвычайно редко.
При оценке лабораторных показателей отмечаются признаки холестатического синдрома. Так, при ВХБ значительно повышена концентрация желчных кислот в сыворотке крови, что может быть первым или единственным лабораторным признаком заболевания [1, 3, 17, 18]. В большей степени в сыворотке крови повышается содержание холевой, чем хенодезоксихолевой, кислоты [19]. Отмечается повышение уровня щелочной фосфатазы в сыворотке крови (неспецифичное для холестаза при беременности из-за экспрессии плацентарного изофермента), 5’-нуклеотидазы и концентрации общего и прямого билирубина [1, 16, 20]. Повышение уровня печеночных аминотрансфераз (аланинаминотрансфераза, аспартатаминотрансфераза) в сыворотке крови при ВХБ, как правило, достигает 10 норм, хотя описаны случаи и 25-кратного увеличения данных показателей [21].
При постановке диагноза ВХБ инструментальное обследование пациентки носит вспомогательный характер. При ультразвуковом обследовании желчные протоки не расширены, эхогенность и эхоструктура печени, как правило, не изменены. Биопсия печени выполняется в редких случаях тяжелого течения ВХБ или при проведении дифференциальной диагностики генеза поражения печени. Морфологически выявляются центролобулярный холестаз и желчные пробки в мелких желчных канальцах, которые могут быть расширены [22].
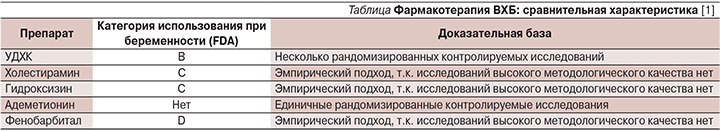
В основные задачи лечения ВХД входят купирование симптоматики заболевания, улучшение или нормализация качества жизни, а также снижение риска осложнений для организма матери и плода [1]. В ряде случаев для лечения ВХБ клиницисты применяют такие лекарственные средства, как холестирамин, гидроксизин, адеметионин, фенобарбитал. Тем не менее с современных позиций перечисленные препараты обладают достаточно ограниченной доказательной базой при лечении ВХБ и в большинстве случаев назначаются на основе эмпирически выработанных подходов. Помимо этого важно помнить о риске побочных эффектов, связанных с применением вышеперечисленных препаратов.
Исследований по применению холестирамина пациентками с ВХБ с высоким методологическим качеством нет [1, 16]. К тому же стоит отметить, что применение препарата в высоких дозах может индуцировать стеаторею и усиливать дефицит витамина К, увеличивая риск послеродовых кровотечений [23].
Гидроксизин снижает интенсивность зуда у пациенток с ВХБ, однако применение антигистаминных препаратов может приводить к развитию респираторных нарушений у новорожденных, особенно в случае их недоношенности [20].
Данные об эффективности адеметионина в рамках терапии ВХБ неоднозначны [24, 25]. В одном из рандомизированных исследований при сравнении эффективности адеметионина и урсодезоксихолевой кислоты (УДХК) было выявлено, что оба препарата снижали зуд, в то время как УДХК значительно более эффективно улучшала биохимические маркеры холестаза (снижала концентрации желчных кислот, билирубина, щелочной фосфатазы) [26].
Применение фенобарбитала при ВХБ снижает интенсивность кожного зуда у 50% пациенток, однако не оказывает влияния на лабораторные показатели и может быть ассоциировано с серьезными побочными эффектами [27, 28].
На настоящий момент большинство специалистов сходятся во мнении, что УДХК является препаратом выбора для лечения ВХБ [1, 3, 16, 20]. В пилотных, а затем и в контролируемых исследованиях пациенток с ВХБ было продемонстрировано, что УДХК достоверно снижает зуд и улучшает функциональные показатели печени, при этом побочные эффекты у матерей и детей не возникали [11, 21].
В мета-анализе девяти рандомизированных исследований 454 пациенток было показано, что применение УДХК приводило к лучшим результатам по сравнению с альтернативными препаратами (адеметионин, холестирамин и дексаметазон), плацебо или в отсутствие специального лечения [29]. У пациенток, принимавших УДХК, интенсивность зуда снижалась (61 по сравнению с 27%; отношение шансов [ОШ]=0,27) и купировалась чаще (42 по сравнению с 6%; ОШ=0,23), чем у лиц контрольной группы. У пациенток, принимавших УДХК, отмечено снижение уровня трансаминаз и желчных кислот в сыворотке крови, была ниже частота преждевременных родов (16 по сравнению с 34%; ОШ=0,44). Важным аспектом служит следующее: применение УДХК приводит к нормализации коэффициента соотношения холевая/хенодезоксихолевая кислота [11, 21]. В исследовании R. Zapata и соавт. (2005) показано отсутствие каких-либо побочных эффектов при длительном применении УДХК беременными, а также в катамнезе при наблюдении 26 детей, родившихся от этих матерей, обследовавшихся на протяжении 12 лет [30]. Оптимальная доза УДХК для лечения ВХБ не определена, хотя в большинстве случаев она составляет 500 мг дважды в сутки, или 15 мг на 1 кг массы тела в сутки. Необходимо специально отметить, что категория использования УДХК при беременности по классификации FDA (Food and Drug Administration) – B (экспериментальные исследования не выявили тератогенного действия; возможно применение препарата строго по показаниям). Для всех остальных препаратов эта категория значительно ниже (см. таблицу), что не оправдывает их применение в рамках терапии ВХБ [1].
Таким образом, диагноз ВХБ можно заподозрить у женщин II или III триместра беременности, жалующихся на наличие кожного зуда в случае отсутствия кожных высыпаний. Важным, но не исключительным фактором считается наличие желтухи различной интенсивности. Диагноз подтверждается с помощью лабораторных данных: повышенного содержания желчных кислот в сыворотке крови, билирубина, реже повышения уровня γ-глутамилтранспептидазы. Несвоевременность диагностики ВХБ приводит к неадекватной медикаментозной коррекции данного состояния у матери и как следствие – возможного развития патологии плода. УДХК является препаратом выбора в лечении ВХБ, что определено существенной доказательной базой эффективности и безопасности данного препарата в рамках терапии рассматриваемой патологии.


