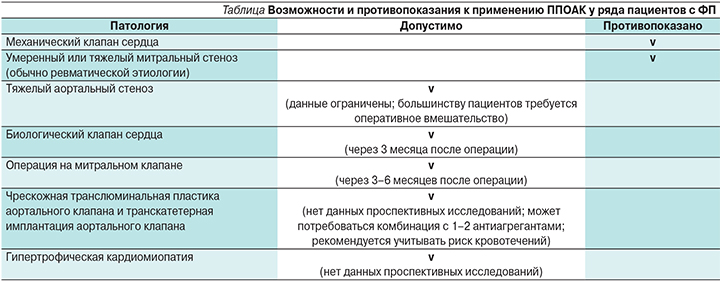
Получив определенный опыт применения класса прямых (новых) пероральных антикоагулянтов (ППОАК) у пациентов с фибрилляцией предсердий (ФП) неклапанной этиологии, оценив удобство использования и меньшие риски геморрагических событий, мы постепенно пытаемся расширять показания к применению препаратов данного класса с целью «охватить» им существенно бóльшие когорты пациентов. В последних (2015) рекомендациях по применению ППОАК, выпущенных Европейской ассоциацией сердечного ритма (EHRA – European Heart Rhythm Association), уже появились официальные предпосылки к продолжению подобной тенденции [1]. Экспертная группа специалистов, в число которых входят всемирно известные невролог Ханс-Кристоф Динер и кардиолог Джон Кэмм, допустила возможность применения ППОАК по целому ряду показаний (см. таблицу).
Несмотря на отсутствие официальных клинических исследований, ряд пациентов с подобными состояниями включались в ранее проводившиеся исследования с ППОАК. Так, например, анализ post-hoc-исследования ARISTOTLE, в котором у больных ФП сравнивали апиксабан и варфарин, показал, что 26,4% включенных в исследование пациентов имели умеренные поражения клапанов сердца (аортальный стеноз и аортальную недостаточность, умеренную митральную регургитацию и незначительный митральный стеноз), а у 5,2% пациентов в анамнезе было оперативное вмешательство на клапанах сердца [2]. Несмотря на более высокий риск тромбоэмболических осложнений и геморрагических событий в данной когорте больных, преимущества апиксабана над варфарином, выявленные для популяции в целом, сохранялись и у пациентов с клапанными проблемами. В исследовании RE-LY было отмечено, что пациенты с поражением клапанного аппарата сердца, включенные в исследование, в целом имели больший риск кровотечений (но не риск инсульта) вне зависимости от проводимой им антикоагулянтной терапии (две дозы дабигатрана против варфарина), а преимущества дабигатрана над варфарином в профилактике системных эмболий не зависели от наличия клапанных поражений [3]. Аналогичный анализ, проведенный по результатам исследования ROCKET-AF, показал сопоставимую эффективность в данной когорте пациентов ривароксабана и варфарина, однако у пациентов с клапанными поражениями сердца частота кровотечений и системных эмболий была выше на ривароксабане [4]. При этом европейские эксперты отмечают, что позиция их американских коллег более жесткая: в соответствии с американскими рекомендациями лечить пациентов с биологическими искусственными клапанами и после операций на клапанах ППОАК категорически не рекомендуется [5].
Если говорить о пациентах с ФП и механическими клапанами, то в свете результатов исследования RE-ALIGN (дабигатран против варфарина), в которое включались только такие пациенты (операция состоялась за неделю и менее до рандомизации в исследование), лечение ППОАК в течение 3–6 месяцев после операции не рекомендуются, т.к. дабигатран по конечным исходам достоверно уступает варфарину [6]. Аналогичных данных по ингибиторам Ха-фактора (ривароксабан и апиксабан) нет.
В связи с этим пациенты с механическими клапанами сердца рассматриваются как фокусная группа, которой противопоказано лечение ППОАК и им могут назначаться только антагонисты витамина К, т.е. в России это преимущественно варфарин. При этом рекомендации не отвечают на один практический вопрос, который задают практикующие врачи: а если у этих пациентов попытки достичь целевого диапазона МНО (международное нормализованное отношение) бесполезны или небезопасны? Их тогда оставлять вообще без антитромботической терапии или назначать антиагреганты «на всякий случай», но совершенно бездоказательно?
Мы приводим ниже клиническое наблюдение, в котором нам не удалось воспользоваться рекомендациями, поскольку под конкретную ситуацию ни одна из существующих рекомендаций не подходила.
Клинический случай
Пациентка Г. 87 лет поступила в тяжелом состоянии в отделение интенсивной терапии одной из городских больниц Москвы с жалобами на сильную слабость, головокружение и стул с примесью крови. Известно, что с детства страдает хронической ревматической болезнью сердца с постепенным формированием митрального стеноза, в 1979 г. была выполнена митральная комиссуротомия. С конца 1980-х гг. отмечалась постоянная форма ФП. Для профилактики тромбоэмболических осложнений в течение последних 20 лет принимала варфарин в стабильной дозе 5 мг/сут, не реже 1 раза в месяц контролировала МНО (показатель был либо в целевом диапазоне, либо ниже ожидаемого). Из сопутствующей терапии получала метопролол в дозе 75–100 мг/сут. Ухудшение состояния наступило 20 января 2015 г., когда без видимой причины отметила сильное кровотечение из прямой кишки и бригадой скорой медицинской помощи была госпитализирована в городскую клиническую больницу.
В стационаре пациентке была выполнена колоноскопия, на которой выявлен дивертикулез сигмовидной кишки с картиной состоявшегося кровотечения из одного из дивертикулов. Показаний к экстренному хирургическому вмешательству выявлено не было. Уровень гемоглобина при поступлении составил 4,9 г/дл, МНО – 4,6, клиренс креатинина – 49 мл/мин. Состояние было расценено как состоявшееся желудочно-кишечное кровотечение на фоне передозировки варфарина. На фоне отмены варфарина отмечена спонтанная остановка кровотечения без признаков его рецидивов. Из отделения интенсивной терапии пациентка была переведена в терапевтическое отделение для плановой коррекции постгеморрагической анемии. Пациентке проводилась парентеральная терапия препаратами железа, в качестве антикоагулянта применялся гепарин в дозе 5 тыс. ЕД 2 раза в сутки (подкожно).
К моменту выписки уровень гемоглобина составил 9,4 г/дл, пациентке было рекомендовано вновь вернуться к терапии варфарином, однако она сама и родственники категорически отказались от этой идеи с учетом последствий передозировки препарата, послужившей причиной данной госпитализации. Пациентка обратилась в кабинет контроля антикоагулянтной терапии УКБ № 1 Первого МГМУ им. И.М. Сеченова для решения вопроса об антикоагулянтной терапии.
Вероятность развития повторного кровотечения на фоне возвращения к терапии антагонистами витамина К, вне всяких сомнений, была большой. Кроме того, анемия, которая не входит в перечень факторов риска геморрагических событий по шкале HAS-BLED (Hypertension Abnormal renal/liver function, Stroke, Bleeding history or predisposition, Labile international normalized ratio, Elderly, Drugs/alcohol concomitantly), рассматривается как независимый фактор риска по другим шкалам, например ATRIA [7]. Но и даже по шкале HAS-BLED пациентка набирает 3 балла (возраст старше 75 лет, лабильное МНО, кровотечение), что позволяет включить ее в группу высокого риска повторных геморрагических событий. В отношении данного контингента пациентов рекомендуется рассматривать ППОАК как препарат выбора. Однако мы уже указывали выше на проблемы, связанные с назначением данной группы препаратов «не по показаниям».
У нашей пациентки отмечался митральная и аортальная регургитация I степени, небольшой митральный стеноз, умеренная недостаточность трикуспидального клапана при сохраненной (60%) фракции выброса левого желудочка. Также определялась легочная гипертензия (давление заклинивания легочной артерии – 40 мм рт.ст.). На фоне постоянной формы ФП отмечалось значительное расширение обоих предсердий. Обычным трансторакальным доступом тромбы в камерах сердца не определялись.
Отказ от антикоагулянтной терапии представлялся маловероятным: пациентка по шкале CHA2DS2-VASc имела 3 балла (2 – возраст старше 75 лет, 1 – женский пол), т.е. высокий риск системных тромбоэмболий. Возможность выбора в пользу ППОАК (за пределами официальных показаний) хотя и рассматривалась на том этапе, однако уровень гемоглобина (93 г/л) продолжал усиливать все возможные риски – и эмболий, и кровотечений.
По данным субанализа исследования RE-LY, 12% пациентов с ФП имели сниженный уровень гемоглобина.
В этой группе больных вне зависимости от вида антикоагулянтной терапии на 50% регистрировали общую смертность и инфаркт миокарда (отношение рисков [ОР]=1,50; 95% доверительный интервал [ДИ] – 1,32–1,71), первичная конечная точка исследования – инсульт или системная эмболия на 41% (ОР=1,41; 95% ДИ – 1,12–1,78), а также риск большого кровотечения – более чем в 2 раза (ОР=2,14; 95% ДИ – 1,87–2,46) [8]. Поэтому было принято решение продолжить восстановление уровня гемоглобина, а в качестве профилактики назначить подкожные инъекции эноксапарина, доза которого с учетом скорости клубочковой фильтрации и возраста пациентки составила 20 мг 1 раз в сутки (как для пациентки с почечной недостаточностью).
На фоне проведенной терапии через 3 месяца наблюдения у пациентки отмечено повышение уровня гемоглобина до 11,0 г/дл, рецидивов кровотечения не отмечалось, тромбоэмболических осложнений зарегистрировано не было. На этом этапе было принято решение перевести пациентку на ППОАК. Индивидуальный выбор ППОАК в зависимости от сопутствующих клинических характеристик основывается главным образом на ключевых исследованиях с антикоагулянтами.
Известная схема Lip GYH и соавт. [9] предписывает сделать выбор для пациента с высоким риском желудочно-кишечного кровотечения, а также для всех пациентов, имеющих 3 и более баллов по шкале HAS-BLED, в пользу апиксабана или сниженной (110 мг 2 раза в сутки) дозы дабигатрана. Ривароксабан в данной концепции не рассматривается, поскольку в ходе субанализа данных исследования ROCKET-AF было показано, что его применение пациентами с ФП приводило к достоверно большему (на 42%; ОР=1,42; 95% ДИ – 1,22–1,66) числу больших и клинически значимых малых желудочно-кишечных кровотечений по сравнению с терапией варфарином [10].
Исходя из нашего собственного алгоритма выбора ППОАК (Д.А. Напалков, А.А. Соколова, 2015), в котором мы добавляем еще и возраст пациента (старше 75 лет), лучшие конечные исходы наблюдали у пациентов на фоне терапии апиксабаном, преимущества которого над варфарином в геометрической прогрессии нарастают с увеличением возраста пациента [11]. Кроме того, вдохновляют данные, представленные в статье R. De Caterina и соавт. [12], по материалам субанализа исследования ARISTOTLE (апиксабан против варфарина), согласно которым преимущества апиксабана над варфарином сохранялись и у пациентов с ФП, имевших в анамнезе желудочно-кишечные кровотечения.
Пациентке была назначена терапия апиксабаном в сниженной дозе (с учетом возраста и функции почек) 2,5 мг 2 раза в сутки, которая продолжается уже более года. Рецидивов кровотечений и тромбоэмболических событий по настоящее время зарегистрировано не было. Уровень гемоглобина, по последним данным, составляет 12,5 г/дл. Клиренс креатинина по формуле Кокрофта–Голта – 30 мл/мин, по CKD-EPI – 41 мл/мин/1,73 м2. Пациентка чувствует себя удовлетворительно.
Заключение
Мы приводим данный клинический случай не для того, чтобы начать в рутинном порядке пересматривать клинические рекомендации и назначать антикоагулянты не по показаниям. К сожалению, ряд пациентов «не вписываются» в существующие стандартизированные подходы к лечению и приходится прибегать к собственному экспертному мнению (и литературным данным), чтобы выйти из сложного положения, как в данном клиническом наблюдении: при сочетании очень высоких рисков и тромбоэмболических, и геморрагических событий. На единичных описаниях клинических наблюдений невозможно выстроить стратегию, поэтому мы призываем наших коллег публиковать подобные описания с тем, чтобы доказательная кардиология не упералась в тупик «нерешаемых вопросов», а персонализированная медицина, основываясь на доказательствах, позволяла находить решение сложных проблем в неоднозначных клинических ситуациях с пользой для пациентов.


