Впоследние годы актуальность разработки действенных методов профилактики тромбозов стентов возрастает в связи с широкой распространенностью и высокой эффективностью малоинвазивных коронарных вмешательств, в т.ч. коронарного стентирования (КС), при различных формах ишемической болезни сердца (ИБС). Совершенствование техники имплантации стентов и введение режима двойной антиагрегационной терапии значительно снизили частоту этого осложнения: c 16±0,4 до 2,8±1,2% [1, 2].
Двойная антитромбоцитарная терапия (ДАТТ), включающая ацетилсалициловую кислоту (АСК) в комбинации с ингибиторами рецепторов P2Y12 (клопидогрел, прасугрел или тикагрелор), – эффективный метод лечения больных как острым коронарным синдромом (ОКС), так и стабильной ИБС, подвергаемых плановым чрескожным коронарным вмешательствам. Выбор второго антиагреганта определяется степенью доказанности в конкретной клинической ситуации, что отражено в современных клинических рекомендациях [3–7].
Согласно существующим рекомендациям, применение ДАТТ (АСК+ингибитор рецепторов P2Y12) является важным аспектом в профилактике тромбозов стентов. Рекомендованная длительность такого лечения составляет до 12 месяцев после имплантации стента при различных формах ОКС.
Однако результаты нового международного рандомизированного контролируемого клинического испытания DAPT [8] продемонстрировали определенные преимущества более длительной ДАТТ. В исследовании были проанализированы данные более 20 тыс. пациентов с ИБС и КС с лекарственным покрытием, предназначенным для профилактики рестенозов. На протяжении первых 12 месяцев после КС все участники принимали АСК и тиенопиридин (65% пациентов – клопидогрел; 35% – прасугрел). После первых 12 месяцев пациентов, у которых не регистрировали тяжелых кардиоваскулярных событий или кровотечений, распределили в две группы: получавшие АСК+ингибитор рецепторов P2Y12 или АСК+плацебо. Этот курс лечения составил 18 месяцев.
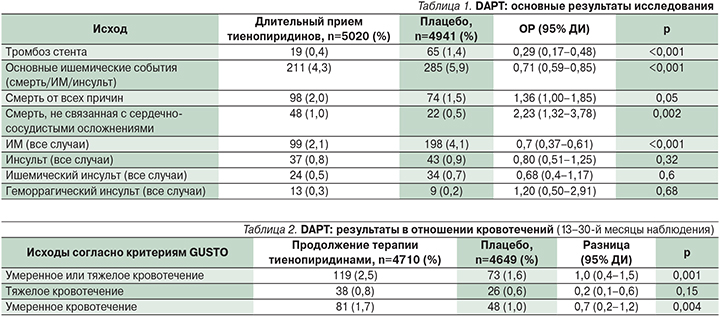
В ходе проведения исследования дополнительное применение ингибитора рецепторов P2Y12 с 13-го по 30-й месяц значительно снизило вероятность возникновения тромбоза стента: инцидентность в группах тиенопиридина и плацебо составила 0,4 и 1,4% соответственно, относительный риск (ОР) – 0,29; 95% доверительный интервал (ДИ) – 0,7–0,48; p<0,001 (табл. 1).
В группе ингибитора рецепторов P2Y12 по сравнению с плацебо достоверно реже отмечены сердечно-сосудистые и цереброваскулярные осложнения в целом (смерть/ИМ/инсульт) – 4,3 и 5,9% соответственно (ОР – 0,71; 95% ДИ – 0,59–0,85; p<0,001), инфаркт миокарда (ИМ) – 2,1 и 4,1% соответственно (ОР – 0,47; 95% ДИ – 0,37–0,61; p<0,001), а также случаи ИМ, которые не были непосредственно связаны с тромбозом стента, – 1,8 и 2,9% соответственно (ОР – 0,59; p<0,001). Между группами не было выявлено достоверных различий в отношении случаев сердечно-сосудистой смерти и инсультов.
Более длительный прием ДАТТ ассоциировался с повышением частоты геморрагических событий, однако частота массивных и/или фатальных кровотечений различалась между группами недостоверно (табл. 2). Частота возникновения умеренных и тяжелых кровотечений (согласно критериям GUSTO) в группе тиенопиридина была достоверно выше, чем в группе плацебо, – 2,5 и 1,6% соответственно (ОР – 1,61; 95% ДИ – 1,21–2,16; p=0,001).
В процессе наблюдения с 13-го по 30-й месяц частота смерти от всех причин составила 2% в группе продолжения терапии тиенопиридином и 1,5% в группе плацебо (ОР – 1,36; 95% ДИ – 1,00–1,85; p=0,05), что стало неожиданным фактом; эти данные исследователи связывали с возможным неодинаковым распределением между группами пациентов с онкологическим заболеванием в анамнезе.
В подтверждение этой гипотезы результаты мета-анализа 14 рандомизированных контролируемых исследований [9] с включением 69 644 пациентов не выявили достоверного повышения риска кардиоваскулярной (ОР – 1,01; р=0,81) и некардиоваскулярной (ОР – 1,04; р=0,66) смертности, смертности от всех причин (ОР – 1,05; 95% ДИ – 0,96–1,19; p=0,33) при ДАТТ длительностью более 12 месяцев по сравнению с более короткой продолжительностью ДАТТ или приемом одного аспирина.
В целом в исследовании DAPT общая смертность в группе тиенопиридина была выше, чем в группе плацебо (2,3 и 1,8%), но различия были на границе статистической значимости (ОР – 1,36; р=0,04). В группе тиенопиридина регистрировали больше летальных исходов, связанных с кровотечениями (11 против 3; p=0,06), фатальной травмой (7 против 2; p=0,07) и раком (31 против 14; p=0,02). Таким образом, некардиоваскулярная смертность в группе тиенопиридина и плацебо составила соответственно 1,1 и 0,6% (ОР – 1,80; p=0,01).
Следует учитывать, что увеличение числа ишемических событий было наиболее выражено в первые 3 месяца после прекращения применения тиенопиридинов независимо от длительности приема, что свидетельствует о возможной целесообразности более длительной терапии, особенно для пациентов с высоким риском сердечно-сосудистых осложнений.
Был проведен анализ результатов отдельной группы участников исследования DAPT – пациентов, которым был установлен стент с паклитакселем Taxus, получавших прасугрел. Данный анализ был представлен как отдельное исследование TL-PAS. Оказалось, что в данной группе пациентов отмечено более выраженное снижение частоты ишемических событий при более длительном приеме ДАТТ (ОР – 0,41; p<0,001), а также более выраженный рост числа событий при отмене тиенопиридина.
Таким образом, применение ДАТТ более года, с одной стороны, снижает риск возникновения тромбоза стента и сердечно-сосудистых осложнений, с другой – ассоциируется с повышенным риском кровотечений.
В противоположность полученным в DAPT данным, результаты нескольких проведенных ранее исследований обосновали наметившиеся тенденции к уменьшению длительности назначения ДАТТ после имплантации стентов с покрытием лекарственным препаратом с 12-го по 6-й и даже 3-й месяцы.
В исследовании PRODIGY [10–14] 2 года ДАТТ после КС были не более эффективными, чем 6 месяцев лечения, в отношении ишемических осложнений, но при этом удвоилось число случаев массивных кровотечений (при исследовании продленной ДАТТ после стент-индуцированной гиперплазии интимы). Эти результаты позволили Марко Вальгимигли сделать следующее заявление: «Так как мы не можем исключить возможность того, что преимущества длительной терапии с применением клопидогрела на протяжении нескольких месяцев после КС могут быть меньше, чем ожидалось, то в нашем исследовании четко отражено, что отношение выгоды длительной терапии к риску было переоценено» [15].
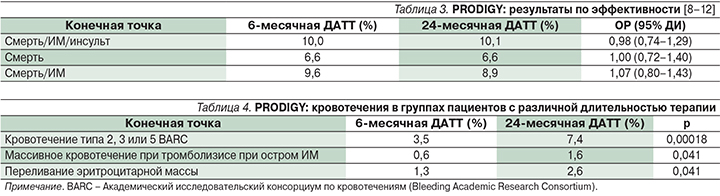
Всего в исследование были включены 2013 пациентов: из них 74% – с ОКС и 26% – со стабильной стенокардией, которые перенесли КС и были рандомизированы для применения ДАТТ (клопидогрел+АСК на протяжении 6 и 24 месяцев). Первичной конечной точкой были общая смертность, повторный ИМ или инсульт в течение 2 лет. Общий риск первичной конечной точки был почти идентичным для обеих групп (табл. 3). При анализе ишемических событий в группах, в которых использовались разные типы стентов, различий не наблюдалось.
Существовали значимые различия между двумя группами с разной длительностью ДАТТ по числу пациентов с кровотечениями (табл. 4).
Cреди ограничений исследования PRODIGY следует отметить его открытое проведение, а также относительно небольшое число включенных пациентов. К достоинствам исследования можно отнести отсутствие спонсорской поддержки со стороны промышленности, вовлечение всех пациентов, желающих пройти лечение с использованием стентов (в т.ч. с ОКС и подъемом сегмента ST), использование непокрытых металлических стентов, а также высокий уровень приверженности лечению. Если в результате предыдущих исследований (PCI-CURE и CREDO) уже было установлено, что терапия с использованием клопидогрела продолжительностью до года является лучшим решением, нежели одномесячное КС с использованием непокрытого стента, то в исследовании PRODIGY проведено сравнение лечения пациентов длительностью от шести месяцев до двух лет с использованием непокрытого металлического стента и стента с лекарственным покрытием.
В двух других исследованиях, REAL-LATE и EXCELLENT, получены сходные с PRODIGY результаты, которые также не выявили преимуществ от длительной ДАТТ [15]. Таким образом, в трех исследованиях были получены схожие результаты: длительная ДАТТ (до двух лет) не обнаружила клинических преимуществ в отношении сердечно-сосудистых осложнений, при этом четко отмечались признаки повышенной частоты кровотечений.
В исследованиях ISAR-SAFE и ITALIC также не было выявлено достоверных различий частоты ишемических и геморрагических событий между группами ДАТТ в течение 6 месяцев и дольше. Ограничением для обоих исследований стало следующее обстоятельство: они были прекращены досрочно в связи с проблемами набора пациентов и низким уровнем регистрируемых событий, однако авторы в обоих случаях сделали вывод, согласно которому 6-месячный прием ДАТТ не уступает более длительной терапии, особенно для пациентов с низким риском сердечно-сосудистых осложнений и наличием факторов риска кровотечений.
В исследовании ISAR-SAFE пациентов рандомизировали в группы 6- и 12-месячной терапии клопидогрелом после имплантации стента с покрытием лекарственным препаратом. По результатам исследования не было выявлено различий между группами в достижении комбинированной первичной конечной точки – смерть/ИМ/тромбоз стента/массивные кровотечения, либо в частоте ишемических и геморрагических событий по отдельности.
В исследование ITALIC были включены пациенты с имплантированным стентом с покрытием лекарственным препаратом, рандомизированные в группы ДАТТ на протяжении 6 или 24 месяцев. Было выявлено отсутствие достоверной разницы между группами в отношении комбинированной точки, включившей смерть, ИМ, ургентную реваскуляризацию целевого сосуда, инсульт и массивное кровотечение в течение 12 месяцев после КС, даже у пациентов высокого риска после перенесенного ОКС.
В обзоре Т. Palmerini и соавт. [16] сравнивали результаты краткосрочной (<6>1 года) ДАТТ после имплантации стентов с лекарственным покрытием. Анализировали результаты 4 исследований, включивших 8180 пациентов, учли такие клинические исходы, как сердечная смерть, ИМ и определенный/возможный тромбоз стента. Краткосрочная ДАТТ по сравнению с долгосрочной характеризовалась аналогичным уровнем сердечно-сосудистых осложнений (ОР – 1,11; 95% ДИ – 0,86–1,43, p=0,44), но статистически значимо низким уровнем кровотечений (ОР – 0,66; 95% ДИ – 0,46–0,94; p=0,03).
В недавнем исследовании OPTIDUAL [17], включившем 1385 пациентов после имплантации стентов с лекарственным покрытием, продолжение ДАТТ клопидогрелом и АСК до 48 месяцев не показало преимуществ по сравнению с проведением терапии на протяжении 12 месяцев в отношении развития сердечно-сосудистых осложнений. Первичная конечная точка была комбинированной и включала сердечно-сосудистые осложнения и показатели безопасности: случаи смерти, ИМ, инсульта, крупных кровотечений. В отношении развития первичной конечной точки между группами с длительной (48 месяцев) ДАТТ и ДАТТ в течение 12 месяцев достоверной статистической разницы выявлено не было: 5,8 против 7,5% (ОР – 0,75; 95% ДИ – 0,5–1,28; p=0,17). Статистический анализ отдельных компонентов первичной конечной точки показал схожие результаты: смерть: ОР – 0,65 (95% ДИ – 0,34–1,22; p=0.18); ИМ: ОР – 0,67 (95% ДИ – 0,31–1,44; p=0,31); инсульт: ОР – 0,9 (95% ДИ – 0,22–2,18; p 0,53); крупные кровотечения: ОР – 0,98 (95% ДИ – 0,47–2,05; p=0,95).
Однако анализ post-hoc продемонстрировал на границе статистической значимости тенденцию снижения сердечно-сосудистых осложнений (смерть, ИМ, инсульт) в группе ДАТТ 48 месяцев по сравнению с группой ДАТТ 12 месяцев: 4,2 против 6,4% (ОР – 0,64; 95% ДИ – 0,4–1,02; p=0,06), при этом с увеличением длительности ДАТТ не отмечено увеличения частоты крупных кровотечений (соответственно 2 против 2%; p=0,95) или смертности от всех причин.
Таким образом, результаты исследования OPTIDUAL согласуются с таковыми исследования DAPT в отношении развития сердечно-сосудистых осложнений у пациентов после имплантации стентов с лекарственным покрытием.
В исследовании PEGASUS-TIMI 54 [18] были рандомизированы 21 162 пациента с ОКС, разделенных на группы, принимавших тикагрелор 90 мг дважды в день, 60 мг дважды в день, и группу плацебо. Продолжительность наблюдения в среднем составила 33 месяца, продемонстрировано достоверное снижение таких сердечно-сосудистых осложнений, как сердечно-сосудистая смерть, ИМ или инсульт, на терапии тикагрелором 90 мг 2 раза в день по сравнению с плацебо (ОР – 0,85; 95% ДИ – 0,75–0,96; p<0,008) и на терапии тикагрелором 60 мг 2 раза в день по сравнению с плацебо (ОР – 0,84; 95% ДИ – 0,74–0.95; p<0,004). При этом отмечено достоверное увеличение частоты крупных кровотечений – 2,6% на терапии тикагрелором 90 мг 2 раза в день, 2,3% на терапии тикагрелором 60 мг 2 раза в день – по сравнению с плацебо – 1,06% (p<0,001). Смертность от всех причин в группах достоверно не различалась.
Заключение
Попытка сформулировать единую рекомендацию по длительности применения ДАТТ представляет большую сложность, поскольку результаты исследований различаются.
Вопрос о длительности ДАТТ определяется двумя основными задачами: защитой пациента от тромбоза стента и вторичной профилактикой сердечно-сосудистых осложнений в рамках существующей ИБС.
В отношении предотвращения тромбоза стента данные свидетельствуют о том, что ДАТТ на протяжении 6 месяцев безопасна в плане геморрагических осложнений, особенно для пациентов низкого риска ишемических осложнений с установленным современным стентом. При наличии у пациента более высокого ишемического риска более полезной может быть длительная ДАТТ, возможно даже на протяжении всей жизни, что подтверждают данные более ранних исследований – CREDO и TRILOGY ACS. Аналогичным образом большая часть преимуществ длительной ДАТТ, выявленных в исследовании DAPT, связана со снижением частоты ишемических событий, не ассоциированных с тромбозом стента, и это свидетельствует о том, что полученные результаты отражают в основном эффект в отношении вторичной профилактики. Европейские исследования ISAR-SAFE и ITALIC главной целью ставили изучение проблемы предотвращения событий, связанных с тромбозом стента у пациентов низкого риска. Эти работы, равно как и ранее проведенные исследования, продемонстрировали, что можно безопасно отменять ДАТТ после 6 месяцев приема, если у пациента есть факторы риска кровотечения.
Следует учитывать и другой факт: польза пролонгированной ДАТТ может зависеть от типа имплантированного стента. По результатам исследования DAPT было выявлено, что преимущество длительной ДАТТ в плане снижения частоты основных неблагоприятных кардио- и цереброваскулярных событий максимально для пациентов, которым были установлены стенты с паклитакселем (ОР – 0,52), а минимально – для пациентов, которым были установлены стенты с эверолимусом (ОР – 0,89; p=0,05). Бурное развитие и усовершенствование технологии производства стентов позволяет надеяться на прогресс в этой важной области кардиологии.
Таким образом, наиболее безопасная и наиболее эффективная длительность приема ДАТТ остается неопределенной и должна рассматриваться индивидуально для каждого пациента. В каждом отдельном случае нужно оценивать и подбирать длительность ДАТТ, исходя из наличия факторов, способствующих атеротромбозу, при одновременном учете риска кровотечений и типа имплантированного стента.


