Причинами крупа (стенозирующего ларинготрахеита – СЛТ) чаще всего являются вирусы гриппа А, парагриппа 1-го, 2-го и 3-го типов, PC- и аденовирусная инфекции, бактерии. Было показано, что клиника острого ларинготрахеита зависит от соотношений вирусов и бактериальной флоры в развитии данного синдрома. В 36 % случаев синдром ларинготрахеита рассматривается как проявление вирусной инфекции в чистом виде. При этом изменения слизистой оболочки дыхательных путей носят поверхностный характер и к 20-му дню полностью исчезают [1, 2].
Круп развивается в результате отека гортани ниже голосовой щели; отек вторичен по отношению к инфекции, обычно вирусной. Воспаление трахеобронхиального дерева вызывает увеличение секреции слизистых желез и отек слизистых оболочек. Поскольку диаметр дыхательных путей у детей грудного и раннего возраста небольшой, даже незначительное набухание слизистой оболочки приводит к выраженному уменьшению поперечного сечения дыхательных путей и возрастания сопротивления воздушному потоку. Наименьший диаметр дыхательных путей у грудного ребенка определяется на уровне перстневидного хряща. Поскольку последний локализуется вне полости грудной клетки, его просвет сужается еще больше во время вдоха; как правило, это выражается в инспираторном стридоре. Отек голосовых связок проявляется в дисфонии (охриплости голоса). В результате избыточного накопления слизи и уменьшения диаметра дыхательных путей возрастает сопротивление току воздуха и увеличивается интенсивность дыхания. Это проявляется ретракцией, тахипноэ и включением в процесс дыхания дополнительных групп мышц. При прогрессировании обструкции возможно нарушение газообмена с последующим развитием гипоксемии, цианоза и накоплением углекислого газа. Это поздние признаки крупа, которые могут быть предвестником полной непроходимости дыхательных путей и остановки дыхания [1–4].
При остром стенотическом ларинготрахеите возникают отечно-воспалительные изменения в подскладочном пространстве, что объясняется его узостью и наличием обильного слоя рыхлой, богато васкуляризированной соединительной ткани, окруженной плотным кольцом перстневидного хряща. Стеноз обычно развивается у детей в возрасте 1–6 лет, потому что у них подскладочное пространство относительно уже, подслизистый слой более выражен, имеется склонность к аллергическим реакциям и повышенной секреции слизи. Однако обструкция может как спускаться ниже, так и подниматься выше. При крупе нередко наблюдается заболевание нижних дыхательных путей и смежных областей вследствие вторичного распространения вирусной инфекции. В результате скопления слизи может произойти закупорка дистальных отделов дыхательных путей, что приводит к пневмонии или образованию ателектазов, может развиться отек легких [1, 2, 5].
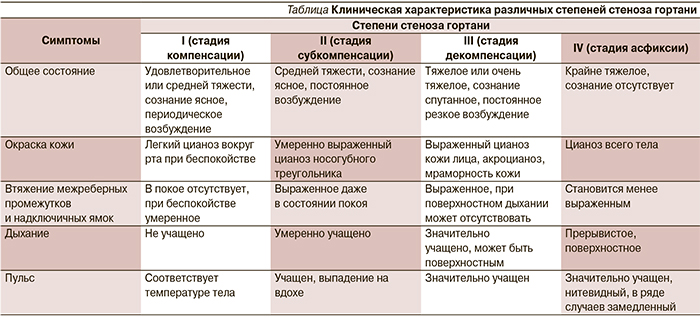
У детей с крупом чаще всего отмечается повышенная температура тела без явлений интоксикации, имеются симптомы инфекции верхних дыхательных путей. При обследовании наибольшее значение имеют следующие признаки: степень обструкции воздухоносных путей, включая стридор, межреберную ретракцию, раздувание крыльев носа, интенсивность поступления воздуха; окраска кожных покровов и степень сохранения сознания. В результате наслоения бактериальной инфекции, особенно стафилококка, возникают более грубые и глубокие поражения слизистой оболочки гортани и трахеи, проявляющиеся более тяжелой клинической картиной: стеноз гортани (см.таблицу) может держаться до 7–10 дней, течение его принимает волнообразный характер. Наслоение бактериальной инфекции на острую респираторную вирусную инфекцию (ОРВИ) может произойти в самые ранние сроки заболевания. При этом помимо поражения гортани и трахеи характерно появление других бактериальных осложнений [4, 5]. Дифференциальный диагноз проводится по основному симптому острого ларинготрахеита, стенотическому дыханию. В первую очередь нужно исключить такие заболевания, как дифтерия, инородное тело гортани, заглоточный абсцесс, ларингоспазм. В ряде случаев необходимо провести дифференциальный диагноз между синдромом ларинготрахеита и бронхиальной астмой. СЛТ наблюдается главным образом у детей в возрасте 1–6 лет, возникает на 1–2-е сутки ОРВИ. Экстренность ситуации обусловлена рано развивающейся декомпенсацией, к которой предрасполагают рыхлая клетчатка подсвязочного пространства гортани, склонность детей к ларингоспазму. У ребенка появляется кашель, чаще лающий, вдох затрудняется, дыхание становится шумным с участием вспомогательной мускулатуры, отмечается тахипноэ [6].
Анатомо-физиологические особенности детской гортани и трахеи:
- малый диаметр, мягкость и податливость хрящевого скелета;
- короткое узкое преддверие и воронкообразная форма гортани;
- высокорасположенные и непропорционально короткие голосовые складки;
- гипервозбудимость мышц-аддукторов, замыкающих голосовую щель;
- функциональная незрелость рефлексогенных зон и гиперпарасимпатикотония [2];
- в слизистой оболочке и подслизистой основе обилие лимфоидной ткани с большим количеством тучных клеток, сосудов и со слабым развитием эластических волокон.
К неблагоприятным фоновым факторам относятся аномалии конституции (экссудативно-катаральный и лимфатико-гипопластический диатезы); лекарственная аллергия; врожденный стридор; паратрофия; родовая травма, роды путем кесарева сечения; поствакцинальный период; сенсибилизация предшествующими частыми ОРВИ.
Основные механизмы развития крупа:
Воспалительный и аллергический отек с клеточной инфильтрацией слизистой оболочки гортани (подскладочное пространство) и трахеи.
Рефлекторный спазм мышц гортани.
Гиперсекреция слизистых желез, скопление в области голосовой щели густой мокроты, корок, фибринозных или некротических наложений.
В Международной медицинской практике для оценки тяжести крупа используется шкала Уэстли [7, 8]. Элементы оценочной шкалы Уэстли учитывают основные характеристики физических параметров. Каждому элементу присваивается оценка в баллах, как показано ниже:
Уровень сознания: нормальный, в т. ч. сон = 0; дезориентированный = 5.
Цианоз: нет = 0, при волнении = 4; в покое = 5.
Одышка: нет = 0, при волнении = 1; в покое = 2.
Проходимость воздуха: нормальная = 0, снижена = 1; заметно снижена = 2.
Западение уступчивых мест грудной клетки: нет = 0; легкое = 1, умеренное = 2, выраженное = 3.
Суммарная оценка колеблется от 0 до 17 баллов:
Легкий круп определяется при сумме баллов Уэстли ≤ 2. Как правило, эти дети имеют лающий кашель, хриплый плач, но не имеют одышки в покое. Дети с легким крупом могут иметь одышку, когда расстроены и плачут, и либо не имеют совсем, либо имеют еле заметное западение уступчивых мест грудной клетки
Средняя тяжесть крупа определяется при сумме баллов Уэстли от 3 до 7. Дети с умеренным крупом имеют одышку в покое, минимум умеренное западение уступчивых мест грудной клетки (ретракцию), возможно, другие симптомы или признаки дыхательной недостаточности, невыраженное или слабовыраженное возбуждение, одышку в покое. Дети с умеренным крупом должны быть госпитализированы в стационар.
Тяжелый круп определяется при сумме баллов Уэстли ≥ 8. Дети с тяжелым крупом имеют выраженную одышку в покое, хотя одышка может снижаться при прогрессировании обструкции верхних дыхательных путей и снижении проведения воздуха. Западения уступчивых мест выражены (в т.ч. втяжение грудины), ребенок имеет тревожный, возбужденный или утомленный вид. Быстрая диагностика и немедленное начало лечения детей с тяжелыми формами крупа имеют первостепенное значение. Детей с тяжелым крупом следует госпитализировать в отделение реанимации. Такие дети требуют агрессивной терапии, мониторинга и поддерживающего лечения [9].
Круп иногда приводит к значительной обструкции верхних дыхательных путей с нарастающей дыхательной недостаточностью, узнаваемой по следующим признакам:
- заторможенность и вялость;
- отмечается ретракция (хотя она может снизиться при прогрессировании обструкции и снижении проходимости воздуха);
- снижение или отсутствие дыхательных шумов;
- подавленный уровень сознания;
- чрезмерная тахикардия, непропорциональная лихорадке;
- цианоз или бледность.
Наиболее частым и не зависящим от степени стеноза гортани осложнением ОСЛТ является обструктивный бронхит. При декомпенсированном (3-я степень) стенозе часто развиваются гнойный ларинготрахеобронхит (треть пациентов) и пневмония. Возможны также бактериальные отиты, синуситы, лакунарная ангина, гнойный конъюнктивит, гнойный менингит. Присоединение пневмонии является ведущей причиной смерти при вирусном крупе [9, 10].
Диагноз основывается на наличии характерной триады симптомов (изменение голоса, лающий кашель, грубое дыхание), а также на других проявлениях ОРВИ.
Учитываются данные анамнеза, лабораторных и инструментальных (прямая ларингоскопия и др.) методов исследования. Ларингоскопическая картина при СЛТ характеризуется образованием валиков под голосовыми складками и наличием слизисто-гнойного отделяемого в трахеобронхиальном дереве. Некоторые авторы кроме отечной формы СЛТ выделяют гнойную, фибринозную, некротическую и др. [8–11]. Вслед за обструкцией на уровне гортани происходит нарушение дренажной функции трахеобронхиального дерева, следствием чего является возникновение воспалительных явлений в нижних отделах дыхательных путей, включая легочную ткань.
В необходимых случаях проводится вирусологическая диагностика.
Обязательно бактериологическое исследование выходного материала (слизь из ротоглотки, носа) для исключения дифтерии. При подозрении на дифтерийный круп (у непривитых или неправильно привитых против дифтерии больных с явлениями ОСЛТ; ребенок из очага дифтерии; сочетание стеноза гортани с ангиной и отеком подкожной клетчатки шеи) показана бактериоскопия мазков, взятых из мест поражения [8, 11, 12].
Терапия ОСЛТ направлена на подавление основных механизмов, формирующих патофизиологические сдвиги и клинические проявления обструкции верхних дыхательных путей.
На ранних стадиях острого ОСЛТ у детей, как правило, преобладают явления эксудации, легко исчезающие при использовании ингаляционных (ИГКС) и системных глюкокортикостероидов. Патогенетически обосновано использование кортикостероидов (оказывают противовоспалительное действие, вызывают снижение проницаемости капилляров, уменьшение отека гортани и экссудации). Кроме того, доказано, что заболевание протекает более тяжело и склонно к рецидивированию у пациентов с недостаточностью глюкокортикоидной функции коры надпочечников [13, 14].
Ингаляционная терапия является оптимальным способом доставки лекарственных средств в дыхательные пути. Это обусловлено быстрым поступлением вещества непосредственно в бронхиальное дерево, его высокой местной активностью, снижением частоты и выраженности системных побочных эффектов. К преимуществам ингаляционной терапии с помощью небулайзеров относятся легкость выполнения ингаляции (в т. ч. и у детей первых месяцев жизни), возможность доставки более высокой дозы препарата и обеспечение его проникновения даже в плохо вентилируемые участки дыхательных путей. При этом к детям раннего возраста необходимо применять маску соответствующего размера. Особенность аэрозольных ингаляций при ОСЛТ состоит в том, что требуется крупнодисперсный (точнее мелкокапельный) аэрозоль, оседающий в самых верхних дыхательных путях [15].
Данные литературы и результаты собственных клинических наблюдений свидетельствуют, что применение современных ИГКС служит высокоэффективным и безопасным методом терапии при крупе тяжелого течения.
В настоящее время в качестве базисной ингаляционной терапии, ориентированной на локальный противовоспалительный эффект, широко используются будесонид суспензии в дозе 2 мг однократно. Будесонид – ИГКС с выраженным местным противовоспалительным действием, препарат оказывает также противоаллергическое и антиэкссудативное действия, эффективно уменьшая обструкцию и гиперреактивность дыхательных путей. Будесонид обладает высоким сродством к ГКС-рецепторам и высокой местной противовоспалительной активностью [8, 16]. Для препарата Пульмикорт суспензия (будесонид) характерно быстрое начало противовоспалительного действия – уже в течение первого часа, а максимальное улучшение наблюдается через 3–6 часов. Системная биодоступность препарата составляет лишь 10–15 %, что практически исключает возможность развития системных побочных эффектов и обеспечивает его высокую безопасность даже для детей первых лет жизни. Клиренс небулизированного Пульмикорта на 1 кг массы тела у детей дошкольного возраста почти на 50 % выше, чем у взрослых. Это означает, что дошкольникам Пульмикорт суспензию можно вводить ингаляционно в тех же дозах, что и взрослым, без увеличения риска системных нежелательных эффектов [17].
Преимущества кортикостероидов и L-адреналина для ингаляций при среднетяжелом и тяжелом крупе были продемонстрированы в мета-анализе и рандомизированных клинических испытаниях соответственно. Для детей с крупом тяжелой степени рекомендованы ингаляции L-адреналина, который дозируется по 0,15 мл/кг за 1 дозу (не более 5 мл) 1 : 1000 разведения. Он ингалируется через небулайзер не более 15 минут. Введение адреналина ингаляционно можно повторять каждые 15–20 минут. Введение трех или более доз в течение 2–3-часового периода требует немедленной установки зажимов кардиомонитора, если это не было сделано ранее [17–19, 23].
Всем детям независимо от тяжести крупа с целью профилактики рецидива рекомендуется прием дексаметазона (0,2–0,6 мг/кг, максимально – 10 мг), наименее инвазивным способом: перорально, если это возможно; внутривенно, если внутривенный доступ налажен; внутримышечно, если пероральный прием невозможен и внутривенного доступа установлено не было. Пероральный дексаметазон (1 мг/мл) имеет неприятный вкус. Внутривенный препарат более концентрированный (4 мг/мл), и его можно давать внутрь, смешав с любым вкусным сиропом [20]. В случае сохранения симптомов стеноза гортани II степени и выше используется повторное введение в той же дозе. Лечебный эффект от введения стероидов наступает спустя 15–45 минут и длится 4–8 часов. При возобновлении симптомов необходимо их повторное введение [21]. Ввиду того что явления СЛТ могут сохраняться до 5–7 дней, стероидная терапия может быть продолжена на протяжении нескольких дней, однако со второго дня дозу кортикостероидов снижают до 3–4 мг/кг в сутки [20–22].
Традиционно принято считать эффективным увлажнение воздуха (эффект «тропической атмосферы») в помещении. Однако в рандомизированном исследовании G.M. Neto и соавт. (2002) было показано, что увлажнение воздуха в помещении не влияет на улучшение клинических симптомов среднетяжелого крупа, сроки госпитализации [24].
Анализируя фармакотерапию крупа, следует подчеркнуть, что с позиций доказательной медицины эффективность антигистаминных препаратов, бронхолитиков и спазмолитиков не доказана. При этом в лечении ложного крупа у детей существует высокий уровень доказательства клинической эффективности ГКС (уровень А (I): мета-анализ K. Russell и соавт., 2004) [25].
Седативную терапию назначают с целью нивелирования негативных психоэмоциональных реакций ребенка, связанных как с заболеванием, так и с лечебными воздействиями. Эти препараты снижают также интенсивность обменных процессов в нервной ткани, уменьшают потребность нервных клеток в кислороде с повышением устойчивости организма к гипоксии.
Отрицательные моменты применения этих препаратов сводятся к следующему:
Расслаблению и уменьшению сократительной активности скелетной (в т. ч. дыхательной) мускулатуры.
Подавлению кашлевого рефлекса.
Угнетению дыхательного центра.
Поэтому их применение оправданно в условиях стационара, т.к. требует постоянного наблюдения за пациентом, периодической стимуляции кашля, эвакуации слизи и мокроты из верхних дыхательных путей [3, 8].
С целью разжижения и удаления мокроты из дыхательных путей назначают отхаркивающие и мукорегуляторные препараты, вводимые преимущественно ингаляционным способом.
В случае отсутствия эффекта от проводимой терапии крупа 2-й степени на протяжении 48 часов, прогрессировании стеноза II степени и крупа 3-й степени обязательна назотрахеальная интубация термопластической трубкой значительно меньшего диаметра, чем нужно ребенку по возрасту [3, 5, 8, 9, 12]. Эндотрахеальная интубация требуется менее чем 1 % пациентов, обращающихся за неотложной помощью, и от 2 до 6 % госпитализированных детей. Необходимость в интубации следует ожидать среди детей с прогрессирующей дыхательной недостаточностью, процедура должна быть выполнена с минимально возможным препятствием дыханию. Трахеальная трубка требуется на 0,5–1,0 мм меньше, чем обычно используемый размер [5, 9].
Дезинтоксикационная терапия проводится по показаниям и под строгим контролем диуреза. Общий объем инфузии рассчитывают, исходя из 30–50 мл на 1 кг массы тела в сутки. При этом необходимо учитывать наличие общетоксических проявлений и степень их выраженности.
Эффективность антибактериальной терапии при вирусном ложном крупе не доказана. Назначение антибиотиков оправданно лишь при крупе, осложненном бактериальной инфекцией. Интубация и трахеостомия осуществляются при неэффективности консервативной терапии и проведении реанимационных мероприятий [8].
При своевременной диагностике и адекватной терапии на догоспитальном этапе прогноз заболевания благоприятен.



