Сегодня в России сахарным диабетом (СД) страдают более 3,1 млн человек, из которых подавляющее большинство (2,8 млн) составляют больные СД типа 2 (СД2). Увеличение числа больных СД2 наблюдается во всех странах мира, ассоциируется с ростом распространенности ожирения и метаболического синдрома [2, 3].
Внедрение новых классов лекарственных препаратов в клиническую практику врачей-эндокринологов позволяет расширять возможности медикаментозного лечения в сравнении с традиционными подходами. В связи с этим необходимо иметь представление об эффективности и безопасности новых методов лечения, понять их место в терапии СД.
В первую очередь речь идет об ингибиторах дипептидилпептидазы-4 (ДПП-4), которые около 2 лет назад стали применяться в клинической практике. Механизм действия этих препаратов основан на повышении активности инкретиновых гормонов путем блокирования фермента ДПП-4. В результате активность основных инкретинов, таких как глюкагоноподобный пептид-1 (ГПП-1) и глюкозозависимый инсулинотропный полипептид (ГИП), продлевается. Это улучшает функцию островковых α- и β-клеток поджелудочной железы. Таким образом, основное действие ингибиторов ДПП-4 сводится к мобилизации внутренних резервов организма. Инкретины, секретирующиеся в кишечнике, отвечают за 60–70 % инсулиновой секреции, поэтому ингибиторы ДПП-4 можно рассматривать в качестве примера физиологического подхода к терапии СД2: восстановление и коррекция собственных ресурсов организма для регуляции углеводного обмена. Кроме того, препараты этой группы могут продлевать жизнь β-клеток, замедлять их апоптоз, т. е. влиять на основное звено прогрессирования СД2 – гибель β-клеток поджелудочной железы. Действие ингибиторов ДПП-4 проявляется только в ответ на повышение уровня сахара в крови (глюкозозависимый механизм действия), поэтому риск развития гипогликемии при их применении минимален. Ингибиторы ДПП-4 улучшают функцию островковых клеток поджелудочной железы, их чувствительность и ответ в соответствии с уровнем гликемии [19]. Препараты нейтральны в отношении повышения массы тела. Следует отметить их хорошую переносимость и сходную эффективность в сравнении с другими классами пероральных сахароснижающих препаратов (ПССП) [36, 37, 40].
В настоящее время основными принципами терапии СД2 являются: изменение диеты, направленное на нормализацию массы тела; регулярная физическая активность с учетом общего состояния пациента; назначение на раннем этапе заболевания ПССП с учетом сердечно-сосудистых рисков.
К лекарственным средствам первой линии терапии относится метформин, препарат группы бигуанидов, применяемый с самого начала лечения СД2. Метформин эффективно снижает гипергликемию натощак, приводит к снижению уровня гликированного гемоглобина (HbA1c) на 1–2 %. Препарат не стимулирует секрецию инсулина, поэтому практически не вызывает гипогликемий. В рамках исследования UKPDS [17] применение метформина у больных СД2 с избыточной массой тела снижало в 2 раза общую смертность и частоту исходов, связанных с патологией сердечно-сосудистой системы. В течение последующих 10 лет у пациентов наблюдалось снижение частоты инфаркта миокарда, общей смертности и макрососудистых осложнений. Другие популяционные и наблюдательные исследования также продемонстрировали положительные сердечно-сосудистые эффекты метформина в сравнении с препаратами сульфонилмочевины (ПСМ) и инсулином [10, 11]. Противопоказания к назначению данного препарата связаны с возможностью развития лактатацидоза у лиц, имеющих повышенную склонность к продукции лактата вследствие гипоксии (сердечная, дыхательная недостаточность, анемия), с тяжелыми поражениями печени и почек (снижение скорости клубочковой фильтрации < 60 мл/мин).
В 2009 г. ингибиторы ДПП-4 были наряду с метформином включены в рекомендации Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологов (AACE/ACE) как препараты первой линии лечения СД2 (при уровне HbA1c 6,5–7,5 %) и далее на всех этапах продолжения терапии в качестве препаратов комбинированной терапии [1]. В настоящее время в РФ зарегистрировано два препарата этой группы: вилдаглиптин (Галвус и его комбинация с метформином Галвус Мет) и ситаглиптин (Янувия). Комбинированный препарат вилдаглиптина с метформином в виде единой лекарственной формы (Галвус Мет) доступен в разных дозировках (50/500, 50/850 и 50/1000 мг), что позволяет успешно подбирать оптимальную суточную дозу и усиливать комплаентность пациентов.
Одним из достоинств указанных препаратов является возможность их применения в группах пожилых пациентов, пациентов с сердечно-сосудистым риском, артериальной гипертензией, нарушением почечной функции средней тяжести. Вилдаглиптин можно комбинировать с любым ПССП, а также с инсулином [20, 21].
Сравнительное исследование по изучению терапии СД2 у пациентов, ранее не получавших метформин или вилдаглиптин [45], показало, что в течение 2 лет лечения вилдаглиптин и метформин обеспечивали аналогичный сахароснижающий эффект без прибавки массы тела (рис. 1). При этом в группе терапии вилдаглиптином частота диспепсических побочных явлений оказалась ниже, а терапия переносилась лучше [21]. Таким образом, терапию вилдаглиптином можно рекомендовать в качестве стартовой как вариант выбора у пациентов с непереносимостью метформина или его производных, или противопоказаниями к его использованию.

При невозможности достижения целевого значения HbA1c через 2–3 месяца на фоне монотерапии или при HbA1c > 7,6 % рационально применять комбинированную терапию. Основу комбинации должны составлять препараты, потенцирующие эффекты друг друга, действие которых направлено на разные звенья патогенеза СД2. Кроме того, требованиями к комбинации препаратов являются отсутствие усиления побочных эффектов каждого из компонентов; возможность использования в единой лекарственной форме; возможные положительные полиорганные эффекты.
Большая часть известных комбинированных препаратов включает метформин как лекарственное средство с хорошо доказанной эффективностью и безопасностью.
Одной из наиболее оптимальных стартовых комбинаций ПССП является использование метформина с ингибитором ДПП-4. Применение данной схемы в дебюте диабета является патогенетически оправданным, т. к. синергично увеличивает активность эндогенного ГПП-1, нормализуя секретогенную активность островковых клеток поджелудочной железы. Кроме того, улучшается утилизация глюкозы периферическими тканями. Благодаря этому комбинация метформина с ингибитором ДПП-4 успешно снижает как гликемию натощак, так и постпрандиальную гликемию. Присоединение ингибиторов ДПП-4 к метформину не сопряжено с риском гипогликемий и повышения массы тела, обеспечивает положительное влияние на факторы сердечно-сосудистого риска и артериальное давление. Помимо этого на фоне применения комбинации метформина с вилдаглиптином происходит улучшение функции β-клеток [21, 22].
Сочетание ингибиторов ДПП-4 с метформином не усиливает побочных эффектов последнего на желудочно-кишечный тракт, что обеспечивает безопасность данной комбинации. Клинические исследования показали, что у пациентов с неудовлетворительным контролем СД2 при применении метформина добавление вилдаглиптина обеспечивает достоверное снижение уровня глюкозы плазмы натощак и HbA1c (на 1,1 %) без повышения массы тела при минимальном риске гипогликемий [22]. Так, сравнение терапии вилдаглиптин + метформин и глимепирид + метформин у больных СД2 с неудовлетворительным контролем на монотерапии метформином показало достоверное и сравнимое улучшение гликемии при применении обоих комбинаций. Однако масса тела у пациентов, получавших комбинацию с глимепиридом, к концу исследования была на 1,8 кг выше, чем в группе вилдаглиптина, при исходном равенстве (рис. 2).
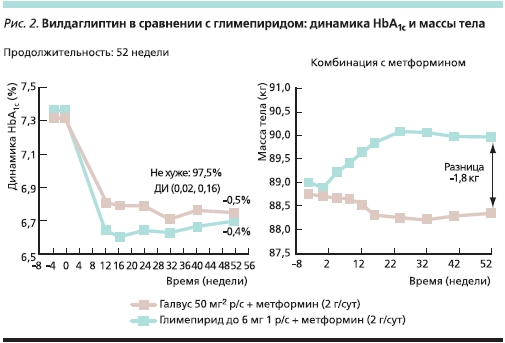
Частота гипогликемий на фоне терапии комбинацией вилдаглиптин + метформин была ниже более чем в 10 раз при полном отсутствии тяжелых эпизодов. Продолжение исследования в течение 2 лет показало сохранение долгосрочного сахароснижающего эффекта терапии вилдаглиптином + метформин, отсутствие влияния на массу тела и низкий риск гипогликемий (рис. 3).
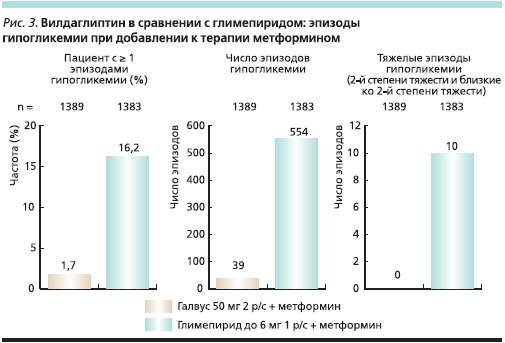
Изучение секреции глюкагона на фоне терапии глимепиридом и вилдаглиптином доказало, что вилдаглиптин подавляет секрецию глюкагона в 3,5 раза, а глимепирид увеличивает ее в 4,0 раза. Именно с этим связывают низкую частоту гипогликемий и возможность восстановления функций β- и α-клеток [22].
Одним из немаловажных достоинств терапии вилдаглиптином является снижение вариабельности гликемии, т. е. достижение ее стабильных показателей без резко выраженных колебаний, особенно в постпрандиальном периоде. Из группы ингибиторов ДПП-4 такое свойство пока показано только в отношении вилдаглиптина. Так, в исследование Marfella и соавт. [23] были включены 38 пациентов с СД2, получавших вилдаглиптин + метформин или ситаглиптин + метформин. Данные гликемического контроля оценивались через 3 месяца терапии. Непрерывный мониторинг гликемии (72 часа) проводился исходно и через 3 месяца. Результаты исследования показали, что гликемический контроль улучшился в обеих группах: уровень HbA1c снизился в среднем на 0,9 %. Основная разница была выявлена в показателях вариабельности гликемии на основании параметра средней амплитуды перепадов гликемии (САПГ), который характеризует вариабельность гликемии в течение суток. Исходно САПГ составлял около 3,5 ммоль/л в обеих группах. Через 3 месяца лечения в группе, получавшей вилдаглиптин, САПГ снизился на 2,2 ммоль/л, в то время как в группе на ситаглиптине изменения данного показателя зарегистрировано не было. Таким образом, была показана способность вилдаглиптина оказывать положительное влияние на вариабельность гликемии.
Авторы исследования также показали более выраженную активность ГПП-1 в постпрандиальные периоды и более выраженное подавление уровня постпрандиального глюкагона на фоне терапии вилдглиптином по сравнению с использованием ситаглиптина (рис. 4).
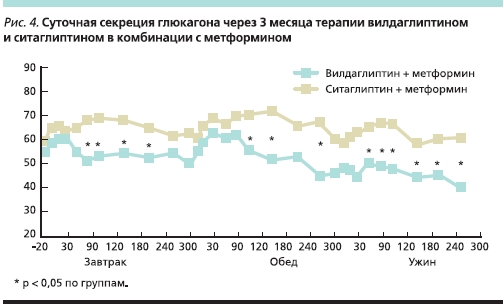
При выборе схемы терапии СД2 необходимо оценивать ее влияние на сердечно-сосудистую заболеваемость и смертность. Во многих работах показаны положительное влияние ингибиторов ДПП-4 на эти параметры [24], особенно в комбинации с метформином, и лучшая динамика липидного спектра [18]. Так, терапия вилдаглиптином обеспечивает достоверное снижение уровня постпрандиальных триглицеридов в плазме, триглицеридов в хиломикроне, аполипопротеинов в хиломикроне, холестерина в хиломикроне после приема жирной пищи [40]. Показано, что терапия вилдаглиптином и его комбинация с метформином усиливают постпрандиальное окисление жиров [6], повышает расходы энергии после приема пищи [18, 19]. При этом вилдаглиптин не оказывает влияния на скорость опустошения желудка, что обусловливает отсутствие тошноты, рвоты и хорошую переносимость терапии [12]. При сравнении с росиглитазоном показано, что терапия вилдаглиптином улучшает липидный профиль пациентов: снижает уровень триглицеридов, общего холестерина и липопротеидов низкой плотности, повышая уровень липопротеидов высокой плотности [13]. Кроме эффективного сахароснижающего действия при добавлении вилдаглиптина к метформину, были показаны еще и гипотензивные эффекты такой терапии у больных СД2 с исходно повышенными цифрами артериального давления [14, 15]. Сердечно-сосудистые эффекты ингибиторов ДПП-4 и аналогов ГПП-1 исследовались у больных СД2 после коронарной ангиопластики. Было показано, что ГПП-1 повышает фракцию выброса левого желудочка и опосредованно улучшает функцию эндотелия миокарда. К положительным эффектам вилдаглиптина на сердечно-сосудистую систему можно отнести повышение концентрации цAMФ в миоцитах сердечной мышцы; защиту сердечной мышцы от ишемии; функциональное восстановление после ишемии [16].
Широкомасштабный мета-анализ сердечно-сосудистых эффектов терапии вилдаглиптином был проведен в 2009 г. у 11 тыс. пациентов с СД2. Результаты анализа показали, что терапия вилдаглиптином не связана с повышенным риском развития каких-либо сердечно-сосудистых или церебро-васкулярного заболеваний у больных любого возраста и пола независимо от наличия исходных факторов сердечно-сосудистого риска [7].
Таким образом, терапия СД2 ингибиторами ДПП-4 дает реальную возможность безопасного улучшения метаболического и клинического контроля заболевания.



