Введение
В патогенезе большинства кожных заболеваний значительная роль принадлежит патологическим процессам, которые происходят во внутренних органах и системах, в частности нарушениям метаболического, гормонального, иммунного гомеостаза [1]. Заболевания эндокринной системы нередко сопровождаются кожными проявлениями, которые могут развиваться параллельно основному заболеванию и могут быть первыми симптомами, на которые обращает внимание пациент из-за значительного влияния на качество жизни [2]. Так, кожа – доступный взору орган, с помощью которого врачи могут диагностировать и контролировать различные соматические заболевания, в т.ч. эндокринные. Механизм эндокринологических дерматозов довольно сложный, их спектр проявлений весьма широк [3]. Некоторые кожные высыпания могут проявляться на ранней стадии гормональных нарушений, помогают в своевременной диагностике и лечении основного эндокринного заболевания. Чем раньше будет заподозрена истинная причина кожных проявлений и пациент будет направлен на обследование, тем раньше он начнет патогенетическое, а не симптоматическое лечение. Знание врачом первого контакта (терапевта, врача общей практики, дерматолога и др.) кожных проявлений эндокринологических заболеваний позволит оптимизировать их диагностику и способствовать улучшению оказания медицинской помощи пациентам. В этой статье мы представляем всесторонний обзор современной литературы по вариантам поражения кожи при заболеваниях эндокринной системы.
Заболевания щитовидной железы
Заболевания щитовидной железы (ЩЖ) распространены в популяции, в структуре эндокринопатий занимают второе место после сахарного диабета (СД); по данным Всемирной организации здравоохранения, в мире более 200 млн человек страдают патологией ЩЖ. Изменения кожи могут быть связаны непосредственно с нарушением функции ЩЖ и быть выявленными уже на ранней стадии болезни, следовательно, служить одним из клинико-диагностических маркеров заболевания, также могут быть следствием вторичных метаболических расстройств, возникающих при декомпенсации [4].
Гипертиреоз. Гипертиреоз развивается вследствие патологического повышения синтеза и секреции тиреоидных гормонов ЩЖ; основной диагностический критерий гипертиреоза – пониженный уровень тиреотропного гормона (ТТГ). Избыток тиреоидных гормонов усиливает термогенез и основной обмен, обусловливает снижение уровня холестерина в крови и снижение системного сосудистого сопротивления. К осложнениям длительно некомпенсированного тиреотоксикоза относятся похудение, остеопороз, фибрилляция предсердий, эмболические осложнения, сердечно-сосудистые заболевания [5]. Распространенность гипертиреоза в общей популяции составляет 1,2–1,6%. Наиболее частой причиной стойкого длительного гипертиреоза служат болезнь Грейвса и узловой токсический зоб.
Кожные проявления. Избыток гормонов ЩЖ приводит к чрезмерной стимуляции как α-, так и β-адренергических рецепторов, что выражается различными клиническими реакциями, в т.ч. повышением температуры тела, развитием гипергидроза, который дерматологически проявляется в виде мягкой, эластичной, теплой и влажной кожи [6]. Гипергидроз обычно наблюдается на ладонях и подошвах. При гипертиреозе также характерна эритема ладоней, а в ряде случаев развивается дисхромия кожи (гиперпигментация век, меланодермия по типу болезни Аддисона, витилиго с гиперпигментацией по периферии очагов), припухлость и менискообразное свисание век (симптом Еллинека). Волосы истончаются, становятся жирными, у 20% пациентов может возникать диффузная алопеция. Ногти становятся тонкими и ломкими, иногда формируется т.н. ноготь Пламмера, или онихолизис. Он представляет собой отделение ногтевой пластины от ногтевого ложа (отделенная часть становится белой и непрозрачной, в отличие от розовой полупрозрачности прикрепленной части) (рис. 1) [4].

Описанные выше кожные проявления связаны с избытком гормонов ЩЖ. Также существуют аутоиммунные механизмы поражения кожи, связанные с высоким титром антител к рецептору ТТГ (рТТГ). Данный рецептор обнаружен в коже и соединительной ткани. Стимуляция рТТГ при гипертиреозе приводит к пролиферации мезенхимальной ткани, развиваются локальные слизистые отеки вследствие отложения в коже кислых гликозаминогликанов, в основном гиалуроновой кислоты и хондроитинсульфата. Данный механизм лежит в основе формирования претибиальной микседемы, известной как дермопатия ЩЖ (может встречаться и при гипотиреозе, тиреоидите Хашимото). Претибиальная микседема встречается у 1–4% пациентов с диффузным токсическим зобом (рис. 2). Кожа передней поверхности голени хрящеподобно утолщается, появляются выпуклые высыпания телесного или желтовато-коричневого цвета, покрывающие утолщение и уплотнение без ямок с характерным признаком «апельсиновой корки», обусловленным расширением отверстий волосяных фолликулов. Такие бляшки безболезненны. Наиболее частым местом претибиальной микседемы является передняя большеберцовая кость, за которой следуют тыльная сторона стопы и пальцы ног [7]. Кроме того, дермопатия ЩЖ может проявляться в виде отека нижних конечностей без ямки, который в своей крайней форме проявляется как слоновая болезнь нижней конечности, связанная с препятствием оттока лимфы. Примерно у 20% пациентов с дермопатией ЩЖ наблюдается акропатия (нарушение сгибания пальцев), что является редким проявлением болезни Грейвса [8].
Гипотиреоз. Гипотиреоз – синдром, обусловленный стойким снижением уровня тиреоидных гормонов в организме (основной диагностический критерий первичного гипотиреоза – повышенный уровень ТТГ). По данным некоторых эпидемиологических исследований, в отдельных группах населения распространенность субклинического гипотиреоза достигает 10–12% [9]. Общие системные признаки гипотиреоза включают непереносимость холода, увеличение массы тела, запоры и депрессию. Наиболее распространенной этиологией развития гипотиреоза является тиреоидит Хашимото, или хронический лимфоцитарный тиреоидит. Эти нарушения сопровождаются увеличением продукции ТТГ гипофизом, что служит основой развития тиреоидной дерматопатии – претибиальной микседемы, результат стимуляции рТТГ в тканях (рис. 2), описанной выше в разделе гипертиреоза.
Кожные проявления. Сниженная адренергическая активность у пациентов с гипотиреозом приводит к низкой скорости метаболизма, что в конечном итоге приводит к холодной и сухой коже [10]. К кожным симптомам гипотиреоза относят сухость кожи, желтушность, вызванную гиперкаротинемией, микседематозный отек лица и/или конечностей и периорбитальный отек, гипотермию, ломкость и выпадение волос на латеральных частях бровей (симптом Хертога), голове (вплоть до гнездной плешивости и алопеции), в области подмышечных впадин и лобка. При сопутствующей анемии цвет кожи приближается к восковому. Эти изменения формируют синдром гипотиреоидной дермопатии и эктодермальных нарушений. Гистологически выявляют пропитывание тканей муцином. Таким образом, принято считать, что дерматологическая «маска» гипотиреоза включает алопецию, ухудшение структуры кожи, волос и ногтей [11]. На более поздних стадиях у пациентов с тиреоидитом Хашимото возможно развитие макроглоссии, расширение носа и утолщение губ, появление эритематозных высыпаний на коже, имитирующих дерматомиозит.
Изменения кожи и ее придатков при гипотиреозе следует дифференцировать от таких заболеваний, как микседематозный лихен, фолликулярный муциноз, амилоидоидный лихен, вторичные муцинозы, лимфостаз. Данные заболевания имеют массу схожих с гипотиреозом симптомов, однако в их основе лежат различные патогенетические механизмы.
Гипоталамо-гипофизарная ось
Гипопитуитаризм – это синдром, характеризующийся дефицитом гормонов передней доли гипофиза (ФСГ – фолликулостимулирующего гормона, ЛГ – лютеинизирующего гормона, АКТГ – адренокортикотропного гормона, ТТГ, пролактина, СТГ – соматотропина). Этиология гипопитуитаризма включает как развитие аденомы гипофиза, так и проведение хирургических манипуляций, воздействие лучевой терапии в анамнезе, а также гранулематозную болезнь или черепно-мозговую травму [12].
Кожные проявления гипопитуитаризма зависят от того, какой именно дефицит гормонов присутствует [13]. Снижение уровня ФСГ/ЛГ вызывает вторичный гипогонадизм. У женщин это может приводить к уменьшению ткани груди. У мужчин это часто клинически проявляется как гинекомастия, уменьшение волос в подмышечных впадинах и на лобке и уменьшение мышечной массы. Снижение уровня АКТГ не вызывает каких-либо специфических кожных проявлений. Снижение ТТГ может вызывать симптомы гипотиреоза, включая сухость кожи и отек лица, описанные выше. Снижение пролактина обычно не вызывает дерматологических проявлений, но может отмечаться снижение потоотделения, уменьшение толщины кожи и повышенная сухость. Относительная потеря пигментации может произойти из-за недостатка меланоцит-стимулирующего гормона [14].
Акромегалия – это тяжелое нейроэндокринное заболевание, обусловленное хронической гиперпродукцией СТГ у лиц с законченным физиологическим ростом и характеризующееся патологическим диспропорциональным периостальным ростом костей, хрящей, мягких тканей, внутренних органов, а также нарушением морфофункционального состояния сердечно-сосудистой, легочной систем, периферических эндокринных желез, различных видов метаболизма [15]. Характеризуется повышением уровня СТГ и инсулиноподобного фактора роста 1 (ИФР-1). Увеличение стимуляции рецептора СТГ вызывает пролиферацию дермальных фибробластов, в то время как ИФР-1 стимулирует синтез кератиноцитов [16].
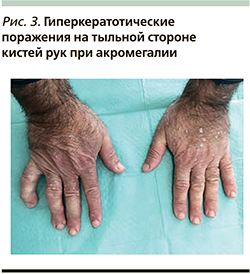
Кожные проявления при акромегалии характеризуются отложением гликозаминогликанов, что способствует утолщению кожи и мягких тканей, проявляются в огрублении и увеличении лицевых и акральных структур. Развиваются характерные грубые черты лица, включая отечность век, макрогнатию (увеличенную челюсть), макроглоссию (увеличенный язык), увеличенный нос и увеличенную складчатость лба, макродактилию (увеличение пальцев) (рис. 3). Кроме того, примерно у 40% пациентов появляется диффузная гиперпигментация [17]. Реже у пациентов с акромегалией может развиваться черный акантоз, гирсутизм. Вовлечение придатков кожи также может приводить к различным клиническим симптомам. Повышенная продукция сальных и потовых желез проявляется жирной кожей и гипергидрозом, соответственно. Поражение волос и ногтей может приводить к гипертрихозу и платонихии (плоский, широкий ноготь) [18].
Поджелудочная железа
Глюкагонома – это злокачественная опухоль α-клеток поджелудочной железы, секретирующая глюкагон, приводящая к развитию гипергликемии, СД и характерной сыпи. Проявления глюкагономы включают потерю массы тела, нормохромную анемию, венозную тромбоэмболию, а также желудочно-кишечные и психиатрические проявления.
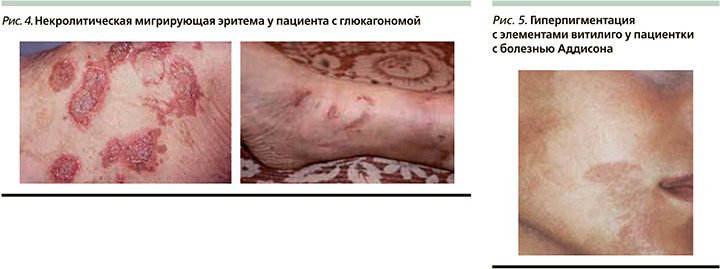
Кожные проявления. Типичный признак глюкагономы – длительно сохраняющаяся сыпь на коже конечностей, часто ассоциированная с изменениями языка (гладкий, блестящий, ярко-красного цвета) и хейлитом. Эта сыпь является шелушащейся коричнево-красной эритемой с явлениями поверхностного некролиза и обозначается как некролитическая мигрирующая эритема, она является ключевым дерматологическим проявлением глюкагономы [19], которое встречается почти у всех пациентов в течение болезни, хотя может отсутствовать (рис. 4). Первоначальная эритема прогрессирует с образованием болезненных зудящих булл в течение 7–14 дней, после разрыва которых образуются корки на пораженных участках, возможна пустулезная трансформация из-за бактериальной суперинфекции. Эритема имеет тенденцию формироваться в паху, а затем распространяется на конечности, бедра, ягодицы и промежность. Эти поражения часто вызывают зуд и могут быть болезненными [20]. Патогенез связывают с уменьшением триптофана из-за избытка глюкагона, который отвечает за функционирование никотиновой кислоты в плане регуляции клеточного состава, формирования эпидермиса. Также отмечают связь с гипоальбуминемией на фоне глюкагона, что вызывает снижение транспорта цинка и нарушение трофики кожи [21].
Сахарный диабет – распространенное хроническое неинфекционное заболевание, принимающее масштабы эпидемии во всем мире, поражающее множество органов, включая кожу, характеризуется гипергликемией в течение длительного периода времени. По данным литературы, дерматологические проявления СД встречается у 30–70% пациентов в течение жизни, различающиеся по тяжести, патогенезу, степени проявления [22]. Основная роль в развитии поражения кожи при СД принадлежит глюкозотоксичности, инсулинорезистентости, присутствию хронического воспаления.
В сочетании с диабетическими осложнениями могут развиваться различные виды сыпи, пигментные пятна, изъязвления, а также гнойно-септические осложнения.
Кожные проявления у пациентов с СД могут быть совершенно разными, некоторые из них специфичные (липоидный диабетический некробиоз – 0,3–1,6%, диабетические буллы – 0,5%, витилиго, диабетическая дермопатия, диабетический ксантоматоз, диабетическая склередема), другие неспецифичны, связаны с метаболическими изменениями (черный акантоз, гиперпигментация кожи локтей, колен и тыла кистей, рецидивирующие кожные грибковые или бактериальные инфекции, генерализованный и локализованный кожный зуд) [23]. В данной статье мы не будем подробно останавливаться на кожных проявлениях СД.
Надпочечники
Синдром Иценко–Кушинга (СИК) характеризуется рядом клинических проявлений, возникающих в результате избыточной секреции глюкокортикоидов. Избыток кортизола может быть АКТГ-зависимым или АКТГ-независимым [24].
Кожные проявления СИК весьма специфичны и широко известны клиницистам. Это аномальное распределение жира на теле, лице («лунообразное лицо») и спине («буйволиный горб»), выраженная атрофия кожи с развитием багровых стрий, медленное заживление ран, персистенция стероидной угревой сыпи (мономорфные фолликулярные папулы или пустулы). Избыточный уровень глюкокортикоидов снижает пролиферацию кератиноцитов и фибробластов кожи. Эти изменения препятствуют образованию коллагена и других компонентов внеклеточного матрикса, в конечном итоге способствуют атрофии и хрупкости кожи. Катаболические эффекты глюкокортикоидов также распространяются на подкожную соединительную ткань [25].
Также при СИК в местах трения в области воротника на шее, в области живота, локтей возникает гиперпигментация вследствие отложения меланина, количество которого увеличивается вместе с количеством адренокортикотропного гормона. Характерна вирилизация женщин с развитием гирсутизма в связи с усилением продукции андрогенов корой надпочечников [26].
Болезнь Аддисона – это медленноразвивающаяся и обычно прогрессирующая дисфункция коры надпочечников, характеризуется дефицитом глюко- и минералокортикоидов. Также ее называют «бронзовая болезнь» из-за характерной пигментации кожи. При этом состоянии по механизму отрицательной обратной связи увеличивается продукция АКТГ и его предшественника проопиомеланокортина. В результате протеолиза проопиомеланокортина кроме АКТГ образуется и меланоцитстимулирующий гормон, который обусловливает гиперпигментацию кожи и слизистых оболочек [27].
Кожные проявления пациентов с болезнью Аддисона проявляются генерализованной гиперпигментацией, приобретающей бронзовый, коричневый или грязно-серый оттенок. Сначала темнеют открытые части тела, наиболее подверженные действию солнца (лицо, шея, руки), а также места, которые и в норме более сильно пигментированы (соски, мошонка, наружные половые органы). Большую диагностическую ценность имеет потемнение кожи в местах трения и видимых слизистых оболочек. Характерна гиперпигментация ладонных линий. В ряде случаев определяется гиперпигментация слизистых оболочек губ, десен, неба. Специфический признак бронзовой болезни – гиперфункция клеток мальпигиевого слоя, выражающаяся в обильном отложении меланина. У пациентов с болезнью Аддисона повышен риск других аутоиммунных состояний, включая витилиго, которое встречается примерно у 10% пациентов (рис. 5) [2].
Андрогенная ось
Гиперандрогения определяется как избыток андрогенов у женщин, наиболее частой причиной служит синдром поликистозных яичников (СПКЯ), другие причины включают врожденную гиперплазию надпочечников, а также опухоли яичников и надпочечников [28].
Кожные проявления при гиперандрогении включают гирсутизм, вульгарные угри и себорею, андрогенную алопецию. Гирсутизм определяется как чрезмерный рост конечных волос по мужскому типу, включая область бороды (лицо и шея), спину, грудь и нижнюю часть живота [29]. Кожа становится утолщенной и грубой [30]. Другие частые проявления этого расстройства включают черный акантоз, вызванный инсулинорезистентностью и гиперинсулинизмом.
Наследственные эндокринные синдромы
Аутоиммунные полигландулярные синдромы (АПС)
АПС 1-го типа обычно манифестирует в детском возрасте (10–12 лет) и является моногенным аутосомно-рецессивным заболеванием (мутация гена AIRE). В состав АПС 1-го типа классически входят такие заболевания, как гранулематозный кандидоз (кандидамикоз кожи и слизистых оболочек), гипопаратиреоз и хроническая надпочечниковая недостаточность, в 7–10% случаев присоединяются изменения функций ЩЖ [31].
Кожные проявления. Помимо обязательного компонента, кандидоза, для пациентов с АПС 1-го типа характерны алопеция (30%), витилиго (5%), дистрофия ногтевых пластин (05–3%).

АПС 2-го типа ассоциирован с нарушениями в области HLA-гаплотипов. Компонентами АПС 2-го типа являются надпочечниковая недостаточность и/или СД 1 типа, поражение ЩЖ [31].
Кожные проявления характеризуются возможным появлением витилиго и алопецией. Алопеция при АПС-2 может быть как гнездной, так и тотальной, или универсальной. Депигментированные пятна обусловлены отсутствием меланоцитов. В ряде случаев развитию витилиго предшествует появление невусов Сеттона. Хроническая надпочечниковая недостаточность, входящая в состав АПС 2-го типа, проявляется наличием бронзовой окраски кожи, механизм развития которой соответствует болезни Аддисона [27].
АПС 3-го типа представляет собой комбинацию заболеваний ЩЖ с одним или несколькими другими аутоиммунными заболеваниями как эндокринного, так и неэндокринного спектра, причем в подтип 3С АПС 3-го типа входят витилиго, алопеция, в подтип 3D – дискоидная красная волчанка, синдромы Шарпа и Шегрена, васкулиты. Все эти заболевания имеют соответствующие кожные проявления [28].
Синдром множественных эндокринных неоплазий (МЭН)
МЭН 1-го типа – генетическое аутосомно-доминантное заболевание, которое возникает в результате инактивации гена – супрессора опухоли менина. Для МЭН1 характерны опухолевые поражения нескольких эндокринных желез: аденомы паращитовидной железы, опухоли островков поджелудочной железы и опухоли передней доли гипофиза [4].
Кожные проявления служат диагностическим критерием для синдрома МЭН1. Ангиофибромы встречаются более чем у 80% пациентов, при этом чаще всего локализуются на лице. Коллагеномы бывают у более 70% пациентов, возникают в верхней части туловища, шеи и плечи. Липомы развиваются в среднем у 30% пациентов, располагаются на туловище, конечностях и волосистой части головы [7].
МЭН 2-го типа возникает из-за активирующих мутаций в протоонкогене RET. Медуллярная карцинома ЩЖ и феохромоцитомы распространены как в МЭН2а-, так и в МЭН2b-типов. Кроме того, аденомы паращитовидной железы часто встречаются при МЭН2а (10–15%), а невриномы слизистой оболочки – при МЭН2b [29]. Распространенность обоих типов МЭН2а и МЭН2b составляет примерно 1 на 35 тыс. человек, при этом МЭН2а встречается намного чаще.
Кожные проявления МЭН2а связаны с развитием амилоидного лихена, который представляет собой мезенхимальный диспротеиноз с отложением амилоида в коже, встречается в половине случаев МЭН2а. Обычно располагаются между лопатками или на разгибательных поверхностях конечностей. Первым симптомом часто является зуд, что приводит к расчесыванию пораженных участков, вызывая повреждение кератиноцитов. Поврежденный кератиноцит затем дегенерирует и приводит к характерным чешуйчатым, пигментным и папулезным поражениям кожи [33]. МЭН2b сочетается с множественными невриномами слизистых оболочек, нейрофиброматозом 1-го типа [4]. Они представляют собой бородавчатые папулы и узелки, могут присутствовать на губах, придавая им неправильный вид, а также на передней трети языка и слизистой оболочке щек и на внутреннем веке, придавая ему утолщенный вид.
Заключение
Эндокринные заболевания помимо поражения внутренних органов-мишеней могут приводить к изменениям функции и морфологии кожи, что отражается в сложной симптоматике. Врач-дерматолог или терапевт часто первым встречается с кожными симптомами эндокринного заболевания, поэтому важно вовремя оценить патогенез и этиологию дерматоза, чтобы пациенты могли получать этиотропное, а не симптоматическое лечение. В ряде клинических ситуаций именно кожные проявления эндокринопатий имеют решающее значение для постановки клинического диагноза. Таким образом, распознавание кожных проявлений эндокринных нарушений важно как для дерматологов, так и для врачей других специальностей.



