Актуальность
Распространенность железодефицитной анемии (ЖДА) у беременных в России составляет в среднем 35,6% к числу закончивших беременность (по данным МЗ РФ, 2018) с наиболее высокими показателями в Сибирском (37,3%), Приволжском (38,2%) и Северо-Кавказском (44,2%) федеральных округах. Дефицит железа (ДЖ) выявляется у 70–100% населения в популяциях с распространенностью ЖДА до 40%, и наиболее частой его причиной среди женщин репродуктивного возраста является низкое потребление железа с пищей (алиментарный фактор) [1] на фоне регулярной менструальной кровопотери.
ЖДА и латентный дефицит железа (ЛДЖ) оказывают неблагоприятное влияние на общее и репродуктивное здоровье женщин, течение и исходы беременности, на состояние новорожденных и детей. Так, у женщин с тяжелым ДЖ повышается частота преэклампсии, плацентарной недостаточности, задержки роста плода, слабости родовой деятельности, послеродовых кровотечений, гнойно-септических осложнений в послеродовом периоде, гипогалактии и/или сокращения сроков грудного вскармливания, психоэмоциональных нарушений (в частности, депрессии), снижение сексуальной функции и удовлетворенности после беременности [2–4]. Данные мета-анализа свидетельствуют о значительно более высоких рисках для новорожденных, чьи матери имеют анемию – относительный риск преждевременных родов составляет 1,63 (95% доверительный интервал [ДИ]: 1,33–2,01), низкой массы тела при рождении – 1,31 (95% ДИ: 1,13–1,51), перинатальной смертности – 1,51 (95% ДИ: 1,30–1,76) и неонатальной смертности – 2,72 (95% ДИ: 1,19–6,25) [5], частота низкой массы анемии у детей в возрасте 1 года достигает 68%, что неблагоприятно отражается на их умственном, психическом и моторном развитии, снижает сопротивляемость организма к инфекциям, увеличивает смертность [6].
Однако в случаях, когда ДЖ выявлен в ранние сроки беременности и назначены препараты железа, это позволяет предупреждать развитие ЖДА и ее осложнений в отношении 87% женщин, а также улучшать качество жизни беременных, что определяет необходимость своевременной диагностики и лечения ЛДЖ [7–8].
С учетом высокой актуальности проблемы анемии среди населения РФ в июне 2020 г. проведен Экспертный совет «Актуальные вопросы железодефицита в Российской Федерации». Сорок членов совета представляли 15 научно-исследовательских и образовательных учреждений из 20 регионов России, которые обсудили различные аспекты проблемы ДЖ и сформулировали предложения для практического здравоохранения. Основные положения резолюции Экспертного совета и результаты исследований, опубликованные в последние годы по проблеме ЛДЖ и ЖДА у беременных, легли в основу разработанных алгоритмов диагностики и лечения этих состояний, представленных в настоящей публикации.
Причины развития ЛДЖ и ЖДА при беременности
Основной патологический фактор развития анемии беременных – это недостаток железа, поступающего с пищей. На ранних сроках беременности потребность в экзогенном железе составляет 0,8 мг/сут, на поздних – увеличивается до 7,5, при средней потребности на протяжении всей беременности – 4,4 мг/сут. [9]. По сравнению с небеременными женщинами этот показатель выше в 2 раза. Однако выделяют еще несколько причин: имеющийся ДЖ до наступления беременности (у 42% женщин) [10], повышенный расход железа на увеличение массы циркулирующих эритроцитов на 15–25%, рост плода и плаценты, влияние плаценты, которая вырабатывает определенные цитокины и интерфероны, что приводит к депонированию железа и развитию анемии по типу воспаления, которая характеризуется железодефицитным эритропоэзом [5].
Клинико-лабораторные характеристики ЛДЖ и ЖДА
ДЖ представляет собой спектр состояний, начинающихся от предрасположенности к ДЖ и предлатентного ДЖ (изменения в клинической картине, анализах крови и обмене железа отсутствуют, но имеется высокий риск их развития) до ЛДЖ (клинически выраженный ДЖ, характеризующийся симптомами сидеропении – нарушениями состояния кожи и ее придатков, слизистых оболочек и иммунной системы) и ЖДА (последняя стадия ДЖ, когда запасов железа уже недостаточно для поддержания нормальной концентрации гемоглобина – Hb). При выраженном ДЖ кроветворение характеризуется гипохромией (снижением среднего содержания Hb в эритроците, МСН – Mean Corpuscular Hemoglobin) и микроцитозом (снижение среднего объема эритроцита, МСV – mean cell volume). Характерно также снижение сывороточного железа (СЖ), ферритина сыворотки (ФС) и процентного насыщения трансферрина железом (НТЖ), наоборот, общая железосвязывающая способность (ОЖСС) и уровень трансферрина повышаются (но могут снижаться при воспалении или недоедании). Стадии ЛДЖ и ЖДА проявляются наличием клинических симптомов – сидеропенических (при ЛДЖ и ЖДА) и анемических (при ЖДА) и описанными изменениями в анализах крови [11].
Организационные аспекты выявления и лечения ЛДЖ и ЖДА у беременных
Клиническими рекомендациями (протокол лечения) «Нормальная беременность» (письмо МЗ РФ от 13.02.2020 № 15-4/368-07) рутинное применение добавок железа во время беременности не рекомендуется. Рекомендуется проведение общего (клинического) анализа крови в I, II и III триместрах беременности и измерение уровня ФС для раннего выявления ЛДЖ.
Федеральные клинические рекомендации «Диагностика, профилактика и лечение железодефицитных состояний у беременных и родильниц» (М., 2013) содержат рекомендации по диагностике и лечению ЛДЖ и ЖДА. Проведение скрининга на ДЖ рекомендуется женщинам в 5–6 недель беременности или в более поздние сроки (при первичном обращении к врачу): определение уровней Hb, эритроцитов, гематокрита, CЖ, коэффициента НТЖ, ферритина сыворотки.
Клинические рекомендации (протокол лечения) «Кровесберегающие технологии у гинекологических больных» (письмо МЗ РФ от 04.09.2015 №15-4/10/2-5079) содержат рекомендации по диагностике и лечению ЖДА и ЛДЖ у беременных врачами-акушерами-гинекологами и врачами других специальностей, работающих в перинатальных центрах, многопрофильных больницах.
Клинические шифры ДЖ, согласно Международной классификации болезней 10-го пересмотра: Анемия, осложняющая беременность, деторождение и послеродовой период О99,0 (состояния, классифицированные в рубрике D50, – железодефицитная анемия; D62 – острая постгеморрагическая анемия), болезни эндокринной системы, расстройства питания и нарушения обмена веществ, осложняющие беременность, деторождение и послеродовой период О99,2 (состояние, классифицированное в рубрике Е61.1 – недостаточность железа).
Современные методы диагностики ЛДЖ и ЖДА во время беременности
Диагностика ЛДЖ в клинической практике недооценивается, поскольку нормальные значения Hb в крови не могут свидетельствовать о достаточных запасах железа в организме, особое значение для своевременной диагностики ЛДЖ приобретает настороженность врачей, выявление групп риска беременных и проведение дополнительного обследования.
Согласно Резолюции Совета экспертов по железодефицитной анемии у женщин (2020) [1], необходимо обращать внимание на женщин, имеющих следующие критерии:
- заболевания, сопровождающиеся хронической кровопотерей (желудочно-кишечные, маточные, носовые, почечные), донорство;
- состояния, связанные с нарушением всасывания железа в кишечнике (энтериты, резекция тонкого кишечника, бариатрические операции, синдром недостаточного всасывания);
- недостаточное поступление железа с пищей (бедность, дефицит питания, анорексия, вегетарианство и др.);
- ЖДА в анамнезе.
Для всех женщин при взятии на учет по беременности необходимо уточнять следующую информацию:
- интервалы между родами и период времени с момента окончания последней беременности, закончившейся родами;
- анамнез кровотечения в родах и способ родоразрешения (при кесаревом сечении кровопотеря выше);
- аномальные маточные кровотечения в анамнезе (миома матки, дисфункция яичников, эндометриоз);
- способ контрацепции, использованный до наступления беременности (негормональные внутриматочные средства увеличивают объем кровопотери).
При наличии хотя бы одного условия, предрасполагающего к наличию ДЖ, необходимо отнести пациентку к группе риска по развитию ЛДЖ или ЖДА и составить план профилактических мероприятий.
Всемирная организация здравоохранения (ВОЗ) рекомендует диагностировать анемию во время беременности при концентрации Hb<110 г/л [12]. Центральным параметром определения ДЖ является ФС крови, снижение уровня которого свидетельствует об истощении железа в депо [13].
ФС – это гликопротеин, который вне воспалительного процесса четко отражает запасы железа в организме. Он также является маркером воспаления в организме и при воспалительном процессе его уровень повышается вне зависимости от истинных показателей феррокинетики. ФС целесообразно использовать для верификации ЛДЖ, когда показатели Hb и СЖ сохраняются в пределах нормы. Нормальное содержание ФС у здоровых женщин – 32–60 мкг/л, что соответствует 356–480 мг железа в депо. Границей, определяющей явный ДЖ у небеременных, является уровень ферритина менее 15 мкг/л, при ФС менее 30 мкг/л можно говорить об истощении запасов железа в организме и необходимости назначения препаратов железа [13]. ФС не может трактоваться однозначно при наличии признаков воспаления (требуется лечение и повторное исследование).
Алгоритм диагностики ЖДА и ЛЖД представлен на рис. 1.
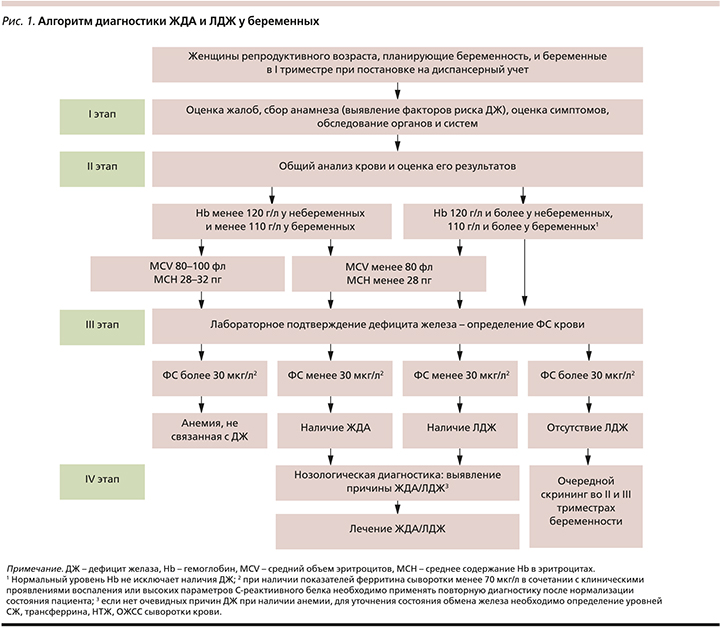
Современные методы лечения ЛЖД и ЖДА у беременных
Наличие доказанных ЛДЖ или ЖДА требует устранения факторов, вызвавших ДЖ, обязательного лечения препаратами железа и проведения мероприятий, направленных на профилактику рецидива.
При снижении ФС менее 30 мкг/л запасы железа считаются отсутствующими или почти отсутствующими, что позволяет ставить диагноз ЛДЖ и требует приема 80–100 мг элементарного железа в сутки [14]. При снижении ФС ниже 60 мкг/л, но больше 30 мкг/л рекомендуются добавки в меньших дозах – 30–40 мг/сут. [15]. Прерывистые курсы добавок железа во время беременности (2–3 раза в неделю) эффективны так же, как и ежедневные, связаны с меньшим числом побочных эффектов [16]. Если ФС выше 60 мкг/л, необходимость в приеме препаратов железа отсутствует.
В настоящее время определено, что наибольшей эффективностью в лечении ДЖ обладают препараты, содержащие двухвалентное железо (соли сульфата, фумарата, глюконата) и аскорбиновую кислоту; именно они являются препаратами выбора для пероральной терапии (рекомендации ВОЗ) [17]. При этом максимальная эффективная и безопасная разовая доза составляет 100 мг, а суточная не должна превышать 300 мг.
Формы железа с замедленным высвобождением (Сорбифер Дурулес) предотвращает контакт атомов металла со слизистой оболочкой желудка, поскольку высвобождение его происходит только при смене кислотности среды в просвете двенадцатиперстной кишки, где осуществляется основной объем абсорбции железа, что значимо снижает число побочных эффектов [18].
Наибольшая эффективность терапии ЖДА наблюдается в первый месяц лечения, что позволяет решать вопрос о дальнейшей тактике лечения: терапия считается эффективной, если прирост Hb 10 г/л в первый месяц лечения и выше. Лечение должно проводиться не менее 2 месяцев для нормализации Hb и еще 2–3 месяца – для нормализации запасов железа в депо. Определение уровня ФС также служит объективным критерием оценки эффективности и длительности использования препаратов железа.
Лечение ЖДА должно проводиться с учетом степени тяжести и варианта анемии. Анемию беременных подразделяют на три степени тяжести (клинические рекомендации, 2013): легкая – 110–90 г/л, среднетяжелая – 89–70 г/л, тяжелая – ниже 70 г/л. Выделяется два варианта: без воспаления и с воспалением.
При лечении легкой анемии (Нb>90 г/л) без воспаления рекомендованы пероральные препараты, с воспалением – противовоспалительная терапия и внутривенное железо, при средней степени, неэффективности или непереносимости перорального железа рекомендуется внутривенное введение железа в условиях стационара (вторая линия терапии), а при тяжелой – наряду с парентеральным введением железа возможно использование препаратов рекомбинантного человеческого эритропоэтина (рч-ЭПО) или даже гемотрансфузии (Hb менее 30–40 г/л, выраженные клинические симптомы анемии, некупируемые другим способом, или необходимость быстрого подъема уровня Hb).
При паренеральном введении железа предпочтение надо отдавать препаратам с новым составом, таким как низкомолекулярный декстран и карбоксимальтозат железа, которые можно вводить одномоментно в виде полной замещающей дозы 1000 мг элементарного железа для ЛЖД или половинной для ЖДА (суммарная доза должна составлять 1500–2000 мг, что зависит от тяжести анемии и массы тела пациентки), что обеспечивает до 95% нормализации Hb и отсутствие тяжелых реакций [19–20]. Однако надо помнить, что для назначения парентеральной терапии требуется обязательное подтверждение наличия тяжелого ДЖ (низкие показатели ФС и анемия), разовая доза новых внутривенных препаратов железа может достигать 1000 мг с возможностью повторного ведения не раньше, чем через неделю, а ее проведение возможно только после 14-й недели беременности. Препараты рч-ЭПО также нельзя вводить до 20-й недели беременности.
Алгоритм лечения ЖДА и ЛЖД представлен на рис. 2.
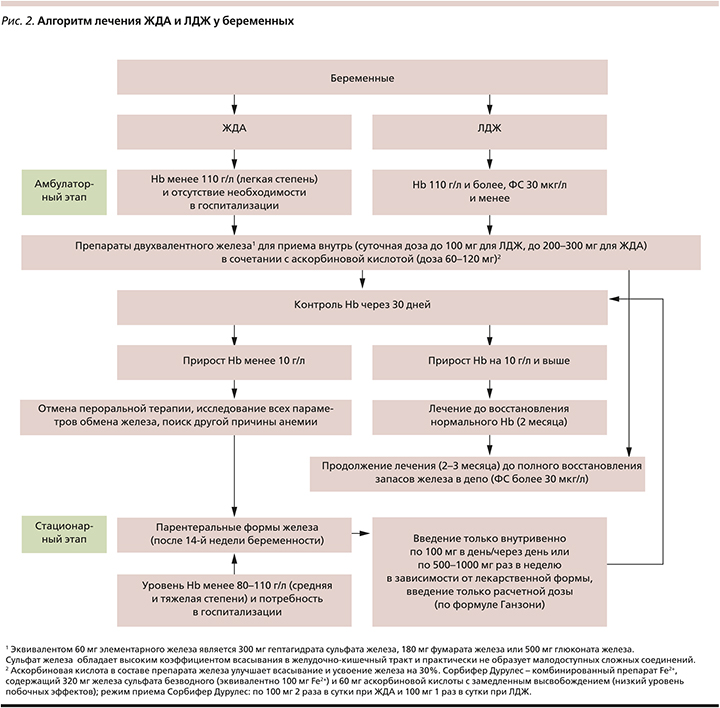
Профилактика ЛДЖ и ЖДА
Российскими клиническими рекомендациями (2013) при нормативных значениях Hb рекомендуется проводить профилактику ДЖ, используя витаминно-минеральные комплексы для беременных и кормящих, содержащих не менее 20 мг элементарного железа. Подчеркивается необходимость своевременного выявления ЛДЖ и при его наличии назначение препаратов железа в дозе 50–100 мг/сут. в течение 6 недель, причем с учетом решения Экспертного совета наиболее оптимальной тактикой можно считать выявление и коррекцию ДЖ до начала беременности.
Заключение
В настоящее время стандартом оказания медицинской помощи беременным должен стать скрининг ДЖ с определением ФС. Необходимо информировать женщин репродуктивного возраста, планирующих беременность, о неблагоприятных последствиях ДЖ и проведении его коррекции до наступления беременности.
Финансирование. Статья подготовлена в рамках выполнения инициативной темы.



