Введение
Целиакия (глютеновая энтеропатия) – иммунозависимое заболевание, характеризующееся развитием воспалительного процесса в слизистой оболочке тонкой кишки (СОТК), вызванного приемом хлебных злаков наследственно предрасположенными лицами. Воспаление ведет к развитию гиперрегенераторной атрофии СОТК, которая постепенно исчезает при исключении из диеты глютена – белка, содержащегося в пшенице, ржи, ячмене [1]. Механизм повреждающего действия глютена обусловлен как его токсическим влиянием на СОТК людей, предрасположенных к целиакии, так и патологической реакцией Т-лимфоцитов на него. На сегодняшний день распространенность целиакии во взрослой популяции большинства стран мира составляет 1:100–1:250 человек. Среди женщин целиакия встречается в 3–4 раза чаще, чем среди мужчин [2]. Заболевание всегда начинается с детства, но нередко может длительно протекать субклинически впервые и проявляться у взрослых или даже в пожилом возрасте – латентная форма целиакии. Фактором, провоцирующим появление первых клинических симптомов у женщин, чаще всего являются беременность и роды. Однако провоцирующим фактором могут также выступать стрессовые ситуации и кишечные инфекции. [3] Одним из постоянных клинических симптомов являются систематические поносы, сопровождающиеся развитием синдрома нарушенного всасывания (СНВ), а также повышенное газообразование и явления мальабсорбции [4]. Важную роль в патогенезе СНВ играет нарушение мебранного пищеварения, оцениваемое по снижению активности карбогидраз в СОТК. В работе О.В. Ахмадуллиной показано, что у больных впервые диагностированной целиакией в 87% случаев наблюдается снижение активности карбогидраз: глюкоамилазы, мальтазы, сахаразы, лактазы. Выявлена обратная корреляционная зависимость между степенью атрофии СОТК и уровнем снижения активности карбогидраз: при уменьшении степени атрофии СОТК возрастает уровень кишечных ферментов в слизистой оболочке. Изменение активности карбогидраз имеет диагностическое и прогностическое значение [5]. Основным методом лечения больных целиакией является строгое пожизненное соблюдение аглютеновой диеты (АГД); при СНВ 3-й степени больным назначается терапия глюкокортикоидами – преднизолон внутривенно с последующим переходом на его пероральный прием и постепенной отменой препарата; также проводится коррекция метаболических нарушений [3].
В многочисленных работах последних лет продемонстрировано гастроэнтеропротективное действие цитопротектора ребамипида, способствующего заживлению язвенных поражений желудка и кишечника [6–9]. Механизм защитного действия ребамипида, его влияния на репаративные процессы объясняется стимуляцией синтеза простагландинов, экспрессией факторов роста, улучшением пролиферации эпителия [10]. Есть данные о положительном влиянии ребамипида при заболеваниях кишечника. [11]
В качестве примера эффективности ребамипида рассмотрим историю болезни пациентки К. с латентной формой целиакии.
Клинический случай
Больная К. 29 лет поступила в кишечное отделение в ГБУЗ МКНЦ им. А.С. Логинова в марте 2018 г. с жалобами на частый обильный стул до 10–15 раз в сутки, вздутие, урчание в животе, эпизоды ноющих болей в подложечной области после прием пищи, отеки нижних конечностей, больше в области бедер, увеличение живота в объеме, сухость кожи, выпадение волос, судороги и онемение конечностей, снижение массы тела на 15 кг за последние 3 месяца. Считает себя больной с июня 2017 г., когда через месяц после родов появился частый жидкий обильный стул без патологических примесей. Госпитализирована в инфекционное отделение областной больницы с диагнозом «острый гастроэнтерит». Инфекционный агент не был установлен. Принимала ферментные препараты, вяжущие средства, лечение было без эффекта. После выписки жалобы сохранялись. Отмечено снижение массы тела, появились отеки ног. Неоднократно находилась на лечении в гастроэнтерологическом отделении с диагнозом «синдром раздраженного кишечника с диареей». В анализах крови отмечены анемия (гемоглобин – 100 г/л), снижение уровня общего белка (36 г/л). Проводилось лечение препаратами 5-аминосалициловой кислоты, кишечными антисептиками, гепатопротекторами, ферментными препаратами. На фоне переливания альбумина и плазмы отмечалось некоторое улучшение состояния в виде уменьшения отеков. Диарея сохранялась, нарастала потеря веса. Направлена на обследование и лечение в кишечное отделение ГБУЗ МКНЦ им. А.С. Логинова ДЗМ.
При поступлении состояние средней тяжести. Телосложение астеническое. Рост – 170 см. Вес – 54 кг. Индекс массы тела – 18,69 кг/м2. Кожные покровы и видимые слизистые оболочки бледные. Отмечаются сухость кожи, положительный симптом «мышечного валика». Периферические лимфоузлы не увеличены, безболезненные. Отеки голеней и стоп. В легких при перкуссии ясный легочный звук, аускультативно – дыхание везикулярное, хрипов нет. Границы сердца в пределах нормы. Тоны сердца ритмичные, ясные. Пульс – 76 ударов в минуту, АД – 90/60 мм рт.ст. Язык влажный, чистый со сглаженными сосочками. Живот вздут, при пальпации мягкий тестоватой консистенции. Определяется асцит. Симптомов раздражения брюшины нет. Печень выступает из-под реберной дуги на 2 см. Селезенка не пальпируется. Почки не пальпируются. Симптом поколачивания отрицательный с обеих сторон. Со стороны 12 пар черепно-мозговых нервов без особенностей. В анализах крови: железодефицитная анемия (Hb – 11,7 г/л, сывороточное железо – 4,8 ммоль/л), гипопротеинемия (общий белок – 41,4 г/л), гипоалбуминемия – 21,3 г/л, гипокальцемия – 1,74 ммоль/л, гипомагниемия – 0,41 ммоль/л, гипертрансаминаземия: АЛТ – 283,2, АСТ – 240,2 ЕД. Коагулограмма: АЧТВ – 41,1 с (норма – 25–36,9), МНО – 2,41 (норма – 0,90–1,2), протромбиновое время – 26,6 с. Анализы мочи и кала без отклонений от нормы. Иммунологическое исследование: антитела (АТ) к глиадину IgA – 120 ЕД/мл (норма до12 ЕД/мл), IgG – 100 ЕД/мл, АТ к тканевой трансглютаминазе, IgA – 200 Ед/мл, IgG – 144 ЕД/мл (норма до 10 ЕД/мл).
Ультразвуковое исследование органов брюшной полости: асцит, увеличение и диффузные изменения печени, хронический холецистит, билиарный сладж. КТ-энтерография: данных за наличие воспалительных изменений стенок тонкой и толстой кишки не выявлено, хронический холецистит, малое количество свободной жидкости в брюшной полости и малом тазу. ЭГДС: слизистая оболочка желудка розовая с очагами гиперемии, в антральном отделе единичные эрозии до 0,3 см с неизмененной слизистой, слизистая оболочка двенадцатиперстной кишки мозаично исчерчена, ворсины сглажены. Заключение: хронический эрозивный гастрит, эндоскопические признаки целиакии.
Заключение по морфологическому исследованию биоптатов слизистой оболочки двенадцатиперстной кишки: кишечные ворсинки отсутствуют (V-0), отмечается гиперплазия крипт; поверхностный эпителий с участками десквамации, уплощен, с вакуолизацией цитоплазмы; количество бокаловидных клеток снижено; количество межэпителиальных лимфоцитов в поверхностном эпителии и эпителии крипт увеличено (65 на 100 эпителиоцитов); в собственной пластинке выраженная лимфо-плазмоцитарная инфильтрация с примесью эозинофилов и гистиоцитов. Заключение: глютеновая энтеропатия на стадии Marsh IIIC.
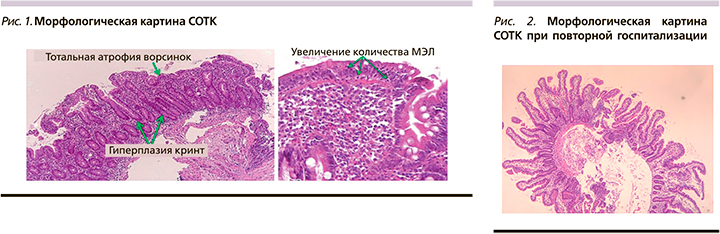
В данную госпитализацию в связи с выраженными электролитными нарушениями и тяжестью состояния при поступлении от проведения фиброколоноскопии было решено воздержаться. Последняя колоноскопия от 19.10.2017 – осмотр на 75 см до печеночного изгиба без органической патологии. Ирригоскопия от 02.03.2018 – без патологии.
Больной было проведено исследование активности кишечных карбогидраз по данным биопсии залуковичного отдела двенадцатиперстной кишки. Как видно из табл. 1, у пациентки отмечалось снижение активности всех исследуемых ферментов. Такое значительное снижение содержания кишечных ферментов, осуществляющих заключительный этап гидролиза и всасывания пищевых веществ, свидетельствует о нарушении функционального состояния СОТК.
На основании клинической картины заболевания – упорной диареи, развившейся через месяц после родов, быстрого появления СНВ (прогрессирующая потеря веса, железодефицитная анемия, гипопротеинемия с гипопротинемическими отеками, асцит), высоких значений иммунологических тестов (АТ к тканевой трансглутаминазе IgA и IgG), результатов морфологического исследования СОТК, выявивших атрофию СОТК на стадии Marsh IIIC, снижения функциональной способности тонкой кишки в виде низкого уровня карбогидраз СОТК больной был поставлен диагноз «целиакия, впервые выявленная, латентная форма. Синдром нарушенного всасывания 3-й степени тяжести с нарушением белкового, электролитного, витаминного обменов. Гипопротеинемия, гипопротеинемические отеки, асцит, гипокалиемия, гипокальциемия. Железодефицитная анемия. Дисахаридазная недостаточность. Хронический эрозивный гастрит, не ассоциированный с Helicobacter pylori, стихающее обострение. Стеатоз печени».
Проводилось лечение: АГД, коррекция метаболических нарушений (инфузии раствора альбумина и аминокислот, растворы электролитов, железа), внутривенные инфузии глюкокортикоидов (преднизолон 60 мг № 4) с переходом на пероральный прием в дозе 60 мг). На фоне терапии отмечено улучшение состояния: урежение стула, уменьшение отеков, нормализация лабораторных показателей – уровней гемоглобина, общего белка, альбумина, электролитов крови.
Выписана в удовлетворительном состоянии с рекомендациями: соблюдение АГД строго и пожизненно, продолжить прием глюкокортикоидов по схеме со снижением дозы, ингибиторы протонной помпы – на время приема преднизолона кальций Д3 длительно, препараты железа до нормализации уровней гемоглобина и сывороточного железа, ферментные препараты во время приема пищи, гастроэнтеропротектор ребамипид 100 мг 3 раза в день в течение 2 месяцев. Динамическое наблюдение в ГБУЗ МКНЦ им. А.С. Логинова и повторная госпитализация через 2 месяца для оценки эффективности терапии. Через 2,5 месяца больная повторно поступила в кишечное отделение ГБУЗ МКНЦ им. А.С. Логинова для динамического наблюдения.
Жалобы при поступлении: на выпадение волос, повышенное газообразование после употребления молочных продуктов. Общее состояние удовлетворительное. Вес – 62 кг, кожные покровы и видимые слизистые оболочки розовые, чистые. Периферические лимфоузлы не увеличены. Со стороны легких и сердца без отклонений от нормы. Язык влажный чистый. Живот не вздут, при пальпации мягкий, безболезненный. Стул оформленный – 1–2 раза в день. Почки не пальпируются. Симптом поколачивания отрицательный с обеих сторон. По данным лабораторных анализов, нормализация клинического и биохимического анализов крови: Hb – 13,0 г/л, сывороточное железо – 32,2 ммоль/л, общий белок – 62 г/л, альбумин – 37,3 г/л, уровни электролитов и трансаминаз в пределах нормальных значений. Оставался незначительно повышенным уровень АТ к тканевой трансглютаминазе IgA – 26 ЕД/мл (при норме до 10 Ед/мл) против показателей в предыдущую госпитализацию – 200 Ед/мл.
По данным ультразвукового исследования органов брюшной полости: диффузные изменения печени и поджелудочной железы.
Проведена ЭГДС: недостаточность кардии, очаговый гастрит, дуоденит, взята биопсия для морфологического исследования.
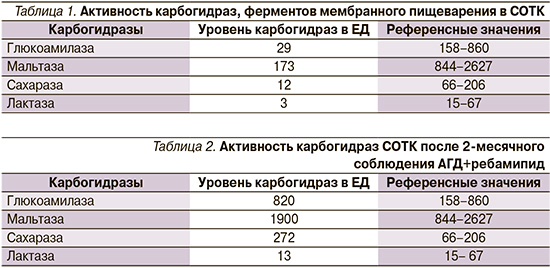
Заключение по морфологическому исследованию биоптатов: в препарате фрагменты слизистой оболочки из дистальных отделов двенадцатиперстной кишки; кишечные ворсины высокие, выстланы клетками высокого цилиндрического эпителия с наличием бокаловидных клеток; контуры щеточной каймы на некоторых участках размыты; крипты неглубокие, в дне крипт масса панетовских клеток; соотношение ворсинка/крипта – 3:1–4:1; количество межэпителиальных клеток – 20 на 100 эпителиоцитов; собственная пластинка неравномерно инфильтрирована лимфоцитами, плазмоцитами с незначительной примесью эозинофилов. Заключение: морфологическая картина может соответствовать глютеновой энтеропатии на фоне лечения АГД. По сравнению с первичной биопсией отмечается положительная динамика в виде практически полного восстановления структуры слизистой оболочки двенадцатиперстной кишки.
Как видно из данных табл. 2, активность исследуемых карбогидраз повысилась до нормальных значений, кроме лактазы, уровень которой оставался несколько ниже нормы.
Больная была выписана в удовлетворительном состоянии с рекомендацией строго пожизненного соблюдения АГД и динамического наблюдения через 1 год либо ранее при ухудшении самочувствия.
Обсуждение
Особенность данного клинического случая заключается в том, что у больной с тяжелым течением латентной целиакии, протекавшей с СНВ 3-й степени тяжести с гипопрортеинемическими отеками, асцитом, выраженными электролитными нарушениями, анемией, высокими значениями АТ к тканевой трансглютаминазе, тяжелой атрофией СОТК, соответствующей Marsh IIIC, дисахаридазной недостаточностью, через 2 месяца после установления диагноза и назначения терапии наступила полная ремиссия – клиническая, морфологическая, функциональная. Это может быть обусловлено быстрым назначением адекватного лечения, включившего АГД, глюкокортикоиды, коррекцию метаболических нарушений. При строгом соблюдении АГД клиническая ремиссия, нормализация иммунологических тестов наступают обычно в срок от 6 до 12 месяцев от начала лечения, а полное восстановление морфологической структуры СОТК и ее функциональной способности – через 1,5–3 года от начала терапии. После первой госпитализации больной был рекомендован препарат ребамипид, который она принимала в течение 2 месяцев. Можно полагать, что именно прием ребамипида стал причиной быстрого наступления клинической ремиссии, полного восстановления морфологической структуры СОТК и ее функционального состояния.
Заключение
Продемонстрирован клинический пример больной латентной формой целиакии, протекавшей с тяжелым СНВ, высокими значениями иммунологических тестов, тотальной атрофией СОТК (стадия Marsh IIIC), тяжелыми нарушениями мембранного пищеварения. У больной на фоне строгого соблюдения АГД и приема ребамипида уже через 2 месяца от начала терапии наступила полная клиническая и морфологическая ремиссия с нормализацией функционального состояния СОТК. Можно предполагать, что такое быстрое наступление полной ремиссии наступило в связи с приемом цитопротектора ребамипида.



