Введение
У каждого четвертого пациента с впервые выявленной меланомой кожи имеет место метастатическая или местнораспространенная неоперабельная стадия этой опухоли, что определяет неблагоприятный прогноз течения заболевания. Приоритетным направлением лечения на этих стадиях считается системная противоопухолевая терапия. Однако использование как химио-, так и иммунотерапии интерфероном альфа принципиально не влияет на общую продолжительность жизни пациентов с диссеминированной меланомой. Последнее десятилетие ознаменовалось значительным прорывом в фундаментальной и клинической онкологии, что существенно расширило перечень препаратов, используемых при этой злокачественной опухоли. Так, в практический арсенал системной терапии этой категории больных введен принципиально новый класс препаратов, блокирующих мутации BRAF и MEK через систему тирозинкиназ сигнального пути. Наряду с этим успешно развиваются направление, изучающее влияние иммунной системы на канцерогенез, и механизмы ускользания опухоли от иммунного надзора. В клиническую практику уже внедрены лекарственные препараты нового класса – модуляторы иммунологического синапса, или блокаторы иммунных контрольных точек, или просто иммуноонкологические лекарственные препараты – anti-CTLA-4 и anti-PD-1 [3, 4]. В данной статье представлен опыт СПбГБУЗ ГКОД в лечении метастатической меланомы у взрослых пациентов с оценкой эффективности применения ниволумаба, ингиботора PD-1.
Методы
Под нашим наблюдением находились 12 пациентов с диагнозом диссеминированной меланомы кожи, получавших лечение в СПбГБУЗ «Городской клинический онкологический диспансер» с 2002 г. по настоящее время. Среди обследованных были 8 женщин (66,7%) и 4 мужчины (33,3%). Возраст пациентов варьировался от 40 до 84 лет. Медиана возраста составила 59,5 лет (95% доверительный интервал [ДИ] – 49,0–67,65), средний возраст пациентов – 59,67±3,73 года (95% ДИ – 51,46–67,87).
При первичной постановке диагноза 1 (8,3%) пациенту стадия процесса была расценена как 1b; 8 (66,7%) – как 2; 2 (16,7%) – как 3b и у 1 (8,3%) больного стадия опухолевого процесса не была определена. У 3 пациентов первичный опухолевый очаг локализовался на коже шеи, у 3 – на коже спины, у 3 – на коже голени, оставшиеся 3 пациента имели поражение кожи подколенной области, торса и руки.
Время развития IV стадии заболевания (от момента первичной постановки диагноза меланомы кожи до выявления отдаленных метастазов) варьировалось от 5 месяцев до 12,5 лет. Медиана времени появления отдаленных метастазов составила 51,5 месяц (95% ДИ – 12,52–111,95). Среднее время развития IV стадии заболевания составило 59,83±15,10 месяца (95% ДИ – 26,61–93,06). Три пациента имели метастатическое поражение только 1 органа, 5 – 2, у 3 больных метастазы локализовались в 3 органах и у 1 выявлено метастатическое поражение 4 органов.
В рамках терапии диссеминированного процесса пациенты получили от 1 до 4 линий лечения цитостатиками и таргетными препаратами (дакарбазин, паклитаксел+карбоплатин, комбинация iBRAF и iMEK, интерферон, ипилимумаб): 4 пациента получили 1-ю линию лечения, 4 – 2-ю, 1 – 3-ю, 2 пациента получили 4 линии и только 1 больной из 12 не получал лекарственного лечения по поводу метастатического процесса. Причем следует особенно отметить, что 9 пациентов из 12 (75,0%) в рамках предшествовавшего лечения получали ипилимумаб. Время от момента регистрации IV стадии заболевания до начала терапии ниволумабом варьировалось от 4 до 31 месяца. Медиана времени до начала анти-PD-1-терапии составила 14,5 месяцев (95% ДИ – 5,69–23,00). Среднее значение данного показателя составило 16,08±2,80 (95% ДИ – 9,93–22,24).
На момент начала терапии ниволумабом общее состояние пациентов, оцененное по шкале ECOG, составило «0» у 1 больного, «1» – у 9 и «2» – у 2 пациентов. Десяти (83,3%) больным из 12 на догоспитальном этапе проведено молекулярно-генетическое исследование для выявления мутации в гене BRAF: опухоль 6 (60,0%) пациентов из 10 оказалась отрицательной по данному показателю, у 4 (40,0%) мутация была выявлена.
На этапе исходной оценки (на момент начала терапии ниволумабом) всем пациентам выполнены стандартные клинико-диагностические процедуры с определением уровня ЛДГ в сыворотке крови, а также был произведен расчет нейтрофильно-лимфоцитарного (НЛИ) и тромбоцитарно-лимфоцитарного (ТЛИ) индексов для оценки изначального иммунологического статуса и возможной корреляции с ответом опухоли на проводимое лечение.
Уровень ЛДГ сыворотки крови варьировался в пределах от 72 до 808 ЕД/л. Средний показатель уровня ЛДГ в данной группе пациентов составил 228,58±55,93 ЕД/л (95% ДИ – 105,48–351,68); медиана – 178,00 ЕД/л (95% ДИ – 138,70–191,62).
У 10 (83,3%) пациентов из 12 исходный уровень ЛДГ находился в пределах референсных значений, у 1 (8,35%) он был повышен в 2 раза от верхней границы нормы и у 1 (8,3%) – более чем в 2 раза.

Абсолютное число нейтрофилов (АЧН) на этапе исходной оценки варьировалось от 2,42 до 9,71×109/л, среднее значение АЧН составило 4,39±0,57×109/л (95% ДИ – 3,15–5,64), медиана – 3,83×109/л (95% ДИ – 3,28–5,02). В отношении большинства пациентов у 10 (83,3%) из 12 уровень АЧН находился в пределах референсных значений, у 2 (16,7%) – он был повышен.
Абсолютное число лимфоцитов (АЧЛ) на этапе исходной оценки в рассматриваемой когорте пациентов варьировалось от 0,54 до 3,26×109/л. Средний показатель АЧЛ составил 1,88±0,26×109/л (95% ДИ – 1,31–2,46); медиана – 1,85 (95% ДИ – 1,05–2,46). У 7 (58,3%) пациентов АЧЛ находилось в пределах референсных значений, у 2 (16,7%) – этот показатель был повышен, у 3 (25,0%) – находился ниже минимального референсного значения.
Исходный уровень тромбоцитов варьировался от 189,00 до 434,00×109/л. Среднее число тромбоцитов составило 265,33±18,81×109/л (95% ДИ – 223,94–306,73), медиана – 265,00 (95% ДИ – 213,11–280,83). Только у 1 (8,3%) пациента из 12 уровень тромбоцитов был выше максимального референсного значения.
Во всех случаях произведен расчет НЛИ и ТЛИ. НЛИ варьировался от 1,00 до 5,12, медиана НЛИ составила 2,56 (95% ДИ – 1,87–3,68), среднее значение – 2,79±0,38 (95% ДИ – 1,94–3,63). ТЛИ варьировался от 78,42 до 638,24. Медиана ТЛИ составила 126,46 (95% ДИ – 87,39–258,04), среднее значение – 205,58±53,17 (95% ДИ 88,56–322,60).
Результаты
К настоящему моменту времени (май 2018 г.) только у 3 (25%) пациентов из 12 зарегистрировано прогрессирование процесса. Время наблюдения за пациентами от начала лечения ниволумабом составило от 15 до 37 месяцев. Медиана времени без прогрессирования еще не достигнута. Среднее время без прогрессирования на этапе данного анализа составляет 25,75±3,13 месяца (95% ДИ – 19,61–31,89).
Медиана общей выживаемости также еще не достигнута: живы 10 (83,33%) из 12 пациентов. Причем следует отметить, что одногодичная общая выживаемость также составила 83,33%: 10 пациентов, получавших ниволумаб, живут более 12 месяцев. Среднее значение общей выживаемости сейчас составляет 28,27±2,49 месяца (95% ДИ – 23,30–33,03). В связи с малым числом пациентов и событий корреляционный анализ влияния уровня ЛДГ, НЛИ, ТЛИ в настоящий момент не демонстрирует значимых зависимостей.
В последующем планируется обосновать их предиктивную значимость.
Клинический пример
Пациентка Л. 1946 г.р. Из анамнеза известно, что в конце 2013 г. больная обратила внимание на невус на коже шеи слева, доставлявший ей эстетический дискомфорт. В непрофильном учреждении в начале декабря 2013 г. выполнено иссечение невуса без гистологического исследования.
В конце декабря 2014 г. пациентка самостоятельно отметила увеличение шейных лимфатических узлов. Проведено комплексное обследование: КТ-исследование органов груди и живота, ультразвуковое исследование периферических лимфатических узлов. Выявлено множественное метастатическое поражение лимфатических узлов (шейных, надключичных с обеих сторон), множественные билобарные очаги в печени.
С целью гистологической верификации 18.12.2014 выполнена биопсия надключичного лимфатического узла слева. При гистологическом, иммуногистохимическом и молекулярно-генетическом исследованиях установлен диагноз «метастаз меланомы кожи без мутации в гене BRAF».
С учетом удовлетворительного общего состояния пациентки (статус по шкале ECOG=1), клинико-лабораторных показателей в пределах незначимых отклонений, «дикого типа» BRAF, отсутствия выраженной сопутствующей патологии, существующих стандартов лечения, отсутствия возможности включения больной в клинические исследования с января 2015 г. начата полихимиотерапия 1-й линии в режиме паклитаксел 175 мг/м2+карбоплатин AUC-5. Однако после двух циклов лечения отмечено прогрессирование опухолевого процесса в забрюшинных лимфатических узлах, селезенке и в т.ч. появление метастазов в головном мозге. С учетом поражения головного мозга пациентка консультирована нейрохирургом и радиологом рекомендовано проведение радиохирургического лечения, которое выполнено в марте 2015 г.
В 2015 г. в СПбГБУЗ «Городской клинический онкологический диспансер» была инициирована программа расширенного доступа к лечению препаратом ипилимумаб, в которую и была включена данная больная. С апреля по июнь 2015 г. проведено лечение по схеме: ипилимумаб 3 мг/кг массы тела в виде 90-минутной внутривенной инфузии, вводимой каждые 3 недели. Были зарегистрированы нежелательные явления от проводимой терапии в виде слабости и диарея 2-й ст., потребовавшие назначения кортикостероидов в стандартных дозах. Нежелательные явления разрешились в течение 4 недель. Однако и на данной терапии у пациентки было зарегистрировано прогрессирование заболевания с ростом очагов в легких и головном мозге.
В июле 2015 г. проведено повторное радиохирургическое лечение. Однако при контрольной магнитно-резонансной томографии головного мозга на фоне уменьшения всех предыдущих очагов появился новый очаг метастазирования в головном мозге. Принято решение о тотальном церебральном облучении, выполненном в августе–сентябре 2015 г. Параллельно по данным КТ органов брюшной полости в августе 2015 г. выявлены множественные метастазы в обеих долях печени. На рис. 1 представлены некоторые, наиболее информативные сканы КТ с метастазами в печень (август 2015 г.).
Несмотря на прогрессирование на 1-й (химиотерапия паклитаксел+карбоплатин) и 2-й линиях системного лечения (иммунотерапия ипилимумабом), поражение головного мозга (неблагоприятный фактор прогноза), с учетом удовлетворительного общего состояния (ECOG 0–1) с сентября 2015 г. начата 3-я линия системной терапии препаратом ниволумаб, обладающим anti-PD-1-активностью, в дозе 3 мг/кг каждые 2 недели.
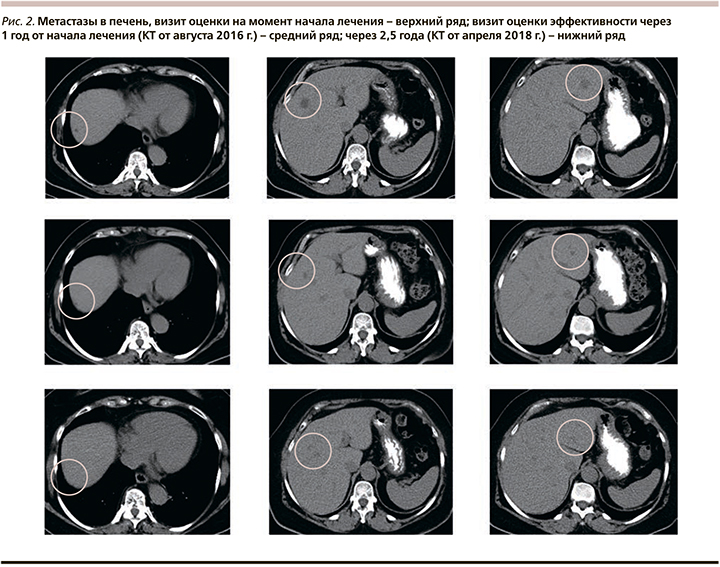
В результате проведения 3-й линии anti-PD-1-терапии ниволумабом отмечен частичный регресс опухолевого процесса в печени с продолжительностью ответа более 2 лет (рис. 2).
По последней оценке результатов лечения (май 2018 г.) проведено 68 введений ниволумаба. По результатам КТ брюшной полости в апреле 2018 г. не отмечено признаков прогрессирования. Общее состояние пациентки остается удовлетворительным (ECOG 0-1), по данным КТ-обследования сохраняется частичный регресс опухолевого процесса на фоне 3-й линии лечения. Пациентка продолжает получать ниволумаб и остается под динамическим наблюдением.
Общая выживаемость пациентки с момента установления 4-й стадии заболевания составила 3,5 года, из них на фоне терапии ниволумабом – 2,5 года. И несмотря на метастатическое поражение головного мозга, по поводу которого было предпринято неоднократное лучевое лечение (радиохирургическое лечение, тотальное облучение всего головного мозга), на данный момент состояние пациентки стабильное и клинически, и по данным объективных методов обследования. Применение современных методов лечения с индивидуальным подходом к больному в реальной клинической практике, без сомнения, дает надежду пациентам с диагнозом метастатической меланомы.
Заключение
Проведенный нами анализ подтверждает высокую эффективность использования иммуно-онкологических препаратов, таких как блокатор PD-1 ниволумаб, в лечении метастатической меланомы, что подтверждается результатами не только многочисленных международных исследований [5, 6], но и нашим клиническим опытом использования этих препаратов в течение последних лет. Важно отметить, что применение ниволумаба помимо достижения объективного ответа позволяет длительно удерживать достигнутый эффект [1, 2]. Таким образом, ингибиторы PD-1 становятся новым стандартом терапии метастатической меланомы.



