Даже в отсутствие какого бы то ни было лечения в первые месяцы после острого повреждения головного мозга (инсульт, черепно-мозговая травма и др.) наблюдается спонтанный регресс неврологических расстройств. Наиболее активно данный процесс протекает в течение первого года после острого церебрального повреждения. Поэтому, согласно общепринятым представлениям, первые 12 месяцев после острого нарушения мозгового кровообращения (ОНМК) называют восстановительным периодом инсульта. Иногда его разделяют на два этапа: ранний восстановительный (первые 6 месяцев) и поздний восстановительный (6–12 месяцев после ОНМК). При этом, чем меньше времени прошло от острого церебрального повреждения, тем быстрее темпы спонтанного восстановления неврологических функций [1–3].
Механизмы восстановления неврологических функций
В основе регресса неврологических расстройств в восстановительном периоде инсульта лежит ряд репаративных процессов. В наиболее ранние сроки (первые дни) после церебральной катастрофы решающее значение имеет уменьшение выраженности локального отека и снятия диашиза (функционального паралича) жизнеспособных нейронов. Как известно, головной мозг на любое локальное повреждение реагирует перифокальным отеком. Он увеличивает зону функционально неактивных нейронов, в то же время не вызывая их необратимого повреждения. Регресс локального отека приводит к восстановлению функциональной активности неповрежденных нейронов под воздействием проводимой терапии или спонтанно [4–6].
Из клинической практики хорошо известно, что ОНМК, особенно с обширной зоной церебрального повреждения, часто сопровождаются изменением состояния сознания, которое в 10–40% случаев может достигать выраженности острой спутанности сознания, ассоциированной с такой локализацией инсульта, как:
- дорзомедиальные и передние отделы таламуса;
- лево- или двустороннее поражение задневисочно-затылочных долей (бассейн задней мозговой артерии);
- право- или двустороннее поражение медиобазальных лобных отделов (бассейн передней мозговой артерии);
- головка хвостатого ядра;
- колено внутренней капсулы;
- правая височная доля (бассейн средней мозговой артерии).
Патофизиологические механизмы данного феномена не совсем ясны: предполагается, что в основе нарушений сознания могут лежать отек головного мозга, активация гипоталамо-гипофизарно-надпочечниковой системы и как следствие – гиперкортицизм или же дисбаланс нейротрансмиттерных систем (ацетилхолинергической, дофаминергической и др.). Нормализация уровня сознания в раннем восстановительном периоде инсульта неизбежно сопровождается уменьшением выраженности когнитивных и других неврологических нарушений [7].
Регресс локального отека, снятие диашиза и нормализация уровня сознания играют саногенетическую роль – в основном в первые дни после острого инсульта. В дальнейшем уменьшение выраженности неврологических расстройств связано в большей степени с другими механизмами, такими как нейропластичность и реадаптация.
Нейропластичность является одним из фундаментальных свойств нервной ткани и важнейшим условием ее адекватного функционирования. Под нейропластичностью понимается способность головного мозга к изменению своих морфологических и функциональных свойств. В основе нейропластичности лежит способность к образованию новых нейронов (нейрогенез), а также микроструктурные и функциональные изменения существующих нейронов [4, 8].
Первые экспериментальные доказательства нейрогенеза были представлены еще в 1962 г. [9]. В настоящее время нет никаких сомнений в том, что нейрогенез представляет собой одну из базисных особенностей функционирования головного мозга и наблюдается в течение всей жизни. При этом в головном мозге приматов ежедневно образуется от 20 до 40 тыс. новых нейронов [10–12].
В головном мозге человека нейрогенез осуществляется в двух отделах: субгранулярной зоне зубчатой извилины гиппокампа и субэпендимальных отделах боковых желудочков [10]. При этом вначале происходят пролиферация и деление стволовых клеток мозга, затем селекция нейробластов путем апоптоза «ненужных» клеток, миграция новообразованных клеток из первичных зон нейрогенеза к ольфакторным луковицам и далее радиально к месту конечного назначения. Показано, что в восстановительном периоде инсульта местом конечного назначения служит в первую очередь периинфарктная зона. Уже непосредственно в периинфарктной зоне происходит дифференцировка новообразованных клеток в зрелые нейроны, астроциты и олигоденроциты и их включение в нейрональные сети путем образования синаптических и функциональных связей с другими нейронами [9–15].
Как известно из экспериментальных данных, локальная церебральная ишемия и гипоксия являются одними из факторов, активирующих процессы нейрогенеза. Другим важным активирующим фактором служит создание т.н. обогащенной внешней среды.
В экспериментальных условиях она создается путем полимодальной сенсорной стимуляции экспериментальных животных (зрительной, слуховой, тактильной), их побуждения к большей двигательной активности, например игровой, предоставления полноценного и оптимального питания [13, 14]. Можно обоснованно предположить, что у человека в реальной клинической практике методом создания «обогащенной среды» является активное проведение реабилитационных мероприятий: они предусматривают как сенсорную, так и двигательную и когнитивную стимуляцию. Большое значение имеет также положительное эмоциональное подкрепление и создание максимально возможного эмоционального комфорта. Указанные мероприятия, возможно, способствуют усилению процессов нейрогенеза и, следовательно, увеличению темпов , а также выраженности восстановления неврологических функций.
Нейрогенез не является ни единственным, ни главным механизмом нейропластичности. Число новообразованных в результате этого процесса нейронов ничтожно мало по сравнению с общей массой головного мозга. Поэтому, возможно, существенно большее значение для церебральных репаративных процессов имеет микроструктурная и функциональная перестройка зрелых и давно сформированных нейронов. В процессе жизнедеятельности нейроны головного мозга непрерывно изменяют число дендритов, шипиков, образуют новые синапсы и новые нейрональные сети [4, 15]. Эти процессы формируют базис познавательной деятельности человека, т.к. лежат в основе приобретения новых знаний и навыков. Восстановление нарушенных неврологических функций после инсульта по своей сути также представляет собой не что иное, как когнитивный процесс: головной мозг приобретает новые навыки по управлению телом в изменившихся условиях. Исследования свидетельствуют, что после инсульта наблюдается весьма активная структурно-функциональная перестройка на клеточном уровне, в особенности в противоположном полушарии головного мозга, в отделах, симметричных очагу поражения [4, 16–21].
Третьим механизмом уменьшения степени функционального ограничения после инсульта является реадаптация. Под этим термином принято понимать приспособление пациента к имеющемуся дефекту. Например, пациент может активнее использовать здоровую конечность, которая начинает выполнять часть функций паретичной. При этом происходит уменьшение степени функциональной недостаточности в отсутствие регресса неврологической симптоматики. Следует отметить, что если процессы нейрогенеза и нейропластичности наиболее активны в первые месяцы после инсульта, то реадаптация может продолжаться в течение существенно большего времени – фактически всю оставшуюся жизнь [1–3].
Роль глутаматергической системы в церебральной репарации
Весьма сложным и не до конца изученным остается вопрос медикаментозной поддержки процессов нейропластичности и нейрогенеза. Теоретически благоприятное воздействие может оказывать модуляция активности церебральной глутаматергической системы. Это связано с тем значением, которое имеет для когнитивного, а следовательно, репаративного процесса феномен постсинаптической потенциации (ПСП). Он связан с наличием на постсинаптической мембране глутаматергического синапса двух типов ионных каналов: быстрых, снабженных АМРА-рецепторами, и медленных, снабженных NMDA-рецепторами. Медленные ионные каналы открываются лишь при определенном отклонении мембранного потенциала от исходного значения в результате активации быстрых АМРА-рецепторов. Их открытие ведет к накоплению внутриклеточного кальция, который затем в отсутствие повторных активаций медленно выводится из клетки. Медленный темп выведения ионов кальция обусловливает достаточно длительное сохранение мембранного потенциала в измененном состоянии. Благодаря этому повторное возбуждение постсинаптической мембраны достигается легче, что облегчает повторное проведение импульсов по активным и функционально значимым нейрональным сетям (феномен «проторения пути») [19–21].
Как при сосудистом, так и при нейродегенеративном процессе нормальный паттерн синаптической передачи в глутаматергических синапсах нарушается вследствие патологического увеличения активности церебральной глутаматергической системы [5, 22, 23]. Это приводит к появлению феномена ПСП как в функционально значимых, так и в незначимых синапсах. Поэтому физиологический смысл ПСП как феномена, призванного выделять из множества функциональных систем головного мозга наиболее важные в актуальной ситуации, теряется. В результате обучение, приобретение новых знаний и, следовательно, церебральные репаративные процессы значительно затрудняются.
В то же время на фоне использования обратимого антагониста НМДА-рецепторов к глутамату Акатинола Мемантина происходит «дозированное» повышение порога чувствительности постсинаптической глутаматергической мембраны, что нормализует паттерн синаптической передачи. Данный эффект препарата лежит в основе положительного симптоматического эффекта Акатинола Мемантина при когнитивных нарушениях различной этиологии, который в настоящее время абсолютно доказан и ни у кого не вызывает сомнений [22–24]. Однако, исходя из вышеизложенного, данный эффект не менее важен для медикаментозной поддержки церебральных репаративных процессов после острого повреждения головного мозга. Действительно, существует ряд наблюдений, о чем будет сказано ниже, который свидетельствует, что на фоне использования Акатинола Мемантина в восстановительном периоде инсульта отмечается уменьшение не только выраженности постинсультных когнитивных расстройств (КР), но и выраженности инвалидизации пациентов в целом [25].
Предикторы восстановления неврологических функций после инсульта
Темпы и степень восстановления нарушенных неврологических функций после ишемического инсульта (ИИ) зависят от ряда факторов [2–4]: возраста пациентов, объема и локализации очага повреждения головного мозга, наличия и выраженности когнитивных и эмоциональных расстройств, а также активности, корректности и своевременности реабилитационных мероприятий.
С возрастом процессы нейрогенеза и нейроплатичности замедляются. Поэтому клинический опыт свидетельствует о том, что компенсаторные возможности головного мозга максимальны в детском и юношеском возрасте и прогрессивно уменьшаются по мере старения. К общим правилам относится следующее положение: чем в более позднем возрасте произошло ОНМК, тем менее быстрым и полным будет регресс неврологических нарушений [3, 4, 26].
Несомненное прогностическое значение имеют объем и локализация очага повреждения головного мозга. Очевидно, что чем больше объем ишемического очага, тем на меньшую степень восстановления неврологических функций следует рассчитывать. Менее благоприятного исхода следует также ожидать при поражении функционально значимых зон головного мозга [4].
Важным предиктором исхода восстановительного периода ИИ является наличие и выраженность когнитивных и эмоционально-поведенческих нарушений, которые часто тесно связаны между собой. Многочисленные клинические наблюдения свидетельствуют о том, что наличие значительных когнитивных нарушений служит неблагоприятным фактором, ассоциированным с низким темпом и небольшой степенью восстановления неврологических функций [3, 4, 26]. Влияние когнитивных и других нервно-психических расстройств на исход восстановительного периода инсульта может иметь несколько объяснений. Во-первых, значительная выраженность КР свидетельствует о тяжелом морфологическом поражении головного мозга, которое часто не ограничено церебральным инфарктом. Так, по данным ряда авторов, у 90% пациентов с когнитивными нарушениями, впервые диагностированными после инсульта, использование методик ретроспективной диагностики позволяет обоснованно заподозрить наличие когнитивных нарушений еще до ОНМК. При этом у 25% больных эти нарушения предположительно достигали выраженности деменции. Нейропсихологические методы исследования свидетельствуют, что приблизительно треть случаев т.н. постинсультных КР, вероятно, связана с сопутствующим нейродегенеративным процессом (болезнью Альцгеймера) [25, 27, 28]. Очевидно, что наличие тяжелого сопутствующего поражения головного мозга, в особенности прогрессирующего нейродегенеративного процесса, крайне снижает как вероятность спонтанного восстановления неврологических функций, так и эффективность реабилитационных мероприятий.
Во-вторых, наличие когнитивных и в особенности коммуникативных расстройств препятствует проведению реабилитационных мероприятий, т.к. пациенты не вполне понимают рекомендаций врача. К аналогичному результату может приводить наличие эмоциональных расстройств, таких как депрессия и апатия. Пациенты с указанными эмоционально-поведенческими нарушениями не выполняют рекомендаций по реабилитации из-за мотивационных расстройств.
Наконец, в основе восстановления нарушенных неврологических функций после инсульта и в основе познавательного процесса лежат аналогичные нейрофизиологические механизмы: нейропластичность, формирование новых синапсов и новых функциональных систем. Следовательно, благоприятное влияние нейрофизиологических механизмов на общие для познавательной деятельности церебральные репаративные процессы будет способствовать регрессу как КР, так и постинсультного неврологического дефицита в целом.
Улучшение когнитивных функций и нейрореабилитация
Исходя из вышеизложенного, оптимизация когнитивных функций может способствовать более эффективной нейрореабилитации. Это положение подтверждается результатами проведенных исследований [25].
В настоящее время для уменьшения выраженности КР используются нейрометаболическая терапия, тренировка памяти и внимания (когнитивный тренинг) и лекарственные средства, воздействующие на процессы синаптической передачи [22, 23, 29, 30]:
- Нейрометаболические препараты:
- производные пирролидона (пирацетам, фенотропил, фенибут и др.);
- пептидергические и аминокислотные препараты (Актовегин, цитиколин, Церебролизин, Кортексин, холина альфосцарат и др.);
- антиоксиданты (этилметилгидроксипиридина сукцинат, гинкго билоба);
- вазотропные препараты (винпоцентин, нимодипин).
- Нейротрансмиттерные препараты:
- ингибиторы ацетилхолинэстеразы (донепизил, ривастигмин, галантамин, ипидакрин);
- мемантин (Акатинол Мемантин – обратимый блокатор НМДА-рецепторов);
- α-адреноблокаторы (ницерголин, дигидроэргокриптин, пирибедил).
Доказанным положительным эффектом в отношении когнитивных функций при их расстройствах различной этиологии обладает Акатинол Мемантин. Механизм действия данного препарата заключается в нормализации глутаматергической передачи в синапсах головного мозга. Как известно, церебральная ишемия и гипоксия, равно как и нейродегенеративный процесс, сопровождаются увеличением глутаматергической активности, что приводит к нарушениям процессов обучения и памяти (см. выше) и ускоряет гибель нейронов (феномен эксайтотоксичности). Акатинол Мемантин является неконкурентным обратимым блокатором НМДА-рецепторов к глутамату. Он повышает порог возбудимости постсинаптической мембраны глютаматергического синапса, тем самым препятствует патологическому увеличению глутаматергической активности. Важно подчеркнуть, что действие Акатинола Мемантина строго дозировано и никогда не приводит к полной блокаде синаптической передачи. Поэтому глутамат продолжает выполнять свою физиологическую роль, в то время как патологическая эксайтотоксичность уменьшается.
Многочисленные экспериментальные работы свидетельствуют о нейропротективном эффекте Акатинола Мемантина как при ишемическом, так и при нейродегенеративном повреждении головного мозга. Показано, что добавление мемантина в культуру клеток гиппокампа, других корковых зон, сетчатки уменьшало повреждающий эффект глутамата или его агонистов без нарушения процессов формирования долговременной постсинаптической потенциации. Последнее свидетельствует об отсутствии полной блокады синаптической передачи и сохранении способности к обучению, приобретению новых знаний и навыков. В отличие от Акатинола Мемантина использование необратимых блокаторов НМДА-рецепторов (+МК-801) вело к нарушению физиологической роли глутаматергической системы [31–34].
Нейропротективный эффект Акатинола Мемантина был показан в ряде работ, посвященных моделированию острой локальной или глобальной церебральной ишемии. При этом предварительное введение высоких доз Акатинола Мемантина способствовало уменьшению зоны ишемического очагового повреждения головного мозга у экспериментальных животных [31, 34–37]. В работах P.E. Stieg и соавт., 1993 [36], Wang и соавт., 1995 [38], Chen и соавт., 1998 [37], было получено, что введение мемантина в первые 30 минут–2 часа после моделирования локальной церебральной ишемии приводит к уменьшению зоны инфаркта мозга по сравнению с таковой в контрольной группе. В других исследованиях введение Акатинола Мемантина в остром периоде глобальной церебральной ишемии способствовало уменьшению выраженности последующих КР [35, 39]. При этом на фоне использования Акатинола Мемантина наблюдалось более полное восстановление не только когнитивных, но и других неврологических функций, что согласуется с изложенными выше теоретическими предпосылками [40].
Косвенным клиническим подтверждением нейропротективного эффекта Акатинола Мемантина является положительная динамика бимаркеров нейродегенеративного процесса в спинномозговой жидкости на фоне использования данного препарата. Об этом сообщают О.В. Успенская и Н.Н. Яхно, которые назначали данный препарат пациентам с амнестическим типом синдрома умеренных когнитивных нарушений (предположительно продромальный период болезни Альцгеймера) [41].
В клинической практике Акатинол Мемантин широко и успешно применяется при деменциях различной этиологии и степени выраженности [42–45]. Есть также положительный опыт использования данного препарата при умеренных когнитивных нарушениях [46, 47].
Целесообразно и обоснованно использование Акатинола Мемантина в восстановительном периоде ОНМК при наличии клинически значимых когнитивных нарушений. Оценку когнитивных способностей после перенесенного инсульта можно проводить уже в первые дни при условии ясного сознания пациента. По данным Л.В. Климова и соавт., оценка когнитивных функций на 2–4-е сутки после ИИ достоверно коррелирует с состоянием когнитивных способностей в дальнейшем, в т.ч. по завершении раннего восстановительного периода. С учетом значения когнитивных функций для нейрореабилитации, о чем говорилось выше, фармакотерапию КР следует начинать как можно раньше [48].
О положительном влиянии терапии Акатинолом Мемантином на когнитивные и другие неврологические функции пациентов в восстановительном периоде ИИ сообщают В.А. Парфенов и соавт. [26]. Авторы проанализировали результаты наблюдения за 40 пациентами (средний возраст – 68,5+3,4 года), которые перенесли ИИ и имели легкую или умеренную выраженность неврологических расстройств, а также постинсультные КР. Все пациенты получали базисную терапию, направленную на профилактику повторного инсульта (антитромбоцитарные, антигипертензивные, гиполипидемические препараты). Кроме того, 20 пациентов, в дополнение к базисной терапии получали Акатинол Мемантин в дозе 20 мг/сут. Акатинол Мемантин назначали с 7–10-го дня после ОНМК, срок наблюдения составил 3 месяца. Исследование носило открытый контролируемый проспективный характер.
Характеристики сравниваемых терапевтических групп представлены в таблице.
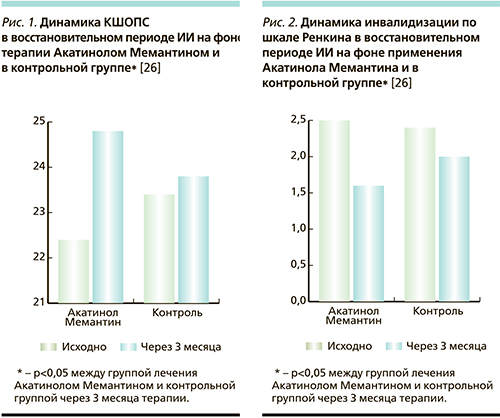
На фоне использования Акатинола Мемантина был зафиксирован более быстрый и выраженный регресс КР по всем используемым в работе нейропсихологическим тестам (краткая шкала оценки психического статуса, батарея лобных тестов, тест рисования часов) по сравнению только с базисной терапией (рис. 1).
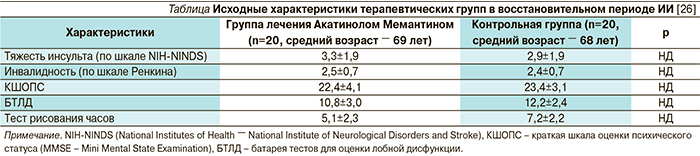
Одновременно был отмечен и более значимый регресс общей выраженности степени инвалидиации, оцениваемый по шкале Ренкина (рис. 2).
Приведенные данные согласуются с предположением о том, что использование Акатинола Мемантина в восстановительном периоде ИИ способствует не только уменьшению выраженности КР, но и регрессу инвалидизации вследствие неврологических нарушений в целом.
Исключительно важной для использования пожилыми пациентами особенностью Акатинола Мемантина являются его высокий уровень безопасности и хорошая переносимость. Более чем 40-летний опыт практического применения свидетельствует, что данный препарат не вызывает опасных для жизни и здоровья осложнений. Его можно назначать пациентам с сопутствующими соматическими заболеваниями, в т.ч. сердечно-сосудистой системы и печени. Осторожность и уменьшение терапевтической дозы требуются пациентам с почечной недостаточностью. Единственным противопоказанием к назначению мемантина является неконтролируемая эпилепсия, т.к. теоретически препарат может увеличивать судорожную активность головного мозга.
Акатинол Мемантин не воздействует на печеночные цитохромные ферментативные системы, поэтому не образует лекарственного взаимодействия с другими лекарственными средствами. Следовательно, Акатинол Мемантин можно комбинировать с другими лекарствами, улучшающими когнитивные функции: нейрометаболической терапией, ингибиторами церебральной ацетилхолинэстеразы [24, 49, 50].
За последние годы весьма активно обсуждается эффективность немедикаментозных методов коррекции КР. Предполагается положительное влияние на когнитивные нарушения физической активности и систематических упражнений по тренировке памяти и внимания [51]. Строго говоря, имеющиеся в настоящее время результаты исследования не позволяют делать каких-либо однозначных выводов. Большинство работ носит наблюдательный характер и анализирует риски возникновения, а также прогрессирования КР в целом, а не только в восстановительном периоде инсульта [29, 30].
Заслуживает особого внимания исследование L.D. Baker и соавт., которые рекомендовали пожилым женщинам с высоким риском развития когнитивных нарушений систематические занятия аэробным фитнесом в течение 6 месяцев. Было показано достоверное улучшение когнитивных показателей, управляющих функций головного мозга на этом фоне [52]. Исходя из того что нарушения управляющих функций чаще всего имеют сосудистую природу, можно предполагать, что физическая активность оказывает благоприятное воздействие на сосудистые когнитивные нарушения, не достигающие выраженности деменции.
Таким образом, наличие когнитивных нарушений после перенесенного ОНМК не только ухудшает качество жизни пациента и его родственников, но и ассоциировано с менее эффективной нейрореабилитацией. Поэтому целесообразна как можно более ранняя оценка когнитивного статуса (при условии ясного сознания) и начало терапии. В качестве препарата выбора при постинсультных КР можно рекомендовать обратимые блокаторы НМДА-рецепторов (Акатинол Мемантин), на фоне использования которых отмечается как когнитивное улучшение, так и регресс степени инвалидизации в целом.



