Экзогенный аллергический альвеолит (ЭАА) – общее название группы аллергических пневмопатий, которые возникают вследствие аллергической реакции легочной ткани на интенсивные и длительные ингаляции определенного антигена. Заболевание представляет собой диффузный гранулематозный воспалительный процесс альвеол и интерстициальной ткани легких, развивающийся под влиянием интенсивной и продолжительной ингаляции органических и неорганических антигенов [1, 2, 5–11]. Термин “экзогенный аллергический альвеолит” был предложен J. Pepys в 1967 г. В литературе встречаются и другие названия этой патологии: “гиперчувствительный пневмонит”, “ингаляционная пневмопатия”, “диффузная интерстициальная пневмония”, “интерстициальный гранулематозный пневмонит”, “зерновая лихорадка” [7, 10, 11, 14–16].
Согласно классификации пневмокониозов, принятой в 1996 г. НИИ медицины труда РАМН (утверждена методическими указаниями № 95/235 МЗ и МП РФ), ЭАА относится к группе пневмокониозов, развивающихся от воздействия аэрозолей токсикоаллергического действия [8].
Этиология
Этиологические факторы, вызывающие развитие профессионального ЭАА, можно разделить на несколько групп [4–8]:
• микроорганизмы (бактерии, термофильные актиномицеты, грибы, простейшие) и продукты их жизнедеятельности (эндотоксины, белки, глико- и липопротеиды, полисахариды, ферменты);
• биологически активные субстанции животного (сывороточные белки, шерсть животных и пр.) и растительного происхождения (опилки деревьев, заплесневелая солома, экстракты кофейных зерен);
• низкомолекулярные соединения (тяжелые металлы и их соли, диизоцианат толуола, тримелитиковый ангидрид и др.), а также многие лекарственные препараты (антибиотики, интал, нитрофураны, антиметаболиты, антимитотические препараты, ферменты, гормоны и др.).
Заболевание под названием “легкое фермера” впервые описано J. Campbell в 1932 г., исследовавшим пять фермеров, у которых наблюдалось развитие острых респираторных симптомов после работы с влажным заплесневелым сеном [13]. Ведущими причинными агентами, приводящими к развитию “легкого фермера”, являются термофильные актиномицеты – бактерии размером менее 1 мкм, обладающие морфологическими свойствами грибов; они широко встречаются в почве, компосте, в воде (табл. 1).
Наиболее частыми видами термофильных актиномицет, ассоциированными с ЭАА, являются Мicropolysporafaeni, Thermoactinomycesvulgaris, Thermoactinomycesviridis, Thermoactinomycessaccharis, Thermoactinomycescandidum. Данные микроорганизмы размножаются при температуре 50–60 °С, т. е. в тех условиях, которые достигаются при прении и гниении органического материала [2, 8, 10, 11].
Описаны случаи ЭАА у зерноводов, тростниководов, хлопкоробов и хлопкопереработчиков, табаководов, мукомолов, сыроделов, скорняков, обувщиков, шлифовальщиков риса, производителей пеньки, рабочих овощехранилищ, зернохранилищ, кофейных плантаций, лиц, изготавливающих солод, лекарственные препараты, в этиологии которых важная роль отводится истинным грибам, термофильным и другим бактериям, бактериальным продуктам (эндотоксинам, гликопротеидам), животным белкам, белкам рыбы, водорослей, растительной пыли.
Возможно развитие ЭАА у работников, контактирующих с пластмассами, полиуретаном, смолами, красителями. Наибольшее значение имеют диизоцианаты, фталиковый ангидрит. Известны случаи ЭАА при воздействии солей тяжелых металлов (хрома, кобальта, золота, мышьяка, меди, цинка), инсектицидов, особенно при использовании сульфата меди для опрыскивания фруктовых деревьев, виноградников, томатов, соединений диизоцианата (диизоцианат толуола, диизоцианат гексаметилена, диизоцианат дифенилметана), широко применяемых в автомобильной, резиновой, лакокрасочной промышленности, в производстве полиуретанов (табл. 2).
ЭАА описан у рабочих производств лекарственных препаратов, а также у больных при использовании ими, например, препаратов из гипофиза крупного рогатого скота (питуитрина, адиурекрина), применяемых в виде ингаляции при лечении несахарного диабета. Тяжелые случаи ЭАА описаны у рабочих производства пепсина, трипсина, пенициллина, стрептомицина, амиодарона, антимитотических препаратов: метотрексата, азатиоприна, 6-меркаптопурина [3, 4, 8].
Патогенез
У большинства больных “легким фермера” были обнаружены преципитирующие антитела к экстрактам заплесневелого сена. Экзогенный аллергический альвеолит считается иммунопатологическим заболеванием, в развитии которого ведущая роль принадлежит аллергическим реакциям 3-го и 4-го типов (по классификации Gell, Coombs), имеет значение и неиммунное воспаление. Циркулирующие иммунные комплексы и специфические антитела активируют систему комплемента и альвеолярные макрофаги. Последние выделяют интерлейкин-2, хемотаксические факторы, протеолитические ферменты, активные кислородные радикалы, способствующие росту фибробластов, продукции коллагена. В результате развивается альвеолобронхиолит, происходит образование гранулем, фиброзирование интерстиция легких.
Для всех видов экзогенного альвеолита, обусловленного действием химических соединений, наряду с развитием иммунных реакций характерно наличие различных токсических поражений легочной ткани (локальных и общих). При данном типе ЭАА почти всегда обнаруживают антитела к комплексам (соответствующее химическое соединение – белок). Выявляются при этом как IgG-антитела, так и IgЕ-антитела той же специфичности.
Клиника
Различают острый, подострый и хронический аллергический альвеолит. Характер течения ЭАА определяется длительностью контакта с антигеном: интермиттирующий контакт с антигеном ведет к острым реакциям, длительный – к хроническому прогрессирующему процессу, когда чрезвычайно трудно заподозрить его аллергический генез.
Для острой формы ЭАА от воздействия органической пыли (“легкого фермера”) характерно появление лихорадки, озноба, недомогания, кашля, одышки (но без астматического компонента) через 4–8 часов после работы с прелым сеном или другими причинными факторами. Его нередко принимают за грипп или пневмонию.
При острой форме ЭАА возможно развитие процесса по пневмониеподобному варианту, когда на первый план выходит выраженная одышка, в легких прослушиваются крепитация, хрипы. При элиминации антигена в течение нескольких дней больные выздоравливают. Возможен также астмоидный вариант заболевания, при котором через 15–20 минут после контакта с соответствующим антигеном наблюдается клиническая картина, весьма сходная с таковой при приступе бронхиальной астмы: явления удушья, в легких выслушиваются свистящие хрипы, после разрешения приступа выделяется серозная мокрота. При любых вариантах острого течения ЭАА выявляется т. н. симптом понедельника (эффект элиминации): за выходные дни (если антиген связан с профессиональной деятельностью) состояние больного улучшается, практически исчезают жалобы и клинические проявления ЭАА, а в первый же день выхода на работу все возобновляется [1, 10].
Подострая форма протекает скрыто в течение нескольких недель после воздействия, проявляясь кашлем и одышкой, и может прогрессировать до появления цианоза и нарушения дыхания, когда требуется госпитализация больного. Иногда подострая форма может развиться после острой, особенно при продолжающемся воздействии антигена. У многих больных острой и подострой формами ЭАА субъективные и объективные признаки болезни исчезают через несколько дней, недель или месяцев после прекращения воздействия вредного фактора. В противном случае болезнь может перейти в хроническую форму, но частота подобной трансформации неизвестна.
Хроническая форма заболевания может быть представлена постепенно прогрессирующей интерстициальной болезнью легких, сопровождающейся продуктивным кашлем и одышкой при физической нагрузке, похуданием без предшествующих проявлений острой или подострой формы. Постепенное начало заболевания происходит при воздействии низких доз антигена. При аускультации в легких выслушиваются мелко- и среднепузырчатые влажные хрипы, ослабленное дыхание, при перкуссии определяется коробочный оттенок звука. Развивается булавовидная деформация концевых фаланг пальцев по типу “барабанных палочек” (Finger clubbing), т. н. пальцы Гиппократа (digiti Hippocratici), что связано с нарушением трофики надкостницы и вегетативной иннервации на фоне длительной эндогенной интоксикации и гипоксемии. В дальнейшем у больных развивается хроническое легочное сердце с прогрессирующей недостаточностью кровообращения.
Среди вариантов ЭАА, развивающихся от воздействия лекарственных препаратов, известны “амиодароновое” и “метатрексатовое легкое” [3, 4, 12]. Известно, что особенности фармакокинетики амиодарона обусловливают характерный для него профиль легочной токсичности, что во многом связано с очень длительным периодом полувыведения – в течение 6–12 месяцев. Характерны медленное начало, вялотекущее улучшение после отмены препарата, возможное развитие или рецидив симптомов после прекращения приема. Поражение легких, вызванное амиодароном, развивается во временнoм интервале от несколько недель до нескольких лет терапии данным лекарственным средством (в среднем через 18–24 месяца).
“Метотрексатовое” легкое может развиться при любой продолжительности приема препарата, но риск возникновения пневмопатий выше при длительности терапии в течение одного года. Пневмопатия, обусловленная метотрексатом, характеризуется подострым течением (недели от начала приема), реже – острым (дни) и хроническим (месяцы). Диагностические критерии “метотрексатового” легкого включают следующие признаки: прогрессирующую одышку, лихорадку свыше 38 °С, тахипноэ более 28 в минуту, наличие признаков интерстициальных изменений при лучевой диагностике, лейкоцитоз, рестриктивные нарушения внешнего дыхания со снижением диффузионной способности легких, PaO2 < 50 мм рт. ст.
Диагноз
Диагноз ЭАА устанавливают на основании наличия следующих критериев в анамнезе признаков контакта при выполнении профессиональных обязанностей с определенным антигеном, указанным в санитарно-гигиенической характеристике условий труда;
• наличия эпизодов одышки, сопровождающейся сухим кашлем, лихорадкой и недомоганием, развивающейся через несколько часов после ингаляции соответствующего антигена, и исчезновение респираторных симптомов заболевания после прекращения контакта с антигеном;
• объективных данных, аускультативных данных, наличия двусторонней крепитация над легкими;
• данных консультации врача-аллерголога, пульмонолога, профпатолога;
• данных лабораторных методов исследования: повышен уровень интерлейкина-8, который является важнейшим фактором хемотаксиса нейтрофилов, тем самым определяя нейтрофилии и лимфоцитопении; увеличен уровень фактора некроза опухоли β, который стимулирует пролиферацию фибробластов и синтез ими коллагена; повышаются скорость оседания эритроцитов, уровень С-реактивного протеина; определяется ревматоидный фактор; эозинофилия выявляется редко; выявляются повышенные уровни общих иммуноглобулина G(IgG) и IgM, специфические преципитирующие антитела к “виновному” антигену (методами двойной диффузии, встречного иммуноэлектрофореза и иммуноферментными методами). данных инструментальных методов исследования.
При исследовании функции внешнего дыхания выявляется рестриктивный тип вентиляционных нарушений со снижением легочных объемов, возможны обструктивные изменения со снижением скоростных показателей форсированного выдоха. Диагностируется гипоксемия как при физической нагрузке, так и в покое. Определяются положительные кожные скарификационные пробы (исследование проводится врачом-аллергологом). Положителен провокационный ингаляционный тест. Материалы, которые используют для тестов, готовят из пыли “подозрительного” материала или из экстрактов смеси антигенов субстанций, полученных с помощью различных химических процессов. У чувствительных пациентов после теста может развиться выраженное обострение заболевания, значительная гипоксемия, поэтому многие пациенты неохотно идут на исследование.
При рентгенографии легких на начальной стадии наблюдается обширное затемнение легочных полей, в дальнейшем – множественные мелкие очаговые тени или сетчато-узелковое поражение; при устранении контакта с органической пылью они полностью исчезают. При острой и подострой формах может отмечаться снижение прозрачности легочных полей по типу “матового стекла”, нечеткие пятна, диффузные или отдельные узелковые инфильтраты; при хронической форме появляется сеть диффузных узелковых инфильтратов, а также такие нарушения, как плевральный выпот, уплотнение или прикорневая аденопатия.
На рисунке мы приводим рентгенограмму больного А-на 66 лет, бывшего работника комбината по добыче и переработке никелевой руды (производственный контакт с никелем, кадмием, кобальтом), которого мы наблюдали с хронической формой ЭАА. В клинике профессиональных болезней был установлен диагноз “хроническая интоксикация кобальтом, экзогенный аллергический альвеолит с исходом в фиброз, кобальтовая дистрофия миокарда. Хронический бронхит. Хроническая эмфизема легких. Дыхательная недостаточность второй степени. Хроническое легочное сердце. Н ІІ А. Заболевание профессиональное”.
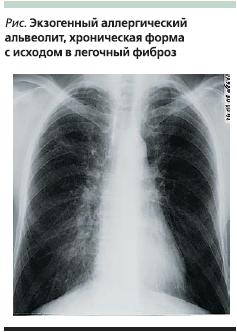
При проведении компьютерной томографии легких с высоким разрешением выявляются множественные мелкие очаговые тени на фоне сетчатой перестройки легочного рисунка. Выявляются узелковые затемнения, зоны “матового стекла”. Часто выявляют буллезное вздутие легочной паренхимы и трансформацию легочной ткани по типу сотового легкого. Иногда наблюдается симптом воздушной ловушки. Сцинтиграфия легких с галлием позволяет выявить острый альвеолит, однако этот метод исследования неспецифичен, его результаты плохо коррелируют с клинической картиной заболевания и морфологическими изменениями в легких, а отрицательный результат не исключает наличия заболевания.
При анализе цитоза бронхоальвеолярного смыва после лаважа можно выявить в 5 раз повышенные уровни различных популяций Т-лимфоцитов (преимущественно CD8+), при “амиодароновом легком” – пенистые макрофаги.
Биопсия легкого показана, если для постановки диагноза недостаточно других критериев. Если биоптат получают в активной фазе болезни, в нем определяют интерстициальный альвеолярный инфильтрат, состоящий из плазматических клеток, лимфоцитов, иногда эозинофилов и нейтрофилов и гранулемы, слабовыраженный интерстициальный фиброз. Возможно наличие гигантских клеток и телец Шаумана, но они не специфичны для ЭАА.
Часто развиваются облитерирующий бронхиолит, перибронхиальные воспалительные инфильтраты. Гранулематоз, альвеолит и бронхиолит составляют т. н. триаду морфологических признаков при ЭАА, при этом все элементы находят не всегда.
Дифференциальный диагноз
Сходная рентгенологическая картина наблюдается и при легочных диссеминациях опухолевой природы (бронхиолоальвеолярном раке, карциноматозе; поражении легких при лимфогранулематозе, лейкозах). Также необходимо проводить дифференциальный диагноз с идиопатическим фиброзирующим альвеолитом, гранулематозами легких: саркоидозом легких, диссеминированным туберкулезом легких (табл. 3), пневмомикозами; легочными проявлениями при системных васкулитах и ангиитах (узелковом периартериите, гранулематозе Вегенера, идиопатическом гемосидерозе легких, синдроме Гудпасчера) [6–8].
Так, верификацию саркоидоза осуществляют на основании гистологического исследования биоптатов легочной ткани, что позволяет выявить специфические изменения. Возможно проведение пробы Квейма.
Карциноматоз легких протекает более тяжело, сопровождается интоксикацией и выраженной дыхательной недостаточностью. На рентгенограммах легких выявляются полиморфные очаговые тени с нечеткими контурами, отсутствует “обрубленность” корней легких. Отмечаются быстрое прогрессирование процесса в легких и изменения в периферических лимфатических узлах. Для уточнения диагноза необходимо исследовать мокроту на наличие атипичных клеток, а при увеличении периферических лимфатических узлов показана их биопсия.
Лечение
Поскольку эффективность лечения зависит главным образом от прекращения воздействия антигена, большое значение имеют его идентификация и устранение контакта. Единственным эффективным средством лечения подострой и хронической форм заболевания являются системные глюкокортикостроиды (при острой форме не применяются). Глюкокортикостероиды отменяют по достижении клинического улучшения или в отсутствие клинического и функционального ответов на них. Если в период снижения дозы глюкокортикостероидов происходит ухудшение состояния больного, следует вернуться на предшествующую ступень терапии. При резистентности заболевания к глюкокортикостероидам иногда назначают Д-пеницилламин и колхицин (эффективность не доказана).
У пациентов с доказанной гиперреактивностью дыхательных путей применяют бронходилатирующие лекарственные средства. Используются β2-адреномиметики (фенотерол, формотерол), антихолинергические препараты (прежде всего ипратропия бромид), реже метилксантины. При назначении метилксантинов следует учитывать, что клиренс теофиллина широко варьируется и снижается с возрастом, при дисфункции печени, декомпенсации сердца, легочном сердце, лихорадке.
При появлении осложнений проводится симптоматическая терапия: длительная кислородотерапия – при дыхательной недостаточности, антибиотики – при бактериальных осложнениях, диуретики – при застойной сердечной недостаточности и др.
Прогноз
Прогноз при ЭАА зависит от своевременности выявления заболевания. При остром и подостром течении ЭАА изменения в легких обратимы и спустя несколько дней, недель или месяцев после прекращения контакта с антигеном симптомы заболевания полностью исчезают. При хронической форме ЭАА прогноз во многих случаях неблагоприятен или по крайне мере сомнителен. Заболевание может прогрессировать даже после прекращения контакта с антигеном и трудно поддаваться лечению.
Профилактика
Профилактика ЭАА основывается на совершенствовании технологических процессов (герметизации, механизации технологий, выносе пультов управления за пределы рабочих помещений, увлажнении воздуха и др.); при поступлении на работу – качественном проведении предварительных профилактических медицинских осмотров, согласно приказу МЗ и МП РФ РФ “Об утверждении перечней вредных и (или) опасных производственных факторов и работ, при выполнении которых проводятся предварительные и периодические медицинские осмотры (обследования), и Порядка проведения предварительных и периодических медицинских осмотров (обследований) работников, занятых на тяжелых работах и на работах с вредными и (или) опасными условиями труда” № 302 н от 12.04.2011, периодическом аллергологическом обследовании работающих.
Дополнительными медицинскими противопоказаниями к приему на работу в контакте с производственными веществами токсикоаллергического действия служат тотальные дистрофические и аллергические заболевания верхних дыхательных путей; хронические заболевания бронхолегочной системы; аллергические заболевания при работе с аллергенными аэрозолями; врожденные аномалии (пороки развития) органов дыхания и сердца.
Правилом при определении трудоспособности больных ЭАА является следующее: наличие заболевания является абсолютным противопоказанием к продолжению работы в контакте с причинным веществом. Больной признается стойко частично утратившим трудоспособность, стойко нетрудоспособным в своей профессии, нуждающимся в постоянном рациональном трудоустройстве, нуждающимся в медицинской и социальной реабилитации.


