Сосудистые заболевания головного мозга занимают второе место в структуре смертности от болезней системы кровообращения (39 %) и в общей смертности населения (23,4 %) [1]. Показатель заболеваемости инсультом среди лиц трудоспособного возраста в России увеличился более чем на 30 % за последние 10 лет [2]. Инсульт является лидирующей причиной инвалидизации населения, треть перенесших его больных нуждаются в посторонней помощи, еще 20 % не могут самостоятельно ходить, лишь каждый пятый способен вернуться к трудовой деятельности [2]. Стоимость лечения одного больного, перенесшего инсульт, включая стационарное лечение, медико-социальную реабилитацию и вторичную профилактику, в нашей стране составляет 127 тыс. руб. в год, т. е. общая сумма прямых расходов на инсульт (из расчета 499 тыс. случаев в год) равна 63,4 млрд руб. [2]. Непрямые расходы на инсульт, оцениваемые по потере внутреннего валового продукта страны из-за преждевременной смертности, инвалидности и временной нетрудоспособности населения, составляют в России около 304 млрд руб. в год [2]. Поэтому вопросы профилактики инсульта являются важной не только медицинской, но и социальной задачей.
Одной из главных задач успешной профилактики как первого, так и повторного ишемического инсульта или транзиторной ишемической атаки является снижение артериального давления (АД) [3]. Хорошо известно, что артериальная гипертензия (АГ) – основной фактор риска развития инсульта [3]. Поэтому главным условием эффективной профилактики инсульта является достижение целевых уровней АД – менее 140/90 мм рт. ст. [3]. Однако это не единственное (хотя и одно из главных) условие минимизации риска инсульта. В последние годы огромное внимание обращают на вариабельность АД как на важный фактор риска развития инсульта у больных АГ.
Артериальное давление – естественно изменяющийся показатель. У здоровых людей физиологическая адаптация к физическим или эмоциональным стимулам, естественно, приводит к изменению АД. Вариабельность АД – это колебания АД, превышающие физиологические.
Различают несколько видов вариабельности АД:
• вариабельность АД в рамках визита – колебания клинического АД (измеряемого на плечевой артерии) при сравнении трех последовательных измерений АД в ходе одного визита к врачу. Согласно методике измерения АД, врач должен выполнить подряд несколько измерений с небольшим промежутком. Различия (вариабельность) значений АД в таком случае называют вариабельностью в рамках одного визита к врачу (within-visit variability);
• суточная вариабельность АД – колебания АД в течение суток (отдельно в дневные и ночные часы, или правильнее – в периоды сна и бодрствования), по данным амбулаторного суточного мониторирования АД (СМАД), превышающие суточные физиологические колебания АД;
• вариабельность АД “от визита к визиту” или между визитами – различия по величине клинического (“плечевого”) АД между визитами (visit-to-visit variability);
• вариабельность АД в разные дни (day-to-day);
• вариабельность АД в разные недели (weak-to-weak);
• вариабельность АД в разные сезоны (зима–весна–лето–осень).
В настоящее время понятие вариабельности АД стремительно расширяется. Например, избыточно резкое повышение АД в ранние утренние часы, которое раньше называли “утренними подъемами АД”, сейчас все чаще называют “вариабельностью АД в ранние утренние часы” и рассматривают в рамках суточной вариабельности АД.
Вариабельность АД (любой из ее видов) определяется как SD (стандартное отклонение) нескольких измерений или как коэффициент вариации (сoefficient of variation, CV), равный стандартное отклонение/среднее значение АД. Однако, поскольку было установлено, что SD и CV хотя и слабо, но достоверно коррелируют с уровнем АД, не прекращаются попытки вывести коэффициент, который отражал бы вариабельность АД, но не зависел бы от уровня АД [4]. Таким коэффициентом, в частности, является VIM (variation independent of mean) – коэффициент вариации, не зависимый от средних значений [4].
В последние годы к вариабельности АД привлечено огромное внимание. Это обусловлено результатами исследования ASCOT (Anglo-Scandinavian Cardiac Outcomes Trial). Исследование ASCOT является центральным исследованием, в котором выявлено влияние вариабельности АД на риск инсульта и других осложнений АГ. В исследовании ASCOT было две ветви – по снижению АД (ASCOT-BPLA – blood pressure lowering arm) и по снижению липидов (ASCOT-LLA – lipid lowering arm). В программу ASCOT-BPLA были включены 19 257 больных АГ. Одна половина (9639 человек) в дальнейшем получала комбинацию дигидропиридинового блокатора кальциевых каналов III поколения амлодипина с ингибитором ангиотензинпревращающего фермента (АПФ) периндоприлом, вторая половина (9618 человек) – комбинацию β-адреноблокатора атенолола с тиазидным диуретиком бендрофлуметиазидом [5, 6].
Помимо согласия участвовать в исследовании, было три критерия включения в программу ASCOT-BPLA [5,6]:
• АГ исходно с АД > 160/100 мм рт. ст. без лечения или >140/90 мм рт. ст. на фоне лечения одним или несколькими антигипертензивными препаратами;
• возраст более 40 и менее 80 лет;
• наличие минимум трех факторов риска развития сердечно-сосудистых событий, к которым относились [5,6] гипертрофия миокарда левого желудочка (ГМЛЖ), наличие патологических отклонений на электрокардиограмме (патологический зубец Q, блокада левой ножки пучка Гиса, изменения сегмента ST или зубца Т ишемического генеза), сахарный диабет (СД) 2 типа (не требующий инсулинотерапии), поражение периферических артерий, наличие цереброваскулярных событий в анамнезе (включая транзиторные ишемические атаки) не менее чем 3 месяца назад, мужской пол, возраст более 55 лет, микроальбуминурия или протеинурия, регулярное курение, отношение концентрации общего холестерина (ХС) к ХС липопротеидов высокой плотности (ЛПВП) в плазме крови > 6, раннее (до 55 лет у мужчин и до 60 лет у женщин) развитие ишемической болезни сердца (ИБС) у родственников первой линии.
Главной задачей программы ASCOT-BPLA (первичная конечная точка) было сравнение частоты развития нефатальных инфарктов миокарда (с клиническими проявлениями и без них) и всех случаев смерти от ИБС на фоне стандартного (“старого”) режима антигипертензивной терапии (β-адреноблокатор ± диуретик) и современного режима лечения (блокатор кальциевых каналов ± ингибитор АПФ) [5, 6]. В число второстепенных задач программы ASCOT-BPLA (вторичные конечные точки) в т. ч. входило сравнение влияния двух антигипертензивных режимов терапии на частоту развития фатальных и нефатальных инсультов.
После рандомизации пациенты в зависимости от того, в какую группу они были включены, начинали получать либо 5 мг амлодипина, либо 50 мг атенолола [5, 6]. В последующем при недостижении целевого уровня АД (< 140 мм рт. ст. для систолического АД [САД] и < 90 мм рт. ст. для диастолического АД [ДАД] для больных без СД и < 130 мм рт. ст. САД и < 80 мм рт. ст. ДАД для больных СД) необходимая корректировка терапии осуществлялась через 6 недель, 3, 6 и 12 месяцев. В начале производили удвоение дозы первоначально назначенных препаратов – амлодипина до 10 мг, атенолола до 100 мг. На следующей ступени переходили уже к комбинированной терапии: к амлодипину добавляли ингибитор АПФ (периндоприл) в дозе 4 мг, к атенололу – бендрофлуметиазид 1,25 мг + К+. В дальнейшем дозу ингибитора АПФ увеличивали до 8 мг, а бендрофлуметиазида – до 2,5 мг. Наконец, если и на такой терапии упомянутые выше целевые уровни АД не были достигнуты, добавляли третий препарат – доксазозин GITS (gastrointestinаl therapeutic system) в дозе 4 мг с последующим увеличением дозы до 8 мг. В конце исследования комбинированную антигипертензивную терапию получали 77,8 % больных. При этом в группе “амлодипина” в 68,4 % случаев использовалась комбинация амлодипина с ингибитором АПФ, в группе “атенолола” – в 55,7 % комбинация атенолола с диуретиком [5, 6].
В октябре 2004 г. Наблюдательный комитет по безопасности рекомендовал досрочно прекратить ASCOTBPLA, поскольку продолжение лечения комбинацией атенолол ± тиазидный диуретик очевидно увеличивало вероятность развития неблагоприятных исходов по сравнению с лечением по схеме амлодипин ± ингибитор АПФ. Координационный комитет принял эти рекомендации, и закрытие исследования началось в декабре 2004 г., при этом средний период наблюдения составил 5,4 года. В том числе было обнаружено значительное и достоверное (p < 0,0001) различие по частоте инсультов [6]. Так, на фоне лечения амлодипин ± ингибитор АПФ частота фатальных и нефатальных инсультов оказалась на 23 % ниже (относительный риск – 0,77, 95 % доверительный интервал – 0,66–0,89) по сравнению с терапией атенолол ± диуретик [6]. Эти различия оказались характерными не только для всех больных в целом, но и для отдельных подгрупп – пациентов, страдающих и не страдающих СД, курильщиков и некурящих, лиц с избыточной и нормальной массой тела, пациентов старше и моложе 60 лет, мужчин и женщин, имеющих и не имеющих ГМЛЖ, пациентов с наличием сосудистых осложнений в анамнезе и без них, с сохраненной и нарушенной функциями почек, лиц, имеющих и не имеющих проявлений метаболического синдрома, т. е. полученный в ходе исследования эффект имел системный характер и, вероятно, должен иметь универсальное объяснение [6].
В исследовании ASCOT режим лечения с применением амлодипина (в т. ч. в комбинации с ингибитором АПФ) привел к выраженному снижению АД (среднее плечевое АД снизилось по сравнению с исходным уровнем на 27,5/17,7 мм рт. ст.) [6]. Это снижение было достоверно больше, чем в группе β-адреноблокатора и диуретика: среднее различие по САД составило 2,7 мм рт. ст., а по ДАД – 1,9 мм рт. ст. [6]. Для такого различия по плечевому САД вычисленная польза в отношении снижения риска коронарных событий находится в интервале от 4 до 8 %, а для инсульта – от 11 до 14 %. Однако в исследовании ASCOT режим с применением амлодипина и ингибитора АПФ снизил риск коронарных событий на 14 % и риск инсульта на 23 % по сравнению с другим активным лечением! Каким образом можно объяснить это практически в 2 раза более выраженное против ожидаемого благоприятное действие режима терапии с применением амлодипина на риск развития инсульта и инфаркта миокарда (ИМ)? Следовательно, существуют еще какие-то механизмы благоприятного воздействия комбинации периндоприла и амлодипина на сердечно-сосудистый риск. Именно тогда и начали изучать роль вариабельности АД в развитии инсульта и ИМ, а также возможности антигипертензивных препаратов уменьшать вариабельность АД.
Было проанализировано влияние на риск инсульта и ИМ для больных АГ трех видов вариабельности АД – вариабельность АД в рамках визита, суточная вариабельность АД и вариабельность АД между визитами [4]. В исследовании АSCOT выявили значение всех трех видов вариабельности САД, в т. ч. суточной вариабельности САД (по СМАД) как предиктора цереброваскулярных, а также коронарных событий [4].
Влияние суточной вариабельности АД (как САД, так и ДАД) на риск сердечно-сосудистых событий широко изучалось в 1990–2000 гг., когда и была выявлена значимость повышенной вариабельности АД как в дневные, так и в ночные часы на риск развития инсульта при АГ [7, 8]. Однако предельно допустимые значения для заключений о повышенной вариабельности АД в течение суток в настоящее время находятся в стадии разработки. В качестве временных нормативов вариабельности (стандартное отклонение SD) для пациентов с АГ I–II степеней (АД 140–160/90–109 мм рт. ст.) в Российском кардиологическом научно-производственном комплексе сформированы (на основе оценки верхних пределов для нормотоников) следующие критические значения: для САД – 15/15 мм рт. ст. (день/ночь), для ДАД – 14/12 мм рт. ст. (день/ночь) [9]. Пациенты относятся к группе повышенной вариабельности АД при превышении хотя бы одного из четырех критических значений [9].
Показатель вариабельности АД особенно чувствителен к числу успешных измерений за время мониторирования. В целом анализ показал, что для достаточно точного расчета всех показателей СМАД, включая вариабельность АД в ночные часы, необходимо не менее 56 измерений АД в течение суток [9]. На основании этого выработан критерий успешности мониторирования при анализе СМАД: при интервалах между измерениями 15 минут в дневные часы/30 минут в ночные часы процент неудачных измерений должен быть < 30 % [9].
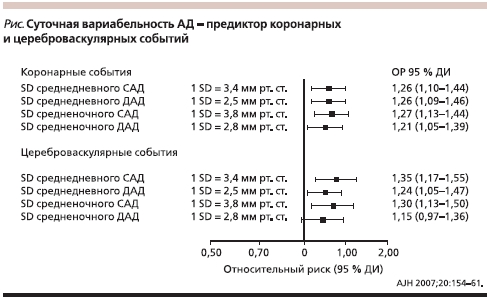
В последние годы интерес к суточной вариабельности АД опять вырос. В 2007 г. опубликована работа, в которой среди прочих факторов риска оценивали и влияние вариабельности АД в течение суток на риск развития осложнений АГ. Обнаружено, что вариабельность (SD) среднедневных САД и ДАД, средненочного САД являются независимыми предикторами развития как кардиальных, так и в цереброваскулярных событий (рис. 1) [10]. Вариабельность (SD) средненочного ДАД была независимым предиктором развития кардиальных, но не цереброваскулярных осложнений (рис. 1) [10].
Также в исследовании ASCOT сравнивали влияние двух лекарственных комбинаций на вариабельность АД в течение суток при помощи СМАД [11]. С этой целью в четырех центрах пациентам проводили СМАД – ABPMsubstudy. Всего в ABPM-substudy участвовали 1905 больных, которым было выполнено от 1 до 10 СМАД за время их участия в исследовании, т. е. в среднем 3,25 [11]. У этих 1905 больных за период наблюдения было зафиксировано 157 сердечно-сосудистых событий (инсульт или ИМ). Исходные характеристики пациентов, включенных в ABPM-substudy, достоверно не различались между группами амлодипин/ингибитор АПФ и атенолол/тиазидный диуретик. За дневные были приняты часы 09.00–21.00, за ночные – 01.00–06.00 [11]. Анализ данных ABPM-substudy показывает, что вариабельность (SD, CV) САД и ДАД в дневные часы была достоверно меньше в группе амлодипин/ингибитор АПФ по сравнению с группой атенолол/тиазидный диуретик. Сходные тенденции выявлены и в отношении вариабельности (SD, CV) САД и ДАД в ночные часы [11]. И стандартное отклонение (SD), и коэффициент вариации (CV) дневного САД были ниже в группе амлодипин/ингибитор АПФ, чем в группе атенолол/тиазидный диуретик, на протяжении всего периода наблюдений (в среднем 5 лет). Пациентам в одном из 4 центров, где проводили СМАД, также было выполнено СМАД в течение 6 месяцев до рандомизации (78 больных в группе атенолол/тиазидный диуретик и 80 – в группе амлодипин/ингибитор АПФ) [11]. Средние значения коэффициента вариации (СV) дневного САД после рандомизации достоверно увеличились в группе атенолол/тиазидный диуретик (7,66 до рандомизации и 8,74 после рандомизации; p < 0,0001), тогда как в группе амлодипин/ингибитор АПФ подобных изменений не обнаружено (8,25 до рандомизации и 8,45 после рандомизации; p = 0,49) [11]. На фоне комбинации амлодипин/ингибитор АПФ в отличие от комбинации атенолол/тиазидный диуретик достоверно уменьшались и другие виды вариабельности АД [11].
Таким образом, комбинация амлодипина и ингибитора АПФ уменьшает вариабельность АД (между визитами, суточную и внутри визита) по сравнению с комбинацией атенолола и тиазидного диуретика. Поправка на вариабельность АД объясняет выявленные в исследовании ASCOT различия по частоте инсультов и ИМ между группами амлодипин/ингибитор АПФ и атенолол/тиазидный диуретик [11]. Поэтому резко возрос интерес к изучению влияния разных антигипертензивных препаратов и особенно их комбинаций на вариабельность АД, в т. ч. в течение суток.
Целью нашего исследования было изучение влияния фиксированной комбинации, содержащей ингибитор АПФ и дигидропиридиновый антагонист кальция (препарат Экватор) лизиноприл 10 мг + амлодипин 5 мг, на вариабельность АД в течение суток.
Материал и методы
В исследование был включен 31 больной 33–59 лет, средний возраст – 50,39 ± 1,18 года, из них 14 мужчин, 17 женщин с гипертонической болезнью II стадии 1–2-й степеней, не получавших антигипертензивной терапии не менее 2 недель до включения в исследование.
Критерии исключения:
• зависимость от алкоголя, лекарственных препаратов;
• психические заболевания или недееспособность;
• отсутствие достаточной готовности к сотрудничеству;
• прогрессирование гипертонической болезни в течение последнего месяца;
• наличие в анамнезе инсульта, преходящего нарушения мозгового кровообращения, ИМ;
• нестабильная стенокардия или стенокардия напряжения I–IV функциональных классов;
• сердечная недостаточность I–IV классов по NYHA (New York Heart Association);
• нарушения ритма и проводимости сердца;
• сахарный диабет;
• клинически значимое заболевание дыхательных органов, желудочно-кишечного тракта, нервной системы, почек, гематологическое заболевание, тяжелые эндокринные нарушения;
• паркинсонизм или другие заболевания, сопровождающиеся дрожанием мышц;
• беременность, лактация;
• индекс массы тела (ИМТ) > 35 кг/м²;
• гиперлипидемия (общий холестерин > 6,0 ммоль/л, триглицериды > 2,8 ммоль/л).
При исходном обследовании проведен сбор анамнеза, полное клиническое обследование, включившее рутинное измерение АД, оценено соответствие пациента критериям включения/исключения, а также СМАД. Пациентам после обследования был назначен препарат Экватор (дигидропиридиновый блокатор кальциевых каналов амлодипин 5 мг и лизиноприл 10 мг, Гедеон Рихтер, Венгрия) в дозе 1 таблетка 1 раз в сутки утром. Через 4 недели при недостижении целевого АД (менее 140/90 мм рт. ст.), по данным рутинного измерения, дозу Экватора удваивали – по 2 таблетки один раз в сутки утром. Длительность наблюдения составила 12 недель. В конце периода наблюдения повторяли все обследования.
Характеристика обследованных больных представлена в табл. 1.
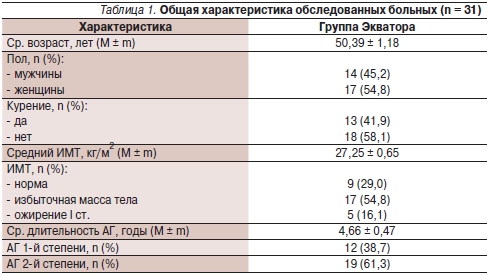
До включения в исследование 10 (32,2 %) больных не получали предшествовавшего лечения по поводу АГ. Среди пациентов, ранее получавших антигипертензивную терапию, наиболее часто применяемыми антигипертензивными препаратами оказались нифедипин (8 больных), каптоприл (5), эналаприл (5), периндоприл (4).
Статистическая обработка данных проведена с помощью пакета программ Excel 97, Statistica 6.0 и SPSS 13.0 на компьютере IBM PC/AT-586. Рассчитаны средние величины, их средние стандартные ошибки и 95 % доверительный интервал. Гипотеза о равенстве средних была оценена по F-критерию (дисперсионный анализ). Попарная связь между двумя и более непрерывными признаками определена методом корреляционного анализа. Корреляционную связь между выборками данных оценивали с уровнем значимости 95 %. Для изучения распределения дискретных признаков в различных группах применен стандартный метод анализа таблиц сопряженности Х-квадрат по Пирсону и метод ранговых корреляций по Спирману. Для анализа малых выборок (до 30 наблюдений) применены непараметрические методы статистической обработки данных. Вероятность того, что статистические выборки отличались друг от друга, существовала при р < 0,05.
Результаты исследования
Таким образом, на фоне антигипертензивной терапии в течение 12 недель отмечено достоверное снижение показателей рутинного измерения АД (табл. 2).
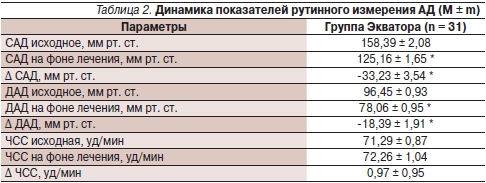
Примечание. ЧСС – частота сердечных сокращений. * p < 0,0001 по сравнению с исходными данными.
Среди пациентов, получавших Экватор, целевые значения АД были отмечены у 31 (100 %) человека. Для достижения целевого АД 23 (74,2 %) пациента принимали 1 таблетку препарата Экватор в сутки и 8 (25,8 %) – 2 таблетки Экватор 1 раз в сутки.
По данным СМАД выявлено достоверное снижение САД и ДАД как в дневные, так и в ночные часы (табл. 3).
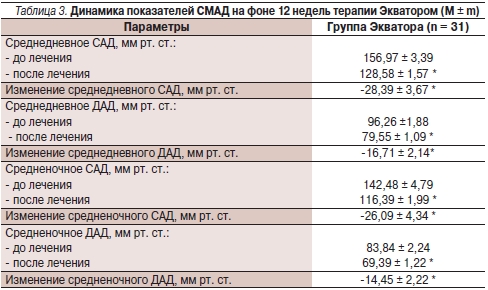
* р < 0,0001 по сравнению с исходными данными.
На фоне 12 недель терапии достоверно улучшились показатели вариабельности САД и ДАД как в дневные, так и в ночные часы (табл. 4).
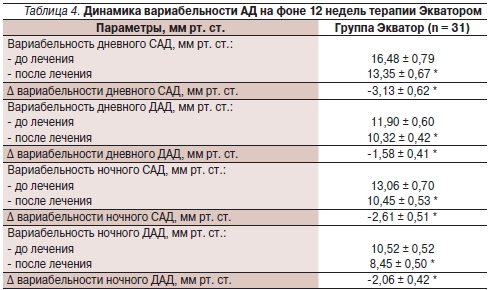
* р < 0,05 по сравнению с исходными данными.
По данным СМАД до лечения норму вариабельности дневного САД имели 13 (41,9 %) пациентов, дневного ДАД – 23 (74,2 %, ночного САД – 24 (77,4 %), ночного ДАД – 22 (71 %) пациента. По данным СМАД, в течение 12 недель терапии Экватором норма вариабельности дневного САД достигнута 21 (67,7 %) пациентом, норма вариабельности дневного ДАД – 30 (96,8 %), норма вариабельности ночного САД – 29 (93,5 %), а норма вариабельности ночного ДАД – 30 (96,8 %) пациентами.
Следовательно, фиксированная комбинация Экватор эффективно снижает как уровни, так и вариабельность САД и ДАД в дневные и ночные часы.
Итак, вариабельность АД, в т. ч. в течение суток, особенно САД – второй, после уровня АД, прогностически значимый и независимый фактор риска развития инсульта при АГ, в т. ч. и у пациентов, получающих медикаментозное лечение. Антигипертензивная терапия препаратом Экватор способна не только снижать уровень АД, но и уменьшать его вариабельность в течение суток.
Более широкое использование препарата в клинической практике, прежде всего в качестве терапии первой линии, позволит повышать эффективность лечения АГ, значит, Экватор станет надежным залогом успешной профилактики инсульта.



