Введение
Заболеваемость сахарным диабетом (СД) растет во всем мире.
В 2019 г. число больных СД достигло 463 млн человек в основном за счет роста числа пациентов с СД 2 типа (СД2). В Москве на 01.01.2020 были зафиксированы 386 тыс. больных СД, из которых 94% (366 тыс. человек) имели СД2 [1]. Достижение и длительное удержание показателей гликемического контроля в целевом диапазоне являются важнейшим фактором, влияющим на риски развития поздних осложнений СД2.
Алгоритмы терапии СД2 постоянно обновляются в связи с внедрением в клиническую практику новых классов сахароснижающих препаратов (ССП) и появлением новых показаний к их использованию. До настоящего времени в качестве препарата 1-й линии терапии СД2 рекомендуется использовать метформин [3], который давно зарекомендовал себя как препарат с достаточной эффективностью, минимальным риском гипогликемий и положительным влиянием на массу тела.
Прогрессирующий характер течения СД2, ассоциированный с постепенным снижением функции β-клеток и ухудшением чувствительности к инсулину, определяет невозможность долгосрочного управления гликемией с помощью монотерапии любым ССП. Как правило, через некоторое время пациентам требуется интенсификация терапии. Результаты проведенного в Великобритании исследования показали, что через 3 года после установления диагноза 50% пациентов для достижения цели лечения требовалась терапия как минимум двумя ССП. Через 9 лет после постановки диагноза около 75% пациентов нуждались в терапии с использованием комбинации ССП [5].
2015 г. стал точкой отсчета новой эры в терапии СД2. Произошла смена парадигмы в терапии этого заболевания, фокус сместился в сторону управления рисками сердечно-сосудистых осложнений и смертности в большей степени, чем просто контроля показателей гликемии. Хорошо известно, что СД2 ассоциируется с высоким риском сердечно-сосудистых осложнений и сам является фактором риска. Для выявления истинной распространенности сердечно-сосудистых заболеваний (ССЗ) среди пациентов с СД2 и оценки доли больных СД2, получающих ССП с кардиопротективными свойствами, в 2019 г. было инициировано исследовании CAPTURE [6]. Исследование проводилось в 13 странах на 5 континентах. Информацию о терапии пациентов (n=9823) собирали в учреждениях как первичной, так и специализированной медицинской помощи. По оценке исследователей, общая распространенность ССЗ составила 34,8% [32,7–36,8%], была аналогичной в условиях учреждений первичной (35,6% [34,0; 37,1]) и специализированной (34,6% [32,1; 37,1]) медицинской помощи. Атеросклеротические ССЗ (АССЗ) были самыми распространенными из всех ССЗ (9 из 10) (рис. 1).

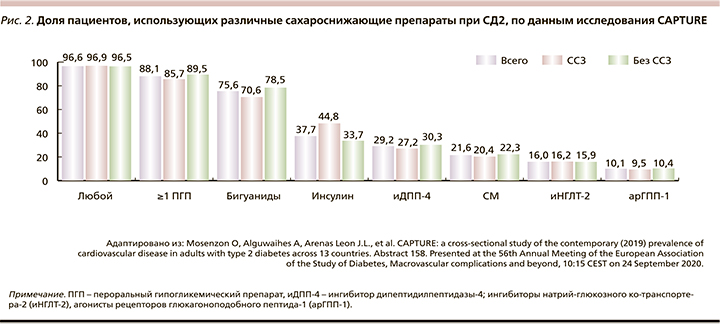
Среди пациентов, участвовавших в исследовании, 96,6% получали хотя бы 1 ССП. При этом чаще всего применяли пероральные ССП (рис. 2).
По результатам исследования CAPTURE, 1 из 3 пациентов исследуемой популяции больных СД2 имел подтвержденное ССЗ (в 9 из 10 случаев атеросклеротического генеза). Только 2 из 10 пациентов получали ССП с доказанными кардиопротективными свойствами. При этом частота их использования в когортах больных СД2 с ССЗ и без них была сопоставимой (рис. 2).
Американская ассоциация диабета (ADA) и Европейская ассоциация по изучению диабета (EASD) рекомендуют назначение препаратов групп агонистов рецепторов глюкагоноподобного пептида-1 (арГПП-1) и ингибиторов натрий-глюкозного ко-транспортера-2 (иНГЛТ-2) с доказанным положительным влиянием на сердечно-сосудистые исходы для лечения пациентов с СД2 с ССЗ или высоким сердечно-сосудистым риском независимо от уровня гликированного гемоглобина (НbА1c) [7].
В российских клинических рекомендациях арГПП-1 и иНГЛТ-2 также рассматриваются в качестве приоритетных для больных СД2 с ССЗ атеросклеротического генеза или факторами риска ССЗ (кроме хронической сердечной недостаточности, при которой приоритет имеют только иНГЛТ-2).
При этом внутри класса арГПП-1 эффективность в профилактике развития атеросклеротических ССЗ продемонстрировали лишь некоторые его представители: лираглутид, дулаглатид, семаглутид [2].
Семаглутид (Оземпик®, «Ново Нордиск») зарегистрирован в России в марте 2020 г. и представляет собой аналог глюкагоноподобного пептида-1 (ГПП-1), имеющий 94% гомологичности с человеческим ГПП-1. Семаглутид действует как арГПП-1, который селективно связывается и активирует ГПП-1Р. ГПП-1Р служит мишенью для нативного ГПП-1. Период полувыведения семаглутида составляет около 1 недели, что позволяет вводить его 1 раз в неделю. Связывание препарата с альбумином служит основным механизмом, пролонгирующим действие семаглутида, что приводит к снижению выведения его почками и защищает от метаболического распада. Начальная доза составляет 0,25 мг 1 раз в неделю. После 4 недель применения дозу следует увеличивать до 0,5 мг 1 раз в неделю, а еще через 4 недели – до 1,0 мг 1 раз в неделю.
Несмотря на высокое положение вышеуказанных групп препаратов в консенсусных рекомендациях ведущих диабетологических ассоциаций, они не заняли подобного места в рутинной клинической практике. В связи с широким разрывом между клиническими рекомендациями и работой практикующего врача такие исследования реальной клинической практики становятся особенно актуальными. Данные о применении семаглутида в реальной клинической практике были получены в рамках исследований EXPERT и SPARE.
Результаты исследований реальной клинической практики
Исследование EXPERT проводилось в 2018–2019 гг. и представляет собой анализ базы данных электронных медицинских карт IBM Explorys. В этом исследовании оценивался контроль гликемии и массы тела пациентов, которые ранее получали терапию арГПП-1 и были переведены на терапию семаглутидом в условиях реальной клинической практики.
В исследование включались пациенты старше 18 лет с СД2, идентифицированные в базе данных электронных медицинских карт Explorys (IBM Watson Health) в США. Включенные пациенты имели хотя бы одно применение семаглутида, применение любого другого арГПП-1 в предыдущие года, определение HbA1c и массы тела через 6 или 12 месяцев после старта исследования и в течение 90 дней до старта исследования. Пациенты имели сопоставимые исходные данные по показателям HbA1c и массы тела [32].
По результатам исследования EXPERT обе группы через 6 и 12 месяцев имели значимое снижение уровня HbA1c и массы тела (рис. 3). Снижение уровня HbA1c, достигнутое через 6 месяцев наблюдения, сохранилось на прежнем уровне и через 12 месяцев, в то время как показатель массы тела к 12-му месяцу продолжил снижаться. Снижение уровня HbA1c и массы тела не зависело от исходного препарата арГПП-1.
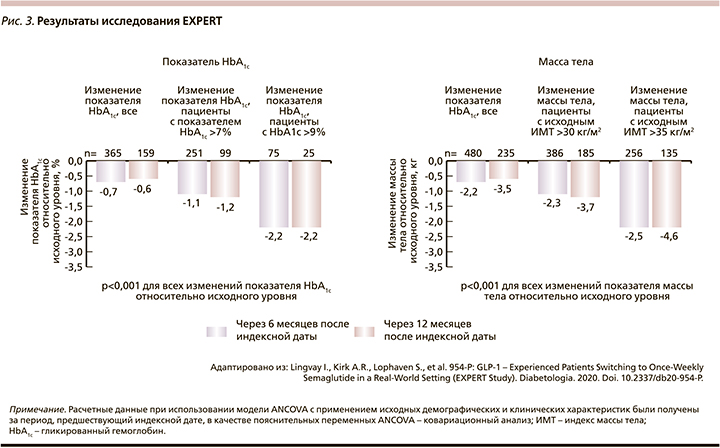
Таким образом, перевод на семаглутид 1 раз в неделю с другого арГПП-1 в рутинной клинической практике ассоциировался со значимым снижением уровня HbA1c и массы тела независимо от того, какой препарат из класса арГПП-1 применялся до назначения семаглутида [32].
Исследование SPARE проводилось в 2018–2019 гг. и представляло собой ретроспективный когортный анализ данных регистра больных СД Канады. Были проанализированы медицинские записи 42 тыс. пациентов из 13 клиник. В исследование были включены пациенты в возрасте >18 лет с СД2 с длительностью ≥6 месяцев, ранее не получавших терапии арГПП-1.
В качестве первичной конечной точки оценивалось среднее изменение уровня HbA1c на старте и через 3 и 6 месяцев наблюдения. Вторичные конечные точки включали среднее изменение массы тела, индекса массы тела (ИМТ), систолического артериального давления (САД), диастолического артериального давления (ДАД), уровня триглицеридов, холестерина липопротеидов низкой плотности (ЛПНП), холестерина не-ЛПВП, расчетной скорости клубочквой фильтрации (рСКФ) и аланинаминотрансферазы (АЛТ), а также частоту развития гипогликемии (≥1 в неделю) и тяжелой гипогликемии (≥1 г). Оценивалась доля пациентов, достигших снижения уровня HbA1c≤7,0 и ≤ 8,0%, доля пациентов со снижением массы тела ≥5 и ≥10%. Также оценивались период времени до интенсификации терапии другим ССП, время до прекращения приема семаглутида и изменение дозы инсулина у пациентов, получавших инсулинотерапию.
Терапия семаглутидом была инициирована с дозы 0,25 мг в неделю. Титрацию дозы приводили через 4 недели до 0,5 мг/нед. При необходимости дозу препарата увеличивали до 1 мг/нед. Семаглутид назначался как препарат 2-й, 3-й и 4-й линий терапии.
Средняя длительность наблюдения в исследовании составила 4,9±1,4 месяца. За время наблюдения уровень HbA1c статистически значимо снизился с 8,34±1,43 до 7,31±1,16% (-1,03±1,24%, 95% ДИ от -1,11 до -0,95; р<0,001). Уровня HbA1c≤7,0% достигли 45,3% (исходно 12,1%) пациентов. При этом 79,1% пациентов достигли уровня HbA1c ≤8,0% (исходно 46,4%). Кроме того, у 66,2% пациентов отмечено снижение уровня HbA1c≥0,5%, а 44,8% больных имели снижение HbA1c≥1,0% в течение периода наблюдения. За время исследования отмечено снижение массы тела на 3,9±4,1 кг от исходного. При этом 33,4% пациентов достигли снижения массы тела ≥5%, 7,3% ≥10% от исходного.
При анализе данных по подгруппам пациентов было отмечено, что у 42% больных, получавших семаглутид в дозе 1,0 мг/нед., наблюдалось более значимое снижение уровня HbA1c (-0,24±0,06%; р<0,001) и массы тела (-1,5±0,3 кг; р<0,001) по сравнению с теми, кто получал 0,25–0,5 мг семаглутида 1 раз в неделю. Не было отмечено разницы в изменении уровня HbA1c или массы тела между пациентами, прекратившими терапию ранее используемыми ССП, и теми, кто данную терапию продолжил. У пациентов, не получавших препаратов инсулина, наблюдалось более значимое снижение уровня HbA1c (-0,21±0,02%; р= 0,003).
При оценке результатов исследования через 6 месяцев было отмечено статистически значимое большее снижение уровня HbA1c (на 0,18±0,06%; р<0,01) по сравнению с результатами через 3 месяца наблюдения.
В подгруппах пациентов, где семаглутид назначался как 2-й или 3-й ССП, было отмечено снижение уровня HbA1c на 1,03%. В то же время, когда семаглутид использовался как 4-й препарат, снижение уровня HbA1c составило 0,76%. Если семаглутид добавляли пациенту, уже получавшему инсулинотерапию, уровень HbA1c снижался на 0,87%. У пациентов на терапии семаглутидом наблюдалось значимое снижение массы тела независимо от исходной комбинации ССП.
При оценке результатов, полученных через 6 месяцев наблюдения, отмечено дополнительное достоверное снижение ИМТ (-1,3±1,3 кг/м2; р<0,001), САД (-4,0±13,1 мм рт.ст.; р<0,001), ДАД (-1,5±8,8 мм рт.ст.; р<0,001), уровня триглицеридов (-0,4±1,3 ммоль/л; р<0,001), ЛПНП (-0,2±0,7 ммоль/л; р<0,001), не-ЛПВП (-0,4±0,8 ммоль/л; р<0,001) и АЛТ (-2,5±12,7 ЕД/л; р<0,001).
При этом не было отмечено статистически значимых различий по рСКФ (-0,5±8,9 мл/мин/1,73 м2; р=0,10).
За время наблюдения не было зафиксировано статистически значимых изменений доли пациентов, еженедельно сообщавших о случаях гипогликемии (4,3% пациентов в начале исследования, 4,7% через 6 месяцев; р=0,70). Также не изменилась доля пациентов, сообщивших по крайней мере об одном случае тяжелой гипогликемии в течение года (исходное значение – 0,4%, через 6 месяцев – 0,5%; р=0,65).
При оценке динамики дозы инсулина в группе пациентов, получавших инсулинотерапию, было отмечено снижение медианы суммарной суточной дозы на 10% только в группе пациентов, проводивших терапию базальным инсулином до назначения семаглутида (с 44,0 до 40,0 и с 0,44 до 0,42 ЕД/кг; р<0,01). У пациентов, получавших до назначения семаглутида базис-болюсную инсулинотерапию, общая суточная доза инсулина снизилась на 20% (с 99,0 до 79,5 и с 0,93 до 0,82 ЕД/кг; р<0,01) (рис. 4).
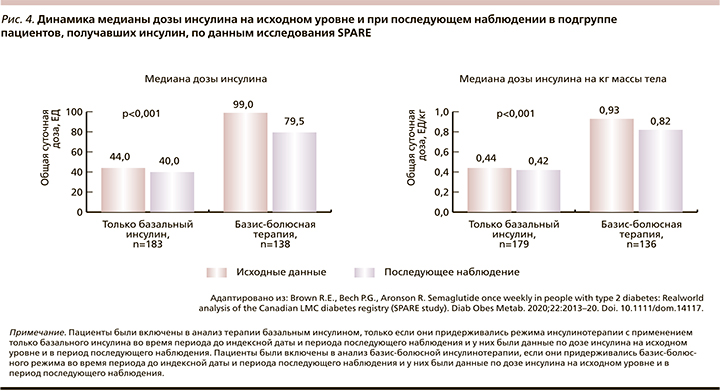
В период наблюдения от 3 до 6 месяцев (±6 недель) 196 (17,3%) человек в общей когорте прекратили прием семаглутида. Среднее время до регистрации прекращения приема препарата составило 14,3±9,2 (14,0) недели.
В период наблюдения не было зарегистрировано ни одного случая панкреатита, медуллярной карциномы щитовидной железы, новых случаев или прогрессирования ретинопатии.
Таким образом, подключение к терапии больных СД2 семаглутида приводило к улучшению гликемического контроля, показателей липидного профиля, снижению массы тела и артериального давления. Модуляция этих факторов снижает риск сердечно-сосудистых и микрососудистых осложнений.
Важность результатов этого исследования определяется выраженной динамикой ключевых показателей контроля СД в условиях реальной клинической практики у большой когорты пациентов с СД2, которым была инициирована терапия семаглутидом в дополнение к ранее получаемой терапии. Добавление к терапии семаглутида 1 раз в неделю приводило к значимому снижению уровня HbA1c и массы тела независимо от исходной схемы терапии. При этом в когортах пациентов, получавших СМ и инсулин, наблюдалось незначительное увеличение числа гипогликемий [33].
Таким образом, арГПП-1 продемонстрировали преимущество в отношении контроля гликемии и массы тела по сравнению с пероральными сахароснижающими препаратами или инсулином. Выбор препаратов данного класса для интенсификации терапии больных СД2 представляется оптимальным выбором, т.к. большинство пациентов имеют избыточную массу тела или ожирение, влияющих на инсулинорезистентность (ИР).
Широко распространенный клинический подход интенсификации терапии путем добавления базального инсулина 40–60% больных СД2 не приводит к достижению целевого уровня НbА1c. При этом возможности для дальнейшей интенсификации ограничиваются только вариантом добавления к терапии арГПП-1 или прандиального инсулина [9].
В подобной ситуации выбор для инициации инъекционной терапии препарата класса арГПП-1 может служить более оптимальной стратегией с точки зрения как большей эффективности в достижении целей гликемического контроля, так и более высокого уровня безопасности в плане развития гипогликемических состояний. Важным дополнительным преимуществом такой тактики будет снижение массы тела. Кроме того, снижение риска гипогликемических состояний и массы тела – это важнейшие компоненты формирования приверженности терапии у пациентов с СД2 [10].
Если попытаться сформулировать, чего же мы ждем от современных ССП, то идеальный препарат для лечения СД2 должен не только снижать гликемию без увеличения риска развития гипогликемических состояний, но и приводить к снижению массы тела, артериального давления, нормализации уровня липидов; восстанавливать функцию β-клеток и обладать кардиопротективными свойствами.
Заключение
Использование семаглутида в комплексной терапии СД2 приводит к статистически значимому безопасному улучшению гликемического контроля, снижению массы тела вне зависимости от исходной терапии как по данным рандомизированных исследований, так и по результатам реальной клинической практики. Применение cемаглутида позволяет реализовывать принципы многофакторного подхода к терапии СД2 и улучшать долгосрочное управление заболеванием, что служит основой стратегии снижения сердечно-сосудистого риска больных СД2.



