Введение
Бронхиальная астма (БА) является одним из наиболее распространенных неинфекционных хронических заболеваний, которое поражает до 339 млн человек во всем мире, и эта цифра может увеличиться до 400 млн к 2025 г. [1, 2]. В РФ в настоящее время, по данным эпидемиологического исследования, распространенность БА составляет 6,9% среди взрослых [3] и около 10% среди детей и подростков [4]. В начале XX в. врачи не считали БА самостоятельным заболеванием и лечили ее как «острое расстройство, эпизодическое обострение» [5], что было связано в первую очередь с низкой распространенностью патологии и недостаточной ее изученностью. В XXI в. астма представляет собой отдельную нозологическую единицу, фармакотерапия которой вызывает интерес специалистов во всем мире.
Значительным успехом можно считать переход БА в категорию контролируемых заболеваний, это обусловлено приверженностью врачей по всему миру единой глобальной стратегии «GINA». Внедрение результатов научных трудов в стандарты диагностики и лечения значительно повысило качество оказываемой помощи. Но, даже несмотря на возможность управлять болезнью, заболеваемость БА возрастает и она сопряжена с огромными экономическими затратами, связанными не только с расходами на лечение, но и с материальными потерями государств из-за снижения трудоспособности болеющего населения.
Рост заболеваемости отчасти обусловлен неправильной тактикой ведения пациентов на начальных этапах заболевания, недостаточной диагностикой и дифференциальной диагностикой, а иногда – неадекватной терапией БА. Вот почему возникает необходимость более квалифицированной подготовки специалистов здравоохранения на современном этапе.
Обеспечить хорошее качество жизни пациентам с БА может только надлежащее их ведение, поэтому лечащему врачу важно обладать высоким уровнем знаний в области ключевых вопросов этиологии, патогенеза, диагностики, лечения и профилактики заболевания.
Именно поэтому особо актуально в настоящее время проведение данного и подобных исследований [6–9], направленных, прежде всего, на повышение практических знаний не только врачей, но и будущих работников здравоохранения.
Цель исследования: определение уровня базовых знаний по БА у студентов старших курсов (специальность «лечебное дело» и «педиатрия») медицинских вузов в вопросах диагностики, лечения и профилактики заболевания, используя метод анонимного анкетирования респондентов.
Методы
Анкетирование в рамках второго этапа многоцентрового проекта «ASSA» (Assessment of senior medical students in the field of bronchial asthma) – исследования по оценке знаний специалистов в области БА – было проведено в 2017–2019 гг. в 6 учреждениях высшего медицинского образования России и Украины: Белгородском государственном национальном исследовательском университете (Белгород), Воронежском государственном медицинском университете им. Н.Н. Бурденко (Воронеж), Южно-Уральском государственном медицинском университете (Челябинск), Саратовском государственном медицинском университете им. В.И. Разумовского (Саратов), Днепропетровской медицинской академии (Днепр), Башкирском государственном медицинском университете (Уфа).
Для проведения исследования в соответствии с основными положениями руководства GINA-2017 [10] была разработана оригинальная анкета, состоящая из 12 вопросов. Каждый вопрос допускал один правильный вариант ответа, за выбор которого респонденту начислялся 1 балл. При указании верного и ошибочного вариантов одновременно ответ считался неполным или частично верным и оценивался в 0,5 балла, при выборе неверного ответа участник исследования получал 0 баллов. Таким образом, при всех правильных ответах максимальный средний балл составлял 1,0. Среднее значение совокупности верных, частично верных и неверных ответов характеризовалось как «средний уровень полноты ответа на вопрос» (СПО), эквивалентное понятие – «средний уровень правильности ответов».
Отдельно оценивались средние значения ответов каждого респондента, средние по отдельным вопросам, средние значения по всей анкете. Также анализировались закономерности ответов на отдельно взятые вопросы; допускались статистически несистемные пропуски на ответы.
В анкете студенту предложено было указать свой курс и специальность, по которой происходит обучение, а также отметить, первичным или вторичным является прохождение предложенной анкеты, после чего приступить к выполнению заданий. Фамилию респонденты не указывали, анонимность анкетирования была применена для получения более независимых результатов, без влияния фактора возможной оценки.
Студенты, принимавшие участие в анкетировании, прошли обучение по стандартным образовательным программам. Следует заметить, что рассматриваемая методика оценки уровня знаний была разработана исключительно для данного исследования, является относительной и не может полноценно отобразить уровень качества образования в вузе.
Вся информация, полученная из анкет, была внесена в электронную базу данных и обработана с помощью прикладных программ Microsoft Excel и Statistica v.10. Статистические данные обрабатывались на основании анализа четырехпольных и произвольных таблиц сопряженности с использованием критерия хи-квадрат (χ2) Пирсона, при необходимости – с поправкой Йейтса и расчетом точного критерия Фишера.
Для корректного подсчета статистической значимости, приняв во внимание условия и ограничения использования таблиц сопряженности, центры с малым количеством респондентов (Саратов, Днепр, Уфа), не имевшие в сравнении между собой статистически значимой разницы (p>0,05), были объединены.
Данное анкетирование является продолжением первого этапа проекта «ASSA», начатого в 2014 г., итоговые результаты которого были опубликованы в журнале «Фарматека» № 5 за 2019 г. [11]. Частичные текущие результаты проекта ASSA-II за 2017–2018 гг. были представлены на конгрессе Европейского респираторного общества (Мадрид, 2019), опубликованы в приложении к «European Respiratory Journal» и в журнале «Research Results in Pharmacology» [12, 13].
Результаты
В анкетировании приняли участие 358 студентов-старшекурсников (из них 43,6% были из Белгорода, 22,3% – из Воронежа, 19,3% – из Челябинска, 6,7% – из Саратова, 4,5% – из Днепра и 3,6% – из Уфы); ранее – на 1-м этапе проекта в 2014–2016 гг. [11] – был опрошен 521 студент из 7 регионов России.
Средний уровень верных ответов по всем вопросам анкеты составил 74,8% (от 68,6 до 85,2% в разных центрах, р<0,01; в исследовании ASSA-I в 2014–2116 гг. нами был выявлен практически идентичный результат – 74,0%). При этом различия в ответах на отдельные вопросы составили от 46,5 до 91,1% в среднем по всему исследованию и от 44,2 до 97,1% по разным вопросам в разных центрах. Минимальный уровень правильных ответов получен на вопросы № 1 (выбор верного определения БА) – 46,5% (от 44,2 до 47,4% по центрам, p>0,05), № 3 (ключевое патогенетическое звено) – 67,6% (от 54,8 до 84,1%, p<0,01) и № 12 (выбор комбинации лекарственных средств в одном доставочном устройстве) – 62,6% (от 46,4 до 73,4%, p<0,01). Максимальный средний уровень правильных ответов зарегистрирован на вопросы № 2 (триггеры приступа БА) – 81,7% (от 75,3 до 95,3%, p<0,01), № 6 (степени тяжести БА) – 88,5% (от 85,9 до 94,2%, p<0,01) и № 9 (определение длительного приступа удушья) – 91,1% (от 88,6 до 97,1%, р>0,05). Сводные данные по уровням верных ответов на все вопросы анкеты приводим на рис. 1.
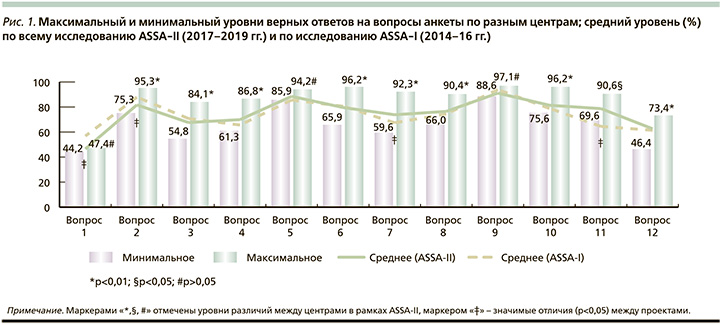
Обсуждение
В первом вопросе анкеты на выбор студентов было предложено 4 варианта определения БА, среди которых необходимо было выбрать, по их мнению, наиболее подходящее. Данное задание с успехом выполнили 46,5% опрошенных (СПО от 44,2 до 47,4% в разных центрах, p>0,05), которые выбрали в качестве ответа следующую формулировку: «гетерогенное заболевание, характеризующееся хроническим воспалением дыхательных путей, наличием респираторных симптомов, таких как свистящие хрипы, одышка, заложенность в груди и кашель, которые варьируются по времени и интенсивности и проявляются вместе с вариабельной обструкцией дыхательных путей» [10]. Наиболее частым (43,4%) ошибочным вариантом ответа среди опрошенных студентов является определение БА, как «хроническое аллергическоезаболевание дыхательных путей с развитием бронхиальной гиперреактивности с проявлениями локальной или распространенной бронхообструкции, обратимой медикаментозно». Еще часть респондентов (8,4%) считают астму «приступообразно-рецидивирующим воспалительно-аллергическим бронхообструктивным заболеванием». Реже в качестве ответа старшекурсники выбирают определение «хроническое аллергическое заболевание с не полностью обратимыми эпизодами бронхообструкции» (1,1%). Вариант «затрудняюсь ответить» выбрали 0,3% респондентов и оставшиеся 0,3% не ответили на данный вопрос. Сравнительный анализ выявил статистически значимую разницу в проектах: уровень ответов в ASSA-I на аналогичный вопрос был выше (56,8%, p=0,003) [11], что мы связываем с изменением привычной формулировки определения БА в новой редакции GINA.
Во втором вопросе анкеты респонденты должны были указать возможные триггерные факторы развития приступа БА. Все предложенные варианты: воздействие бытовых аллергенов, физическое напряжение, воздействие холода, прием нестероидных противовоспалительных средств [10, 14, 15], оказались верными. Студенты, выбравшие ответ «любой из вышеназванных», составили большинство опрошенных, а именно – 81,7% (СПО от 75,3 до 95,3%, p<0,01). На этот вопрос в 1-й фазе проекта респонденты отвечали лучше, различия статистически значимые (87,9%, p=0,014).
Ключевое патогенетическое звено БА любого генеза – гиперреактивность бронхов, которая развивается в ответ на воздействие ряда неспецифических раздражителей окружающей среды и приводит к инициации IgE-обусловленных реакций гиперчувствительности. При контакте с аллергеном у предрасположенных к атопии лиц В-лимфоциты продуцируют большое количество аллерген-специфических IgE-антител, фиксирующихся на высокоаффинных рецепторах, локализованных на мембранах тучных клеток. Это приводит к сенсибилизации клеток и слизистой оболочки дыхательных путей. Последующий контакт с аллергеном и обусловленная им агрегация IgE на поверхности клеток вызывают активацию тучных клеток и сопровождаются выбросом медиаторов воспаления, таких как гистамин, серотонин, триптаза, протеазы, фактор хемотаксиса эозинофилов, нейтрофилов. Первичные медиаторы воспаления и продукты метаболизма арахидоновой кислоты – простагландины (РGD2) и лейкотриены (LTC4) – вызывают повышение проницаемости сосудистого русла, отек слизистой оболочки дыхательных путей, спазм гладкой мускулатуры бронхов, инфильтрацию ткани эозинофилами и нейтрофилами, усиливают секрецию бронхиальных желез [10, 16].
В третьем вопросе, в отличие от таких предложенных вариантов ответов, как аллергизация организма, гиперчувствительность слизистой оболочки дыхательных путей, нарушение тонуса бронхиальной мускулатуры, старшекурсникам необходимо было верно выделить основное патогенетиченское звено развития БА: гиперреактивность бронхов.
Правильный вариант ответа выбрали 67,6% респондентов (СПО от 64,8 до 84,1%, р<0,01). В исследовании ASSA-I получен близкий результат (70,8%, р=0,323).
В четвертом вопросе респондентам необходимо было выбрать наиболее подходящие инструментально-лабораторные маркеры БА. С данным заданием справились 69,9% студентов (СПО от 61,3 до 86,8%, p<0,01), считавших основными диагностическими критериями заболевания снижение ОФВ1, повышение уровня IgЕ и эозинофилию; в первой фазе проекта выявлены сходные знания (65,6%, р=0,192) [10, 14–16].
В пятом вопросе анкеты старшекурсникам на выбор были предложены следующие методы диагностики БА: рентгенография легких, бронхография, бронхоскопия, исследование функции внешнего дыхания, среди которых необходимо было выделить основной. Поскольку для данного заболевания характерно вариабельное ограничение скорости воздушного потока, в качестве диагностического мероприятия обязательно проводят спирометрию, т.е. применяют методы, направленные на исследование функции внешнего дыхания (ФВД) [10,16]. 88,5% опрошенных студентов успешно справились с заданием, выбрав данный вариант ответа (СПО от 85,9 до 94,2%, p>0,05); в исследовании ASSA-I получены результаты без статистически значимых различий (85,6%, р=0,217).
Согласно классификации, тяжесть течения БА оценивают, исходя из клинических симптомов, потребности в бронхолитических препаратах и объективной оценки проходимости дыхательных путей. Эксперты международной организации GINA и члены Российского респираторного общества выделяют четыре степени тяжести БА [10, 14]:
- Легкая интермиттирующая: симптомы реже 1 раза в неделю; короткие обострения; ночные симптомы не чаще 2 раз в месяц; ОФВ1 или пиковая скорость выдоха (ПСВ) ≥80% от должного, разброс ПСВ или ОФВ1 <20%.
- Легкая персистирующая: симптомы чаще 1 раза в неделю, но реже 1 раза в день; обострения могут снижать физическую активность и нарушать сон; ночные симптомы чаще 2 раз в месяц; ОФВ1 или ПСВ ≥80% от должного, разброс ПСВ или ОФВ1 20–30%.
- Персистирующая средней тяжести: ежедневные симптомы; обострения могут приводить к ограничению физической активности и нарушению сна; ночные симптомы чаще 1 раза в неделю; ежедневное использование ингаляционных короткодействующих β2-агонистов (КДБА); ОФВ1 или ПСВ 60–80% от должного, разброс ПСВ или ОФВ1 >30%.
- Тяжелая персистирующая: ежедневные симптомы; частые обострения; частые ночные симптомы; ограничение физической активности; ОФВ1 или ПСВ ≤60% от должного, разброс ПСВ или ОФВ1 >30%.
В шестом вопросе анкеты студентам необходимо было указать существующие по классификации степени тяжести БА. С заданием успешно справилось 79,6% респондентов (СПО по участвовавшим центрам составил от 65,9 до 96,2%, p<0,01). В ходе первого этапа исследования был получен аналогичный уровень знаний старшекурсников в данном вопросе (80,6%, р=0,729).
Необходимо понимать, что степень тяжести БА зависит не только от выраженности симптомов заболевания, но и от эффективности проводимой терапии. Кроме того, степень тяжести не является неизменной характеристикой пациента и может меняться в течение определенного временного промежутка. Исходя из этого положения, в настоящее время в современной клинической практике целесообразно руководствоваться классификацией БА по уровню контроля. Контроль БА определяет выраженность симптомов заболевания у пациента и степень их уменьшения с возможностью полного устранения в результате проведенного лечения. Он состоит из двух основных составляющих: контроль уже имеющихся симптомов (текущий контроль) и оценка риска неблагоприятных исходов в будущем (оценка будущего риска). Важно оценивать обе эти составляющие для того, чтобы предотвратить развитие обострений БА [10, 14, 16–18].
Эксперты международной организации GINA классифицируют астму как хорошо контролируемую, неконтролируемую и частично контролируемую по четырем параметрам: наличие дневных симптомов, ночное пробуждение из-за симптомов, частота использования препаратов неотложной помощи и степень ограничения активности. Данные параметры оценивают за последние 4 недели с учетом также факторов риска обострений, для выявления которых проводят исследование функции внешнего дыхания в начале лечения, через 3–6 недель и время от времени в дальнейшем [10, 17].
Большинство пациентов склонны недооценивать имеющиеся у них симптомы заболевания и переоценивать эффективность терапии. Чтобы правильно оценить уровень контроля БА, существует ряд методик: скрининговая «Три вопроса Королевской коллегии врачей»; категорийная методика экспертов GINA; методики «численной» оценки контроля БА, которые в отличие от категорийных методик более чувствительны к изменению контроля симптомов: тест по контролю над астмой – Asthma Control Test™ (АСТ™) и вопросник по контролю астмы – Asthma Control Questionnaire (ACQ) [10, 14, 16–18].
В седьмом вопросе анкеты студентам необходимо было указать уровни контроля БА, согласно существующей классификации. На этот вопрос верно ответили 73,8% опрошенных, выбрав следующие варианты: полный, неполный, неконтролируемая БА. СПО составил от 59,6 до 92,3% в разных центрах, p<0,01. По сравнению с данными ASSA-I знания улучшились, что подтверждается и в ходе статистической обработки данных (67,4%, р=0,042).
Важным методом оценки эффективности терапии БА является пикфлуометрия, которая подходит для ежедневного определения степени выраженности бронхиальной обструкции пациентами самостоятельно в домашних условиях. Метод основан на измерении ПСВ, т.е. максимальной скорости, с которой человек может выдохнуть после глубокого вдоха. Пикфлуометрия обеспечивает раннее выявление обострений БА и дает возможность определить провоцирующие их факторы, кроме того, с помощью данного диагностического метода симптомы заболевания находятся под контролем непосредственно пациента [13, 16, 19].
В восьмом вопросе респонденты определяли метод самоконтроля течения БА, который врач должен посоветовать использовать пациенту в домашних условиях. Вопрос не вызвал сомнений у 76,5% студентов, которые, среди предложенных методов диагностики (дыхательный тест, пикфлуометрия, пневмометрия, спирография), остановили свой выбор на методе пикфлуометрии (СПО от 66,0 до 90,4%, p<0,01). В период проведения 1-го этапа был отмечен аналогичный уровень верных ответов 74,5% (р=0,498).
БА – циклическое заболевание, для которого характерны периоды ремиссии и периоды обострения. Обострения (синонимы: приступ БА, острая БА) представляют собой изменения относительно обычного статуса пациента, достаточно выраженные для того, чтобы потребовалось изменение терапии. Эти изменения характеризуются ухудшением уже имеющихся симптомов и показателей функции внешнего дыхания (снижение ПСВ и ОФВ1) или первичными проявлениями астмы. Спровоцировать приступ могут как воздействие внешних раздражающих факторов, так и неэффективность базисной терапии, направленной на контроль заболевания. Согласно классификации, выделяют легкое, среднетяжелое и тяжелое обострения БА, жизнеугрожающую астму и БА, близкую к фатальной. Приступ у одних пациентов может сформироваться в течение нескольких минут или часов, у других – в течение нескольких дней (до 10–14). Полное исчезновение симптомов обострения наблюдается в интервале от 5 до 14 дней [10, 16, 20].
Длительный приступ удушья, развивающийся при неблагоприятном течении обострения БА, называется «астматический статус» (синонимы: «жизнеугрожающая астма»; «астма, близкая к фатальной»), клиническим проявлением которого является эпизод острой дыхательной недостаточности.
Выбрав этот вариант ответа в девятом вопросе анкеты, правы оказались 91,1% тестируемых студентов (СПО от 88,6 до 97,1%, р>0,05). Статистически значимых отличий от результатов проекта ASSA-I не выявлено (93,9%, р=0,117).
Целью лечения обострений БА являются быстрое купирование эпизода бронхообструкции и гипоксемии, лечение воспаления и предотвращение рецидива. При легком и среднетяжелом обострении начальный этап терапии заключается в многократном применении ингаляционных быстродействующих β2-агонистов (БДБА; от 2 до 4 ингаляций каждые 20 минут в течение первого часа). После первого часа необходимая доза β2-агонистов будет зависеть от степени тяжести обострения [10, 20–24].
В десятом вопросе анкеты студентам было предложено указать первый шаг неотложной помощи при обострении БА. Были предложены такие варианты ответов: 1) искусственная вентиляция легких (ИВЛ), 2) КДБА, 3) ингаляционные глюкокортикостероиды (ИГКС), 4) системные ГКС, 5) эуфиллин, 6) затрудняюсь ответить. Правильный ответ (КДБА) выбрали 81,4% опрошенных. СПО составило от 75,6 до 96,2% в разных центрах (р<0,01). В 2014–2016 гг. уровень ответов не отличался статистически значимо – 78,9% (р=0,318).
Проанализировав выбранные варианты ответов по данному вопросу, авторы статьи резюмировали, что 18,6% опрошенных ошиблись в определении группы препарата (от 3,8 до 24,4% неправильных ответов в разных центрах). Структура ошибочных ответов была следующей: 42,1% респондентов считают, что первым шагом терапии обострения БА являются ИГКС, 31,3% в качестве препарата неотложной помощи выбрали эуфиллин, 17,2% старшекурсников купировали бы острое состояние системными гормонами и 4,7% считают, что начать лечение необходимо с ИВЛ. Также 3,1% опрошенных испытали затруднение при ответе на данный вопрос и еще 1,6% студентов оставили поле без ответа (рис. 2).

Помимо купирования обострений заболевания, лечение БА также включает назначение базисной терапии для постоянного контроля над симптомами, профилактики осложнений и нежелательных побочных эффектов лекарств. Ступенчатый подход к терапии астмы предполагает назначение необходимого объема лечения с учетом уровня контроля заболевания и наличия факторов риска [10, 14].
В одиннадцатом вопросе анкеты студенты выбирали подходящую комбинацию препаратов для базисной терапии БА средней тяжести из таких вариантов:
- ИГКС+эуфиллин;
- ИГКС+длительнодействующий β2-агонист (ДДБА;
- Эуфиллин+ДДБА;
- М-холинолитик+ДДБА;
- Затрудняюсь ответить.
Правильное сочетание (ИГКС+ДДБА) определили 78,7% студентов (СПО от 69,6 до 90,6% по центрам, p<0,05) [13, 16, 20–25]. На втором этапе исследования выявлено статистически значимое улучшение уровня знаний (в проекте ASSA-I – 64,5%, p<0,001).
Таким образом, 21,3% (от 9,4 до 30,4% неверных ответов в разных группах) студентов указали варианты с неправильной комбинацией препаратов. Среди них 43,4% в качестве базисной терапии выбрали сочетание эуфиллин+ДДБА, 39,5% посчитали верной комбинацию М-холинолитик+ДДБА, которая не соответствует современным клиническим рекомендациям, 10,5% опрошенных для лечения БА средней тяжести применили бы сочетание ИГКС+эуфиллин и 6,6% выбрали вариант «затрудняюсь ответить» (рис. 3).
Самая важная цель лечения пациентов с БА заключается в предотвращении развития обострений, т.к. они служат причиной прогрессирования заболевания, снижения качества жизни и инвалидизации. Для достижения лучшего контроля БА в клиническую практику был введен режим «терапия единым ингалятором», основанный на применении комбинации фиксированных доз ИГКС и ДДБА в одном устройстве [10, 16, 20–25].
В заключительном, двенадцатом, вопросе анкеты старшекурсникам было предложено определить существующую комбинацию лекарств в одном доставочном устройстве, которая используется для лечения БА.
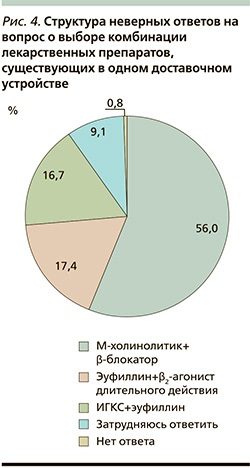 Выбрать правильное сочетание препаратов (ИГКС+ДДБА) смогли 62,6% опрошенных студентов (СПО от 46,4 до 73,4% в разных центрах, p<0,01); в 1-й фазе проекта верно ответили 61,4% студентов (р=0,715). Ошибочные ответы дали 37,4% респондентов (от 26,6 до 53,6% в разных центрах), и они были представлены следующими вариантами: в 56,0% случаев комбинацией М-холинолитик+β-адреноблокатор (при этом многие респонденты не акцентировали внимание на специфической подсказке в виде «β-блокатор», а не «β-агонист»), в 17,4% – сочетанием эуфиллин+ДДБА, 16,7% студентов в качестве ответа выбрали ИГКС+эуфиллин, 9,1% респондентов испытали затруднение с определением правильного варианта и 0,8% оставили вопрос без ответа (рис. 4).
Выбрать правильное сочетание препаратов (ИГКС+ДДБА) смогли 62,6% опрошенных студентов (СПО от 46,4 до 73,4% в разных центрах, p<0,01); в 1-й фазе проекта верно ответили 61,4% студентов (р=0,715). Ошибочные ответы дали 37,4% респондентов (от 26,6 до 53,6% в разных центрах), и они были представлены следующими вариантами: в 56,0% случаев комбинацией М-холинолитик+β-адреноблокатор (при этом многие респонденты не акцентировали внимание на специфической подсказке в виде «β-блокатор», а не «β-агонист»), в 17,4% – сочетанием эуфиллин+ДДБА, 16,7% студентов в качестве ответа выбрали ИГКС+эуфиллин, 9,1% респондентов испытали затруднение с определением правильного варианта и 0,8% оставили вопрос без ответа (рис. 4).
Заключение
Анкетирование, проведенное среди студентов старших курсов медицинских вузов в 2017–2019 гг. в рамках второго этапа мультицентрового исследования (проект ASSA), показало, что базовые знания старшекурсников по вопросам этиологии, патогенеза, клиники, диагностики и лечения БА находятся на уровне выше среднего. В целом в течение двух лет проведения данного опроса респонденты успешно справлялись с поставленными задачами и показали достаточно высокий уровень знаний по некоторым вопросам анкеты, таким как поиск триггера БА, классификация степеней тяжести заболевания и выбор определения длительного приступа удушья.
При сравнении с 1-м этапом исследования (ASSA-I) по большинству вопросов не было выявлено статистически значимых различий в уровне знаний, а общие средние результаты в проектах ASSA-I и ASSA-II оказались практически идентичными. Самый низкий процент правильных ответов был получен на следующие вопросы: определение БА, ключевое патогенетическое звено БА любого генеза, комбинация лекарств для терапии БА, существующая в одном доставочном устройстве.
Выводы
Проведение данного и подобных исследований среди студентов старших курсов медицинских вузов, будущих специалистов здравоохранения, обусловлено прежде всего необходимостью повышения качества знаний в области диагностики, лечения и профилактики различных нозологических единиц. Для достижения этой цели необходимо комплексное обучение, заключающееся в преемственности клинических дисциплин в медицинских вузах. Проведение дополнительных образовательных мероприятий, семинаров, создание учебно-методической литературы, базирующейся на актуальных нормативных документах, а также увеличение количества академических часов по базовым дисциплинам поможет улучшить качество оказываемой медицинской помощи.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов. Исследование проводилось без участия спонсоров. По результатам исследования получено Свидетельство о государственной регистрации базы данных [26].a


