Введение
Несмотря на то что при лимфоме Ходжкина (ЛХ) поражение легких достаточно распространено (15–40% случаев), первичная легочная лимфома Ходжкина (PPHL – Hodgkin’s primary pulmonary lymphoma) является довольно редким проявлением болезни Ходжкина. PPHL представляет <1% всех лимфом, в т.ч. и среди первичных легочных злокачественных новообразований [1]. Клиническая картина PPHL иногда может имитировать наличие инфекционного или воспалительного агента, что затрудняет диагностический процесс. Хотя опухолевый очаг с распадом и изъязвлением не редкость во время проведения химиотерапии по поводу PPHL, но на момент постановки диагноза это считается исключительно редким проявлением болезни. Описываемый нами случай служит примером сложности распознавания нетипичной патологии органов средостения и легких.
Клинический случай
Больная Т. 1989 г. рождения 26.03.2019 обратилась в поликлинику по месту жительства с жалобами на сухой кашель, периодические боли в левой половине грудной клетки, слабость и потерю массы тела на 12 кг за последние 3 месяца. Произведена рентгенография грудной клетки, осмотрена хирургом и направлена на консультацию онколога.
В консультативную поликлинику ТГФ РСНПЦОиР больная обратилась 6 апреля 2019 г., где в амбулаторных условиях была обследована.
Фибробронхоскопия (ФБС) от 07.04.2019: сдавление и прорастание извне верхнедолевого бронха слева.
Патогистологическое исследование № 530/19 от 10.04.2019: плоскоклеточный с-r in situ.
Мультиспиральная компьютерная томография (МСКТ) органов грудной клетки от 13.04.2019: в верхней доле левого легкого (в прикорневой области 3-го сегмента), прорастая в переднее средостение и в перикард, определяется объемное образование неправильной формы размером (АР×ТR×СС) 7,5×6,5×7,3 см. Образование неоднородной сóлидной структуры (+29+39 НU) с нечеткими контурами. Перифокально в верхней доле левого легкого отмечаются единичные сóлидные узелки диаметром до 1,0 см с нечеткими контурами. Диффузное интерстициальное поражение левого легкого: меж- и внутридольковые перегородки утолщены. В средостении определяются множественные паратрахеальные, субкаринальные, парааортальные, левые корневые лимфоузлы диаметром до 4,0 см. Правое легкое без особенностей. В подключичной области слева отмечаются множественные лимфатические узлы диаметром до 15 см. Заключение: признаки объемного образования верхней доли левого легкого, прорастающего в переднее средостении и в перикард. Умеренный гидроперикард. Единичные сóлидные узелки в верхней доле левого легкого. Интерстициальное поражение левого легкого (лимфангаитический карциноматоз?). Лимфаденопатия средостения и левой подключичной области.
МСКТ органов грудной клетки с в/в контрастированием от 15.04.2019: после в/в контрастирования плотность образования повысилась до +40+68 НU. Образование муфтообразно охватывает и прорастает левую верхнюю легочную вену, левую ветвь ствола легочной артерии, верхнедолевую легочную артерию и перикард. Также данное образование тесно прилежит к стволу легочной артерии – к медиастинальной и костальной частям плевры. В средостении, проекции яремной вырезки, в левой подмышечной области преимущественно субпекторально определяются множественные увеличенные лимфатические узлы размером до 20 мм, образующие конгломераты. В субкаринальной области конгломерат размером 26×64×53 мм. Во II сегменте левого легкого выявлено образование округлой формы с неровными нечеткими контурами размером 17×17×14 мм, плотностью +28+31 НU. После в/в контрастирования плотность повысилась до +53+58 НU. Заключение: признаки объемного образования средостения и корня левого легкого с признаками прорастания в прилежащие структуры. Узловое образования II сегмента левого легкого. Выраженная ЛАП средостения и левой подмышечной области. Гидроперикард (см. рисунок).
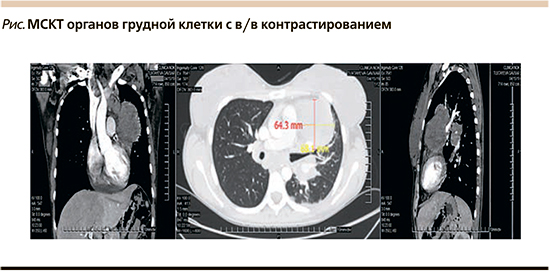
В связи с расхождением заключений специалистов компьютерной томографии (КТ), а также для полноценного морфологического исследования патологического очага произведена повторная ФБС с биопсией.
Патогистологическое исследование № 8309/19 от 12.04.2019: клеточные элементы слизистой оболочки бронха с воспалительно-геморрагической инфильтрацией.
Несмотря на двукратную ФБС с биопсией, окончательную морфологическую картину опухолевого очага установить не удалось.
Магнитно-резонансная томография (МРТ) головного мозга от 14.04.2019: признаки умеренной атрофии лобно-височной областей с обеих сторон. Левосторонний гайморит.
МРТ органов брюшной полости от 08.04.2019: признаки диффузного поражение печени. Гепатомегалия. Хронический холецистит.
МРТ органов малого таза от 14.04.2019: признаки состояния после кесарево сечения.
По решению консилиума 18.04.2019 больная госпитализирована в хирургическое отделение торакоабдоминальной онкологии ТГФ РСНПМЦОиР.
Со стороны клинико-биохимических показателей крови существенных изменений не выявлено.
20.04.2019 у больной развилось легочное кровотечение, проявившееся обильным кровохарканьем, неподдающимся консервативной гемостатической терапии. На основании решения консилиума по витальным показаниям выполнена расширенно-комбинированная пульмонэктомия слева с резекцией перикарда, интраперикардиальной обработкой сосудов.
Протокол операции от 20.04.2019. Ревизия. В плевральной полости жидкости нет. В корне левого легкого пальпируется плотная опухоль, умеренно подвижная размером 11×10×10 см, прорастающая в перикард. Отмечается увеличение бронхопульмональных и корневых лимфоузлов до 2,0 см, паратрахеальных до 4,0 см.
С помощью биполярной электрокоагуляции и острым путем рассечена медиастинальная плевра и перикард кзади от диафрагмального нерва и кпереди от корня левого легкого. Рассечена нижняя легочная связка. При вскрытии перикарда отмечается серозный выпот около 300 мл. Инфильтрированная медиастинальная клетчатка мобилизована острым путем, обнажены передние стенки верхней и нижней легочных вен и легочной артерии.
Учитывая характер интраоперационной находки, решено выполнить комбинированно-расширенную пульмонэктомию с интраперикардиальной обработкой сосудов.
Органокомплекс. Удаленное левое легкое, медиастенальная клетчатка с лимфатическими узлами (бронхопульмональные корневые до 4,0 см; паратрахеальные до 2,0 см) и лимфатическими сосудами, ткань перикарда с опухолью плотно-эластической консистенции размером 11×10×10 см. Послеоперационное течение гладкое. Пациентка выписана из стационара в удовлетворительном состоянии.
Патогистологическое исследование операционного материала № 8507 от 22.04.2019. ЛХ по нодулярно-склерозному варианту.
Пересмотр препарата в условиях НМИЦ онкологии им. Н.Н. Блохина № 8507 от 20.05.2019. В лимфоузлах картина ЛХ, для уточнения диагностики рекомендуется иммуногистохимическое (ИГХ) исследование.
ИГХ-исследование от 13.06.2019. Морфоиммуногистохимическая картина соответствует классической ЛХ, вариант – NS I, EBV, инфильтрация эозинофилами умеренно выражена.
С учетом окончательно установленной морфологической картины патологического очага по решению консилиума 28.06.2019 от 20.09.2019 проведено 3 курса химиотерапии по схеме ABVD (адриамицин, блеомицин, винбластин, дакарбазин).
По данным контрольного обследования от 04.10.2019, признаков болезни не отмечено. С 07.10 по 31.12.2019 проведено 3 курса химиотерапии по аналогичной схеме.
На сегодняшний день пациентка чувствует себя удовлетворительно, жалоб не предъявляет, ECOG-1. По данным контрольного обследования признаков болезни не выявлено. Медиана наблюдения составила 10 месяцев.
Обсуждение
PPHL является редкой нозологией. С 1927 г. зарегистрировано около 100 случаев [2–3]. Как правило, для постановки диагноза необходимо наличие трех критериев: характерные гистологические особенности ЛХ, ограничение заболевания легкими с минимальным поражением лимфатических узлов и отсутствие внелегочного заболевания [4]. У данной пациентки имели место все три критерия. Рентгенологически PPHL может имитировать пневмонию, рак легких или метастатическую опухоль [5]. В отличие от метастатической опухоли ЛХ в легких, которая распределяется по всей паренхиме легкого, PPHL в большинстве случаев поражает исключительно верхние отделы легких [6]. С учетом специфичности течения PPHL инструментальные методы исследования имеют низкую разрешающую способность, что приводит к использованию более инвазивных диагностических методов, в частности трансторальной пункции, торакоскопической хирургии с использованием видео- или открытой биопсии легкого. В самой большой серии работ A.I. Radin et al. из 39 проведенных бронхоскопий только одна оказалась диагностической [1]. Помимо этого имеются данные, будто диагноз PPHL в ряде случаев был установлен после оперативного вмешательства. Это подчеркивает трудности в подтверждении диагноза с помощью КТ-биопсии.
Наиболее распространенным гистологическим подтипом, встречающимся в PPHL, считается узловой склерозирующий подтип ЛХ, который также чаще встречается у женщин [7]. Данные по выживаемости по-прежнему отсутствуют из-за низкой частоты встречаемости патологии.
В данном случае объем хирургического вмешательства был адекватным с онкологической точки зрения, в связи с чем не было показаний к проведению радиотерапии.
Тем не менее, т.к. ЛХ имеет системный характер, пациентке был проведен стандартный режим химиотерапии с учетом иммуногистохимии опухоли. Режим адриамицина, блеомицина, винбластина, дакарбазина (ABVD) предпочтительнее, чем мехлоретамин, винкристин, прокарбазин и преднизон (MOPP), с точки зрения эффективности и токсичности [8]. Превосходство блеомицина, этопозида, адриамицина, циклофосфамида, винкристина, прокарбазина и преднизона (BEACOPP) еще предстоит определить.
Выводы
PPHL не имеет классической картины течения болезни и одновременно лучевые методы визуализации при данной патологии не высокочувствительны. Наличие осложнения болезни в виде легочного кровотечения при данной патологии является казуистикой в литературе. Соответственно, осведомленность коллег о заболевании с нетипичным течением имеет первостепенное значение из-за высоких шансов на излечение, особенно для молодых пациентов.


