Введение
Люди, страдающие сахарным диабетом 2 типа (СД2), могут прожить долгую и здоровую жизнь, если им вовремя поставлен диагноз и назначено лечение. Целый ряд относительно недорогостоящих мероприятий может помочь людям, у которых диагностирован СД, успешно справляться с ним. К этим мероприятиям относятся контроль уровня глюкозы крови посредством комбинации соответствующего питания, физической активности и лекарственной терапии; контроль артериального давления и уровня холестерина для снижения риска сердечно-сосудистых заболеваний (ССЗ) и других осложнений; регулярная диспансеризация для выявления осложнений со стороны глаз, почек и стоп для назначения своевременного лечения. Ранние диагностика и начало лечения – отправная точка благополучной жизни с диабетом [2].
СД2 является хроническим прогрессирующим заболеванием, течение которого требует тщательного контроля со стороны как врача, так и самого пациента. Заболеваемость СД2 несколько сократилась в последние годы, однако мы все же можем наблюдать неуклонный рост новых случаев болезни (рис. 1).
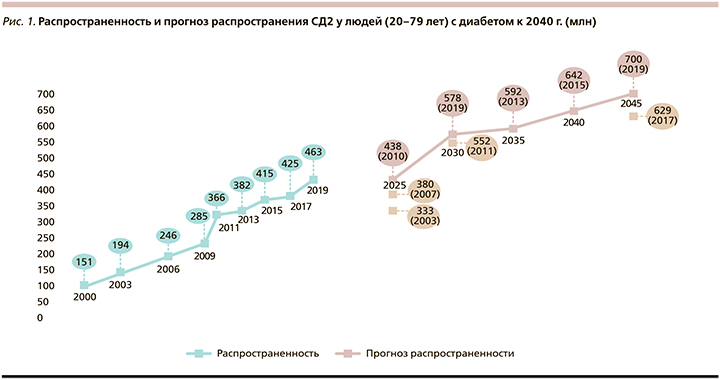
К 2040 г. в мире ожидается рост заболеваемости до 642 млн [1]. Такому тревожному увеличению распространенности СД2 на фоне возрастания продолжительности жизни способствуют известные факторы: избыточная масса тела и ожирение, усугубляемые низкой физической активностью, избыточное потребление быстроусвояемых углеводов и низкое – овощей и фруктов.
Другой не менее важной проблемой является выраженная декомпенсация углеводного обмена как на момент постановки диагноза, так и в дальнейшем, когда пациент уже получает сахароснижающую терапию. По данным исследования NATION, средний уровень гликированного гемоглобина (HbA1c) у пациентов с впервые диагностированным СД2 составил 7,4%. При этом у 19,3% данный показатель достиг более 9%. Это свидетельствует о выраженной декомпенсации углеводного обмена на момент постановки диагноза, необходимости более тщательного скрининга пациентов.
В связи с вышеизложенным в 2019 г. были обновлены основные диабетологические рекомендации (Американской и Европейской диабетических ассоциаций), одним из пунктов которых является рассмотрение инициации терапии с комбинированной сахароснижающей терапией пациентов с впервые выявленным СД2. Так, например, при исходном уровне HbA1c, превышающем целевой уровень на 1,5%, рекомендовано инициировать сахароснижающую терапию с двух препаратов.
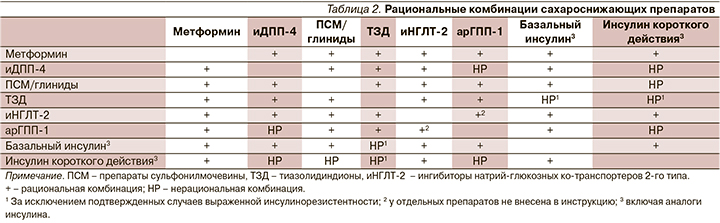
Кроме этого выбор лечебной стратегии предлагается оценивать в зависимости от клинической ситуации и особенностей пациента, его коморбидных патологий. В табл. 1 представлены варианты сахароснижающей терапии в зависимости от коморбидности и других особенностей.

Как видно из представленной табл. 1, одна из главных терапевтических задач сегодня – это влияние на исходы: сердечно-сосудистые и почечные при сохранении эффективного сахароснижающего действия с высокой безопасностью в отношении гипогликемических событий.
На сегодняшний день у нас есть три инновационных класса сахароснижающих препаратов, которые продемонстрировали сердечно-сосудистую нейтральность или кардиопротективное действие в отношении сердечно-сосудистых исходов и нефропротективный эффект.
Класс иДПП-4 обладает хорошо изученным, патогенетически обоснованным воздействием. Ингибиторы ДПП-4 высокоселективно воздействуют на фермент ДПП-4, что обусловливает минимальную частоту побочных эффектов при приеме препаратов. Однако не все представители класса обладают одинаковыми свойствами. Так, повышенная частота госпитализации по поводу сердечной недостаточности (СН) была отмечена при применении саксаглиптина [14], аналогичная тенденция наблюдалась у алоглиптина [17]. Ситаглиптин и линаглиптин показали сердечно-сосудистую нейтральность в отношении MACE (нефатальный инфаркт миокарда – ИМ, нефатальный инсульт, сердечно-сосудистая смертность) и частоты госпитализаций по поводу СН [12], что делает выбор этих препаратов более приоритетным.
Исследование TECOS по оценке сердечно-сосудистых исходов при применении ситаглиптина, проведенное с участием 14 671 пациента с СД2 длительностью 6 лет, продемонстрировало высокий профиль безопасности ситаглиптина в отношении MACE и влияния на частоту госпитализаций по причине СН, что дало возможность данному препарату иметь очень высокий рейтинг в своем классе (рис. 2).
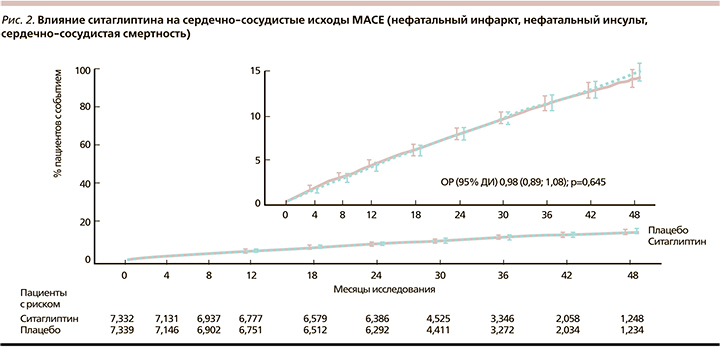
Как обсуждалось ранее, современная сахароснижающая терапия для большинства пациентов с СД2 должна быть комбинированной. В табл. 2 представлены современные рациональные комбинации сахароснижающих препаратов, где показано, что сочетанное применение иДПП-4 возможно с достаточно большим числом других лекарственных средств.
По данным Московского регистра, 22% пациентов с СД2 получают в качестве комбинации или мононазначений инсулинотерпию (Московский сегмент ФРСД, 2019).
По данным исследования CREDIT, средний уровень HbA1c для старта инсулинотерапии составляет 9,7% в Российской Федерации.
В реальной клинической практике эндокринологи опасаются применения инсулина из-за риска развития гипогликемий. Глюкозозависимые эффекты иДПП-4 позволяют сделать терапию инсулином более безопасной.
В исследование CompoSIT-I включены 746 пациентов со средним возрастом 58,3 года, HbA1c – 8.8%, индексом массы тела – 31,1 кг/м2 и длительностью СД2 – 10,8 года. Пациенты были разделены на две группы: 1-я – ситаглиптин+гларгин±метформин, 2-я – плацебо+гларгин±метформин. Период наблюдения составил 30 недель. Исследование продемонстрировало высокую эффективность комбинации ситаглиптина с базальным инсулином, в которой 54,2% пациентов добились целевого уровня HbA1c менее 7%. Во второй группе «плацебо+базальный инсулин» целевых значений гликемии добились 35,4%. В исследовании показано, что комбинация базального инсулина и ситаглиптина более безопасна в отношении гипогликемических событий. Так, отношение шансов развития гипогликемии в течение 30 недель составило 0,73 (0,54; 0,98; р=0,039), что означает, что в группе ситаглиптина с базальным инсулином риск развития гипогликемии на 27% ниже, чем в группе сравнения. Сахароснижающая эффективность ситаглиптина и базального инсулина представлена на рис. 3 А и В.
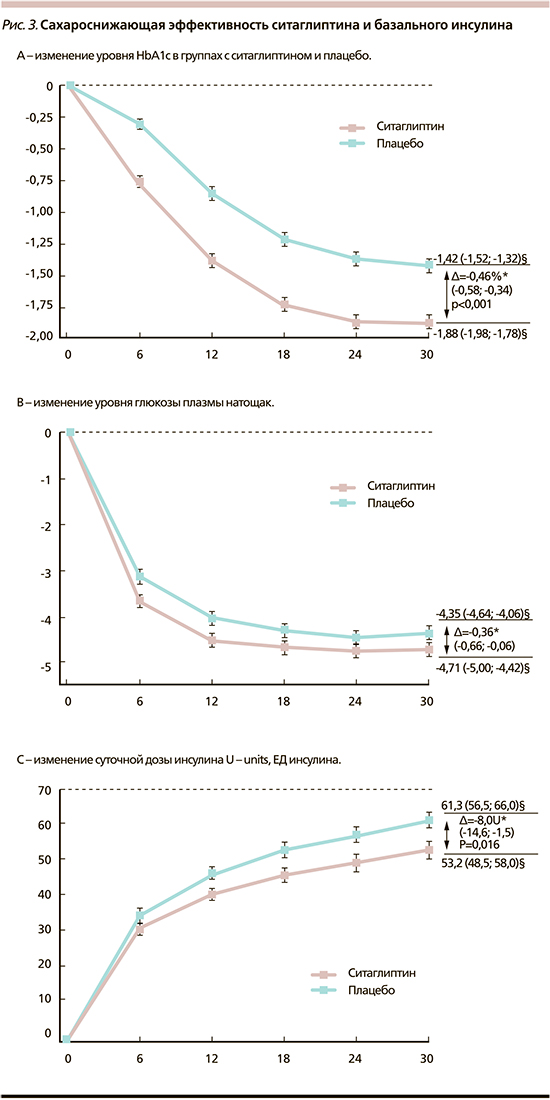
Так, в группе плацебо к 30-й неделе наблюдения уровень HbA1c снизился на 1,42%, в группе ситаглиптина – на 1,88%. Разница в снижении уровня HbA1c оказалась достоверной, и дельта снижения составила 0,46%. Такая же тенденция сохраняется в отношении динамики гликемии натощак: отмечается снижение уровня более чем на 4 ммоль/л от исходного, однако в группе ситаглиптина динамика более выражена (рис. 3 С) [24].
Часто у пациентов с СД2 обнаруживается чрезмерная инсулинизация, которая приводит к прибавке массы тела, повышенному аппетиту и дополнительным гипогликемическим событиям. Как известно, максимальной дозы инсулина не существует, но часто имеет место быть его передозировка.
В связи с этим данное исследование глюкозозависимого действия иДПП-4, в частности ситаглиптина, показало, что в группе комбинированной терапии дозы инсулина, потребовавшиеся для достижения целевого уровня HbA1c и глюкозы крови натощак, в среднем были на 8 ЕД меньше, чем в группе сравнения, что делает выбор данного варианта комбинированной терапии высокоэффективным, безопасным и дающим возможность пациентам положительно влиять на массу тела.
Заключение
Ингибиторы ДПП-4 доступны в течение последнего десятилетия и показаны к лечению пациентов с СД2. Обладающие высокой эффективностью и малым числом побочных эффектов, эти препараты получили мировое признание и широко используются во врачебной практике. Учитывая прогрессирующий характер течения СД2, необходимо преодолевать клиническую инертность и интенсифицировать сахароснижающую терапию, если того требует клиническая ситуация. Немало пациентов с СД2 имеют осложнения и сопутствующие заболевания, поэтому добавление лекарственных препаратов к терапии должно сопровождаться как можно меньшим риском лекарственных взаимодействий и быть безопасным для пациента.
Результаты рандомизированных клинических исследований по влиянию на сердечно-сосудистые исходы c участием нескольких молекул класса иДПП-4 обеспечили подтверждение сердечно-сосудистой и общей безопасности в отношении данных представителей группы. Учитывая активное изучение и распространение препаратов новых классов сахароснижающей терапии, иДПП-4 остаются важным классом пероральных сахароснижающих препаратов, обеспечивающих уникальное глюкозовисимое патогенетически направленное действие с массой других хорошо изученных негликемических эффектов, позволяя широко их использовать в реальной клинической практике на разных этапах подбора сахароснижающей терапии.


