Актуальность
Инсульт представляет собой одну из основных причин смертности и инвалидизации в мире. После инсульта часто встречаются нарушения когнитивных функций, бремя которых оказывает существенное влияние как на самого пациента, так и на его семью и общество в целом [1, 2]. Изучению когнитивных нарушений после инсульта посвящены многочисленные исследования, в которых анализируются эпидемиология, патогенез, особенности вариантов клинических проявлений, прогноза развития, коморбидные состояния, наиболее эффективные подходы к лечению [3, 4]. При этом, как известно, само по себе «познание» не является унитарной концепцией, оно неразрывно связано с эмоциональным состоянием, физической активностью человека, его социальным функционированием [5, 6]. Все эти процессы, тесным образом сопряженные с многоуровневой интеграцией системы, позволяют головному мозгу осуществлять сложные умственные процессы, дают возможность выбирать и обрабатывать поступающую информацию, при этом формируется более или менее гармоничная ответная реакция, зависящая от исходного функционального состояния пациента [7, 8].
С учетом сложной природы когнитивного функционирования сегодня предпринимаются многочисленные попытки восстановления после инсульта, включая ряд нефармакологических вмешательств, таких как музыкотерапия, аэробные и силовые тренировки с всевозможными комплексами физических упражнений, эрготерапия, рациональное питание, массаж, мануальная терапия, рефлексотерапия, электростимуляция и вибротерапия [9, 10]. С развитием компьютеризированных высокотехнологичных устройств в арсенал средств восстановительного лечения вошли методы виртуальной реальности, транскраниальная магнитная стимуляция, роботизированные устройства с биологической обратной связью [11, 12].
Результаты фундаментальных исследований в области нейробиологии, нейрофизиологии когнитивной деятельности последних десятилетий свидетельствуют: объединение информации от различных сенсорных модальностей является перспективным для формирования адекватной поведенческой реакции пациента, особенно когда сигнал от единственной модальности вызывает недостаточный поведенческий отклик или когда сенсорная система в целом ослаблена [13, 14].
Мозг обладает способностью к автоматической одновременной обработке и интеграции сенсорной информации. Объединение информации из различных сенсорных модальностей облегчает способность обнаруживать, различать и распознавать сенсорные стимулы, поэтому обучение в мультисенсорной среде представляется эффективным [15, 16].
Исследования, проведенные на животных, демонстрируют, что особи, перенесшие экспериментальный инсульт, а затем подверженные мультисенсорной стимуляции через воздействие обогащенной среды, демонстрируют результаты, свидетельствующие о повышении пластичности мозга и восстановлении его функции после перенесенного острого церебрального эпизода [17].
Один из недавних систематических мета-обзоров, целью которого было объединение и оценка доказательств эффективности мультисенсорной стимуляции (т.е. стимуляции по крайней мере двух из следующих сенсорных систем: зрительной, слуховой и соматосенсорной) в качестве возможного метода реабилитации после инсульта, объединил электронные базы данных Scopus и PubMed для поиска статей, которые были опубликованы до 2015 г. (21 исследование) и, несмотря на положительные свидетельства позитивного влияния данного подхода, рекомендует проведение дальнейших исследований с рассмотрением потенциальных механизмов мультисенсорной стимуляции для реабилитации [18].
На сегодняшний день на основе полученных данных формируется целое направление в нейрореабилитации, подтверждающее, что стимулирование множественных сенсорных модальностей (т.е. мультимодальная стимуляция – ММС) может быть полезным для коррекции неврологического дефицита после инсульта, включая снижение силы в конечностях, повышение мышечного тонуса, утрату равновесия, сенсорные, вегетативные нарушения, когнитивные и эмоционально-поведенческие расстройства [19, 20].
Используемые в настоящее время в реабилитации после инсульта методы ММС включают двигательные образы, наблюдение за действиями, тренировки с помощью зеркал или в виртуальной среде, различные виды музыкальной терапии [21, 22].
В настоящее время уже имеется опыт использования мультидоменного влияния с использованием комплексных реабилитационных методик при восстановлении не только двигательных функций, но и когнитивного дефицита, включающий физические упражнения, ходьбу, когнитивные и аэробные тренировки [23, 24]. Высокую эффективность показали мультидоменные тренинги, в т.ч. с использованием биологической обратной связи, включавшие занятия на стабилометрической платформе по опорной реакции [25], на программно-аппаратном комплексе «Экзокисть-2» [26, 27].
Именно мультимодальное воздействие, сочетание традиционных и современных высокотехнологичных методов лечения могут оказать эффективное влияние на процесс восстановления после перенесенного церебрального инсульта [28, 29].
Ранее нами уже были опубликованы результаты исследования, в котором программа ММС использовалась в лечении больных в восстановительном периоде инсульта. Лечебные результаты после проведенного курса ММС продемонстрировали эффективность предложенного подхода в восстановлении когнитивных функций после инсульта и регрессе эмоционально-поведенческих расстройств [30]. По результатам работы был получен патент РФ на изобретение «Способ реабилитации пациентов с постинсультными нарушениями» (№ 2688723), зарегистрированный 22.05.2019 [31].
Цель настоящего исследования: изучение влияния повторных курсов программы ММС на регресс когнитивных и эмоционально-поведенческих нарушений у пациентов после церебрального инсульта.
Методы исследования
В когортном проспективном исследовании приняли участие 12 пациентов, проходивших реабилитационное лечение в условиях неврологического отделения ГБУЗ МО МОНИКИ им. М.Ф. Владимирского с диагнозом «церебральный инсульт» сроком от 2 месяцев до двух лет с момента развития заболевания. Диагноз устанавливали на основании жалоб пациента, оценки неврологического статуса, данных нейровизуализационного исследования (компьютерная томография, магнитно-резонансная томография головного мозга). У 10 пациентов был диагностирован ишемический инсульт, у 2 – геморрагический инсульт. Средний возраст больных составил 61,5 (52–66,5) год. Все пациенты имели постинсультный гемипарез с выраженностью от 1 до 4 баллов по 6-балльной шкале оценки мышечной силы, преимущественно в руке, а также когнитивные нарушения со степенью выраженности от легкой до умеренной.
Критерии включения пациентов при отборе для настоящего исследования включали ознакомление с информацией с подписанием информированного согласия на участие в нем; возраст от 18 до 80 лет; подтверждение наличия ишемического или геморрагического инсульта данными нейровизуализационного исследования (КТ/МРТ головного мозга); давность инсульта от одного месяца до двух лет; постинсультный спастический парез руки различной степени выраженностью от 0 до 3 баллов по шкале Ashworth и от 1 до 4 баллов по Британской шкале оценки мышечной силы; постинсультные легкие или умеренные когнитивные нарушения (более 23 баллов по шкале MMSE).
Критерии исключения: отказ пациента от участия в исследовании; когнитивные нарушения уровня деменции; наличие выраженных когнитивных нарушений до инсульта и иной этиологии; клинически выраженное тревожно-депрессивные расстройство, требующее прием препаратов группы антидепрессантов; наличие леворукости; сенсорная афазия, грубая моторная афазия (≥3 баллов по коммуникационной шкале Гудгласса–Каплана); наличие соматической патологии в стадии декомпенсации; тяжесть состояния, не позволяющая пациенту самостоятельно передвигаться; эпилепсия; наличие патологии зрения и слуха, препятствующее проведению занятий; уровень спастичности в руке более 3 баллов по шкале Ashworth; двигательные нарушения в руке иной природы; наличие очагов головного мозга непостинсультной этиологии по данным нейровизуалиции (КТ/МРТ головного мозга).
Для оценки эффективности лечения пациентам было проведено обследование с использованием оценочных клинических шкал и тестов в динамике при каждом курсе лечения (до начала лечения и по его окончании). Были использованы: Монреальская шкала оценки когнитивных функций (МоСА), тест «Запоминание 10 слов» по методике А.Р. Лурия, тест Струпа, субтест 9 «Кубики Коса» теста Векслера, таблицы Шульте, шкала тревоги и депрессии (HADS).
В соответствии с целью исследования все пациенты проходили 2 курса лечения с использованием программы ММС, интервал между курсами лечения составил 3–4 месяца. Пациентам наряду со стандартными методами лечения, включившими фармакотерапию по вторичной профилактике инсульта, проводилась программа ММС, в т.ч. занятия на комплексе «Экзокисть-2», когнитивные тренинги с использованием наглядного материала или компьютерной программы, занятия на стабилометрической платформе с биологической обратной связью по опорной реакции и вибротерапию [31].
Каждое занятие на комплексе «Экзокисть-2» включала 3 сессии по 10 минут с перерывами на 3–5 минут. Количество проведенных занятий на курс лечения составило 8–10. Занятия на стабилометрической платформе с биологической обратной связью по опорной реакции с использованием зрительных и слуховых каналов проводились путем выполнения игровых заданий, целью которых было удержание центра давления в пределах предлагаемой мишени [23]. Когнитивные тренинги, длительность которых определялась индивидуально и составляла в среднем 20–30 минут, основывались на решении пациентом логических задач на счет, праксис, пространственно-конструктивное мышление, внимание. Вибротерапия проводилась в количестве 8–10 процедур на курс на виброплатформе (POWERFUL STEP) длительностью 10–15 минут для верхних и нижних конечностей.
Статистический анализ проведен с применением пакета прикладных программ STATISTICA 12.0 (StatSoft®, 2011) и Excel (Microsoft Office Excel, 2016). Были использованы критерий Манна–Уитни (p<0,05) и непараметрический критерий Вилкоксона (p<0,05).
Результаты исследования
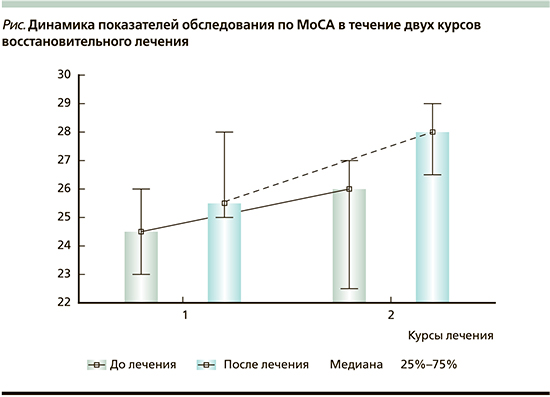
В результате проведенного повторного курса лечения с использованием программы ММС от пациентов после инсульта были получены следующие результаты. При оценке динамики когнитивных функций с использованием МоСА отмечено статистически значимое повышение общего балла как после первого (p<0,01), так и после второго курса лечения (p<0,01). Между курсами лечения значение показателя не снижалось. Таким образом, полученный лечебный эффект сохранялся на протяжении нескольких месяцев, что стало значимым результатом для пациентов при проведении реабилитационных мероприятий после инсульта (см. рисунок).
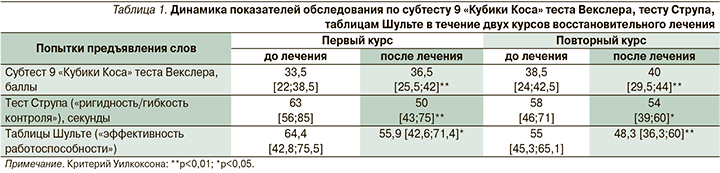
При оценке результатов обследования пациентов с использованием субтеста 9 «Кубики Коса» теста Векслера медиана показателя до первого курса лечения составила 33,5 [22; 38,5] балла, после лечения – 36,5 [25,5; 42] баллов (p<0,01). Медиана показателя до второго курса лечения составила – 38,5 [24; 42,5] баллов, после повторного курса лечения – 40 [29,5; 44] баллов (p<0,01). Таким образом, после каждого курса лечения было отмечено статистически значимое улучшение в отсутствие ухудшения между курсами лечения, что свидетельствовало о стойкости лечебного эффекта (табл. 1).
После проведенного лечения, согласно тесту Струпа, у пациентов отмечалось улучшение способности к когнитивной переключаемости, в результате чего уменьшался эффект «интерференции», что вело к уменьшению ригидности познавательного контроля.
При проведении первого курса лечения медиана показателя «ригидность/гибкость контроля» теста Струпа до лечения составила 63 [56;85] секунды, после лечения – 50 [43;75] секунд (p<0,01). В результате повторного курса лечения медиана показателя до лечения составляла уже 58 [46;71] секунд, а после лечения – 54 [39;60] секунды (p< 0,05). Таким образом, после каждого курса лечения отмечалось статистически значимое улучшение когнитивного контроля (табл. 1).
При оценке показателя «эффективность работоспособности» по таблицам Шульте было выявлено статистически значимое улучшение после каждого курса лечения. Медиана данного показателя до первого курса лечения составила 64,4 [42,8;75,5], после – 55,9 [42,6;71,4] секунды (p<0,05); при втором курсе – 55 [45,3;65,1] и 48,3 [36,3;60] секунды соответственно (p<0,01). Улучшение показателя «эффективность работоспособности» свидетельствовало о повышении концентрации внимания у пациентов, проходивших два курса лечения с использованием программы ММС (табл. 1).
После проведенного лечения у пациентов отмечалось улучшение памяти. Изменение показателей наблюдалось и после первого, и после повторного курса терапии с использованием программы ММС.
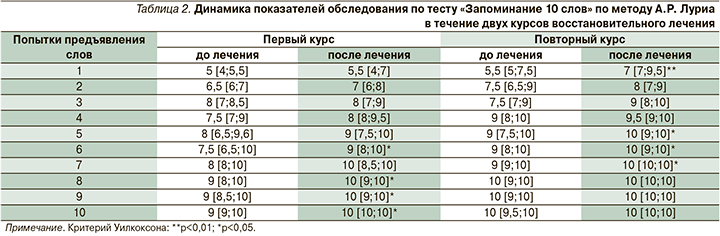
Согласно данным проведенного теста «Запоминание 10 слов» по методу А.Р. Лурия, после первого курса лечения статистически значимое улучшение было выявлено при 6-й (p<0,05), 8-й (p<0,05), 9-й (p<0,05) и 10-й (p<0,05) попытках.
После второго курса лечения статистически значимое улучшение запоминания слов было отмечено при первой (p<0,01), 5-й (p<0,05), 6-й (p<0,05) и 7-й (p<0,05) попытках. Таким образом, при каждом курсе лечения отмечалось статистически значимое улучшение процессов запоминания и воспроизведения аудиальной информации (табл. 2).
На фоне проведенной терапии у пациентов отмечался регресс эмоционально-поведенческих нарушений. Согласно данным обследования пациентов до и после лечения с использованием шкалы HADS, после первого и повторного курсов лечения отмечалось снижение медианы показателя «депрессия» (р<0,01). После первого курса лечения она снизилась с 9 [3;9] до 5 [3;6] баллов (p<0,01); после второго курса – с 7 [4;10] до 6 [2;7] баллов (p<0,01). В перерыве между курсами лечения статистически значимого ухудшения данного показателя не наблюдалось (р>0,05), что свидетельствовало о стойкости лечебного эффекта.
Обсуждение
Таким образом, как показали результаты проведенного исследования, повторные курсы лечения с применением программы ММС были эффективными и безопасными для пациентов в восстановительном периоде инсульта. После каждого из двух курсов комплексного лечения отчетливо отмечалось статистически значимое изменение показателей, свидетельствующее об улучшении в состоянии больных, восстановлении когнитивных функций, по данным обследования в динамике по шкале МоСА (p<0,01). Улучшении памяти было отмечено по тесту «Запоминание 10 слов» по методу А.Р. Лурия (p<0,01, p<0,05); конструктивно-пространственных навыков – по субтесту 9 «Кубики Коса» теста Векслера (p<0,01); концентрации внимания – по таблицам Шульте (p<0,01, p<0,05), способности к когнитивной переключаемости – по тесту Струпа (p<0,01, p<0,05). Улучшалось эмоциональное состояние пациентов, наблюдался регресс депрессивных нарушений, согласно данным обследования по шкале HADS (p<0,01).
Заключение
Использование программы мультимодальной стимуляции с применением повторных курсов в лечении пациентов в восстановительном периоде инсульта целесообразно с учетом полученных данных результатов исследования. При оценке состояния когнитивных функций и эмоционального состояния больных была отмечена положительная динамика. Лечебный эффект от проведенного лечения характеризовался стойкостью, не было выявлено статистически значимого снижения показателей оценочных шкал между курсами лечения. Более того, наблюдался эффект «умножения» результата в восстановлении утраченных функций после каждого проведенного курса.
Использованный подход мультидоменного воздействия является, безусловно, перспективным. Полученные данные свидетельствуют о необходимости продолжения данного исследования, получения нового опыта с целью решения проблем нейрореабилитации пациентов после инсульта с использованием комплексных методик, включающих применение высоких технологий.
Вклад авторов
Исакова Е.В. – информационный поиск по данной теме и редактирование статьи.
Слюнькова Е.В. – сбор и обработка данных исследования


