Введение
На протяжении многих лет хроническая обструктивная болезнь легких (ХОБЛ) входит в состав основных заболеваний, лидирующих в причинах летальности, в т.ч. среди лиц трудоспособного возраста. Являясь прогрессирующим заболеванием, ХОБЛ, несомненно, приводит к развитию тяжелой дыхательной недостаточности [1].
В настоящее время накоплен определенный опыт комплексного лечения хронических бронхообструктивных заболеваний, в котором лидирующее место принадлежит ингаляционной терапии. Результаты клинических исследований, составляющих основу доказательной медицины, позволяют выделить длительнодействующие бронходилататоры в качестве базового лечения ХОБЛ. Монопрепараты, имеющие в составе либо длительнодействующий антихолинергический компонент (ДДАХП), либо длительнодействующий β2-агонист (ДДБА), рекомендованы для стартовой терапии ХОБЛ пациентам с невыраженными симптомами [1, 2], на фоне отказа от курения пациентам с ХОБЛ. Кроме того, ДДАХП применяются в качестве третьего компонента при необходимости усиления бронхолитической терапии при сохраняющейся симптоматике, если пациент уже получает комбинацию ингаляционного кортикостероида и ДДБА [1, 2]. Добавление ДДАХП в последнем случае благоприятно воздействует на функцию легких и обострения ХОБЛ [2].
В последние несколько лет в медицинскую практику вошли ингаляционные бронходилатационные препараты с 24-часовым действием. Их удобно принимать пациентам, что повышает приверженность терапии. Кроме того, непрерывная бронходилатация обеспечивает эффект фармакологического стентирования и снижает гиперреактивность бронхов. Из группы ДДБА с 24-часовым действием в Российской Федерации зарегистрирован только индакатерол. ДДАХП с суточным эффектом бронходилатации представлены в нашей стране тиотропия бромидом и гликопиррония бромидом [2].
Фармакокинетические и фармакодинамические особенности гликопиррония
Гликопирроний реализует бронходилатационный эффект, блокируя мускариновые рецепторы (М). Препарат обладает значительно более высокой селективностью к М1–3-рецепторам, чем к рецепторам М2, в связи с чем оказывает незначительное влияние на сердечно-сосудистую систему: частота тахикардий, аритмий и других побочных эффектов со стороны сердечно-сосудистой системы в клинических исследованиях была сопоставимой с плацебо [3, 4]. Кроме того, гликопирроний отличает быстрое начало действия: показано, что бронходилатационный эффект наступает через 6,1±2,1 минуты, что почти в 5 раз превосходит действие тиотропия (29,4±4,2 минуты) [5]. Быстрота наступления эффекта имеет значение даже для базисной терапии ХОБЛ, поскольку в данном случае пациенты могут быстро ощутить эффект от ингаляции и связать улучшение симптомов с действием препарата.
Двадцатичетырехчасовое действие гликопиррония доказано как клинически, так и фармакокинетически. Во всех исследованиях с серийным измерением объема форсированного выдоха в первую секунду (ОФВ1) подтверждено достоверное увеличение показателя в каждой точке суточного промежутка без тенденции к снижению в конце 24-часового периода.
Что касается фармакокинетики гликопиррония, то при ингаляционном пути введения чуть более половины (52%) ингаляционной дозы гликопиррония депонируется в легких, 4–7% поступает в желудочно-кишечный тракт и абсорбируется в нем.
В легких происходит накопление гликопиррония, который быстро диссоциирует и повторно связывается с М3-рецепторами (т.н. эффект повторного связывания – rebinding effect). В связи с чем рецепторы не остаются надолго заблокированными (через 4,5 часа 50% рецепторов способны реагировать на воздействие других препаратов, что важно, в т.ч. в случае обострения ХОБЛ при необходимости применения комбинированных короткодействующих бронходилататоров – КДБД). Следует отметить, что у тиотропия через аналогичный период освобождаются только 10% рецепторов. При этом 24-часовой бронходилатирующий эффект гликопиррония реализуется за счет длительного периода накопления молекулы в легких, а также rebinding-эффекта. Относительно короткий период полувыведения гликопиррония (Т1/2=6 часов) из плазмы крови свидетельствует о хорошем профиле безопасности препарата [6].
Необходимо еще раз подчеркнуть, что, с одной стороны, гликопирроний имеет длительное депонирование в легких, что и определяет его эффект в течение суток, с другой – препарат быстро выводится из системного кровотока, что в свою очередь определяет высокий профиль безопасности в режиме ежедневного долговременного применения [7].
В то же время в режиме регулярных ежедневных ингаляций равновесное состояние гликопиррония бромида достигается в течение недели.
Результаты популяционного фармакокинетического анализа позволили сделать вывод, согласно которому у пациентов с ХОБЛ и нарушением функции почек легкой и средней степеней тяжести (оцениваемой по скорости клубочковой фильтрации – СКФ ≥30 мл/мин/1,73 м2) препарат гликопирроний может применяться без ограничения дозы [8].
Ингаляционное устройство типа Бризхалер®
Бризхалер® – современное ингаляционное устройство, обладающее рядом преимуществ, к которым относятся низкое внутреннее сопротивление (не требуется усиления вдоха во время ингаляции), эффективная доставка лекарства в дыхательные пути вне зависимости от возраста и тяжести ХОБЛ. Больные, страдающие тяжелыми формами ХОБЛ, показали более высокую скорость вдоха через Бризхалер® по сравнению с ХандиХалером®, а именно 72 против 36 л/мин, что подтверждает более низкое внутреннее сопротивление формы доставки Бризхалер® [9]. Гликопирроний выпускается в капсулах для ингаляций с дозой 50 мкг; доставленная доза препарата составляет 44 мкг.
Клиническая эффективность гликопиррония
Клиническая эффективность и безопасность гликопиррония в суточной дозе 50 мкг однократно в сутки доказана в ряде рандомизированных плацебо-контролируемых двойных слепых клинических исследований (РКИ) III фазы с участием более 2000 больных ХОБЛ среднетяжелой и тяжелой степеней, а также при сравнении с тиотропием в суточной дозе 18 мкг в открытом режиме в качестве препарата сравнения. Длительность наблюдения составила от 6 до 12 месяцев. Приведенные результаты суммированы по итогам выполнения РКИ GLOW I–III (GLycopyrronium bromide in COPD airWays).
Влияние на ОФВ1. В исследовании GLOW I [10] на фоне однократного применения гликопиррония бромида 50 мкг/сут отмечено достоверное увеличение ОФВ1, измеренного перед следующей плановой ингаляцией (т.н. конечного ОФВ1), на 108 мл по сравнению с плацебо. В результате терапии тиотропием получен сходный прирост конечного ОФВ1, который составил 83 мл по сравнению с плацебо [11]. В обоих РКИ бронходилатационный эффект гликопиррония стойко сохранялся в течение суток, а также на протяжении всего последующего периода наблюдения за больными ХОБЛ при однократном режиме дозирования препарата в дозе 50 мкг/сут.
Показана быстрота наступления эффекта гликопиррония: через 5 минут после первой ингаляции ОФВ1 достоверно увеличился на 87–93 мл, через 15 минут – на 143–144 мл по сравнению с плацебо. Результатом первой ингаляции тиотропия было повышение ОФВ1 через 5 и 15 минут только на 45 и 78 мл соответственно по сравнению с плацебо [10, 11]. Достоверное различие в степени бронходилатации, обусловленной гликопирронием и тиотропием, отмечается в течение первых 4 часов после ингаляции (площадь под кривой ОФВ1 в течение 4 часов составила 0,197±0,0095 л в группе гликопиррония и 0,141±0,0109 л в группе тиотропия с достоверной разницей между ними 0,056±0,0095 л [р<0,001]) [11].
Влияние на одышку и другие симптомы ХОБЛ. Через 26 недель лечения гликопирроний существенно уменьшает выраженность одышки – в 1,3 раза по сравнению с плацебо [10], сравнимые результаты демонстрирует лечение тиотропием [11].
В результате терапии гликопирронием число суток, включая ночное время без симптомов ХОБЛ и дней, когда симптомы ХОБЛ не нарушали повседневной активности, было существенно больше, чем в группе плацебо, и сопоставимо с аналогичными показателями в группе тиотропия [10, 11]. Частота применения быстродействующих бронхолитиков для облегчения симптомов ХОБЛ была достоверно ниже у пациентов, получающих гликопирроний, по сравнению с плацебо и сопоставимой с группой лечения тиотропием [10, 11].
Влияние на переносимость физических нагрузок. В конце 3-недельного периода лечения гликопирронием больные среднетяжелой и тяжелой ХОБЛ отметили повышение толерантности к физической нагрузке – время выполнения субмаксимальной нагрузки на тредмиле увеличилось на 21% по сравнению с группой плацебо. Важно отметить, что уже на второй день применения препарата исследуемый показатель повысился на 10%, что дополнительно свидетельствует в пользу его высокой и быстрой эффективности [12].
Обострения ХОБЛ, в т.ч. потребовавшие госпитализации. Частота среднетяжелых и тяжелых обострений ХОБЛ уменьшилась на 31% через 26 недель лечения и на 34% через 52 недели лечения гликопирронием по сравнению с плацебо [10, 11].
Риск тяжелых обострений, послуживших основанием для госпитализации, через 26 недель терапии гликопирронием был на 65% ниже, чем в группе плацебо (отношение рисков [OР]=0,35; 95% доверительный интервал [ДИ] – 0,141–0,857), стационарное лечение потребовалось только 1,7% больных, получавших гликопирроний, по сравнению с 4,2% пациентов группы плацебо [10]. Частота обострений в течение года составила 0,54 в группе гликопиррония против 0,80 эпизода в группе плацебо [11].
Важно отметить, что риск обострений, потребовавших назначения системных стероидов или антибиотиков по сравнению с плацебо, снизился в группе гликопиррония на 39 и на 31% соответственно, в группе тиотропиума различия с плацебо составили 38 и 35% [11].
За последние 2 года препарат Сибри® Бризхалер® был успешно применен нами в отношении более чем 70 пациентов c ХОБЛ, прослеженных в динамике на протяжении 3 месяцев и более. Ниже приведены отдельные клинические наблюдения, демонстрирующие эффективность использования данного препарата.
Клинический случай 1
Пациент Б. 47 лет, программист, стаж интенсивного курения – 19 лет по 1 пачке в день, обратился с жалобами на сильный утренний кашель с отделением небольшого количества вязкой слизистой мокроты, одышку при значительной физической нагрузке. Продуктивный кашель отмечает на протяжении последних 10 лет, в последние полгода отметил появление одышки при физической нагрузке. По рекомендации участкового врача для уменьшения одышки применяет сальбутамол, потребность в сальбутамоле ежедневная, до 2–4 ингаляций в сутки. Год назад был госпитализирован по поводу пневмонии.
При осмотре: грудная клетка нормостенична, дыхание жесткое, сухие хрипы на выдохе, частота сердечных сокращений (ЧДД) – 16 в минуту, тоны сердца ритмичные, частота сердечных сокращений (ЧСС) – 76 уд/мин, артериальное давление (АД) – 120/70 мм рт.ст., отеков нет. Индекс массы тела (ИМТ) – 23 кг/м2. Оценка одышки по шкале mMRC (Modified Medical Research Council)=1 балл, CAT (COPD Assessment Test) – 9 баллов. Сатурация кислорода – 98%. Спирометрия (постбронходилатационная): ОФВ1 – 65%, ФЖЕЛ (форсированная жизненная емкость легких) – 95%, ОФВ1/ФЖЕЛ – 0,57, обратимость бронхообструкции ∆ОФВ1 – 5%. Уровень α1-антитрипсина сыворотки в пределах нормы. На электрокардиограмме (ЭКГ) изменений не выявлено.
Пациенту поставлен диагноз «ХОБЛ с нарушением бронхиальной проходимости средней степени тяжести (II), невыраженными клиническими симптомами (САТ=9, mMRC=1), редкими обострениями. Дыхательная недостаточность (ДН)=0». Индекс курения – 19 пачка/лет. С пациентом проведена беседа о необходимости отказа от курения. Пациент рассказал, что пытался бросить курить несколько раз, но его попытки не привели к успеху в связи с усилением кашля при отказе от курения. В качестве базисной терапии ХОБЛ, а также для облегчения отказа от курения, был назначен препарат гликопиррония бромид (Сибри® Бризхалер®) в дозе 50 мкг/сут. Через 3 недели больной отметил уменьшение выраженности симптомов, значительно сократилось использование сальбутамола «по потребности», уменьшил число выкуриваемых сигарет, но полностью от курения отказаться не мог. Была назначена никотинзамещающая терапия на фоне продолжения базисной терапии ХОБЛ Сибри® Бризхалер® 50 мкг/сут. Пациент смог отказаться от курения через 2 месяца. Через 12 месяцев терапии Сибри® Бризхалер® получена объективная положительная динамика с улучшением легочной функции (табл. 1); пациент не курит, самочувствие хорошее, состояние удовлетворительное, потребности в скоропомощных препаратах нет. Рекомендовано продолжить базисную терапию Сибри® Бризхалер® 50 мкг/сут.
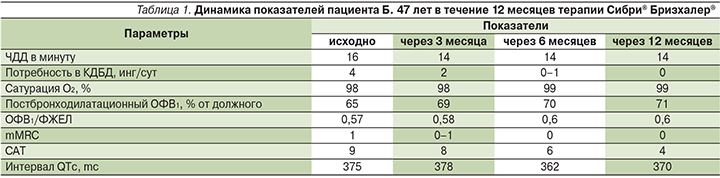
Клинический случай 2
Пациентка К. 54 года, закройщица в меховом ателье, страдает бронхиальной астмой с 20-летнего возраста.
Курит с 16 лет по 1 пачке в день (индекс курения – 38 пачка/лет). Обратилась с жалобами на появление одышки при умеренной физической нагрузке, не связанной с приступами удушья, а также на учащение приступов кашля с отделением небольшого количества вязкой слизистой мокроты. Больная в качестве базисной терапии бронхиальной астмы применяла Симбикорт® Турбухалер® 160/4,5 мкг 2 раза в сутки на протяжении последних 8 лет, однако в последний год астма контролируется плохо, сохраняется ежедневная потребность в короткодействующих бронхолитиках до 4–6 ингаляций в сутки, было 2 обострения на фоне острой респираторной вирусной инфекции, потребовавших дополнительного назначения парентеральной антибактериальной терапии. При осмотре: грудная клетка нормостенична, дыхание жесткое, сухие разнокалиберные хрипы, ЧДД – 18 в минуту, тоны сердца ритмичные, ЧСС – 82 уд/мин, АД – 130/80 мм рт.ст. ИМТ – 24 кг/м2, сатурация кислорода – 96%.
Спирометрия (с бронхолитиком): ОФВ1 – 63%, ФЖЕЛ – 94%, ОФВ1/ФЖЕЛ – 0,53, обратимость бронхообструкции ∆ОФВ1 – 12%. Одышка по шкале mMRC=2 балла, CAT – 15 баллов. На ЭКГ изменений не выявлено. R-графия органов грудной клетки: эмфизематозность верхних отделов легких, опущение нижнего края легких. Диагноз: «бронхиальная астма средней степени тяжести, неконтролируемая, III ступень терапии, в сочетании с ХОБЛ средней степени тяжести по бронхиальной обструкции, с выраженными симптомами. ДН=0».
В дополнение к применяемой базисной терапии Симбикорт® Турбухалер® 160/4,5 мкг 2 раза в сутки назначен препарат гликопиррония бромид (Сибри® Бризхалер®) 50 мкг/сут. Через неделю больная отметила снижение выраженности одышки, уменьшение кашля, приступов удушья не было, потребность в скоропомощных препаратах снизилась до 1–2 раз в неделю, что позволило рассматривать достижение медикаментозного контроля сочетания бронхиальной астмы и ХОБЛ и продолжить трехкомпонентную терапию. Через 12 месяцев наблюдался полный медикаментозный контроль (табл. 2), самочувствие пациентки оставалось хорошим, состояние удовлетворительным, признаков дыхательной недостаточности не было, не отмечено ни одного обострения.
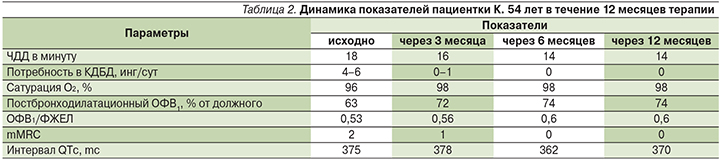
Клинический случай 3
1. Больной Т. 76 лет, пенсионер. Страдает ХОБЛ в течение 30 лет. Несмотря на рекомендации, регулярную базисную терапию не применял, для уменьшения одышки периодически использовал Беродуал®. Обратился через 2 недели после выписки из стационара, где находился в связи с обострением ХОБЛ, с жалобами на возобновление интенсивного кашля с трудноотделяемой слизистой мокротой, усиление одышки при небольшой физической нагрузке. Обострение ХОБЛ, потребовавшее госпитализации, было связано с инфекцией, получал в стационаре парентеральную антибактериальную терапию. При выписке из стационара была назначена базисная терапия препаратом тиотропия бромид (в ингаляторе Респимат®) 5 мкг/сут. Сопровождающий пациента родственник подтвердил, что в стационаре пациент отмечал положительный эффект после ингаляции тиотропия, медицинский персонал неоднократно проводил демонстрацию правильного использования устройства, однако дома пациент самостоятельно не смог правильно пользоваться ингалятором и положительного эффекта не ощущал. Для облегчения одышки опять начал применять Беродуал® до 6 ингаляций в сутки.
При осмотре: несколько астеничен, грудная клетка эмфизематозна, в легких дыхание жесткое, сухие хрипы, ЧДД – 20 в минуту. Тоны сердца ритмичные, ЧСС – 88 в минуту, АД – 135/80 мм рт.ст. Отеков нет. ИМТ – 25кг/м2. Спиромерия (постбронходилатационная): ОФВ1 – 54%, ФЖЕЛ – 79%, ОФВ1/ФЖЕЛ – 0,58, обратимость бронхообструкции ∆ОФВ1 – 1%; Оценка одышки по шкале mMRC=2 балла, CAT – 12 баллов.
При анализе амбулаторной карты выявлено, что пациент в течение 15 лет наблюдается с сахарным диабетом 2 типа, получает терапию пероральными сахароснижающими препаратами. В биохимических анализах крови на протяжении последних 3 месяцев отмечалось преходящее повышение уровня креатинина до 137 мкмоль/мл, снижение СКФ по MDRD (Modification of Diet in Renal Disease Study) при повторных анализах до 47 мл/мин, что было расценено как проявление диабетической нефропатии. Рекомендовано наблюдение диабетолога. Выявленное снижение СКФ ограничивало дальнейшее применение тиотропия бромида (инструкция препарата Спирива® Респимат®). Назначен препарат гликопиррония бромид (Сибри® Бризхалер®) 50 мкг/сут. Проведено обучение технике ингаляции. Через неделю регулярной терапии отмечена устойчивая положительная динамика: уменьшились кашель, одышка, потребность в дополнительном применении коротко действующего ингалятора сократилась, самочувствие хорошее, состояние удовлетворительное (табл. 3). Использование ингалятора Бризхалер® затруднений не вызывает.
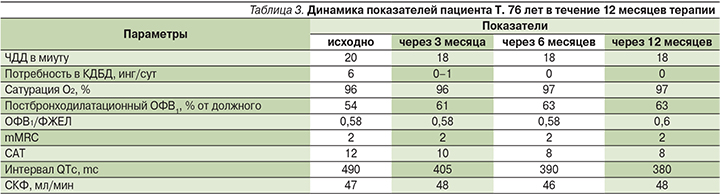
Заключение
Приведенные клинические примеры показывают высокую эффективность и безопасность терапии гликопирронием, демонстрируют возможность быстро и действенно уменьшить выраженность симптомов, значительно улучшить легочную функцию, не оказывая негативного влияния на сердечно-сосудистую систему. Важным компонентом эффективности ингаляционной терапии является простота использования системы доставки лекарственного средства. Необходимо обучение пациента и проверка правильности техники ингаляции.
Таким образом, поскольку ХОБЛ является прогрессирующим, инвалидизирующим заболеванием, важно своевременное начало высокоэффективной патогенетически обоснованной бронхолитической терапии. Терапия гликопирронием способствует быстрому уменьшению симптомов ХОБЛ, улучшению легочной функции а следовательно, способствует увеличению продолжительности времени без обострений, что ассоциировано с более высоким качеством жизни пациентов с ХОБЛ и лучшим контролем заболевания [1, 13].


