ЭПИДЕМИОЛОГИЯ
Аллергический ринит представляет собой глобальную проблему здравоохранения. В мире аллергическим ринитом страдают по крайней мере 10–25% населения. В США число больных аллергией превышает 40 млн человек, из них 25–30 млн страдают аллергическим ринитом. В Англии распространенность аллергического ринита составила 16%, в Дании – 19%, в Германии от 13 до 17%.
Многолетние эпидемиологические исследования показывают прогрессирующий рост числа лиц, страдающих аллергическим ринитом. Так, по данным статистики из Швейцарии, распространение сенной лихорадки в 1926 г. было ниже 1%, а впоследствии этот показатель увеличился до 4,4% в 1958 г., 9,6% – в 1985 г. и 13,5% – в 1993 г. В других странах мира обследования, проведенные среди различных социальных слоев населения, дали сходные результаты. В разных регионах Российской Федерации распространенность аллергического ринита колеблется в пределах от 12,7 до 24%.
В Европе прямые затраты, связанные с аллергическим ринитом, ежегодно составляют 1–1,5 млрд евро, а непрямые затраты – 1,5–2 млрд евро. При оценке социально-экономического значения болезни необходимо учитывать ассоциации аллергического ринита с другими заболеваниями, в т.ч. бронхиальной астмой, синуситами, средним отитом, полипозом носа, инфекциями дыхательных путей. Поэтому знание алгоритмов диагностики и лечения аллергического ринита является необходимым как для специалистов, так и для врачей общей практики.
В последние годы отмечены следующие тенденции, касающиеся распространенности и особенностей клинического течения аллергического ринита:
- ежегодный рост заболеваемости;
- пик заболеваемости приходится на возраст от 18 до 24 лет;
- наиболее высокая распространенность аллергического ринита отмечается в экологически неблагоприятных регионах (в частности, у населения, подвергающегося воздействию химического и радиационного факторов, аллергический ринит составляет в структуре аллергопатологии более 50%).
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Этиология
Основными этиологическими факторами аллергического ринита являются:
- Пыльца растений. Для России характерны три основных сезона поллинации (цветения), определяющие три основных пика манифестации симптомов аллергического ринита: в весеннее время он связан с пылением деревьев (береза, ольха, орешник, дуб), в первой половине лета – злаковых растений (ежа, тимофеевка, рожь), в конце лета и осенью – сорных трав (полынь, подорожник, амброзия). Пыльца может переноситься ветром на значительное расстояние и вызывать появление симптомов аллергического ринита в необычное время.
- Аллергены клещей домашней пыли (видов Dermatophagoides pteronyssinus и Dermatophagoides farinae), эпидермальные аллергены (кошки, собаки, лошади и т.д.), реже – библиотечной пыли, плесневых грибков, тараканов. Хотя споры грибов и аллергены клещей домашней пыли относятся к круглогодичным аллергенам, их количество в окружающем воздухе также зависит от времени года. Обычно оно снижается в зимние месяцы и увеличивается летом и осенью. Таким образом, персистирующий аллергический ринит может иметь волнообразное течение и сопровождаться сезонными вспышками.
- Профессиональный аллергический ринит наблюдается у лиц, постоянно контактирующих по роду своей деятельности с разными группами аллергенов, например с мукой, медикаментами, пухом, пером, животными, латексом и другими аллергенами (встречается у зоотехников, работников хлебозаводов, фармацевтов, медицинских работников и др.).
Патогенез
Основные симптомы аллергического ринита обусловлены IgE-зависимой активацией тучных клеток в слизистой оболочке носа с последующей специфической либерацией медиаторов аллергии. Важную роль в реализации клинических симптомов данного заболевания наряду с тучными клетками играют эозинофилы, макрофаги, Т-лимфоциты. Участие этих клеток определяет раннюю и позднюю фазы аллергической реакции.
Механизм, посредством которого слизистая оболочка носа распознает аллергены, реализуется за счет фиксации аллерген-специфических IgE-антител на его высокоаффинных рецепторах (Fc ε рецепторы I типа – Fc ε RI) тучных клеток, которые в физиологических условиях всегда присутствуют в подслизистом слое слизистой оболочки. Связывание аллергена с аллерген-специфическими IgE-антителами является фактором, запускающим активацию тучных клеток. Дегрануляция этих клеток приводит к выделению в ткани медиаторов воспаления – гистамина, триптазы, простагландина D2, лейкотриенов (B4 и C4) и кининов. Действием этих медиаторов на нейрорецепторы и сосуды объясняется возникновение симптомов ринита в раннюю фазу аллергического ответа. Наряду с гистамином важную роль при аллергическом рините играют метаболиты арахидоновой кислоты – простагландин D2, тромбоксан А2 (циклооксигеназный путь) и лейкотриены, гидроксиэйкозатетраеновые кислоты и липоксины (5-липооксигеназный путь), медиатор ФАТ (фактор активации тромбоцитов).
Через несколько часов после разрешения ранней фазы без дополнительной экспозиции аллергена возникает поздняя (отсроченная) фаза аллергического ответа. В этот период в собственном слое слизистой оболочки увеличивается содержание эозинофилов и базофилов. Т-лимфоцитам приписывают участие в конечном звене патогенеза аллергического ринита. Для активации Т-лимфоцитов необходимо их взаимодействие с антигенпредставляющими клетками, роль которых могут выполнять клетки Лангерганса, несущие высокоаффинные рецепторы для IgE. Для накопления в ткани лимфоцитов требуется довольно продолжительное время, поэтому цитокины Т-лимфоцитов (Тh2-профиля) вовлекаются в процесс поддержания аллергического воспаления только на заключительных этапах. Принято считать, что изменения в клеточном составе за счет поступления эозинофилов, базофилов, Th2-клеток и поддержания активности тучных клеток во время поздней фазы аллергического ответа имеют отношение к сдвигу общей реактивности слизистой оболочки носа. На таком измененном фоне последующие воздействия аллергена вызывают более выраженные клинические симптомы. Неспецифическая гиперреактивность слизистой оболочки носа у больных аллергическим ринитом выражается в повышенной чувствительности к разнообразным неспецифическим раздражающим воздействиям. В основе неспецифической тканевой гиперреактивности также могут лежать конституциональные особенности, изменение рецепторной чувствительности к медиаторам и раздражающим стимулам, нарушение рефлекторных реакций, сосудистые и микроциркуляторные изменения.
КЛАССИФИКАЦИЯ
АР классифицируют по форме, характеру, тяжести течения, стадии заболевания.
Формы аллергического ринита:
- сезонный аллергический ринит (САР) возникает при сенсибилизации к пыльцевым (поллиноз) и грибковым аллергенам: пыльце деревьев, злаковых и сорных трав, спорам грибов Cladosporium, Penicillium, Alternaria и других;
- круглогодичный аллергический ринит (КАР) развивается у пациентов с сенсибилизацией к аллергенам клещей домашней пыли, библиотечной пыли, эпидермальным аллергенам животных и птиц, инсектным аллергенам, аллергенам плесневых грибов, пищевых продуктов и лекарственных препаратов при постоянном их приеме, профессиональным аллергенам.
По характеру течения:
- интермиттирующий аллергический ринит (симптомы беспокоят менее 4 дней в неделю или менее 4 недель в году),
- персистирующий аллергический ринит (симптомы беспокоят более 4 дней в неделю или более 4 недель в году).
По тяжести течения:
- легкая степень тяжести аллергического ринита (у пациента имеются лишь незначительные клинические проявления болезни, не нарушающие дневную активность и сон);
- средней степени тяжести аллергического ринита (симптомы нарушают сон пациента, препятствуют работе, учебе, занятиям спортом. Качество жизни существенно ухудшается;
- тяжелая форма аллергического ринита (симптомы настолько выражены, что пациент не может нормально работать, учиться, заниматься спортом или проводить досуг и спать ночью, если не получает лечения).
По стадии течения аллергический ринит подразделяется на стадию обострения и стадию ремиссии.
ДИАГНОЗ
Клинические признаки и симптомы
Опрос
Сбор анамнеза имеет основное значение в диагностике данного заболевания. Необходимо выявить сезонность заболевания, возникновение или усиление симптомов аллергического ринита при непосредственном контакте с тем или иным аллергеном (контакт с пыльцой, домашними животными, обострение при уборке квартиры и др.); наличие или отсутствие эффекта элиминации, влияние факторов погоды, продуктов питания, смены климатической зоны.
При выявлении жалоб необходимо учитывать количественные показатели (продолжительность симптомов в течение дня, количество используемых носовых платков за сутки, количество чиханий, дозу используемых сосудосуживающих капель и т.д.). Наилучшим способом количественного учета является запись пациентом степени выраженности симптомов аллергического ринита в баллах в специальном дневнике самоконтроля. Необходимо обратить внимание на такие сопутствующие жалобы пациента, как чувство распирания и боли в придаточных пазухах носа, головные боли, боли в области среднего уха, снижение слуха, изменение голоса, носовые кровотечения, явления дерматита около носа, частые фаринголарингиты, снижение внимания и работоспособности.
Наследственность. Необходимо обратить внимание на наличие аллергических заболеваний у родственников.
Условия труда и быта. Профессиональные (производственные аллергены, различные раздражители), бытовые факторы (загрязнение помещения) являются триггерными в развитии аллергического ринита.
Сочетание с другими аллергическими заболеваниями. Наиболее часто аллергический ринит сочетается с аллергическим конъюнктивитом, атопической бронхиальной астмой, атопическим дерматитом.
Основные клинические симптомы аллергического ринита:
- ринорея (водянистые выделения из носа);
- чихание – нередко приступообразное, чаще в утренние часы, пароксизмы чихания могут возникать спонтанно;
- зуд, реже – чувство жжения в носу (иногда сопровождается зудом неба и глотки); зуд носа может проявляться характерным симптомом – «аллергическим салютом» (постоянное почесывание кончика носа с помощью ладони движением снизу вверх), в результате чего у части больных появляются поперечная носовая складка, расчесы, царапины на носу;
- заложенность носа, характерное дыхание ртом, сопение, храп, изменение голоса;
- снижение обоняния.
Дополнительные симптомы аллергического ринита развиваются вследствие обильного выделения секрета из носа, нарушения дренирования околоносовых пазух и проходимости слуховых (евстахиевых) труб:
- раздражение, отечность, гиперемия кожи над верхней губой и у крыльев носа;
- носовые кровотечения вследствие форсированного сморкания и ковыряния в носу;
- боль в горле, покашливание (проявления сопутствующего аллергического фарингита, ларингита);
- боль и треск в ушах, особенно при глотании;
- нарушение слуха (проявления аллергического туботита).
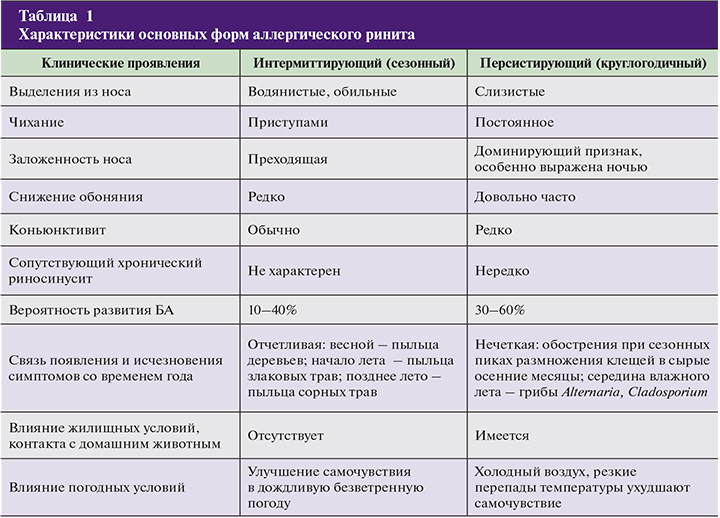
Общие неспецифические симптомы, наблюдаемые при аллергическом рините (табл. 1):
- слабость, недомогание, раздражительность;
- головная боль, повышенная утомляемость, нарушение концентрации внимания;
- нарушение сна, подавленное настроение;
- редко – повышение температуры.
Лабораторные и инструментальные исследования
Кожные пробы проводят в аллергологических кабинетах специально обученным персоналом. Обычно используют пробы уколом (прик-тест). Результаты кожных проб очень важны для диагностики аллергического ринита, однако они не являются абсолютными. На их достоверность могут влиять различные факторы: одновременный или предшествовавший прием антигистаминных препаратов или кетотифена, молодой или, наоборот, преклонный возраст, атопический дерматит, хронический гемодиализ (ложноотрицательный результат), а также красный дермографизм (ложноположительный результат).
Определение уровня общего IgЕ и специфических IgЕ-антител в сыворотке особенно важны при неубедительных результатах кожных проб либо при невозможности их постановки. Определение аллерген-специфических антител в сыворотке может быть проведено радиоаллергосорбентным, радиоиммунным, иммуноферментным или хемилюминесцентным методами при помощи стандартных наборов (панелей) диагностикумов.
Назальный провокационный тест проводится после постановки кожных проб. Тест необходим для подтверждения того, что данный аллерген действительно является причиной аллергического ринита. Этот тест в редких случаях может вызывать бронхоспазм, поэтому он, как и кожные пробы, должен проводиться подготовленным персоналом в специальном кабинете.
Цитологическое исследование мазков и смывов из полости носа помогает провести дифференциальную диагностику между аллергическим ринитом (преобладание эозинофилов) и инфекционным ринитом (преобладание нейтрофилов), а также оценить эффективность лечения аллергического ринита.
Эндоскопическое исследование полости носа выполняется до и после анемизации слизистой оболочки носа. Характерными находками являются типичный серый или синюшный цвет слизистой оболочки и обильные пенистые выделения. Проба с адреналином обычно демонстрирует обратимость выявленных изменений.
Активная передняя риноманометрия и акустическая ринометрия позволяют объективно оценить носовое дыхание. Сущность метода риноманометрии заключается в количественном измерении градиента давления и воздушного потока, которые создаются в условиях физиологического носового дыхания. Результаты риноманометрии выдаются прибором в виде графика в системе координат, причем форма полученной кривой определяет степень нарушения носового дыхания. Прибор для акустической ринометрии работает по принципу эхолота и дает возможность «зондировать» полость носа акустическим сигналом, имеющим частоту слышимого человеком звука (от 150 до 10 000 Гц). Звук, продвигаясь в полости носа, отражается от ее стенок, а отраженная звуковая волна регистрируется микрофоном, анализируется компьютером и представляется в виде кривых, характеризующих площадь поперечного сечения полости носа на различном расстоянии от его преддверия. Это помогает выявить основные преграды на пути воздушной струи.
Исследование порогов обоняния и мукоцилиарного транспорта имеет второстепенное значение в диагностике аллергического ринита. При ольфактометрии используют пахучие вещества в градиентных разведениях, а также наборы специальных полосок, импрегнированных одорантами (например, пенсильванский обонятельный тест). При определении скорости мукоцилиарного транспорта обычно применяют сахариновый тест.
Рентгенография, компьютерная и магнитно-резонансная томография полости носа и околоносовых пазух могут иметь определенное значение в диагностике осложненных форм аллергического ринита, в частности при полипозном риносинусите, и для планирования объема хирургического вмешательства.
Дифференциальный диагноз
Аллергический ринит дифференцируют с некоторыми хроническими заболеваниями полости носа. Чаще всего с ринитом, вызванным анатомическими аномалиями строения носовой полости или инфекционным ринитом.
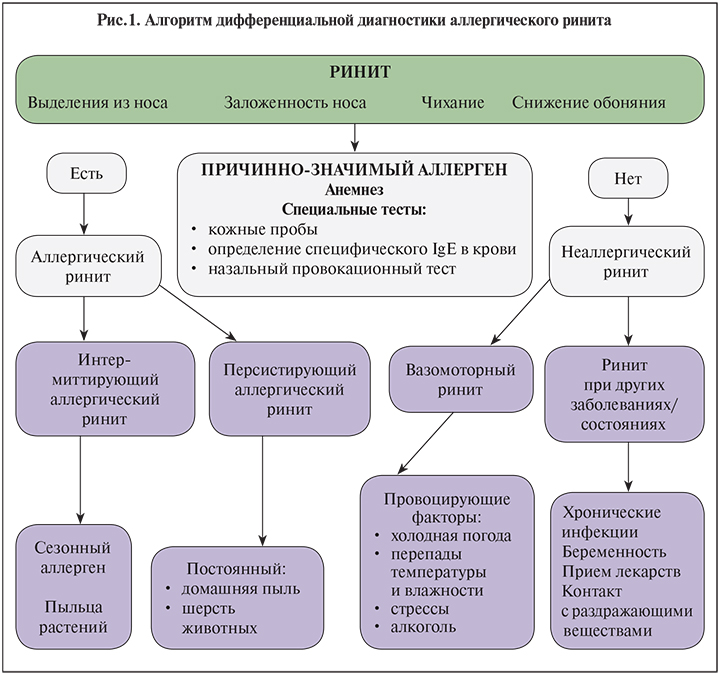
Дифференциальный диагноз аллергического ринита базируется на данных анамнеза, клинической картины и специфического обследования (кожные пробы, провокационные тесты, определение уровней общего IgE и специфических IgЕ-антител) (рис. 1).
Для неаллергического эозинофильного ринита характерно высокое содержание эозинофилов (до 80–90%) при цитологическом исследовании, при этом не удается выявить сенсибилизацию ни одним из методов аллергодиагностики, при риноскопии характерна бледная рыхлая отечная слизистая оболочка носа, возможно дальнейшее развитие полипоза.
При вазомоторном (идиопатическом) рините слизистая полости носа бледная, отечная; отделяемое из носа водянистого или слизистого характера, не имеется признаков атопии.
Ринит неаллергического характера может быть вызван патологией эндокринной системы, приемом медикаментов, психогенными факторами, беременностью и др.
Учитывают данные анамнеза и результаты клинического и аллергологического обследований, наличие сопутствующей патологии и прием медикаментов, которые могут привести к появлению симптомов ринита. Пациенты с подозрением на аллергический ринит ведут дневник, в котором они ежедневно регистрируют выраженность симптомов, влияние условий окружающей среды на течение заболевания, а также указывают лекарственные препараты, которые были использованы в этот день. Анализ полученных из дневника сведений позволяет предположить аллергическую природу заболевания и причинный аллерген, эффект от применения препаратов. При сезонном течении необходимо сопоставить календарь цветения растений в данной климатической зоне с моментами появления и исчезновения симптомов у пациента.
Осложнения аллергического ринита
Аллергические синуситы. Частота встречаемости синуситов, связанных с аллергическим процессом, колеблется от 25 до 70% случаев в зависимости от использованных критериев включения в группу обследования и применяемых методов лечения. Аллергия может лежать в основе как острых, так и хронических синуситов. В результате аллергического воспаления развивается отек слизистой оболочки не только носа, но и околоносовых пазух, чаще всего этмоидальных и гайморовых пазух, клинически проявляющийся отечной формой синусита. Воспаленная слизистая оболочка носа и сниженная функция цилиарного аппарата могут нарушить естественный дренаж из околоносовых пазух и вызвать стаз назального секрета с последующим присоединением бактериального воспаления.
Полипозный риносинусит – гипертрофическое изменение слизистой оболочки носа и пазух с формированием полипов.
Серозный средний отит – особенно характерен для детского возраста. Эпидемиологические данные указывают на 40–50% частоту средних отитов у детей старше трех лет, у которых имеется аллергический ринит. У взрослых аллергический ринит осложняется средним отитом примерно в 1–5% случаев. В основе патогенеза лежит нарушение проводимости слуховой трубы как результат аллергического воспаления слизистой оболочки носа, вследствие чего меняется давление в полости среднего уха и нередко присоединяется вторичная бактериальная инфекция.
ЛЕЧЕНИЕ
Цель лечения – полный контроль над симптомами аллергического ринита. Лечение в большинстве случаев проводят в амбулаторно-поликлинических условиях.
Рекомендуется ступенчатый подход к лечению ринита с учетом его формы и тяжести. Лечение аллергического ринита должно включать следующие меры:
- устранение контакта с аллергеном (если возможно);
- аллерген-специфическую иммунотерапию;
- фармакотерапию;
- обучение пациента.
Также необходимо добиваться оптимизации факторов окружающей среды и социальных факторов, чтобы больной мог вести нормальный образ жизни.
Госпитализация в стационар показана при тяжелом и/или осложненном течении заболевания, а также при необходимости проведения ускоренного курса аллерген-специфической иммунотерапии (АСИТ).
Немедикаментозное лечение
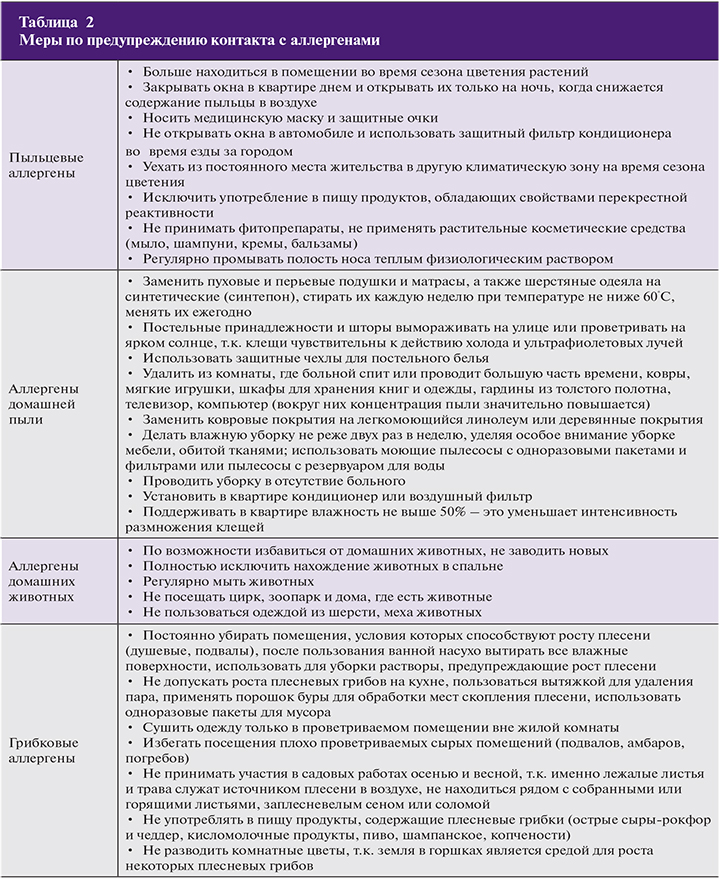
Для повышения эффективности лечения необходимо прекратить (или максимально сократить) дальнейший контакт пациента с причинными аллергенами. Больной в соответствии с его сенсибилизацией должен получить лечебно-профилактические рекомендации. Благоприятный эффект различных мер, направленных на удаление аллергена из окружающей среды, в полной мере проявляется лишь через несколько недель или месяцев. В большинстве случаев полное исключение контакта с аллергеном по практическим или экологическим причинам невозможно. Тем не менее по возможности до назначения лекарственных препаратов или на фоне их применения целесообразно предпринять меры с целью уменьшения контакта с аллергеном (табл. 2).
Обучение пациентов
В ведении больных аллергическим ринитом немаловажное место занимает ориентация пациентов на необходимость проведения грамотного и своевременного лечения, ознакомление с современными методами специфической и неспецифической терапии, обучение правильному использованию лекарственных препаратов, различным мерам профилактики обострений, психологической реабилитации, самоконтролю, знакомство с последними научными достижениями в области аллергологии и иммунологии. Поскольку врач-аллерголог часто не имеет возможности провести такую работу, большое значение в настоящее время уделяется созданию астма- и аллергошкол, в которых проводятся специальные регулярные занятия квалифицированным специалистом – аллергологом и оториноларингологом в виде лекций или практических занятий, а также с помощью компьютерной сети, благодаря которой пациент может не только получить информацию, но и задать интересующий его вопрос и получить ответ от конкретного специалиста, участвовать в конференции по интересующей проблеме.
Медикаментозное лечение
Медикаментозное лечение аллергического ринита включает симптоматическую терапию (купирование обострения и базисное лечение) и патогенетическое лечение – аллерген-специфическую иммунотерапию (АСИТ).
Препараты для местного применения
В случае полной блокады носового дыхания за несколько минут до интраназального введения противоаллергических препаратов применяют стимуляторы адренорецепторов: нафазолин, или оксиметазолин, или ксилометазолин по 2–3 инстилляции 2–4 раза в сутки. Длительность их применения составляет в среднем 3–5 сут, но не более 10 суток.
При обильной назальной секреции показаны антихолинергические препараты, содержащие ипратропиум бромид по 2–3 дозы в каждый носовой ход 3 раза в сутки.
Не следует забывать, что при передозировке и постоянном (в течение нескольких месяцев, а иногда и лет) приеме стимуляторов-адренорецепторов наступает тахифилаксия, а также развивается ряд побочных эффектов и осложнений (гипертрофия носовых раковин, необратимые изменения слизистой оболочки носа, возможно развития ряда системных реакций со стороны сердечно-сосудистой системы).
При наличии легких и умеренных клинических проявлений ринита применяют кромоглициевую кислоту в виде интраназального спрея в дозе 2,8 мг в каждый носовой ход 4–6 раз в сутки.
В качестве альтернативы применяют антигистаминные препараты в виде интраназальных средств: левокабастин по две инсуффляции в каждый носовой ход 2–4 раза в сутки, азеластин по одной инсуффляции в каждый носовой ход 2 раза в сутки (табл. 3).
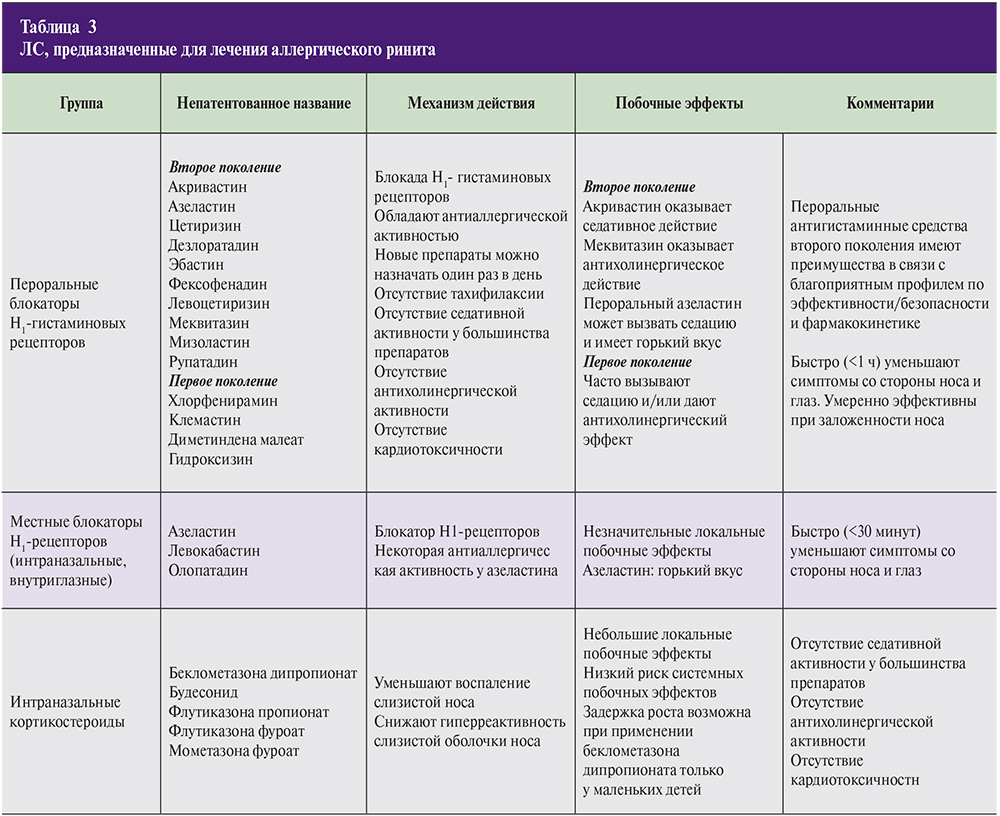
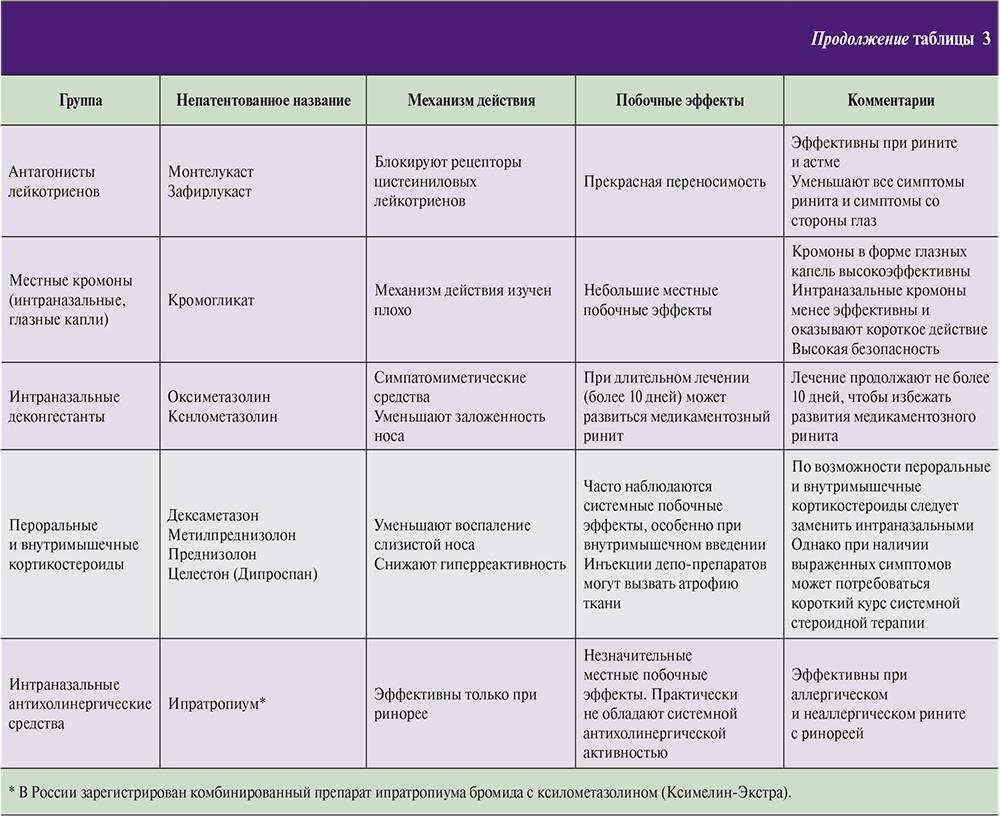
Интраназальные ГКС (ИНГКС)
Следует помнить, что аллергический ринит и бронхиальная астма являюся взаимозависимыми заболеваниями, поэтому своевременное и адекватное лечение аллергического ринита, раннее назначение ИНГКС способствуют уменьшению интенсивности аллергического воспаления как в слизистой оболочке носа, так и в бронхах, снижению уровня их гиперреактивности.
Беклометазон дипропионат в дозе 400 мкг/сут, мометазон фуроат в дозе 200 мкг 1–2 раза в сутки, или будесонид в дозе 100–200 мкг 2 раза в сутки, или флутиказона пропионат в дозе 200 мкг 1 раз в сутки, либо 200 мкг 2 раза в сутки. Флутиказона фуроат в дозе 110 мкг 1 раз в сутки.
Лечение аллергического ринита – длительный процесс, а наличие качественных генериков способствует снижению стоимости терапии и повышению приверженности пациентов лечению.
Препарат Момат Рино (мометазона фуроат), спрей назальный дозированный, показал в рандомизированном многоцентровом клиническом исследовании, что его эффективность и безопасность полностью соответствуют эффективности и безопасности оригинального мометазона фуроата.
Отдельно стоит выделить комбинированный препарат Момат Рино Адванс, представляющий собой комбинацию топического антигистаминного препарата азеластин и кортикостероида мометазона фуроата. Применение препарата позволяет уже в первые минуты после использования активно влиять на основные симптомы аллергического ринита, оказывая лечебный эффект до активации клинического воздействия топического глюкокортикостероида. Это позволяет исключить применение деконгестантов для восстановления назальной проводимости. Такая комбинация значительно повышает приверженность пациентов к лечению, т.к. больной немедленно ощущает эффект от проводимой терапии.
Антигистаминные препараты (АГ)
Несмотря на эффективность пероральных АГ первого поколения, их применение не рекомендуется, если доступны препараты второго поколения, учитывая седативные и антихолинергические свойства первых. Установлена низкая эффективность АГ первого поколения по анализу эффективности затрат, стоимость лечения увеличивается из-за вызываемой ими седации. Целесообразно применять только безопасные АГ второго поколения, характеризующиеся благоприятным отношением эффективность/безопасность.
АГ (блокаторы Н1-рецепторов гистамина) второго поколения: лоратадин или цетиризин в дозе 10 мг/сут или дезлоратадин в дозе 5 мг/сут. Возможно применение эбастина в дозе 10–20 мг/сут, фексофенадина в дозе 120–180 мг/сут, или левоцетиризина в дозе 5 мг/сут, или рупатадина фумората в дозе 10 мг/сут.
Одним из высокоэффективных современных антигистаминных препаратов второго поколения является левоцетиризин. Существует большое количество клинических исследований, демонстрирующих высокую эффективность левоцетиризина в отношении симптомов аллергического ринита. Одно из наиболее значимых среди них исследование XPERT® – длительное (6-месячное) международное многоцентровое двойное слепое плацебо-контролируемое исследование эффективности левоцетиризина у 550 больных персистирующим аллергическим ринитом (как сезонным, так и круглогодичным) из разных стран Европы. В этом исследовании была показана эффективность левоцетиризина в отношении всех симптомов аллергического ринита на протяжении всего периода лечения, в т.ч. включая такой трудно поддающийся лечению АГП симптом, как заложенность носа. Кроме этого было продемонстрировано повышение качества жизни больных персистирующим аллергическим ринитом в результате лечения левоцетиризином.
Аллервэй (левоцетиризин 5 мг) рекомендован к применению у детей с 6 лет и взрослых для лечения симптомов аллергического ринита, поллиноза, крапивницы и других аллергодерматозов, сопровождающихся зудом и высыпаниями. Аллервэй обладает мощным антигистаминным эффектом за счет самого высокого среди АГП 2-го поколения сродства с Н1-рецепторами и низкого объема распределения; начинает действовать уже через 12 минут; обеспечивает стойкий эффект на 24 часа при приеме 1 раз в день; безопасен при длительном применении. Аллервэй практически не метаболизируется в печени, благодаря чему он не вступает во взаимодействие с другими лекарственными препаратами и с пищей.
В рекомендованных дозах Аллервэй не оказывает воздействия на ЦНС, не обладает седативным и снотворным действиями, не влияет на скорость психомоторных реакций и интервал QT. Доказана биоэквивалентность препарата Аллервэй оригинальному препарату левоцетиризин.
В качестве альтернативной терапии могут использоватся блокаторы Н1-рецепторов гистамина первого поколения: клемастин в дозе 1 мг 2–3 раза в сутки или хлоропирамин (B, 2+)в дозе 25 мг 2–3 раза в сутки в течение 10 суток. В случае выраженной симптоматики первые несколько суток эти препараты применяют парентерально (в/м или в/в): клемастин в дозе 2 мг 1–2 раза в сутки, хлоропирамин в дозе 40 мг 1–2 раза в сутки. Отечественные АГ представлены препаратами: мебгидролина нападизилат по 0,1–0,3 г в сутки; секвифенадин гидрохлорид по 0,05–0,1 г 2–3 раза каждый день, хифенадина гидрохлорид по 25–50 мг 2–4 раза в день.
АГ системные препараты со стабилизирующим действием на мембраны тучных клеток: кетотифен в дозе 1 мг 2 раза в сутки, на протяжении до 3 месяцев.
Блокаторы рецепторов лейкотриенов
По эффективности монтелукаст натрия по 10 мг в сутки и зафирлукаст по 40 мг в сутки превосходят плацебо, но уступают АГ и ИНГКС.
Системные глюкокортикостероиды
В редких случаях больным с выраженными симптомами, которые не отвечают на лечение другими препаратами или не переносят интраназальные средства, может потребоваться системное применение ГКС (например, преднизолон в начальной дозе 5–10 мг/сут перорально) в течение короткого срока. Длительное лечение пероральными ГКС или их внутримышечное введение сопровождается хорошо известными системными побочными эффектами.
Базисная терапия
При сезонной форме предупреждающая противоаллергическая терапия должна быть назначена после проведения анализа данных о течении заболевания в предыдущий сезон (выраженность клинических проявлений, эффективность назначенных препаратов и результаты обследования) за 1–2 недели до предполагаемого сезонного обострения. Базисная терапия круглогодичного аллергического ринита обеспечивает стабильность состояния в условиях контакта с аллергеном.
В качестве базисной терапии при легком течении аллергического ринита применяют следующие ЛС:
- таблетированные формы блокаторов Н1-рецепторов гистамина;
- предпочтительнее применение блокаторов Н1-рецепторов второго поколения;
- АГ со стабилизирующим действием на мембраны тучных клеток;
- препараты кромоглициевой кислоты;
- При тяжелой и средней степени тяжести течениях заболевания необходимо лечение ИНГКС. Перечень препаратов и дозировки указаны выше. Подбор и комбинирование препаратов базисной терапии проводят индивидуально с учетом тяжести заболевания, переносимости препаратов, условий жизни пациента.
Аллерген-специфическая иммунотерапия (АСИТ)
Эффективная аллерген-специфическая иммунотерапия приводит к снижению чувствительности пациента к данному аллергену, выявляемой проведением аллерген-специфических провокационных проб, к исчезновению клинической симптоматики в период естественного воздействия аллергена или к уменьшению ее выраженности и к сокращению потребности в противоаллергических лекарственных препаратах.
В отличие от всех существующих методов лечения аллергических заболеваний положительный эффект от аллерген-специфической иммунотерапии сохраняется на длительный (как минимум в течение нескольких лет) период.
Чем в более раннем возрасте пациент и чем при более ранних стадиях заболевания проведена аллерген-специфическая иммунотерапия, тем выше ее лечебное действие.
Своевременно проведенная эффективная аллерген-специфическая иммунотерапия предупреждает переход более легких форм заболевания в более тяжелые и трансформацию аллергического ринита в бронхиальную астму.
Клинически лечебное действие аллерген-специфической иммунотерапии достигается при завершении повторных (3–5) курсов лечения, но может проявиться после первого курса.
По данным многочисленных исследований, положительный терапевтический эффект аллерген-специфической иммунотерапии достигается в 80–90% случаев и более. Столь высокого уровня терапевтической эффективности удается добиваться при соблюдении ряда условий:
- подбор пациентов с четко установленной IgЕ-зависимой природой заболевания;
- ограниченное число аллергенов, которые имеют значение в клинической симптоматике заболевания у данного пациента;
- использование разрешенных к применению стандартизированных лечебных форм аллергенов;
- склонность пациента к проведению аллерген-специфической иммунотерапии и настроенность на выполнение повторных курсов лечения.
Аллерген-специфическая иммунотерапия показана больным с клиническими признаками IgE-опосредованного заболевания, начинать ее следует на ранних этапах аллергических заболеваний, чтобы добиться максимального эффекта. Аллерген-специфическую иммунотерапию должен проводить врач-аллерголог.
Лечебные аллергены
В России для аллерген-специфической иммунотерапии используются водно-солевые экстракты, представляющие собой смесь аллергенных и неаллергенных материалов, депонированные и модифицированные формы лечебных аллергенов. Депонированные и модифицированные лечебные аллергены обладают меньшей аллергенностью и большей иммуногенностью, в связи с чем показали себя более эффективными средствами при меньшем количестве побочных эффектов, регистрируемых в процессе аллерген-специфической иммунотерапии.
Назначение аллерген-специфической иммунотерапии
При квалифицированном подходе к отбору больных и адекватной предварительной лекарственной терапии показания к применению данного метода лечения могут быть значительно расширены.
Аллерген-специфическая иммунотерапия назначается пациентам с аллергическим ринитом (риноконъюнктивитом) при любой степени тяжести заболевания.
Следует помнить, что аллерген-специфическую иммунотерапию при ингаляционной аллергии назначают:
- при доказанной IgE-зависимой природе заболевания;
- с учетом того, что за развитие клинических проявлений заболевания ответственны именно эти аллергены;
- при проведении элиминационных мероприятий до начала лечения;
- с учетом и при необходимости терапией потенциальных обострений интеркуррентных болезней.
Противопоказания к аллерген-специфической иммунотерапии:
- тяжелые иммунопатологические состояния и иммунодефициты;
- онкологические заболевания;
- тяжелые психические расстройства;
- лечение β-блокаторами, включая топические формы;
- невозможность соблюдения пациентом схемы назначенного лечения;
- тяжелая форма бронхиальной астмы, неконтролируемая фармакотерапией (объем форсированного выдоха за 1-ю секунду менее 70% после проведения адекватной фармакотерапии);
- сердечно-сосудистые заболевания в стадии декомпенсации, при которых возможны осложнения при использовании адреналина (эпинефрина);
- дети до 5 лет.
Беременность является относительным противопоказанием: в случае наступления беременности на фоне проведения аллерген-специфической иммунотерапии прекращать курс не следует, но начинать аллерген-специфическое лечение на фоне уже наступившей беременности не рекомендуется.
Давно признанным и обоснованным положением аллергологии является то, что первым обязательным этапом противоаллергического лечения должно быть проведение комплекса мероприятий, направленных на исключение или ограничение аллергенного воздействия на пациента. Если элиминационные меры недостаточны, то проведение аллерген-специфической иммунотерапии становится необходимым, разумеется, при соблюдении упомянутых выше условий.
Алгоритм проведения аллерген-специфической иммунотерапии
Для проведения аллерген-специфической иммунотерапии отбирают аллергены, элиминация которых невозможна (пыльца растений, клещи домашней пыли) и которые провоцируют появление симптомов аллергического ринита у данного пациента. Установление клинически значимого аллергена проводится на основании анализа данных аллергологического анамнеза, кожных проб, провокационных назальных тестов.
 Выделяют несколько схем проведения аллерген-специфической иммунотерапии:
Выделяют несколько схем проведения аллерген-специфической иммунотерапии:
- классическая (при первых инъекциях аллерген вводится подкожно ежедневно или через день, последующие вводят с интервалами 7–10 дней);
- ускоренная (подкожное введение аллергена 2–3 раза в день);
- «молниеносная» (вся терапевтическая доза вводится в течение трех суток подкожно в равных дозах через 3 часа с адреналином);
- «шок-метод» (курсовая доза аллергена вводится в течение одних суток подкожно через 2 часа в равных дозах с адреналином).
Применение всех краткосрочных вариантов аллерген-специфической иммунотерапии рекомендовано только в условиях аллергологического стационара.
Классическая схема проведения аллерген-специфической иммунотерапии
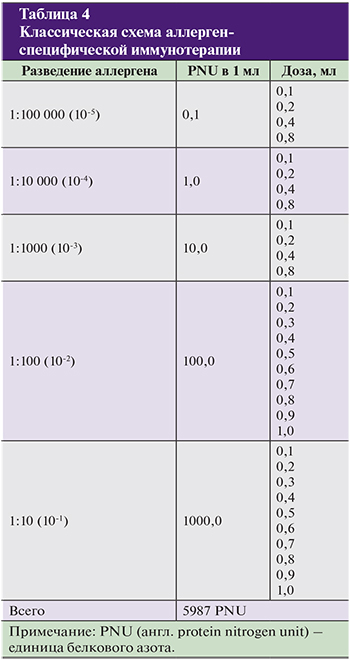
Начинается сразу после обращения пациента к аллергологу. Если терапия будет проводиться пыльцевыми аллергенами, она должна быть начата не позднее, чем за 1,5 месяца до начала цветения растений, к пыльце которых имеется повышенная чувствительность. Первые инъекции делают ежедневно или через день, последующие – с интервалами 7–10 дней. Дозу аллергена 0,9–1,0 мл в разведении 1:10 повторяют с интервалом 5–7 дней до начала сезона цветения растений. Классическая схема аллерген-специфической иммунотерапии представлена в табл. 4.
Перед каждой инъекцией аллергена, а также в течение 40–60 минут после нее врач должен наблюдать за пациентом, т.к. в этот период наиболее высока вероятность развития системных реакций. Наблюдение включает:
- физикальное обследование (перкуссия, пальпация, аускультация);
- контроль артериального давления.
Контроль за показателями клинического исследования крови и мочи, биохимического исследования крови, электрокардиографического исследования и исследования функции внешнего дыхания осуществляется при наличии показаний, а также после каждой 10-й инъекции аллергена.
Ускоренная схема проведения аллерген-специфической иммунотерапии
К ускоренным методам проведения аллерген-специфической иммунотерапии прибегают в тех случаях, когда необходимо сократить период, затрачиваемый на достижение поддерживающих доз аллергена. Такая необходимость возникает при коротком интервале времени, остающемся до начала очередного сезона цветения аллергенных растений, или по желанию пациента провести лечение за более короткий отрезок времени. Применение данного метода возможно только в условиях аллергологического стационара.
Наиболее часто применяют ускоренный метод аллерген-специфической иммунотерапии водно-солевыми аллергенами. Больные получают инъекции аллергенов 2–3 раза в день с интервалом 2 часа. Инъекции делают в нижнюю треть плеча по латеральной поверхности. Схема ускоренной аллерген-специфической иммунотерапии представлена в табл. 5.

Перед каждой инъекцией аллергена, а также в течение 40–60 минут после нее врач должен наблюдать за пациентом, т.к. в этот период наиболее высока вероятность развития системных реакций. Наблюдение включает:
- физикальное обследование (перкуссия, пальпация, аускультация);
- контроль артериального давления.
Контроль за показателями клинического исследования крови и мочи, биохимического исследования крови, электрокардиографического исследования и исследования функции внешнего дыхания осуществляется при наличии показаний, а также 1 раз в 5 дней. Курс лечения составляет 10–15 дней. После выписки из стационара назначают поддерживающие дозы аллергена раз в 14 дней. В качестве поддерживающей дозы выбирают максимально переносимую дозу аллергена. Лечение заканчивают за 1–2 недели до начала пыления растений, к пыльце которых имеется повышенная чувствительность.
Аллерген-специфическую иммунотерапию ускоренным методом проводят на фоне приема антигистаминных препаратов. При этом предпочтение отдается неметаболизируемым блокаторам Н1-гистаминовых рецепторов второго поколения.
Описанная схема является примерной. С учетом данных обследования и наблюдения за пациентом аллерголог может изменить схему проведения аллерген-специфической иммунотерапии, либо уменьшая дозу аллергена при очередной инъекции, либо сохраняя ее прежней при исключении очередной инъекции в случае появления предвестников аллергической симптоматики, при возникших инфекциях, при предшествовавшей аллергенной экспозиции, при системных реакциях на предыдущие инъекции, при удлинении интервалов между инъекциями и др.
Оценка эффективности лечения
Критерии эффективности лечения включают достижение полного контроля над симптомами аллергического ринита, снижение выраженности клинических проявлений, уменьшение количества ежегодных обострений, улучшение качества жизни.
Осложнения и побочные эффекты лечения
Многие антигистаминные препараты II поколения (астемизол, лоратадин, терфенадин, эбастин) трансформируются в печени в активные метаболиты с помощью системы цитохрома Р450, которая отвечает также и за метаболизм и других ЛС. Одновременное применение этих ЛС с противогрибковыми ЛС или макролидными антибиотиками может создать повышенные концентрации неметаболизированных препаратов, которые, действуя на цикл реполяризации сердечной мышцы, вызывают удлинение интервала QT на ЭКГ и повышают риск развития сердечной аритмии (вплоть до мерцания желудочков). Кардиотоксический эффект, обусловленный повышением концентрации исходных соединений в крови, убедительно доказан для астемизола и терфенадина, которые уже изъяты из употребления в целом ряде стран, включая Россию. Другие метаболизируемые ЛС данной группы (лоратадин, эбастин) можно считать относительно безопасными при условии соблюдения правил их назначения: исключения одновременного приема макролидных и противогрибковых антибиотиков, ограничения применения у пациентов с патологией печени и страдающих нарушениями ритма сердца.
Ошибки и необоснованные назначения
В отсутствие клинических проявлений аллергического ринита в анамнезе и на момент обращения даже при доказанной (по результатам кожных проб) сенсибилизации к отдельным аллергенам никаких лечебных мероприятий не требуется.
Применение антигистаминных препаратов I поколения при фармакотерапии аллергического ринита оправданно только по экономическим мотивам и соображениям доступности для конкретного пациента. При их назначении следует тщательно оценивать стоимость курсового лечения и отдавать предпочтение препаратам с наилучшим профилем безопасности.
Некоторые пероральные сосудосуживающие ЛС (псевдоэфедрин, фенилпропаноламин) считаются допингом для спортсменов.
Из-за побочных эффектов использование сосудосуживающих ЛС для местного применения у детей до 2 лет и при наличии у пациентов атрофических и субатрофических изменений слизистой оболочки ограничено.
Применение кетотифена у детей школьного возраста ограничено из-за его седативного эффекта.
ПРОГНОЗ
Своевременно и правильно проведенная комплексная терапия, включающая элиминацию аллергенов, АСИТ и фармакотерапию, позволяет устранить все симптомы аллергического ринита и предотвратить развитие осложнений. Эффект от успешного курса АСИТ сохраняется и после его завершения, иногда в течение нескольких лет.