Введение
Функциональные гастроинтестинальные нарушения (ФГН) занимают одно из ведущих мест в структуре патологии органов пищеварения у детей, характеризуясь хроническими рецидивирующими эпизодами клинических симптомов в отсутствие определенной органической причины [1, 2]. Обязательным критерием всех форм ФГН (табл. 1) является отсутствие анатомических, метаболических и воспалительных изменений желудочно-кишечного тракта (ЖКТ) [3–5].
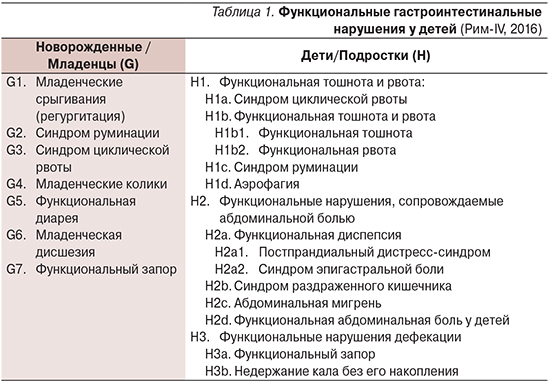
Актуальность проблемы обусловлена высокой распространенностью и социальной значимостью ФГН:
- Функциональные заболевания ЖКТ, начавшись в детстве, могут сохраняться во взрослом возрасте.
- Показано, что качество жизни пациентов и их семьи было значительно хуже, чем таковое жизни детей с такими органическими заболеваниями, как воспалительные заболе-вания кишечника и гастроэзофагеальная рефлюксная болезнь [6]. Кроме того, при ФГН снижено качество обучения в школе и появляются трудности в усвоении школьной программы детьми [7].
- Отсутствует отчетливое улучшение клинических симптомов при проведении традиционной терапии, что затрудняет взаимодействие в системе врач–пациент–родители.
- У детей с ФГН чаще выявляются тревожные нарушения и депрессия, требующие дифференцированного подхода к терапии с участием психолога, психотерапевта.
- Имеется ежегодное увеличение расходов на обследование и оказание медицинской помощи [8, 9].
Цель написания обзора – ознакомить врачей с классификацией ФГН у детей в свете Римских критериев-IV, их распространенностью, последствиями, общими патогенетическими механизмами, алгоритмом диагностики и принципами терапии.
Распространенность и последствия функциональных нарушений
Наиболее часто (55–75%) ФГН выявляются у детей раннего возраста (до 4 лет) и в большинстве случаев обусловлены анатамо-физиологическими особенностями, процессами адаптации нервной и пищеварительной систем к быстро меняющимся потребностям растущего организма [10–13]. Среди ФГН преобладают срыгивания (23,1%), кишечные колики (20,5%) и функциональный запор (17,6%) в различных комбинациях, реже – как изолированное проявление [11].
У детей старшего возраста (старше 4 лет) ФГН наблюдается в среднем в 30% случаев [12–14]. Согласно результатам обзора S. Rajindrajith и N.M. Devanarayana (2013), лидирующие позиции занимают функциональные запоры (15,3%) и ФГН с болевым абдоминальным синдромом, такие как синдром раздраженного кишечника (4,9–19,2%), функциональная абдоминальная боль (4,4–5,6%), функциональная диспепсия (2,5–15,7%) и абдоминальная мигрень (1%) [15]. Недержание кала встречается примерно в 2% случаев и в 80% ассоциируется с запорами [12]. Согласно данным китайских исследователей (Z. Huiqing и соавт., 2011), полученным при обследовании 3671 подростка, синдром раздраженного кишечника выявлялся в 19,9% случаев, функциональный запор и функциональная диарея – в 24,9 и 5,4% случаев соответственно [16].
В Российской Федерации (РФ) данные по эпидемиологической распространенности ФГН представлены недостаточно и касаются отдельных форм. Так, частота выявляемости функционального запора, по данным анкетирования, проведенного в детских поликлиниках Центрального, Северо-Западного, Южного, Сибирского и Уральского федеральных округов РФ среди 2195 детей в возрасте от 0 до 17 лет, составила 53% [17].
Таким образом, результаты имеющихся эпидемиологических исследований позволяют заключить, что ФГН весьма распространены среди детской популяции всего земного шара [18]. При этом наиболее часто выявляются кишечная колика и запоры у детей раннего возраста и функциональная диспепсия, запоры и синдром раздраженного кишечника у детей старшего возраста, тогда как такие состояния, как синдром руминации и аэрофагия, встречаются относительно редко, составив не более 3–5% случаев [12, 16, 18]. Последствия ФГН можно разделить на ближайшие и отдаленные (табл. 2).
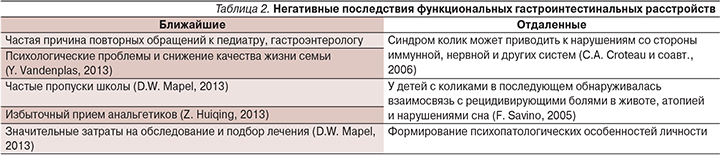
Обеспокоенность вызывают данные о взаимосвязи ФГН в раннем возрасте и хронических заболеваний в более старшем возрасте. Так, B.D. Gold (2006) и S.R. Orenstein (2006) отметили, что дети со срыгиваниями в анамнезе составляют группу риска по развитию хронического гастродуоденита, формированию гастроэзофагеальной рефлюксной болезни, а также пищевода Барретта в более старшем возрасте [19, 20]. Сходные данные приводят C. Canivet (2000) и F. Savino (2005), наблюдавшие в течение 10 лет детей с коликами: чаще выявлялись аллергические заболевания и абдоминальный болевой синдром, который, несмотря на функциональный характер, в 2/3 случаев требовал стационарного лечения [21, 22]. В школьном возрасте у детей с ФГН в анамнезе чаще, чем в популяции, отмечались психоэмоциональные нарушения, нарушения сна (трудности засыпания и частые ночные пробуждения) [23, 24], снижение показателей общего и вербального коэффициента интеллектуального развития [13], синдром гиперактивного поведения и другие поведенческие нарушения [14].
Общие патогенетические механизмы функциональных нарушений
Независимо от того, какой отдел ЖКТ вовлекается в патологический процесс, функциональные заболевания объединяют следующие характерные признаки (D.A. Drossman, 2006, 2016):
- общие патофизиологические механизмы;
- отсутствие анатомических и метаболических дефектов, которые могли бы объяснить имеющиеся симптомы;
- обязательным компонентом патофизиологических изменений является нарушение нормальной нейромышечной регуляции и функции пораженного отдела ЖКТ;
- нет патогномоничных симптомов; имеющиеся жалобы носят неопределенный характер, в случае болевого синдрома отсутствует типичная локализация болей;
- показано значение психосоциальных факторов на всех этапах развития ФГН у детей, начиная с повышения чувствительности ЖКТ к различным воздействиям до модифицирующего влияния на течение заболевания и эффективность проводимой терапии [1, 2].
Как свидетельствуют результаты анкетирования педиатров (S. Rajindrajith, N.M. Devana-rayana, 2014), отношение врачей к диагнозу ФГН неоднозначно: от полного отрицания до необоснованно частой медикаментозной терапии, даже в отсутствие симптомов тревоги [25]. Это связано со следующими факторами: недостатком эпидемиологических данных; недопониманием патофизиологических механизмов; приверженности биомедицинскому подходу к развитию болезни; отсутствием осведомленности о критериях постановки диагноза; сложностями в определении тактики лечения и наблюдении пациентов этой группы [18, 25].
Возможной причиной недоверия ряда врачей к диагнозу ФГН служит приверженность традиционной биомедицинской модели развития болезни, когда определенному заболеванию должны соответствовать характерные морфологические нарушения [3]. На практике это приводит к тому, что, следуя традиционным подходам, большинство врачей ставят детям с болями в животе диагноз «гастрит» или «гастродуоденит», даже в отсутствие надежных доказательств [25].
Изменение к подходам в диагностике ФГН связано с внедрением в 1970-е гг. биопсихосоциальной модели, предусматривающей комплексное интегративное воздействие биологических, психологических и социальных факторов в развитии заболевания. Подобная модель помогает объяснить сценарий развития болезни, который не может быть объяснен с позиций традиционной биомедицинской модели и с учетом возможностей современных методов обследования [1, 2, 25].
Патогенез ФГН, согласно биопсихосоциальной модели, включает комплекс патофизиологических сдвигов со стороны нервной системы и гастроинтестинального тракта, вызванных нарушением регуляции по оси мозг–кишечник, с изменениями в серотониновой сигнальной системе и избыточной активацией участков головного мозга, ответственных за нисходящую регуляцию болевых сигналов [26].
В качестве факторов, инициирующих, а затем поддерживающих патологический процесс, рассматривается комбинация стрессорных воздействий окружающей среды, особенностей реактивности и копинг-стратегий ребенка, а также реакции родителей на симптомы, беспокоящие ребенка [1, 27, 28]. Изменения со стороны ЖКТ включают дискоординацию взаимодействия нервного и мышечного компонентов с развитием нарушения моторики, повышение проницаемости кишечника, изменение состояния кишечной микробиоты (снижение представителей нормофлоры и повышение уровня условно-патогенной флоры), изменение висцеральной гиперчувствительности (рис. 1) [1, 29, 30].

Алгоритмический подход к диагностике заболеваний
Гастроинтестинальные симптомы при заболеваниях могут варьироваться и включают рецидивирующие боли в животе, периодическую рвоту, вздутие живота, нарушения дефекации и т.д.
В связи с отсутствием характерных клинических проявлений для диагностики ФГН, согласно международным и отечественным соглашениям, используется комплекс признаков. В 1997 г. была предпринята первая попытка стандартизировать диагностические критерии для ФГН в педиатрии, представленная в 1999 г. в виде II Римских критериев [31] с последующим уточнением в 2006 г. (III Римские критерии). В нашей стране в 2004 г. на XI Конгрессе детских гастроэнтерологов России (Москва) был принят Рабочий протокол диагностики и лечения функциональных нарушений органов пищеварения у детей [32].
В связи с тем что некоторые функциональные нарушения выпали из классификации, согласно Римским критериям-III (2006), и не все представленные варианты нашли свое отражение в Международном классификаторе болезней 10-го пересмотра, разработаны и в настоящее время представляются широкой медицинской общественности Римские критерии-IV (2016) [2].
Критерии, созданные на основании обследования большой когорты пациентов, рассматривались как диагностический инструмент для практикующих врачей, предназначенный для повышения эффективности и упрощения диагностического процесса ФГН, уменьшения числа диагностических процедур и, соответственно, снижения стоимости обследования [12]. Этому способствовал алгоритмический подход, позволяющий проводить диагностику функциональных нарушений на основании соответствия симптомов, имеющихся у пациентов, Римским критериям в отсутствие симптомов тревоги, характерных для органических заболеваний [33]. В связи с этим может быть предложен следующий обобщенный алгоритм диагностики ФГН (рис. 2).
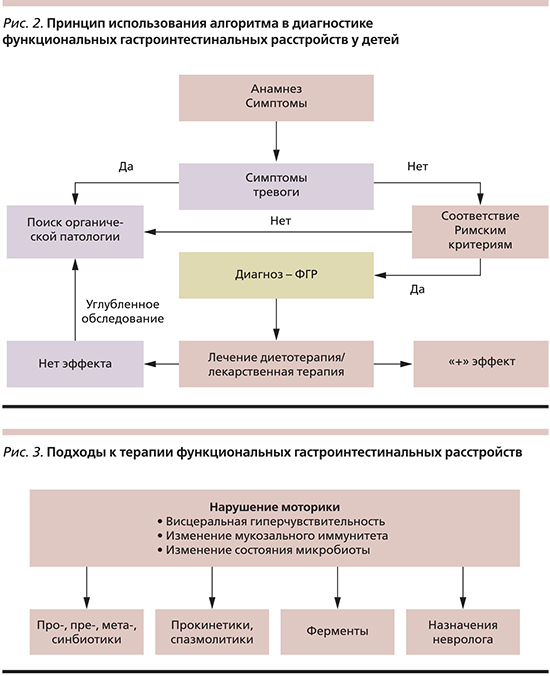
Симптомы тревоги («красные флаги» в зарубежной литературе) могут свидетельствовать о наличии органической патологии и требуют проведения углубленного обследования пациента (табл. 3).
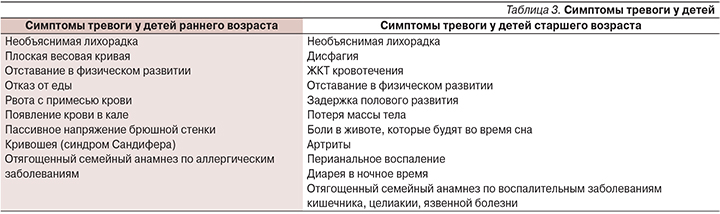
Кроме того, необходимо учитывать симптомы тревоги, указывающие на наличие психосоциальных проблем, которые присутствуют не менее чем в течение последней недели, а именно: чувство напряжения (признак тревоги); упадок духа (признак депрессии); нарушение ежедневной активности; мысли, что самочувствие уже никогда не улучшится (нарушение со стороны стратегий совладания–копинг-стратегии) [34].
Лечение детей с ФГН
Медикаментозная терапия, учитывающая основные звенья патогенеза ФГН, должна быть направлена на нормализацию состояния микробиоты кишечника, улучшение процессов кишечного пищеварения, восстановление нарушенной моторики и снижение висцеральной гиперчувствительности (рис. 3). Дополнительное обследование необходимо, если у пациента есть симптомы тревоги или отсутствует эффект от проведенной терапии.
Коррекция диеты предусматривает исключение продуктов, содержащих трудноусвояемые жиры, сырые овощи и фрукты, в случае явлений недостаточности лактазы – молочные продукты, при непереносимости глютена – исключение ряда злаков (пшеница, рожь, овес, ячмень) [35, 36].
Принимая во внимание биопсихосоциальную природу заболевания, при лечении ФГН следует учитывать психологические и поведенческие особенности пациентов, иначе эффект от лечения будет неполным или кратковременным [4, 5, 32]. Кроме того, необходимо учитывать, что эффективное лечение зависит от установления терапевтического альянса с родителями ребенка.
В многочисленных исследованиях показано положительное влияние пробиотических штаммов бактерий на иммунную систему, связанное с усилением синтеза иммуноглобулина А (IgA), цитокинов, фагоцитарной активности гранулоцитов крови [36–38]. Синбиотики, представляющие собой комбинацию пре- и пробиотиков, подавляют рост условно-патогенных микроорганизмов, оказывают влияние на характер стула, способствуя его размягчению [36, 38], улучшают кишечный транзит, нормализуют функцию кишечника [39]. Клинические проявления нарушений со стороны микробиоты при ФГН возникают вследствие появления непереваренных пищевых субстратов в полости кишки, дефицита желчных кислот, из-за снижения пула свободных жирных кислот, образующихся при гидролизе липидов и обладающих бактерицидной функцией [32, 33]. Избыточный бактериальный рост в свою очередь усугубляет нарушения полостного пищеварения, т.к. бактериальные токсины повреждают панкреатические ферменты в полости кишки и в пристеночной слизи. Кроме того, токсины снижают активность мембранных ферментов, усугубляя имеющиеся нарушения.
К синбиотикам относится Максилак – уникальная пищевая добавка, созданная по запатентованной инновационной технологии MURE (Multi Resistant Encapsulation), которая сохраняет жизнеспособность микроорганизмов и защищает содержимое капсул или микрогранул даже при воздействии агрессивных факторов ЖКТ. Максилак не подвержен разрушению ферментами поджелудочной железы и соляной кислотой желудочного сока, предназначен для устранения нарушений микробиоты, возникших в ЖКТ при ФГН; его применение допускается при непереносимости лактазы. Состав средства сбалансирован, представлен уникальными компонентами – оптимальными концентрациями 9 культур бактерий (Lactobacillus helveticus, Lactobacillus lactis, Bifidobacterium longum, Bifidobacterium breve, Streptococcus thermophilus, Lactobacillus rhamnosus, Lactobacillus casei, Lactobacillus plantarum, Bifidobacterium bifidum) и фруктоолигосахаридами. Концентрация пробиотических компонентов составляет 4,5×109 КОЕ, отсутствуют консерванты и казеин, что позволяет считать препарат безопасным продуктом для детей с аллергией на указанные вещества. Форма выпуска: капсулы с кишечнорастворимой оболочкой и саше (порошки). Детям до 2 лет назначают по 1 пакетику саше Максилак Бэби, старше 2 лет – по 1–2 пакетика в сутки, старше 3 лет и взрослым– по 1 капсуле в сутки во время еды или после приема пищи. Курс лечения составляет 10–14 дней, при необходимости может быть увеличен до 30 дней. Капсулы можно запивать молоком, кисломолочными напитками, компотом, чаем, соками, водой.
Лечение ФГН независимо от этиологического фактора и клинической формы требует комплексного подхода, направленного не только на купирование симптомов, но и на лечение вторичных изменений, нарушений муконазального гомеостаза и микробной контаминации.
Заключение
Принимая во внимание накопленные данные, очевидно, что ФГН являются распространенными патологическими состояниями у детей. Диагноз может быть поставлен на основании соответствия симптомов, имеющихся у пациента, Римским критериям-IV. Для этого необходимо уточнить жалобы, анамнез заболевания, провести физикальный осмотр и исключить наличие симптомов тревоги. Установление правильного диагноза, определение факторов риска, оценка степени воздействия данного ФГН на качество жизни обеспечивает оптимальный подход к терапии и предотвращает использование инвазивных методов исследования (рентгенологическое, эндоскопическое обследование), повышающих стоимость обследования при низкой информативности и риске ухудшения психоэмоционального состояния пациента.
При лечении необходимы комплексный подход, включающий применение препаратов с учетом патогенетических механизмов, психологическая поддержка пациента и последующая продолжительная реабилитация.
С позиций биопсихосоциальной модели в развитии ФГН признается роль нарушений муконазального гомеостаза и микробной контаминации. Это позволяет обосновать необходимость применения синбиотических препаратов, способствующих уменьшению характерных клинических проявлений в виде учащенного стула или запоров, метеоризма, болей в животе и устранению проявлений, обусловленных нарушением со стороны микробиоты кишечника.


