Атопический дерматит (АтД) является хроническим рецидивирующим аллергическим заболеванием кожи, дебютирующим преимущественно в раннем детском возрасте при наследственной предрасположенности [1–3].
Термин «атопия» используется с 1920-х гг., позже стали применять термин «атопический дерматит», характеризовавшийся необычным ответом кожи на распространенные раздражители [4]. В 1980 г. J.M. Hanifin и G. Rajka [5] предложили критерии диагностики АтД. За последующие 37 лет применения критерии были модифицированы.
В настоящее время наиболее эффективным подходом к терапии АтД признана комплексная терапия. У детей необходимой составляющей является гипоаллергенная диета, элиминация факторов риска в быту. Среди лекарственных препаратов используются антигистаминные средства, по показаниям – тиосульфат натрия, сернокислая магнезия [1, 6].
В комплексном лечении АтД существенное значение имеет наружная терапия, целью которой служат подавление воспаления кожи, профилактика и устранение вторичного инфицирования, улучшение барьерных функций кожи. Выбор наружных средств для лечения обусловлен возрастом ребенка, стадией заболевания, наличием осложнений [1, 6, 7]. Применение таких традиционных средств, как деготь, сера, нафталан, ихтиол, АСД (антисептик-стимулятор Дорогова, 3-я фракция), ограничено их резким специфическим запахом, что может приводить к обострению как кожного процесса, так и респираторного синдрома, который может наблюдаться при АтД. Некоторые противозудные составляющие (ментол, анестезин) помимо запаха нередко сами обладают сенсибилизирующим действием. Значительно эффективнее обострение процесса купируют топические глюкокортикоидные средства – ГКС [1, 6]. Препараты признаны средством первой линии терапии АтД, тогда как топические ингибиторы кальциневрина – второй по причине недоказанной безопасности. Топические ГКС являются оптимальным препаратом при выраженных воспалительных явлениях АтД с позиций доказательной медицины [8].
Первое использование топического ГКС гидрокортизона в 1950 г. произвело революцию в дерматологии.
В 1960–1970-е гг. были синтезированы более эффективные средства, потенциал которых возрастал за счет либо галогенизации, либо метилирования основной молекулы стероидного каркаса [8].
Топическое ГКС, применяемое в педиатрической практике, должно обладать сильным противовоспалительным действием, низкой системной биодоступностью, быстрым началом действия и минимальными местными побочными эффектами [6–8].
В дерматологической практике широко используются галогенизированные топические средства.
В Российской Федерации применяется масса галогенизированных кортикостероидов [9]. При их назначении необходимо учитывать, что такие средства обладают генотоксичностью in vitro, показаны хромосомные аберрации периферической крови. Применение галогенизированных стероидных препаратов приводит к снижению синтеза фибробластов, коллагена, гликозаминогликанов, замедлению темпа деления клеток эпидермиса и дермы, что предрасполагает к развитию атрофии кожи. Длительная циркуляция в крови галогенизированных препаратов предопределяет подавление выработки и нарушение циркадного ритма эндогенного кортизола. Все вышеперечисленное лежит в основе развития таких нежелательных явлений, как периоральный дерматит, стрии, гипертрихоз, акнеформный фолликулит, нарушения пигментации.
В педиатрической практике предпочтительнее использовать негалогенизированные топические средства. К ним относится метилпреднизолона ацепонат (Адвантан, Bayer), обладающий высокой противовоспалительной активностью, липофильностью, улучшенной по сравнению с ранее созданными препаратами фармакокинетикой [4].
Препарат легко проникает в кожу, и в очаге воспаления под влиянием ферментов воспаления эстераз трансформируется в активный метаболит 6α-метилпреднизолон-17-пропионат, который имеет значительно более высокое сродство к ГКС-рецепторам, чем исходное вещество. Таким образом, действие Адвантана реализуется локально – в очаге воспаления.
Активный метаболит Адвантана – 6α-метилпреднизолон-17-пропионат – связывается с внутриклеточными ГКС-рецепторами. Стероид-рецепторный комплекс взаимодействует с определенными участками ДНК, таким образом вызывая серию биологических эффектов. В частности, это приводит к индукции синтеза белка липокортина-1, который подавляет активность ключевого фермента каскада арахидоновой кислоты – фосфолипазы А2. Вследствие этого нарушается синтез провоспалительных простагландинов и лейкотриенов. Установлены и другие механизмы противовоспалительного действия ГКС: торможение образования и всех функций макрофагов, угнетение синтеза провоспалительных цитокинов, усиление сосудосуживающего действия адреналина и др. [7, 8].
Наружное использование Адвантана приводит к подавлению воспалительных и аллергических кожных реакций, так же как и реакций, связанных с усиленной пролиферацией, что приводит к уменьшению объективных симптомов (таких, как эритема, отек, лихенификация) и субъективных ощущений (зуд, раздражение, боль). При применении Адвантана наружно в эффективной дозировке (0,1%) системное воздействие минимально. После многократного нанесения препарата на большие поверхности (40–60% поверхности кожи), а также применения под окклюзионную повязку нарушений функций надпочечников не отмечается, уровень кортизола в плазме и его циркадный ритм остаются в пределах нормы, снижения уровня кортизола в суточной моче не происходит [6, 8].
При попадании в системный кровоток 6α-метилпреднизолон-17-пропионат быстро и полно связывается с транспортным белком – транскортином, а затем в печени подвергается конъюгации с глюкуроновой кислотой и в конъюгированном виде экскретируется почками.
Корректный выбор оптимальной лекарственной формы препарата позволяет повышать эффективность терапии. При выборе формы необходимо учитывать такие морфофункциональные особенности кожи у детей, как постоянное анатомо-физиологическое развитие, быстрая смена слоев эпидермиса, рыхлость расположения ороговевающих клеток, интенсивный митоз не только в базальном, но и в шиповидном, и зернистом слоях, повышенная чувствительность кожи к внешним воздействиям, обильная васкуляризация кожи, один слой эндотелиальных клеток у сосудов [6].
Кроме того, выбор наружных средств для лечения обусловлен возрастом ребенка, фазой заболевания, наличием осложнений [10–12]. Адвантан разрешен к использованию детьми начиная с 4-месячного возраста [9].
К несомненным достоинствам препарата относится возможность применения на наиболее уязвимых, например на открытых, участках кожного покрова, в т.ч. на лицо. Применение Адвантана позволяет выбирать оптимальную лекарственную форму для соответствующей возрастной группы. Для детей первого года жизни предпочтительна эмульсия, в основе которой содержится 67,5% воды, до 3 лет – эмульсия и крем, в основе которого – 60% воды. С 3-летнего возраста на очагах хронического воспаления может быть использована мазь, на очагах упорного хронического воспаления, в особенности на участках с выраженным роговым слоем, жирная мазь [6–8].
В разных странах проведены исследования свойств метилпреднизолона ацепоната. В отечественной практике также накоплен опыт эффективного применения Адвантана в педиатрической практике [6].
Опыт применения Адвантана показал, что устранение зуда и воспаления под действием препарата приводит к улучшению общего состояния, в частности устраняет расстройства сна, что играет весьма существенную роль при лечении детей, страдающих АтД [12, 13].
Целью исследования была оценка эффективности и безопасности применения различных лекарственных форм Адвантана в комплексной терапии детей, страдающих АтД.
Материал и методы
Под нашим наблюдением с апреля 2013 по апрель 2017 г. находились 133 пациента, страдавших АтД. Среди них были 68 мальчиков, 65 девочек в возрасте от 4 месяцев до 15 лет. Все пациенты страдали признаками экзацербации кожного процесса, постоянным зудом, повышенной возбудимостью, беспокойством. 22 детей сильный зуд приводил к расстройству сна. Впервые диагноз был установлен от 3 дней до 15 лет назад. Диагноз «атопический дерматит» (код по МКБ-10 L20) был поставлен в соответствии с Федеральными клиническими рекомендациями по диагностике и лечению АтД Российской ассоциации аллергологов и клинических иммунологов [1].
С этой целью применены модифицированные критерии J.M. Hanifin и G. Rajka:
- зуд кожи;
- возрастные изменения характерных поражений кожи;
- хроническое рецидивирующее течение;
- наличие атопических заболеваний у пациента и/или его родственников;
- начало заболевания в раннем возрасте;
- сезонность обострений;
- обострение процесса под влиянием провоцирующих факторов-аллергенов, ирритантов, пищевых продуктов, эмоционального стресса;
- сухость кожи;
- белый дермографизм;
- склонность к кожным инфекциям;
- хейлит;
- симптом Денье–Моргана;
- гиперпигментация кожи периорбитальной области;
- повышение содержания общего и аллерген-специфических иммуноглобулина E в сыворотке;
- эозинофилия периферической крови.
Ранее получали повторные курсы терапии, включившие антигистаминные, десенсибилизирующие препараты, про- и пребиотики, наружные противовоспалительные средства, включая топические ГКС, 120 из 133 пациентов, 13 пациентов в возрасте 4–12 месяцев ранее какого-либо лечения не получали.
К моменту обследования клинические проявления заболевания соответствовали возрастному периоду пациентов. У 24 пациентов в возрасте от 4 месяцев до 3 лет преобладали везикуло-папулезные высыпания. В очагах поражения отмечено мокнутие, образование обильных и толстых серозных корок, эрозий, трещин, выделявших серозный экссудат и серозно-геморрагическую жидкость, имела место значительная отечность очагов. На щеках выделялись эритематозные очаги, сопровождавшиеся отечностью и шелушением, иногда с явлениями мокнутия и появлением серозных корок. Процесс распространялся на кожу лба, волосистую часть головы. При существовании очагов поражения свыше 3 месяцев возникали плоские папулы, очаги лихенификации, экскориации. У всех 24 детей этой группы ухудшение течения кожного процесса отмечалось в холодное время года, улучшение – в летнее.
У 62 пациентов в возрасте от 3 до 12 лет в клинической картине преобладали лихеноидные папулы сероватого цвета, фолликулярные папулы, экскориации. Отмечена преимущественная локализация очагов в локтевых сгибах и подколенных складках, на шее, за ушными раковинами. У детей этой группы выявлена разной степени выраженности отечность век с углублением естественных складок на них. На коже боковых поверхностей туловища, спины распространялись полушаровидные фолликулярные папулы. На кистях имелись инфильтрированные очаги. У 58 из 62 детей этой группы отмечены выраженная сухость кожных покровов, явления атопического хейлита. У 61 пациента ухудшение кожного процесса имело место в холодное время года, улучшение – в летнее.
У 1 из 62 детей выраженной зависимости кожного процесса от времени года не было.
У 47 пациентов в возрасте от 12 до 15 лет очаги поражения имели преимущественную локализацию в верхней части тела. Отмечена выраженная лихенификация в локтевых сгибах, подколенных впадинах. На руках очаги выявлены не только на сгибательной, но и на разгибательной поверхности. Диффузно располагались лихеноидные плоские полигональные и округлые полушаровидные папулы. У 37 пациентов наблюдалось ухудшение течения кожного процесса в холодное время года, улучшение – в летнее. У 10 из 47 пациентов выраженной зависимости кожного процесса от времени года не отмечено, но у 9 из них наблюдалось значительное улучшение состояния после морских купаний в сочетании с солнечной инсоляцией в летнее время.
Критерии включения в настоящее исследование:
- клинические признаки АтД в стадии обострения;
- степень тяжести АтД от 20 до 60 баллов SCORAD (Scoring of Atopic Dermatitis);
- возраст старше 4 месяцев.
Критерии исключения:
- состояние эритродермии;
- гиперчувствительность к компонентам применяемых средств;
- возраст младше 4 месяцев;
- наличие любого состояния, которое может создать неоправданный риск нанесения вреда здоровью пациента;
- терапия системными ГКС, топическими ингибиторами кальциневрина, средствами, восстанавливающими целостность кожного барьера и увлажняющими в течение предшествовавших 4 недель;
- терапия топическими ГКС в течение предшествовавших 3 недель.
В ходе исследования была обязательной регистрация любых побочных эффектов для дальнейшей оценки безопасности Адвантана.
Всем пациентам лечение проведено амбулаторно.
Адвантан применен на очагах поражения в соответствующей лекарственной форме. Адвантан в виде эмульсии применяли всем детям в возрасте от 4 месяцев до 3 лет, а также пациентам старше 3 лет на очагах, расположенных на лице, и участках поражения с выраженными экссудативными явлениями.
Детям старше 3 лет эмульсию применяли на очагах поражения, расположенных на лице, а также в случаях острого воспаления, сопровождавшегося везикулами, эрозиями, мацерациями. В этих возрастных группах наряду с эмульсией применяли и другие лекарственные формы Адвантана. На очаги острого и подострого воспаления детям старше 3 лет применяли Адвантан в виде крема. При хроническом воспалении без мокнутия использовали мазь. На очаги хронического воспаления, сопровождавшегося значительной сухостью, выраженной лихенизацией и утолщением кожных покровов, применяли жирную мазь. Все лекарственные формы Адвантана применяли в виде аппликаций 1–2 раза в день.
Помимо наружной терапии все пациенты получали внутрь антигистаминные, десенсибилизирующие средства в возрастных дозировках в течение первых 10 дней терапии, затем продолжали монотерапию Адвантаном.
Результаты исследования
У всех пациентов было отмечено выраженное уменьшение зуда, эритемы, отечности на 2-й день применения Адвантана, в дальнейшем регресс высыпаний постепенно продолжался. К 5-му дню лечения самочувствие всех детей улучшилось, уменьшилось беспокойство. Через 7–10 дней применения Адвантана в виде эмульсии либо крема отмечен полный регресс островоспалительных явлений, ночной сон был восстановлен. На 12–14-й день у всех пациентов отмечено значительное улучшение (см. таблицу).

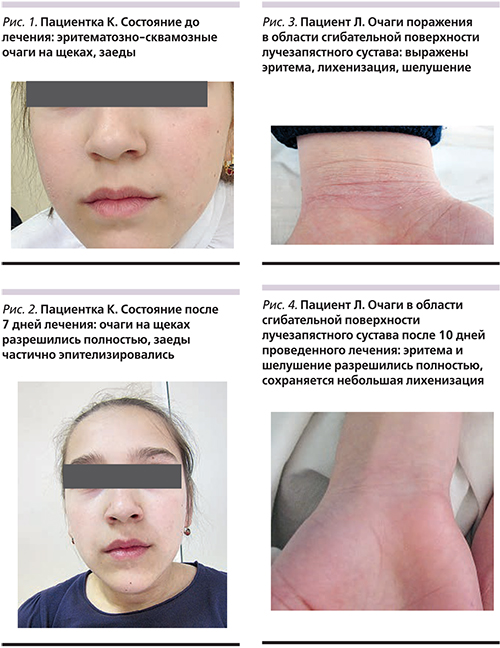
На рис. 1–4 показаны клинические примеры результатов лечения.
По окончании курса терапии индекс SCORAD снижался до 4–8 баллов.Терапию все пациенты переносили хорошо, побочных эффектов ни в одном из случаев отмечено не было.Не отмечено какого-либо отрицательного воздействия проводимой терапии на показатели периферической крови, мочи.
Обсуждение
Полученные результаты подтверждают ранее описанную высокую терапевтическую эффективность и безо-пасность наружной терапии детей с применением соответствующих лекарственных форм Адвантана [10–14].
В различных возрастных группах у детей, страдавших АтД, отмечен высокий терапевтический эффект Адвантана у пациентов в возрасте от 4 месяцев до 3 лет в виде эмульсии. У детей старше 3 лет аналогичный результат был достигнут при применении эмульсии на очаги на лице и на участки поражения с выраженными экссудативными явлениями, крема, мази, жирной мази – на другие участки. Курс лечения способствовал быстрому регрессу островоспалительных явлений, восстановлению ночного сна, устранению зуда и беспокойства.
Побочных эффектов от применения препаратов отмечено не было, терапию все дети переносили хорошо, что согласуется с данными, ранее представленными в литературе [6–14].
Полученные нами данные позволяют рекомендовать Адвантан в виде соответствующих лекарственных форм в комплексном лечении АтД у детей различных возрастных групп. После снятия обострения препарат может использоваться в виде монотерапии.
Выводы
- Адвантан в виде эмульсии эффективен в отношении пациентов в возрасте от 4 месяцев до 3 лет, а также в других возрастных группах на очаги, расположенные на лице, а также участки поражения с выраженными экссудативными явлениями.
- Адвантан в виде крема эффективен при применении у детей старше 3 лет с острым/подострым воспалением в очагах поражения.
- Адвантан в виде мази эффективен при применении у детей старше 3 лет с хроническим воспалением без мокнутия.
- Адвантан в виде жирной мази эффективен при применении у детей старше 3 лет на очаги, характеризующиеся сухостью, выраженной лихенизацией и утолщением кожных покровов.
- Все лекарственные формы Адвантана хорошо переносятся детьми. Лечение не сопровождается побочными эффектами.



