Введение
При вальгусной деформации коленного сустава (КС) в результате деформирующего остеоартроза в патологический процесс вовлекаются как костные, так и мягкотканные структуры КС [4, 10]. Ситуацию усугубляют потеря костной массы наружных мыщелков бедра и голени, перерастяжение или отсутствие медиальной коллатеральной связки, укорочение латеральной коллатеральной и задней крестообразной связок, высокий индекс массы тела у многих пациентов.
Неудовлетворительные результаты и как следствие – ревизионные артропластики зачастую связаны с предварительным неверным подбором конструкции для пациентов с тяжелым поражением сустава, значительным дефицитом костной массы мыщелков бедра и голени и скомпроментированностью связочного аппарата, применением несвязанных или малосвязанных имплантатов [11]. В то же время использование полностью связанных эндопротезов с петлевым механизмом контакта между бедренным и большеберцовым компонентами приводит к концентрации нагрузок в зоне контакта имплантат–цемент и цемент–кость, что может приводить к нестабильности компонентов [1–3]. Применение полусвязанных эндопротезов, известных как варус-вальгуссвязанные, позволяет добиваться коррекции грубых вальгусных деформаций одновременно с достижением адекватной стабильности во фронтальной плоскости в отсутствие петлевого механизма между бедренным и большеберцовым компонентами [8, 9].
Цели исследования:
- анализ результатов применения полусвязанного эндопротеза КС при выраженной вальгусной деформации КС;
- оценка эффективности ривароксабана (Ксарелто) при профилактике тромбозов глубоких вен нижних конечностей.
Материал и методы
Всем исследуемым пациентам были имлантированы эндопротезы LCCK Zimmer NexGen (варус-вальгуссвязанные, заднестабилизированные). В тотальных полусвязанных эндопротезах КС конструктивно предусмотрена возможность использования модульных интрамедуллярных стандартных и офсетных ножек как на большеберцовом, так и на бедренном компонентах, что обеспечивает большую стабильность первичной фиксации и равномерное распределение нагрузок в зоне имплант–цемент–кость [5]. При дефиците костной массы мыщелков большеберцовой или бедренной кости конструкция позволяет использовать металлические аугменты.
В данной работе были изучены результаты тотального эндопротезирования 60 КС 60 пациентам. Среди пациентов исследуемых групп мужчин было 3 (5 %), женщин 57 (95 %). Средний возраст пациентов составил 64 года (SD ± 12).
У всех больных был клинически и рентгенологически диагностирован остеоартроз коленного сустава III–IV стадий. Согласно классификации Кельгрена, дегенеративнодистрофический характер поражения, соответствующий III стадии, был констатирован у 9 (15 %), IV стадии у 51 (85 %) из обследованных больных.
Все включенные в исследование пациенты имели грубую вальгусную деформацию (более 15 °).
На основании вышеперечисленных признаков пациенты были разделены на две группы.
Первая группа (контрольная) – пациенты с деформирующим артрозом КС III–IV стадий по Kellgren– Lawrence, вальгусной деформацией, которым выполнено эндопротезирование с использованием несвязанной заднестабилизированной конструкции LPS Zimmer NexGen, – 37 (61,6 %) человек.
Вторая группа (основная) – пациенты с деформирующим артрозом КС III–IV стадий с вальгусной деформацией более 15 °, которым выполнено эндопротезирование с использованием полусвязанной заднестабилизированной конструкции LCCK Zimmer NexGen, – 23 (38,3 %) человека.
Все пациенты страдали первичным или вторичным гонартрозом от 2 до 10 лет, в среднем 3,5 года (SD ± 3,7).
Клинические методы исследования
При клиническом обследовании обращали внимание на походку, использование дополнительной опоры. Оценивали выраженность болевого синдрома при нагрузке и в покое, а также интенсивность ночных болей. Во время клинического исследования определяли степень деформации оси конечности, состоятельность крестообразных и коллатеральных связок, наличие внутрисуставного выпота. Оценивали мобильность сустава (с применением нейтрально-нулевого метода, как активного, так и пассивного), мышечную силу, наличие боли при пальпации, степень подвижности надколенника, отдельно оценивались ретропателлярные боли (при помощи теста Цолена). Клиническую деформацию исследовали при помощи гониометра с нагрузкой и без нее. Полученные результаты обследования пациентов обеих групп сравнивали.
Рентгенологические методы исследования
Для контроля смещения бедренной оси (до операции, в рамках хирургической подготовки) использованы стандартные рентгеновские снимки, а также рентгеновские снимки нижних конечностей на протяжении.
Рентгенограммы в переднезадней проекции выполнены при полностью разогнутом КС, снимки в боковой проекции произведены в положении сгибания колена под углом 30 °.
Кроме того, выполнены рентгенограммы нижних конечностей – от тазобедренных до голеностопных суставов – для определения истинной оси нижних конечностей. Это исследование выполнено с нагрузкой (в положении стоя) и без нагрузки (в положении лежа). После оперативного вмешательства также сделаны рентгеновские снимки: в раннем послеоперационном периоде, затем через 1, 3, 6 и 12 месяцев, в дальнейшем – 1 раз в год ежегодно.
Показания к имлантации полусвязанного эндопротеза
Показанием к эндопротезированию КС служил клинически, рентгенологически и интраоперационно диагностированный остеоартроз КС (III–IV стадий) при наличии следующих условий:
- вальгусная деформация во фронтальной плоскости более 15 °;
- тяжелое поражение КС с наличием контрактуры более 20 ° и вальгусной деформацией более 15 °;
- несостоятельность или отсутствие медиальной коллатеральной связки;
- интраоперационное повреждение медиальной коллатеральной связки.
Интраоперационно выявленная тотальная нестабильность КС во фронтальной и сагиттальной плоскостях стали основанием для исключения пациента из настоящего исследования.
При вальгусной деформации колена мы отдавали предпочтение латеральному парапателлярному доступу. Проводили резекцию краев надколенника и только при необходимости выполняли частичный релиз связки надколенника от бугристости большеберцовой кости.
В первую очередь произвели дистальный опил бедренной кости с использованием межмыщелковой линии в качестве ориентира. Проксимальный опил большеберцовой кости выполнен перпендикулярно ее механической оси.
Передне-задний опил бедренной кости выполнен параллельно ранее сформированному плато большеберцовой кости. Легкое наружное ротационное позиционирование бедренного компонента обеспечивается за счет первоначального формирования сгибательной щели КС.
Балансировка КС проведена поэтапно по следующей схеме:
- Удаление остеофитов дорзальных отделов мыщелков бедренной и большеберцовой костей.
- Полный релиз задней крестообразной связки.
- Релиз заднелатерального кармана, задней капсулы от m. popliteus, множественные насечки контрагированных структур заднелатерального отдела, релиз m. popliteus от бедренной кости.
- Релиз латеральной коллатеральной связки от бедренной кости.
В дальнейшем проведены окончательная подготовка большеберцового костного ложа, имплантация компонентов эндопротеза, дренирование полости сустава, послойное ушивание раны. В случае наличия дефектов костной ткани мыщелков размером до 5 мм в зоне контакта с компонентом эндопротеза произвели импакционную пластику губчатой аутокостью. В том случае если присутствовали массивные дефекты костной ткани мыщелков (размером не менее 10 мм), использовали аугментные блоки. Замена суставной поверхности надколенника ни в одном случае не производилась.
При несостоятельности коллатеральных связок полусвязанная конструкция обеспечивает адекватную стабильность, если же отмечается полная нестабильность в двух плоскостях, целесообразно применять полностью связанный эндопротез.
Уже в первые сутки после операции больные начинали заниматься дыхательной гимнастикой, статическими упражнениями для мышц бедра и голени, активными движениями пальцами стоп обеих конечностей. В течение первых суток послеоперационного периода проводилась форсированная мобилизация сустава при помощи аппаратов непрерывной пассивной разработки коленного сустава (Kinetec Performa Knee CPM и Artromot K1). Мобилизация осуществлена в условиях блокады бедренного нерва 20 мл 0,75 %-ным раствором наропина, при этом максимальный угол сгибания был задан на уровне 100 °, угол разгибания – на уровне 5 °. Такие мероприятия позволили обеспечить хорошую функцию сустава в последующем послеоперационном реабилитационном периоде. По истечении первых суток пациентам разрешили вставать и ходить с дополнительной опорой на костыли. Дальнейшая мобилизация выполнена как с применением СРМаппаратов (continuous passive motion), так и самостоятельно пациентами. Регионарную анестезию в послеоперационном периоде не использовали. Швы снимали на 14–15-е сутки. Через 4 недели разрешили полную нагрузку на оперированную конечность, дополнительную опору (трость) рекомендовали использовать в течение 2 месяцев.
Клинический осмотр с обязательным рентгенологическим обследованием проведен через 3, 6 и 12 месяцев, в последующем – ежегодно 1 раз в год.
Профилактика тромбоэмболических осложнений у больных после эндопротезирования КС проводилась во всех наблюдениях и состояла из двух основных групп мероприятий: неспецифических и специфических. Неспецифическая тромбопрофилактика включила использование эластичного бинтования нижних конечностей в послеоперационном периоде и применялась всеми больными. Для профилактики тромбоэмболических осложнений использовали ривароксабан (Ксарелто). Схема применения включила прием 10 мг препарата перорально 1 раз в сутки в течение 40 дней с момента операции. Проведенный анализ показал, что ни в одном из наблюдений тромбоэмболий не было.
Результаты и обсуждение
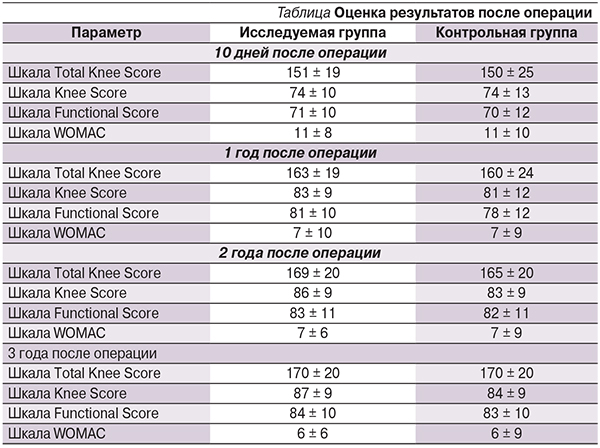
За весь период трехлетнего наблюдения были проанализированы результаты лечения 49 пациентов из 60 прооперированных, 11 человек выбыли из исследования по различным причинам. Таким образом, исследование было проведено на анализе результатов 32 пациентов контрольной и 17 исследуемой групп (см. таблицу).
Для объективизации данных о преди постоперационном состоянии коленного сустава использованы шкалы WOMAC, TKS (Knee Society Score и Function Score) и инструментальное обследование.
При предоперационном осмотре больных шкала WOMAC составила 37,2 (SD ± 13,1) балла в первой группе, 40 (SD ± 12,3) – во второй. Результатом оценки по шкалам Knee Score и Function Score явились дооперационные средние значения: от 92,5 (SD ± 20,1) баллов в первой группе и 101,3 (SD ± 18,7) – во второй. Первая часть шкалы TKS (KSS) – 46,1 (SD ± 11,1) балла в первой группе, 50,8 (SD ± 10,1) – во второй.
Во второй части KSS (Function Score) были получены средние значения: от 46,3 (SD ± 9,2) балла в первой группе, 50,3 (SD ± 8,5) – во второй.
Средняя продолжительность операции составила 70,5 (SD ± 8,7) минут в первой группе, 79,3 (SD 8,6) – во второй.
Средняя длина разреза составила 16,8 см (SD ± 2,0) в первой группе, 17,5 (SD ± 0,8) – во второй.
Результаты трехлетнего наблюдения в исследуемой группе через год после операции: у 14 (82,3 %) пациентов – отличные, у 2 (11,7 %) – хорошие, у 1 (5,8 %) – неудовлетворительные. Через 2 года после операции у 15 (88,2 %) пациентов – отличные, у 1 (5,8 %) – хорошие, у 1 (5,8 %) – неудовлетворительные результаты. Через 3 года после операции у 15 (88,2 %) пациентов – отличные, у 1 (5,8 %) – хорошие, у 1 (5,8 %) – неудовлетворительные результаты. У 23 (71,8 %) пациентов контрольной группы за весь период наблюдений отмечены отличные результаты, у 5 (15,6 %) – хорошие, у 5 (15, 6 %) – неудовлетворительные.
При предоперационном обследовании амплитуда движений в контрольной группе в среднем составила 80 ° (SD ± 2), 79 ° (SD ± 2) – в исследуемой группе. Результаты трехлетнего наблюдения: у пациентов в контрольной группе амплитуда движений составила в среднем 112 ° (SD ± 2), у исследуемых – 114 ° (SD ± 2).
Результаты трехлетнего наблюдения: у 3 пациентов контрольной группы было установлено постоперационное смещение оси > 6 ° (вальгус); у 2 пациентов постоперационное смещение оси > 3 ° (варус). В основной группе показатели всех пациентов находились в целевой области от 4 ° (варус/вальгус), в среднем 5 ± 2 °. Необходимость в ревизионном вмешательстве возникла у пяти пациентов из контрольной группы. Причиной стала асептическая нестабильность компонентов эндопротеза. Во всех случаях потребовалась ревизионная операция полусвязанным эндопротезом с использованием аугментных блоков и длинных ножек. Интраоперационно во всех случаях было выявлено нарушение баланса мягких тканей.
Заключение
При планировании тотального эндопротезирования у пациентов с грубой вальгусной деформацией оси конечности во фронтальной плоскости в операционной следует иметь набор несвязанных заднестабилизированных, варус-вальгус-связанных и полностью связанных эндопротезов и соответствующий инструментарий.
После выполнения стандартного доступа, мягкотканного релиза, дебридмента и подготовки суставных поверхностей по стандартным ориентирам следует выполнять костные опилы и устанавливать пробные компоненты эндопротеза соответствующих размеров. При этом сохраняются области проксимального и дистального прикрепления коллатеральных связок. После этого следует проверять стабильность КС во фронтальной плоскости. При несостоятельности коллатеральных связок полусвязанная конструкция обеспечит адекватную стабильность, если же отмечается полная нестабильность в двух плоскостях, целесообразно применять полностью связанный эндопротез.
Использование полностью связанных эндопротезов при сохранности хотя бы одной из коллатеральных связок считаем нецелесообразным, т. к. при этом происходит избыточная концентрация нагрузки в зоне эндопротез–цемент–кость.
Применение данной тактики позволило получить статистически значимое улучшение показателей состояния КС по всем параметрам в обеих группах пациентов, а также удовлетворительную выживаемость эндопротезов при сроке наблюдения 3 года.
Препарат ривароксабан (Ксарелто), в течение длительного времени применявшийся нами для профилактики тромбоэмоболических осложнений, зарекомендовал себя как эффективное средство профилактики тромбоэмболических осложнений у ортопедических пациентов.



