Высокая эффективность остеопластических материалов (ОПМ) в дентальной имплантологии обеспечивается их сочетанным остеокондуктивным и остеоиндуктивным действиями. В НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи на основе высокоочищенных нанокристаллических гидроксиапатита и костного коллагена разработан ОПМ Gamalant™-паста-ФОРТЕ Плюс [1, 3–11].
Gamalant™-паста-ФОРТЕ Плюс содержит факторы роста костной ткани – костные морфогенетические белки человека, полученные с использованием генно-инженерных технологий, обладает комплексным остеокондуктивным и остеоиндуктивным действиями. Материал прошел все процедуры, разрешающие его применение в клинической практике на территории России.
Целью представленного ниже исследования являлась оптимизация предимплантологической подготовки альвеолярной лунки (АЛ) удаленного зуба с помощью отечественного наноструктурированного остеопластического материала Gamalant™-паста-ФОРТЕ Плюс.
Материал и методы исследования
Клиническая часть исследования базировалась на целенаправленном обследовании 122 больных (средний возраст – 38,4 ± 2,4 года; 80 женщин, 42 мужчин), которым проводилось удаление зуба в боковом отделе нижней челюсти по поводу хронического пародонтита (K05.3) или дистопии (K07.3) и планировалась внутрикостная имплантация после периода перестройки АЛ.
В контрольной группе (69 человек) АЛ после удаления зуба подвергалась естественной репаративной
перестройке под кровяным сгустком, в основной группе (53 человека) АЛ заполнялась ОПМ Gamalant™-пастаФОРТЕ Плюс. Через 6 месяцев 48 пациентам контрольной группы и 51 – основной в область удаленных зубов устанавливались внутрикостные титановые имплантаты Alfa Bio (Израиль); раскрытие имплантатов проводилось спустя 3 месяца.
Клинико-рентгенологическое обследование больных до удаления зубов и при раскрытии имплантатов
проводилось с использованием ортопантомографа OP100D (Финляндия) и рентгенрадиовизиографа IRIX 70 (Германия); перед установкой имплантатов осуществлялась компьютерная томография (КТ) на аппарате Galileos (Германия); при установке и раскрытии имплантатов выполнялся частотно-резонансный анализ (ЧРА) стабильности имплантатов с использованием прибора Osstell Mentor (Германия).
При формировании ложа внутрикостных имплантатов производился забор костной ткани трепаном с последующей стандартной гистологической обработкой биоптатов и их морфометрическим исследованием.
Для целей представленного исследования использован модифицированный коэффициент эффективности предимплантологической аугментации [2]:
КЭПУЗА = % (НПУЗ + НА) + % НОИ/2, где
КЭПУЗА – интегральный коэффициент эффективности предимплантологического удаления зубов и аугментации;
НПУЗ – неосложненное предимплантологическое удаление зубов;
НА – неосложненная аугментация;
НОИ – неосложненная остеоинтеграция имплантатов.
Результаты исследований
Выявлено положительное клиническое значение ОПМ Gamalant™-паста-ФОРТЕ Плюс для перестройки
и сохранения объема АЛ удаленных нижних моляров с целью оптимизации условий отсроченной имплантации.
При сравнении процесса заживления АЛ под кровяным сгустком и ее заполнении Gamalant™-паста-ФОРТЕ Плюс установлено, что:
• развитие воспаления в месте удаления зуба отмечено у 5,8 % обследованных контрольной группы и у 3,8 % – основной (эти больные из дальнейшего наблюдения исключались);
• атрофия костной ткани альвеолярного гребня или частичное восстановление дефекта в области экстракции зуба, по данным КТ, через 6 месяцев составили 1,97 ± 0,34 мм в контрольной группе и выявились у 95,4 % обследованных, а в основной – 0,44 ± 0,20 мм и 21,6 % соответственно;
• КТ-структура костной ткани перед имплантацией соответствовала в контрольной группе крупноячеистой трабекулярной кости, в большинстве наблюдений не происходило заполнения АЛ костной тканью до вершины альвеолярного гребня, в ряде случаев была заметна граница регенерата и стенки АЛ; в основной группе ячеистость костной ткани была менее выражена, она выявлялась по всему объему альвеолярного дефекта практически без разграничения с окружающей костью, прослеживался ровный контур вершины альвеолярного гребня без снижения его уровня или с небольшой атрофией по гребню у 1/5 больных;
• плотность костной ткани в области удаленного зуба достигла 612,1 ± 44,3 ЕД по шкале Хаунсфилда в контрольной группе и 1210,7 ± 62,1 ЕД – в основной (рис. 1);
• возможность установки внутрикостного имплантата длиной 10 мм без дополнительного использования ОПМ имелась у 75,4 % больных контрольной группы и у 100 % – основной.
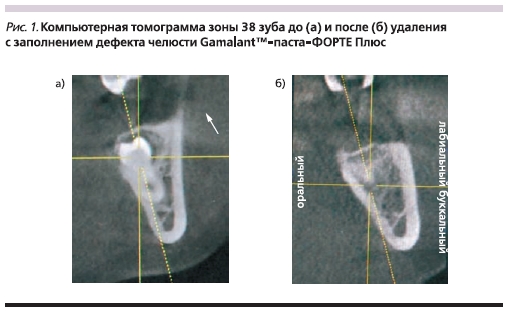
Таким образом, эффективность предимплантологической подготовки с учетом случаев развития воспаления в АЛ удаленного зуба составила 60,4 % в контрольной группе и 96,2 % в основной.
При установке имплантатов их стабильность, ЧРА, составляла 51,1 ± 7,3 ЕД в контрольной и 57,4 ± 8,3 ЕД в основной группах; после 3-месячного периода остеоинтеграции – соответственно 59,2 ± 4,5 и 62,3 ± 3,8 ЕД (все имплантаты были клинически неподвижны). Послеоперационный период протекал без воспалительных осложнений в обеих группах, однако в контрольной группе выявлено 4 (8,5 %)
случая резорбции костной ткани в пришеечной части имплантата (в среднем на 1,1 ± 0,5 мм). В целом клиническая эффективность имплантации составила в обеих группах 100 % (см. таблицу).
Таблица. Клинико-рентгенологические показатели процесса перестройки АЛ после удаления зуба,
костной аугментации и остеоинтеграции имплантатов.
В биопсийных образцах костной ткани при формировании ложа имплантатов через 6 месяцев после
удаления зуба в контрольной группе пациентов тонкие костные балки располагались хаотично, занимали половину объема регенерата, на их поверхности выявлялись остеобласты. Остальное пространство было заполнено фиброретикулярной стромой с включениями очагов кроветворения (рис. 2).
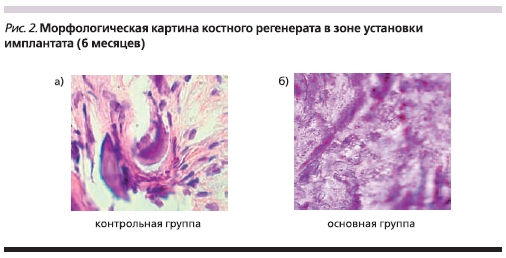
В основной группе выявлен более значительный объем зрелых костных балок с их кальцификацией
(до 70 % объема регенерата), между балками были сформированы костные перекладины; присутствовали остеоциты и единичные остеокласты. В костно-мозговых полостях, заполненных соединительной тканью, обнаруживались кровеносные сосуды.
Таким образом, в проведенном исследовании отмечен эффект стимуляции процесса остеорегенерации в присутствии ОПМ Gamalant™-паста-ФОРТЕ Плюс, проявившийся большей интенсивностью образования костных структур, дифференцировки костных клеток и межклеточного вещества.
Интегральный усовершенствованный показатель – коэффициент эффективности предимплантологического удаления зубов и аугментации (КЭПУЗА) – позволил дифференцированно и детально оценить эффективность применения ОПМ Gamalant™-паста-ФОРТЕ Плюс на разных этапах
предимплантологической подготовки и имплантации.
Показатель неосложненного предимплантологического удаления зуба и аугментации (НПУЗ + НА)
составил в контрольной и основной группах 7,2 и 75,5 % соответственно. Показатель неосложненной остеоинтеграции имплантатов (НОИ) составил в контрольной и основной группах 91,5 и 100 %.
В целом показатель КЭПУЗА в сравниваемых группах был равен 49,4 и 87,8 %, что подтверждает целесообразность спользования ОПМ Gamalant™-паста-ФОРТЕ Плюс в качестве остеопластического материала в хирургической стоматологии и имплантологии.


