Введение
Острый бронхит (ОБ) представляет собой острое диффузное воспаление трахеобронхиального дерева – преимущественно инфекционной этиологии, ведущим клиническим проявлением которого является кашель (продуктивный или непродуктивный), продолжающийся не более 3 недель [1–3].
В настоящее время ОБ является одной из наиболее частых причин обращения пациентов за медицинской помощью на амбулаторном этапе. Заболеваемость ОБ колеблется в широких пределах – от 20 до 40 % в зависимости от времени года и обследуемой популяции [4]. Эпидемиологические исследования, проведенные в США, выявили, что около 5 % жителей этой страны в возрасте старше 18 лет хотя бы один раз в течение календарного года перенесли ОБ. Из 30 млн пациентов, обратившихся за медицинской помощью с жалобами на кашель, 50 % был поставлен диагноз ОБ [5–7]. С учетом неполной регистрации заболеваемости ОБ, особенно его легких форм, что связано с предпочтением больных лечиться самостоятельно и не обращаться за медицинской помощью, истинные масштабы распространенности данной патологии у взрослых оценить крайне сложно. Тем не менее ОБ диагностируют более чем у 40 % амбулаторных пациентов с заболеваниями органов дыхания [8]. В России достоверных данных по эпидемиологии ОБ до настоящего времени не существует [6].
В ходе эпидемиологических исследований показано, что в 85–95 % случаев этиологическим агентом ОБ у взрослых являются респираторные вирусы. Спектр возбудителей представлен вирусами гриппа А и В, парагриппа, а также респираторно-синцитиальным вирусом и человеческим метапневмовирусом, реже – коронавирусами, аденовирусами и риновирусной инфекцией [9–11]. Существовавшая долгое время гипотеза о преобладании бактериальных возбудителей в этиологии ОБ, например Streptococcus pneumoniae, Staphylococcusaureus, Haemophilusinfluenzae, Moraxellacatarrhalis, и других пневмотропных агентов, не нашла подтверждения. В связи с этим обнаружение в мокроте пациентов с ОБ вышеуказанных бактериальных агентов рассматривается скорее как колонизация, а не острая инфекция. В настоящее время эти возбудители обусловливают возникновение ОБ у лиц с угнетенным иммунитетом, детей, больных, перенесших трахеотомию либо подвергшихся эндотрахеальной интубации [4]. Вне сезонных эпидемических вспышек вирусных респираторных инфекций ОБ может быть вызван такими возбудителями, как Bordetella pertussis и Вordetellaparapertussis, Mycoplasmapneumoniae, Chlamydophilapneumoniae. Однако, согласно многочисленным исследованиям, на их долю приходится не более 5 % всех случаев ОБ [12, 13].
Патологический процесс при ОБ связан с проникновением возбудителей (вирусов) в клетки слизистой оболочки, в которых происходит активная репликация вирусного генома, приводящая к деструкции эпителия нижних дыхательных путей, активации медиаторов воспаления и нарушению мукоцилиарной функции. В слизистой оболочке бронхов развиваются различные формы экссудативного воспаления с накоплением серозного, слизистого, гнойного или смешанного экссудата [7].
Поскольку причиной ОБ в большинстве случаев является вирусная инфекция, применение противовирусных и иммуномодулирующих лекарственных средств представляется целесообразным для лечения данного заболевания. Вышеописанные свойства сочетаются в препаратах интерферона альфа (ИФН-α), которые широко применяют для лечения многих заболеваний, прежде всего вирусной этиологии, в т. ч. в терапии острого обструктивного бронхита [14–16].
Одним из новых препаратов интерферонового ряда является Генферон®, который выпускается в виде суппозиториев для вагинального или ректального введения в различных дозировках и представляет собой комбинацию рекомбинантного человеческого ИФН-α, таурина и бензокаина.
Целью исследования явилось изучение эффективности и безопасности препарата Генферон® (БИОКАД, Россия) в лечении ОБ с целью расширения арсенала средств терапии данного заболевания.
Материал и методы
Для реализации поставленной цели проведено многоцентровое открытое проспективное рандомизированное сравнительное исследование с участием 150 пациентов, удовлетворяющих следующим условиям:
- возраст от 18 до 55 лет;
- диагноз – острый бронхит или острый трахеобронхит с суммарной оценкой по шкале оценки тяжести симптомов бронхита (Bronchitis Severity Score – BSS) не менее 6 баллов;
- продолжительность заболевания не более 48 часов;
- отсутствие локальных рентгенологических изменений;
- отсутствие местной и/или системной терапии иммуномодулирующими препаратами в течение одного предшествующего месяца.
В исследование не включали пациентов с установленной гиперчувствительностью к препаратам интерферона; иными заболеваниями нижнего отдела респираторного тракта, помимо ОБ; ВИЧ-инфекцией; необходимостью системного применения глюкокортикостероидов и/или цитостатиков; любыми острыми и хроническими заболеваниями, которые, по мнению исследователя, могли оказывать влияние на общее состояние больного в период исследования; беременных и кормящих грудью женщин.
Включенные в исследование пациенты были рандомизированы в три группы по 50 человек в каждой. Пациенты первой группы получали суппозитории Генферон® в дозе 1 млн МЕ ректально 2 раза в сутки (утром и на ночь) в течение 5 дней параллельно стандартной терапии. Больные второй группы получали суппозитории, содержащие препарат сравнения1, – ИФН-α в дозе 1 млн МЕ с витаминами С и Е, введенные ректально 2 раза/сут (утром и на ночь) в течение 5 дней на фоне стандартной терапии. Пациентам третьей группы проводилось только стандартное лечение, которое включало бромгексин в дозе 8 мг 3 раза в сутки, витамины, обильное щелочное питье, по показаниям – жаропонижающие, антигистаминные препараты, антибактериальные средства, щелочные ингаляции.
В процессе наблюдения производили физикальный осмотр больных на 1-е, 2-е, 4-е сутки и по завершении лечения на 6-й день с оценкой тяжести симптомов ОБ по шкале BSS. В 1-й и 6-й дни проводили общий анализ крови и рентгенографию грудной клетки в двух проекциях (на 6-й день рентгенографию проводили выборочно только при наличии показаний). На 15-й ± 2 дня от начала терапии лечащий врач устанавливал телефонный контакт с пациентом с целью оценки его состояния за период, прошедший с момента окончания приема исследуемого препарата.
Статистическую обработку полученных результатов проводили с помощью программы STATISTIСA 8.0 с использованием критерия Стьюдента при нормальном распределении значений и равной дисперсии признаков в каждой группе. При нарушении хотя бы одного из условий использовали непараметрические критерии Манна–Уитни и Вилкоксона, точный критерий Фишера. Если признак имел нормальное распределение данных, меры центральной тенденции и рассеяния представляли в формате Среднее (среднеквадратичное отклонение). Если признак имел распределение данных, отличное от нормального, меры центральной тенденции и рассеяния представляли как Медиана (интерквартильный размах).
Результаты
После рандомизации существенных различий в клинической картине заболевания, оценке тяжести симптомов ОБ по шкале BSS между исследуемыми группами пациентов не наблюдалось (табл. 1). Средний возраст участников в группе Генферона® составил 26 [18; 53] лет, в группе ИФН-α с витаминами С и Е – 25 [17; 55] и в группе стандартной терапии – 24 [18; 51] года. Длительность заболевания до момента включения в исследование составляла от 0 до 2 суток.
Таблица 1. Клиническая характеристика больных на скрининговом визите (1-й день лечения).
Анализ динамики регресса отдельных симптомов ОБ продемонстрировал нормализацию температуры тела на 7-й день лечения в группе пациентов, применявших Генферон®, а в группах стандартной терапии и препарата сравнения – на 8-й день. При сопоставлении сроков купирования лихорадки было установлено, что в группе Генферона® начиная со 2-го дня регресс лихорадочного синдрома происходил более интенсивно, чем в остальных двух группах. В первые 3 дня лечения лихорадка купировалась у 30,62 % пациентов группы Генферона®, у 28,99 % – группы препарата сравнения и у 17,78 % пациентов, применявших стандартную терапию (рис. 1).
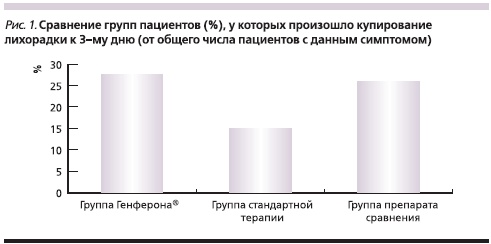
При сопоставлении данных о купировании хрипов по результатам аускультации было установлено, что в целом в группах применения препаратов интерферона данный симптом начинал купироваться раньше по сравнению с группой стандартной терапии (p > 0,05). Так, на 5-й день после начала лечения хрипы купировались практически у половины пациентов групп Генферона® и препарата сравнения и всего лишь у 10,0 % из группы стандартной терапии (р > 0,05).
Полное исчезновение кашля у 100 % пациентов в группах Генферона® и препарата сравнения наступило на 9-й день исследования, а в группе стандартной терапии – не достигалось в течение 10 дней, во время которых производился детальный анализ симптомов заболевания. В группах препарата Генферон® и препарата сравнения прослеживалась тенденция к более быстрому началу купирования кашля и более раннему его исчезновению (рис. 2). Так, на 7-й день в группе Генферона® кашель исчез у 84 % пациентов, группе препарата сравнения – у 74 %, а в группе стандартной терапии – всего у 64 % пациентов (р > 0,05).
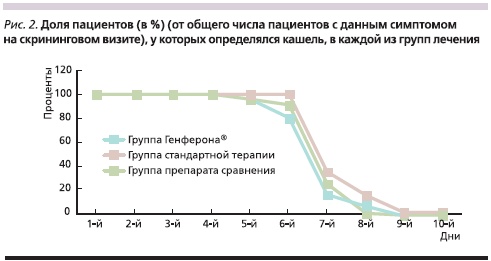
Полное исчезновение интоксикации у 100 % пациентов в группе Генферона® наступило на 7-й день, а в группах препарата сравнения и стандартной терапии – на 8-й день (рис. 3). В отношении купирования данного синдрома препарат Генферон® оказывал более выраженное действие по сравнению с двумя другими методами лечения. Так, в группе Генферона® к 5-му дню лечения интоксикация регрессировала у 70,8 % пациентов, в двух других группах аналогичный показатель составил 47,8 % (группа препарата сравнения) и 53,1 % (группа стандартной терапии; р > 0,05) (рис. 4).
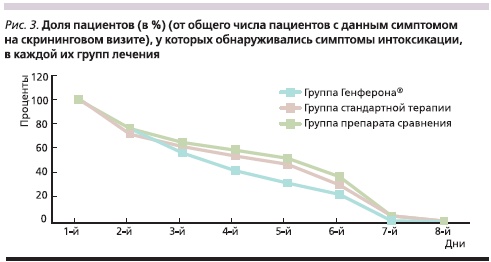
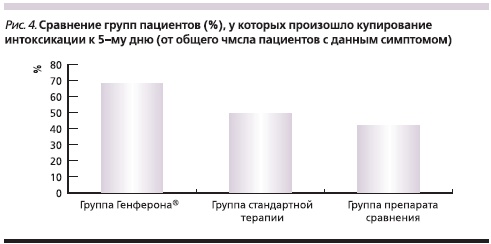
В группах пациентов, использовавших в лечении препараты интерферона, прекращение отхождения мокроты также наблюдалось в более ранние сроки по сравнению со стандартной терапией. Так, к 7-му дню после начала терапии купирование продуктивного кашля было отмечено у 92 % пациентов группы Генферона®, у 89,8 % пациентов группы препарата сравнения и всего лишь у 74 % пациентов группы стандартной терапии (р > 0,05).
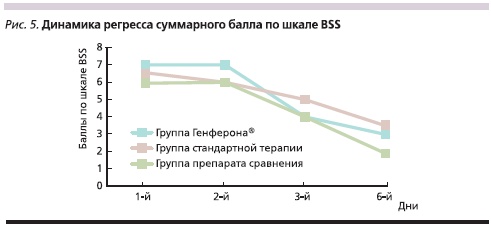
При анализе суммарного балла по шкале BSS у исследуемых пациентов на 1-й, 2-й, 4-й и 6-й дни было установлено, что в группе стандартной терапии к 6-му дню он был несколько выше (3,5 балла) и снижался более медленно, чем в двух остальных группах (3,0 – в группе Генферона® и 2,0 в группе препарата сравнения; рис. 5). Получение более низкого балла в группе препарата сравнения связано прежде всего с тем, что в 1-й день лечения суммарный балл в этой группе был на 1 ниже, чем в группе Генферона®.
Дополнительная терапия (кроме препаратов, выписанных врачом на первом визите) потребовалась 16 % больных группы Генферона® (половине из этих пациентов к схеме лечения были добавлены антибиотики). Аналогичные результаты были установлены и для группы препарата сравнения. Дополнительные лекарственные средства потребовались 30 % больных, лечившихся по стандартной схеме (у 40 % из этих пациентов в терапию были включены антибиотики).
Следует также отметить более выраженное снижение показателей воспаления от исходных значений по данным общего анализа крови (лейкоцитоз, сдвиг лейкоцитарной формулы влево, ускорение СОЭ) на 6-й день от начала лечения у пациентов, применявших интерферонотерапию, по сравнению с группой стандартного лечения.
Оценка эффективности проведенной терапии производилась лечащим врачом на основании определения продолжительности временной нетрудоспособности пациента, динамики регресса клинических проявлений ОБ, выраженной в виде оценки суммарного балла по шкале ВSS, а также отсутствия осложнений. При расчете медианы времени до купирования симптомов заболевания в группе стандартной терапии учитывали только 47 из 50 пациентов, поскольку на момент проведения данной оценки у 3 пациентов не произошло полного купирования всех симптомов. В группах препарата сравнения и Генферона® медиана временной нетрудоспособности была на 3 дня меньше, чем в группе стандартной терапии (р < 0,05; табл. 2). При анализе времени до купирования симптомов имелись аналогичные различия: при использовании препаратов ИФН-α данный показатель был на3 дня меньше, чем в группе стандартной терапии (р < 0,05).
Таблица 2. Медианы и интерквантильные диапазоны продолжительности временной нетрудоспособности и времени до купирования симптомов.
Во всех группах лечения осложнения ОБ отсутствовали. Анализ заключения об эффективности терапии на основании мнения исследователей показал, что стандартная терапия была эффективной всего в 54 % случаев, а лечение в группах препарата сравнения и Генферона® – в 100 % случаев (р < 0,05).
В период проведения исследования было зарегистрировано одно нежелательное явление на 2-й день лечения в виде гриппоподобного синдрома в группе ИФН-α в дозе 1 млн МЕ с витаминами С и Е, которое носило легкий характер и не потребовало медикаментозного вмешательства.
Обсуждение
С учетом преимущественно вирусной этиологии ОБ одним из приоритетных направлений в рациональной фармакотерапии этого заболевания в настоящее время является применение в комплексе со стандартной терапией лекарственных средств, способных сочетать неспецифическое противовирусное действие в отношении большинства вирусов и выраженную иммуномодулирующую активность. Одним из таких препаратов является Генферон®. Помимо противовирусного действия ИФН-α оказывает выраженное иммуномодулирующее действие, он активирует цитотоксические Т-лимфоциты, NK-клетки, моноциты/макрофаги, вследствие чего происходит лизис пораженных вирусом клеток, усиливает дифференцировку и пролиферацию В-лимфоцитов, а также продукцию ими антител. ИФН-α оказывает опосредованное антибактериальное действие, обусловленное повышением фагоцитарной активности и образования иммуноглобулинов [17]. Генферон® также содержит аминокислоту таурин, оказывающую мембраностабилизирующее, антиоксидантное, репаративное действие, что значительно ускоряет регенерацию поврежденных в результате патологического процесса тканей и повышает биологическую активность ИФН-α.
Результаты проведенного исследования продемонстрировали преимущества включения в стандартную терапию препаратов ИФН-α, что способствовало более динамичному регрессу лихорадочного, интоксикационного синдромов, более раннему купированию симптомов заболевания, снижению потребности в дополнительных лекарственных средствах и сокращению сроков временной нетрудоспособности пациентов. Терапевтическая эффективность Генферона® и ИФН-α в дозе 1 млн МЕ с витаминами С и Е в целом сопоставима, однако клинические данные свидетельствуют о более быстром купировании интоксикации при использовании препарата Генферон®.
Резюмируя вышесказанное, можно констатировать, что суппозиторная форма, имеющая в своем составе рекомбинантный человеческий ИФН-α, таурин и бензокаин, которая применяется у взрослых ректально в дозе 1 млн МЕ 2 раза в сутки в течение 5 дней, оказывает положительное влияние на течение ОБ, сокращая сроки заболевания и повышая эффективность проводимого лечения. Это может служить рекомендацией для включения препарата Генферон® в комплексную терапию данного заболевания.
Выводы
Использование Генферона® в качестве дополнительного средства стандартной терапии ОБ оказывает выраженное терапевтическое действие, которое заключается в более быстрой нормализации температуры тела, более быстром купировании симптомов заболевания, исчезновении симптомов интоксикации и сокращении продолжительности временной нетрудоспособности.
1 Суппозитории Виферон® в дозе 1 млн МЕ
Информация об авторах:
Зайцев Андрей Алексеевич – главный военный клинический госпиталь им. Н.Н. Бурденко, кафедрапульмонологии Государственного института усовершенствования врачей МО РФ.
E-mail: a-zaicev@yandex.ru
Алпенидзе Д.Н. – Санкт-Петербургское государственное учреждениездравоохранения “Городская поликлиника № 117”.
Салафет О.В. – ЗАО “Биокад”.
Синопальников Александр Игоревич – доктор медицинских наук, профессор, главный военныйклинический госпиталь им. Н.Н. Бурденко, начальник кафедры пульмонологии
Государственного института усовершенствования врачей МО РФ.
E-mail: aisyn@ya.ru, aisyn@list.ru


