Введение
Одним из достаточно часто встречающихся патологических состояний костно-мышечной системы в последние годы стал остеоартрит суставов кистей (ОАСК). По мнению медицинского международного сообщества, данная локализация заболевания одна из самых частых и занимает 2-е место по распространенности после остеоартрита (ОА) коленных суставов [1, 2]. Диагноз ОАСК, согласно классификационным критериям ACR (American College of Rheumatology), в дебюте основывается только на оценке клинических проявлений [3, 4]. Перед лечащим врачом нередко встают сложности лечения этих пациентов. Объясняется данная проблема формированием остеофитов (узелки Гебердена) и как следствие – появлением интенсивного болевого синдрома, сопутствующей длительной скованностью, приводящей к значительной потере трудовых и витальных навыков пациентом. Эта ситуация грозит больному инвалидизацией, утратой качества жизни.
Проблема настолько серьезна, что EULAR (European League Against Rheumatism) в 2018 г. разработала клинические рекомендации по лечению таких больных [4]. Одной из основных целей медикаментозной терапии, поставленной EULAR перед врачами, является уменьшение болевого синдрома на основании купирования воспаления. Согласно рекомендациям, оправданно применение парацетамола, локальное применение нестероидных противовоспалительных средств (НПВС) и симптом-модифицирующих препаратов замедленного действия (SYSADOA) на основе хондроитин сульфата. Эффективность препаратов хондроитин сульфата была доказана в ряде исследований, где показано улучшение клинических признаков заболевания и замедление его прогрессирования [5].
В последнее десятилетие стал популярным среди ревматологов препарат для парентерального введения – Алфлутоп [6], хондропротектор на основе компонентов биоактивного концентрата из четырех видов мелких морских рыб. Главной составляющей этого успешного средства является хондроитин сульфат [6, 7]. Его противовоспалительные и ходропротективные свойства привлекли внимание практикующих врачей [8]. Кроме того, Алфлутоп успешно подавляет местное воспаление в суставах кистей, гиперпродукцию провоспалительных цитокинов, таких как интерлейкин-1β (ИЛ1β), ИЛ-6 и ИЛ-8 и металлопротеиназ [9, 10].
Цель исследования: проанализировать противовоспалительное, обезболивающее действия препарата Алфлутоп, а также его безопасность и эффективность для пациентов с ОАСК с узелками Гебердена.
Методы
После предварительного подписания информированного согласия в ходе лечения наблюдали за 130 больными женщинами, страдающими узелковым ОАСК. Выбор пациентов по гендерному принципу обосновывался развитием заболевания преимущественно у женщин среднего и пожилого возраста [11]. Диагноз «ОАСК, стадия 2, с узелками Гебердена» установили в соответствии с Российскими клиническими рекомендациями (2017) и критериями ACR (1991). Рентгенологическую стадию ОА поставили по Келлгрену–Лоуренсу всем пациенткам, участвовавшим в исследовании. Применяли рутинные ультразвуковые, биохимические и лабораторные исследования в динамике лечения и наблюдения.
Были выделены 2 группы: группа 1 (основная), которую составили 66 женщин 66,2±3,4 года, пролеченных Алфлутопом по 2,0 мл через день, курс 10 инъекций. Группа 2 (контрольная), 64 женщины в возрасте 64,7±6,5 лет, получившие традиционное лечение НПВС в парентеральной форме и перорально препарат диацереин (производное антрахинолина, деацетилированное производное реина, обладает симптом-модифицирующим эффектом замедленного действия). Оценили пальпаторную боль по визуально-аналоговой шкале (ВАШ) в мм и длительность утренней скованности в минутах у пациенток обеих групп до лечения и на 20–21-й день лечения. Проанализировали безопасность Алфлутопа, оценив побочные эффекты. Для этого применили в динамике наблюдения физикальные методики (жалобы, пальпация живота, измерение артериального давления – АД) и дополнительные (ультразвуковые и эндоскопические, электрокардиография по показаниям) методы исследования. Статистическую обработку проводили с использованием программы Statistica, 10.0. Количественные показатели представлены в виде медианы, интерквартильного размаха (Ме; Q1, Q3) и среднего значения±SD.
Сравнение проводили с использованием критерия рангов Вилкоксона, для независимых групп – теста Манна–Уитни. Связь между показателями изучали с применением критерия Спирмена и линейного регрессионного анализа. Статистически достоверным считали различия при р<0,05.
Результаты
Оценка лабораторных и биохимических параметров под влиянием лечения Алфлутопом в основной группе и в группе сравнения, получавшей диацереин и НПВС, показала значимое улучшение в основной группе. Такие показатели, как СОЭ, С-реактивный белок (СРБ), лейкоциты, уже на 20–21-й день лечения уменьшились вдвое (р<0,05). Тогда как в группе сравнения снижение данных показателей было несущественно в те же сроки лечения, р>0,05 (табл. 1).
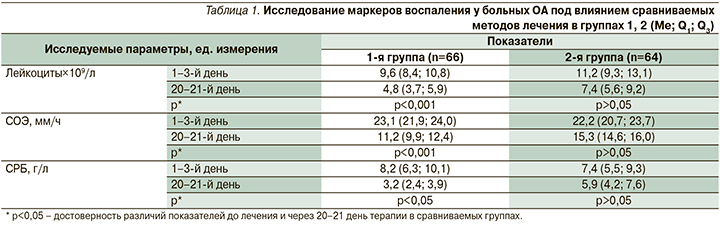
Сравнительный анализ параметра «боль при пальпации» по ВАШ в мм в группах 1, 2 был следующим: средний уровень боли при пальпации в наиболее пораженном суставе до лечения составил 62,5 (60,3; 64,7) и 64,1 (61,4; 66,7) мм соответственно. Уже на 20–21-й день лечения Алфлутопом в 1-й группе боль уменьшилась до 32,9 (30,1; 34,8) мм и эти изменения были достоверны (р<0,001), в контрольной группе боль снизилась до 49,8 (48,4; 51,2) мм, однако снижение боли было недостоверным (р>0,05) (табл. 2).
Длительность утренней скованности достоверно уменьшилась в динамике лечения у больных 1-й группы, получавших Алфлутоп. Так, до начала лечения длительность утренней скованности и в основной, и контрольной группах составила 43,2 и 38,5 минут (p>0,05), при этом на 20–21-й день у больных, получавших Алфлутоп, скованность уменьшилась до 21,2 (19,9; 22,5) минуты (p<0,01), тогда как во 2-й группе скованность значимо не изменилась – 32,5 (31,3; 35,0) (p<0,05) (табл. 3).
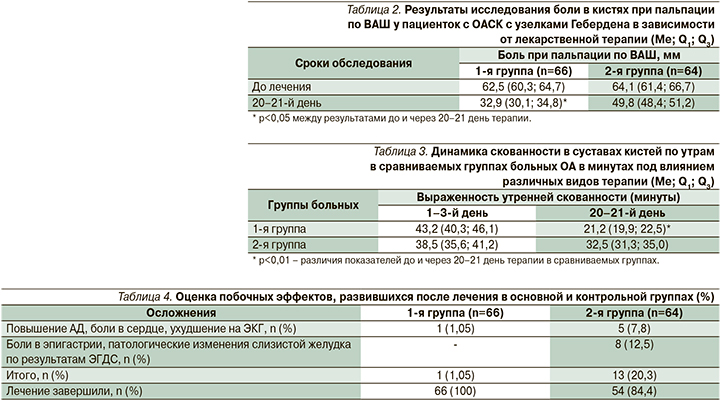
Анализ безопасности лечения пациентов, получавших в 1-й группе Алфлутоп, во 2-й группе сравнения диацереин и НПВС, путем оценки появления побочных эффектов показал следующую картину. До лечения больные обеих групп не предъявляли жалоб на головные боли, боли в сердце и в желудке. Уже на 12-й день лечения в группе сравнения у 7,8% больных появились головные боли, сопровождавшиеся эпизодическими подъемами АД. Тогда как в основной группе только один больной пожаловался на повышение АД, подтвержденное при динамическом измерении. На боли в желудке в процессе лечения обратили внимание 12,5% пациенток контрольной группы. Изменения в слизистой оболочке желудка (отек, единичные эрозии) были подтверждены результатами эзофагогастродуоденоскопии (ЭГДС). Жалоб со стороны органов пищеварения никто из пациентов основной группы не предъявил (табл. 4).
Заключение
Таким образом, результаты исследования убедительно показали, что безопасность и существенная эффективность лечения наблюдались в группе пациенток, пролеченных Алфлутопом. Все 66 (100%) пациенток закончили лечение, тогда как в группе сравнения только 22 (84,4%) пациентки из 54 завершили курс лечения из-за побочных эффектов. В группе, пролеченной Алфлутопом, у всех 66 пациенток отмечалось достоверное улучшение уже на 20–21-й день применения Алфлутопа, (р<0,05). Лечение пациентов только традиционной терапией (НПВС и диацериин) сопровождалось положительной динамикой суставного синдрома, но она была несущественной (р>0,05). Данный феномен мы объясняем тем, что препарат создан из биоактивных концентратов мелкой морской рыбы. Все вышеизложенное (безопасность и эффективность препарата) дает нам основание рекомендовать всем врачам, занимающимся лечением ОАСК, широко применять данное лечебное средство в рамках амбулаторного приема.



