Обоснование
Сахарный диабет (СД) – одна из наиболее серьезных проблем клиники внутренних болезней [1–4]. Его распространенность в мире за последние 10 лет увеличилась не менее чем на 30% [1, 2]. Полагают, что доля лиц с СД среди взрослых в общей популяции составляет около 9,5%. В 2020 г. в США эта цифра достигала 14% (у 30,7% из них диабет еще не был диагностирован), а в некоторых странах Южной Азии – даже 30% [2]. В Российской Федерации число лиц с установленным диагнозом СД составляет около 4,5 млн (3,1% населения). Считается, что примерно у такого же (если не более значительного) числа больных диабет остается недиагностированным, что влечет за собой значительные недостатки в лечебной помощи [1, 4]. Риск развития СД в течение предстоящей жизни (по подсчетам для новорожденных в США) может достигать 32,8% у лиц мужского и 38,5% женского пола [2]. СД – известный независимый и мощный фактор риска развития поражений органов-мишеней [1–4]. Это признанный лидер среди причин слепоты в развитых странах [2]. Диабет – ведущая причина развития терминальной стадии почечной недостаточности, требующей лечения с замещением функции почек; доля лиц с диабетической нефропатией (ДНП) в структуре диализных больных и реципиентов почечных трансплантатов составляет около 40% [2]. Среди больных СД риск развития инфаркта миокарда и инсульта в 2–4 раза [2, 5], а риск ампутаций нижних конечностей – в 20 раз выше, чем у лиц без диабета [2, 6]. Ожидаемая продолжительность жизни больных СД в развитых странах примерно на 10 лет меньше, чем в отсутствие диабета. СД – серьезная экономическая проблема. Подсчитано, что затраты системы здравоохранения на человека с СД примерно в 2,3 раза выше, чем на лицо такого же пола и возраста, но без диабета; в мировом масштабе ежегодные затраты на лечение таких больных составляют громадную цифру >1,3 трлн долл. США (около 1,8% глобального валового внутреннего продукта – ВВП) [2].
Основу лечения больных СД 1 и 2 типов (СД1 и СД2) составляет контроль уровней гликемии с применением современных сахароснижающих препаратов (ССП) [1–3]; широкое использование находят и изменения образа жизни, и назначение органопротекторных лечебных подходов (антигипертензивных препаратов, включая блокаторы ренин-ангиотензин-альдостеороновой системы, статины, антитромбоцитарные и др.) [1–3, 5]. Цель: настоящего сообщения рассмотрение принципов медикаментозного контроля гликемии у лиц с СД.
Для контроля гликемии отечественные и международные эксперты рекомендуют оценку уровней гликированного гемоглобина (HbA1с) не реже 2 раз в год, а если целевые уровни не достигнуты или лечение было изменено, то 4 раза в год [1, 2]. Для большинства взрослых лиц с СД1 и СД2 целевым считают уровень HbA1с<7%. Для части больных, которым без значимых эпизодов гипогликемии и побочных эффектов лечения возможно достижение HbA1с <6,5%, этот уровень может быть приемлемой целью. Менее жесткий целевой уровень HbA1с (<8,0%) предпочтителен для лиц с эпизодами тяжелой гипогликемии в анамнезе с относительно небольшой ожидаемой продолжительностью жизни, отчетливыми микро- и макрососудистыми осложнениями СД, тяжелыми сопутствующими заболеваниями, длительно протекающим СД, при невозможности достижения более низких величин HbA1с, несмотря на применение комбинаций ССП, включая инсулины.
Для контроля гликемии может быть использована методика ее ежедневного самоконтроля (домашний глюкометр, тест-полоски, ведение дневника). Целевые уровни гликемии (в капиллярной крови), измеренной натощак, обычно составляют 4,4–7,2 ммоль/л, пиковая гликемия после еды (т.е. через 1–2 часа после начала еды) должна быть <10,0 ммоль/л [1, 2].
В течение последних лет для лиц с СД предложены различные системы непрерывного мониторинга уровня глюкозы в крови, в т.ч. с оценкой амбулаторного гликемического профиля (уровень гликемии определяется многократно в течение 14 дней, выстраиваются соответствующие кривые и подсчитываются индексы, весьма ценные для выбора лечебной тактики). Этот метод пока недостаточно доступен, но весьма перспективен; однако других методов оценки гликемии, рассмотренных выше, он не заменяет [1, 2].
Медикаментозный контроль гликемии при СД1
Поскольку для СД1 характерно полное или частичное отсутствие функции β-клеток островкового аппарата поджелудочной железы, применение инсулина абсолютно необходимо в лечении этих больных [1, 2, 7, 8]. При СД1 наряду с гипергликемией имеется инсулинопения, оказывающая ряд самостоятельных неблагоприятных метаболических эффектов, включая развитие гипертриглицеридемии, кетоацидоза и нарушений тканевого катаболизма [1, 2, 7, 8]. Эти тяжелые метаболические нарушения при СД1 могут эффективно предотвращаться ежедневными инъекциями инсулина. Накоплены убедительные свидетельства того, что более интенсивная тактика инсулин-заместительной терапии (включая неоднократное его введение в течение суток либо постоянное подкожное – п/к применение с использованием технологии инсулинового насоса) позволяет дополнительно существенно улучшать прогноз (со снижением риска развития микрососудистых осложнений СД на 50% за 6 лет лечения) [2, 7, 8].
В настоящее время разработаны и внедрены в клиническую практику многочисленные варианты аналогов инсулина (ультракороткого и длительного действий, см. табл. 1), которые по фармакокинетике отличаются от ранее доминировавших рекомбинантных человеческих инсулинов (короткого и среднего по продолжительности действий) [2, 7, 8].
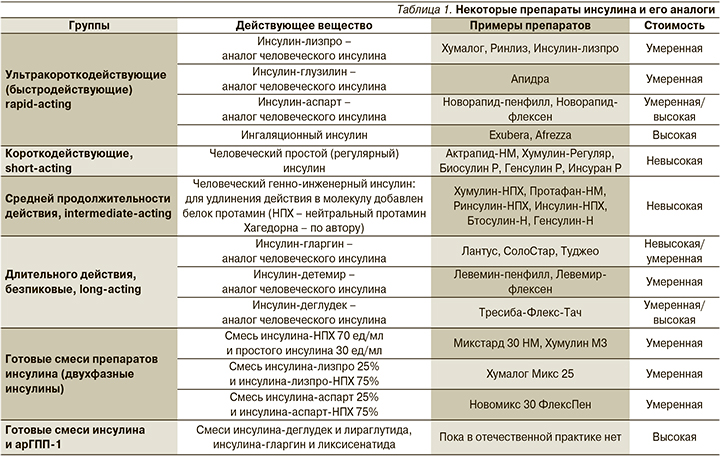
Ультракороткие формы имеют более быстрое начало действия и более короткую его продолжительность по сравнению с простым инсулином; препараты длительного действия (безпиковые, базальные) по сравнению с НПХ-инсулинами (НПХ – «нейтральный протамин Хагедорна») отличаются большей продолжительностью и плавностью эффекта. Показано, что при СД1 применение аналогов инсулина ассоциировано с меньшим риском развития гипогликемии и увеличения массы тела, а также с улучшением контроля HbA1с по сравнению с использованием человеческих инсулинов [2, 7, 8]. Многие из форм лекарственных препаратов, представленных в табл. 1, используются в виде заранее заполненных шприц-ручек, рассчитанных на многократное введение. Недавно было введено в клиническую практику несколько новых лекарственных форм как с ультракоротким (ингаляционный инсулин, инсулин-аспарт), так и с длительным действием (инсулин-гларгин U-300, инсулин-деглудек) [2, 7, 9]. Необходимо отметить, что широкое использование ряда высокотехнологичных современных форм инсулина и его аналогов ограничивает их достаточно высокая стоимость.
В последнее время в лечении лиц с СД1 используют новые способы доставки препаратов ультракороткого и короткого действий: инсулиновые насосы (для прерывистого болюсного или постоянного введения), оснащенные возможностями мониторного контроля гликемии [2, 7–9].
Примерную суточную потребность в препаратах инсулина можно рассчитать исходя из массы тела больного СД1. Эксперты American Diabetes Association (2021) указывают, что для метаболически стабильного больного СД1 стандартная начальная доза должна составлять 0,5 ЕД/кг/сут. [2]. Обычно она составляет от 0,4 до 1,0 ЕД/кг/сут. Более высокие дозы обычно требуются в периодах полового созревания, беременности, при наличии сопутствующих заболеваний (инфекции и др.). Половина этой дозы вводится перед приемом пищи в виде ультракоротких (за 15–20 минут) или короткодействующих (за 30 минут) препаратов (прандиальный инсулин, обеспечивающий контроль гликемии в период после еды). Вторая половина суточной дозы в виде препаратов среднего или длительного действия вводится вне приема пищи (базальный инсулин, применяется чаще на ночь, подбор дозы требует учета утреннего уровня гликемии натощак) [2].
Предпочтительное место введения препаратов инсулина – живот, ягодицы, возможно, бедро, плечо. Препараты вводятся подкожно (п/к), следует избегать внутримышечного введения (иной вариант фармакокинетики, опасность гипогликемии), лучший вариант – использование 4-миллиметровых игл в современных шприц-ручках. Необходима своевременная смена (ротация) мест введения, чтобы избежать липогипертрофии (накопления подкожного жира в ответ на адипогенное действие многократно вводимого в одно и то же место п/к инсулина). Важную роль играет обучение больного (и его родственников) методике выполнения инъекций [2, 8].
Место неинсулиновых ССП в контроле гликемии у лиц с СД1 пока недостаточно ясно. Также пока четко не установлены возможности использования у лиц с СД1 таких хирургических методов лечения, как трансплантация поджелудочной железы или ее островкового аппарата [2].
Медикаментозный контроль гликемии при СД2
Основу сахароснижающей терапии при СД2 составляют неинсулиновые препараты (преимущественно пероральные, см. табл. 2), обязательно используемые в сочетании с изменениями образа жизни; при необходимости к ним могут быть добавлены препараты инсулина или его аналоги [1–3, 10–13]. Выбор неинсулиновых ССП требует учета наличия сопутствующих ишемической болезни сердца, хронической сердечной недостаточности (ХСН) и ДНП, степени риска гипогликемии, влияния препаратов на массу тела, побочных эффектов и стоимости [1–3, 10–14].
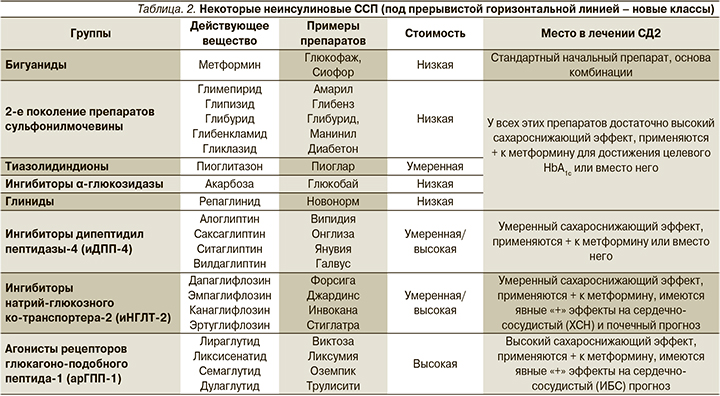
Во многих случаях начальным препаратом при СД2 является метформин [1–3, 10–13, 15]. Он может применяться в качестве монотерапии в добавление к изменениям образа жизни. Препарат доступен в виде лекарственных форм с немедленным и пролонгированным высвобождением. Максимальная суточная доза – 2,000–2,500 мг. Метформин отличается высокой сахароснижающей эффективностью, не влияет на массу тела, не повышает риска развития гипогликемии [1–3, 10, 11, 15]. Препарат противопоказан при скорости клубочковой фильтрации (СКФ) <30 мл/мин и пациентам с декомпенсацией ХСН [1–3, 10, 11, 15, 16]. Побочные эффекты (диарея, тошнота) достаточно часты и могут требовать снижения дозы или перевода на лекарственные формы с пролонгированным высвобождением. При непереносимости метформина или противопоказаниях к его применению в качестве начальной терапии могут быть использованы и другие препараты [1–3, 10, 11].
Так как СД2 у многих больных является прогрессирующим заболеванием, поддержание гликемических целей с помощью монотерапии часто возможно лишь в течение первых нескольких лет, после чего становится необходимым использование комбинаций ССП [1–3, 10, 11, 15]. Если исходный уровень HbA1с выше целевого на ≥1,5%, то обычно сразу же следует выбирать комбинированную сахароснижающую терапию. При уровне гликемии ≥16,7 ммоль/л или HbA1с >10,0%, а также в отношении лиц с полиурией, полидипсией и снижением массы тела начинать лечение следует с назначения препаратов инсулина, а после устранения этих глюкотоксических проявлений возможен перевод на прием неинсулиновых препаратов [1–3, 10, 11, 15].
Если через 3 месяца лечения метформином целевой уровень HbA1с не достигнут, к нему следует добавить любой из считающихся сейчас предпочтительными 6 классов препаратов: 1) сульфонилмочевины; 2) тиазолидиндионы; 3) иДПП-4; 4) иНГЛТ-2; 5) арГПП-1; 6) базальные препараты инсулина среднего или длительного действия [1–3, 10, 11, 15] – сокращения см. табл. 2. Перечисленные классы ССП достаточно хорошо комбинируются друг с другом, но не следует сочетать ИДПП-4 с арГПП-1. Каждый новый класс неинсулиновых препаратов, добавляемый к метформину, позволяет дополнительно снижать уровни HbA1с на 0,7–1,0% [2].
Лицам с наличием атеросклеротических сердечно-сосудистых заболеваний (инфаркт миокарда в анамнезе, стабильная стенокардия, перенесенные процедуры коронарной реваскуляризации, инсульты, транзиторные ишемические атаки, поражения периферических артерий предположительно атеросклеротической природы), с факторами их риска (возраст ≥50 лет, гипертрофия ЛЖ, коронарные, каротидные или периферические артериальные стенозы), а также лицам с ДНП и ХСН метформин предпочтительно комбинировать с иНГЛТ-2 или арГПП-1 [1–3, 11, 12, 14, 16]. При этом если доминируют сердечно-сосудистые заболевания или факторы риска их развития, препаратом выбора являются арГПП-1, а если ДНП или ХСН – иНГЛТ-2 [2, 3, 11, 16]. иНГЛТ-2 не применяют при СКФ<30 мл/мин [2, 3, 11, 16]. К лечению можно добавлять и другие классы ССП.
Если у больного нет сердечно-сосудистых заболеваний, факторов риска их развития, нет ДНП и ХСН, для усиления контроля гликемии к метформину следует добавлять иДПП-4 или иНГЛТ-2, или арГПП-1, или тиазолидиндионы (все эти средства характеризуются относительно невысоким потенциалом развития гипогликемии), затем можно использовать их комбинации [2, 3, 11, 16]. В качестве последнего добавляемого класса используются базальные препараты инсулина (предпочтительно выбирать менее ассоциированные с развитием гипогликемии – инсулин-деглудек или гларгин U-300, несколько выше этот риск для гларгина U-100 и инсулина-детемир, еще выше – для инсулина НПХ, см. табл. 1) [2, 3, 11, 17, 18]. С целью снижения массы тела метформин следует комбинировать с иНГЛТ-2 или арГПП-1 [2, 3, 11]. Если же наиболее важным фактором при выборе препаратов является их стоимость, к метформину добавляются препараты сульфонилмочевины или тиазолидиндионы, которые впоследствии при необходимости можно комбинировать между собой, а затем добавлять к ним недорогой базальный инсулин НПХ [2, 3, 11].
Многим больным на определенном этапе развития СД2 становится необходим инсулин. Лечащему врачу важно представить препараты инсулина больному как важные помощники пероральных средств в поддержании целевых уровней гликемии; вовлечь его в сотрудничество по самоконтролю (глюкометр, дневник), выполнению диетического режима, выявлению и предупреждению гипогликемии. Ни в коем случае не использовать назначение инсулина как угрозу, неудачу лечения, как наказание. Лица с СД2 по сравнению с больными СД1 обычно более резистентны к применению инсулина (что зачастую требует применения более высоких суммарных суточных доз, до ≈1 ЕД/кг), но имеют и меньшую частоту развития гипогликемии [2, 3, 11, 17, 18].
Удобным начальным подходом служит применение прандиального (быстродействующего) инсулина, добавляемого к метформину и иным пероральным препаратам в стартовых дозах 0,1–0,2 ЕД/кг/сут. (с учетом уровней гипергликемии), с подбором дозы в течение нескольких дней/недель [2, 3, 11, 17, 18]. Распространенным вариантом начала прандиального инсулина является доза 4 ЕД перед наибольшим приемом пищи.
Также обычно требуется применение базального инсулина [2, 3, 11, 17, 18]. Основным его эффектом служит уменьшение образования глюкозы в печени, снижение гликемии ночью и между приемами пищи. Этого может достигать применением человеческих инсулинов НПХ или длительно действующих аналогов инсулина. Титрование препаратов инсулина проводят на основании данных домашнего мониторинга гликемии или результатов оценки HbA1с [2, 3, 11].
Особенности тактики у больных СД в период пандемии COVID-19
Высокая распространенность СД в популяции делает диабет частым сопутствующим заболеванием среди лиц с COVID-19. Наличие СД увеличивает восприимчивость к респираторным вирусным инфекциям, включая и COVID-19. Больные СД обоих типов имеют высокий риск тяжелого течения инфекции COVID-19 и развития ее осложнений [2, 19–24].
Хроническая гипергликемия неблагоприятно влияет на иммунный ответ (вызывает дисфункцию фагоцитов, нарушает хемотаксис нейтрофилов, угнетает клеточные иммунные реакции), увеличивая риск развития любой (в т.ч. любой вирусной) инфекции и смертность от нее. В период пандемии COVID-19 смертность от этой инфекции больных СД примерно в 3 раза выше, чем у лиц без диабета; среди умерших от коронавирусной инфекции более 40% приходится на долю больных СД [19–24]. Способность вируса SARS-CoV-2 вызывать поражения эндотелия сосудов, миокарда и почек может дополнительно усиливать тяжесть состояния лиц с СД, уже имеющих сердечно-сосудистые и почечные осложнения [25–28].
Рекомендуемые профилактические меры для лиц с СД в период пандемии включают строжайший контроль гликемии и артериального давления, а также стандартные меры профилактики (социальное дистанцирование с максимальным исключением пребывания в местах скопления людей, включая общественные и семейные мероприятия, меры респираторной гигиены, при необходимости – самоизоляцию). Необходимо свести к минимуму личные визиты к врачу, шире использовать возможности дистанционных консультаций (телефон, скайп, электронная почта и др.) [23, 24, 27–30].
Больным СД необходимо рекомендовать иметь дома адекватный запас лекарственных препаратов и расходных материалов для самоконтроля гликемии на случай домашней самоизоляции. Также необходимо обеспечить лиц с СД согласованным с лечащим врачом планом действий на случай появления у них симптомов возможной инфекции COVID-19 (включая субфебрилитет, одышку, кашель, слабость, утрату обоняния и др.).
У лиц с СД и COVID-19 нередко наблюдается ухудшение контроля гликемии, что ассоциировано с неблагоприятным течением инфекции [19–24, 30, 31]. По сравнению с лицами с СД, имеющими нормогликемию, пациенты с гипергликемией чаще имеют лимфопению и лейкоцитоз, у них выше уровни С-реактивного белка, прокальцитонина, интерлейкина-6, D-димера, аминотрансфераз; обычно выше темп прогрессирования пневмонии, по данным компьютерной томографии органов грудной клетки, чаще развиваются респираторный дистресс-синдром, острое повреждение почек, септический шок, диссеминированное внутрисосудистое свертывание [19–24].
Инфекция COVID-19 способна оказывать прямой повреждающий эффект на β-клетки поджелудочной железы, что у лиц с СД1 может увеличивать потребность в препаратах инсулина [2, 24, 30–35]. Лицам с СД, имеющим COVID-19, желательно контролировать уровни гликемии не реже 2 раз в сутки. При COVID-19 у лиц с СД, особенно СД1, увеличивается частота кетоацидоза и гиперосмолярных гипергликемических состояний, что требует контроля уровней кетонов крови у всех пациентов с гипергликемией [2, 24, 30–32].
Часть лиц, имеющих инфекцию COVID-19, могут получать гидроксихлорохин. У некоторых больных этот препарат способен снижать уровни гликемии, что изменяет потребность в ССП (так, потребность в инсулине может уменьшаться на 30–35%) [36]. Усиливать гипергликемию могут используемые в лечении некоторых больных COVID-19 противовирусные препараты, такие как лопинавир-ритонавир [37].
Лицам с СД в период пандемии COVID-19 не следует отменять ингибиторы ангиотензинпревращающего фермента или сартаны, которые они принимали ранее. Показано, что препараты этих групп не повышают вероятность развития осложнений COVID-19 [2, 29–31, 34]. Больным СД при нетяжелом течении инфекции (в амбулаторных условиях) можно продолжать применение всех основных классов ССП. По данным ряда сообщений, метформин может оказывать благоприятное влияние на прогноз у лиц с сочетанием СД2 и COVID-19, однако механизм этого эффекта остается неясным [2, 30, 31, 38]. Также высказываются предположения о возможном позитивном действии иДПП-4 на течение инфекции COVID-19, однако эти данные требуют подтверждения [39].
Госпитализированным больным СД с более тяжелым течением инфекции COVID-19 может требоваться замена по крайней мере части из неинсулиновых ССП на препараты инсулина [2, 24, 29, 30]:
- метформина – при нарушении функции почек, декомпенсации ХСН, рвоте, диарее (из-за повышения риска лактоацидоза);
- препаратов сульфонилмочевины и глинидов – могут увеличивать риск гипогликемии, особенно при нарушениях питания;
- арГПП-1 – могут увеличивать тошноту, рвоту, диарею;
- иНГЛТ-2 – повышают риск гипотонии, эугликемического кетоацидоза, особенно у лиц с риском дегидратации.
Суточные дозы инсулина для госпитализированных лиц могут составлять:
- 0,3 ЕД/кг – для лиц с острым повреждением почек, хронической болезнью почек при СКФ<30 мл/мин, при выраженном снижении функции печени, у истощенных и для пожилых пациентов;
- 0,4 ЕД/кг – для лиц с СД1, ранее не получавших инсулина больных СД2 при индексе массы тела (ИМТ)<30 кг/м2;
- 0,5 ЕД/кг – для ранее не получавших инсулина больных СД2 при ИМТ≥30 кг/м2;
- 0,6 ЕД/кг – для лиц с СД2, получавших глюкокортикоиды.
В случае если к лечению больного, который уже получает препараты инсулина, добавляются глюкокортикоиды, стандартным шагом будет увеличение суточной дозы инсулина на 20% по сравнению с исходной (для преднизолона или гидрокортизона) или на 10% (для дексаметазона), причем это увеличение в равной степени касается как базального, так и прандиального инсулина [2, 24, 29, 30]. Потребность в инсулине больных такого рода необходимо переоценивать ежедневно.
Заключение
В завершение обсуждения отметим, что в распоряжении врача сейчас имеется богатый арсенал ССП. Выбор лечебной тактики должен основываться на современных отечественных и международных рекомендациях.


