Введение
Мигрень – это хроническое неврологическое заболевание. Оно входит в тройку самых распространенных в мире и является самым часто встречаемым неврологическим заболеванием [1]. Распространенность мигрени в мире затрагивает около 15% населения, в России – более 20% [2]. Помимо высокой распространенности мигрень оказывает значительное снижение качества жизни пациентов: по показателю YLD (Years Lived with Disability, число лет, прожитых с нетрудоспособностью) мигрень находится на седьмом месте в мире среди всех известных заболеваний [3]. Сочетание высокой распространенности и значительного снижения качества жизни приводит к значительным экономическим затратам – более 111 млрд евро ежегодно в Европейском Союзе [4] и около 23 млрд долл. США в России [5]. Сочетание этих фактов делает поиск эффективных и безопасных методов лечения крайне актуальной проблемой.
Основные подходы к лечению мигрени: изменение образа жизни, лечение (купирование) приступа мигрени и профилактическое лечение (предотвращение возникновения приступов). Для купирования приступов в настоящее время применяются нестероидные противовоспалительные средства, триптаны, эрготаминсодержащие средства, противорвотные препараты [6, 7], некоторые методы нейростимуляции. Основу профилактического лечения мигрени до недавнего времени составляли β-адреноблокаторы, антидепрессанты, противосудорожные, ингибиторы ангиотензинпревращающего фермента, блокаторы рецептора АТ2, ботулинический токсин типа А [8]. Как видно из этого списка, большинство препаратов для лечения мигрени неспецифические и не были разработаны непосредственно для ее лечения. Эта ситуация связана в первую очередь с тем, что патогенез мигрени до конца не изучен [9]. Однако в последнее время произошел значительный прогресс в понимании этого вопроса, что привело к появлению совершенно новых групп препаратов для лечения мигрени.
Нейробиология мигрени
Патофизиология мигрени представляет весьма сложное сочетание изменения активности различных зон головного мозга (коры, гипоталамуса, моста), изменений концентрации нейромедиаторов, а также генетической предрасположенности [9]. За последние 50 лет произошел сдвиг от «сосудистой теории» мигрени [10], предложенной еще в 1940-х гг., к пониманию мигрени как неврологического заболевания. В 1979 г. М. Московиц впервые показал анатомическую связь между волокнами тройничного нерва и сосудами твердой мозговой оболочки и предложил тригемино-васкулярную (или нейроваскулярную) теорию мигрени [11]. В 1985 г. Л. Эдвинссон определил, что одну из ключевых ролей в работе этой системы играет CGRP (calcitonin-gene related peptide, кальцитонин-ген родственный пептид) [12]. Этот пептид представляет собой молекулу из 37 аминокислот и образуется в результате альтернативного сплайсинга гена, кодирующего кальцитонин, содержится в центральной и периферической нервных системах, а также является мощным вазодилататором [13]. В дальнейшем в серии экспериментов Л. Эдвинссон и П. Годсби показали, что концентрация белка CGRP в крови повышается при стимуляции ганглия тройничного нерва у кошек и человека [14], при стимуляции верхнего сагиттального синуса у кошек по сравнению с уровнем до стимуляции [15]. Эти данные показывают, что CGRP играет одну из ключевых ролей в тригемино-васкулярной системе, выделяясь при стимуляции как ее «невральной», так и «сосудистой» части. Кроме того, П. Годсби и Л. Эдвинссон продемонстрировали, что у пациентов с мигренью уровень CGRP в крови, взятой из яремной вены, значительно выше в момент приступа мигрени по сравнению с концентрацией в межприступный период [16]. Ряд последующих работ показал влияние суматриптана на падение концентрации CGRP одновременно с регрессом приступа мигрени [17] и то, что введение CGRP провоцирует типичный для пациентов приступ мигрени [18]. CGRP достаточно широко распространен в центральной и периферической нервных системах (менингеальная оболочка, ганглий тройничного нерва, ядро спинномозгового пути тройничного нерва, мост, гипоталамус, мозжечок) [19]. Л. Эдвинссон показал, что в ганглии тройничного нерва находятся небольшие нейроны, которые содержат преимущественно CGRP, и более крупные нейроны, содержащие рецептор к CGRP. Подобная ситуация сохраняется и в области твердой мозговой оболочки, где рецептор и лиганд находятся в различных волокнах тройничного нерва [20]. Эти данные позволяют предполагать, что в CGRP-опосредованном пути развития приступа мигрени ключевые события происходят именно в этих зонах тригемино-васкулярной системы.
Антагонисты CGRP-рецепторов («джепанты»)
Эти и ряд других данных привели к пониманию того, что воздействие на путь CGRP может быть использовано для терапии мигрени. В начале 2000-х гг. появился новый класс препаратов – антагонисты CGRP-рецепторов, или «джепанты». Первым из этой группы препаратов был олцеджепант. Датский невролог J. Olesen показал его преимущество над плацебо для купирования приступа мигрени по показателю устранения головной боли через 2 часа [21]. Олцеджепант был разработан для внутривенного введения как подтверждение концепции эффективности джепантов и не предполагался к клиническому применению. Второй препарат этой группы, телкаджепант, был разработан для перорального приема и также был эффективнее, чем плацебо, для купирования приступов мигрени [22]. К сожалению, в исследованиях телкаджепанта для профилактики мигрени была выявлена гепатотоксичность [23] и все исследования этого препарата и других джепантов были на некоторое время прекращены. Но через некоторое время стало ясно, что этот побочный эффект не стал класс-специфичным, а присущ только одному телкаджепанту, и исследования других молекул были продолжены. В настоящее время успешно закончились клинические исследования уброджепанта и римеджепанта для купирования приступа мигрени. Препараты были эффективнее плацебо как по показателю устранения боли через два часа, так и по устранению сопутствующих симптомов (тошноты, фоно/фотофобии). Побочных эффектов, связанных с повреждением печени, в исследованиях выявлено не было [24–26]. Также успешно закончилась 2b/3 фаза клинического исследования атоджепанта для профилактики мигрени [27]. Поскольку CGRP является мощным вазодилататором, особое внимание было уделено кардиоваскулярной безопасности. Ни в одном из исследований джепантов не было получено побочных эффектов, связанных с сердечно-сосудистой системой [24–27].
Моноклональные антитела к рецептору CGRP/белку CGRP
Помимо обычных препаратов («маленьких молекул») для влияния на путь CGRP были разработаны моноклональные антитела к рецептору CGRP и самому белку CGRP. Моноклональные антитела (МАТ) являются таргетной терапией и имеют ряд особенностей: большой период полувыведения, отсутствие метаболизма в печени, большой размер молекулы [28]. Их характеристики делают эти препараты максимально подходящими для профилактической терапии мигрени: редкий режим дозирования (1 раз в месяц или 1 раз в три месяца), сниженный риск межлекарственного взаимодействия, отсутствие проникновения через неповрежденный гематоэнцефалический барьер в существенных количествах [29]. В настоящее время разработано одно МАТ, блокирующее рецептор CGRP, – эренумаб, и три МАТ, блокирующих сам белок CGRP, – фреманезумаб, галканезумаб и эптинезумаб. Сводная характеристика этих молекул представлена в табл. 1 [30].
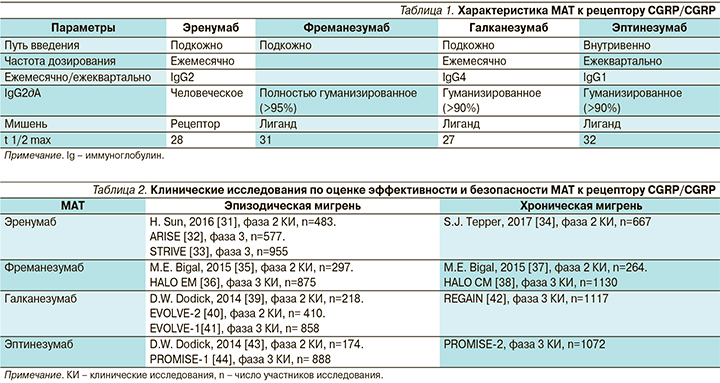
Все исследования фаз 2 и 3 всех четырех препаратов были положительными как при эпизодической, так и при хронической мигрени, и 3 из них (эренумаб, фреманезумаб и галканезумаб) уже доступны для клинического применения в ряде стран. Клинические исследования по оценке эффективности и безопасности МАТ к рецептору CGRP/CGRP суммированы в табл. 2.
Среди побочных эффектов, отмеченных в ходе клинических исследований, наиболее частыми были боль в месте инъекции и инфекции верхних дыхательных путей. Число этих побочных эффектов не различалось между группами активного препарата и группой плацебо ни в одном из опубликованных исследований МАТ к рецептору CGRP/CGRP. Число серьезных побочных эффектов не различалось между группами активного препарата и плацебо. Также незначительным было число анти-МАТ-антител и нейтрализующих антител, при этом наличие нейтрализующих антител не приводило к изменению эффективности или возникновению побочных эффектов [45].
Помимо исследований 2-й и 3-й фаз, показавших эффективность МАТ при эпизодической и хронической мигрени, были опубликованы результаты долгосрочных исследований безопасности и эффективности применения эренумаба в течение 3 лет [46] и фременезумаба в течение 12 месяцев [47]. В исследованиях было показано, что эффект препаратов сохраняется и даже имеет тенденцию к усилению на протяжении времени, а также не было выявлено дополнительных проблем с безопасностью.
Важным фактором для профилактической терапии мигрени является скорость наступления эффекта при назначении МАТ. В исследовании эренумаба и фреманезумаба различия между группами активного препарата и плацебо по числу дней с мигренью отмечались уже после первой недели после инъекции [48, 49]. В исследованиях эптинезумаба эффект проявлялся уже в первый день после введения препарата [50].
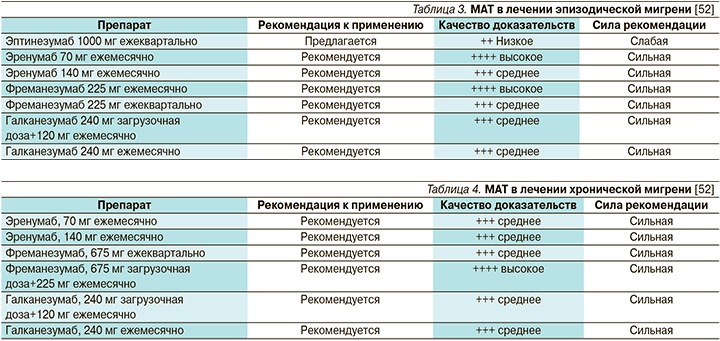
В 2019 г. Европейская федерация головной боли опубликовала клинические рекомендации по применению МАТ в лечении мигрени [52] (табл. 3, 4).
Заключение
Накопление научных данных о природе мигрени в последние 30 лет, в частности об участии CGRP в развитии приступа, позволило совершить качественный скачок в лечении этого заболевания: были разработаны и внедрены в клиническую практику новые препараты для профилактики мигрени – моноклональные антитела к рецептору CGRP/CGRP, успешно завершены клинические исследования антагонистов CGRP-рецепторов (джепантов). Но это лишь начало большого пути разработки новых классов специфических противомигренозных препаратов. В настоящее время успешно завершены или продолжаются исследования дитанов (агонистов 5HT-1F-рецепторов) для купирования приступа мигрени, а также моноклональных антител, влияющих на путь PACAP (Pituitary adenylatecyclase-activating peptide; пептид, активирующий аденилатциклазу гипофиза). Появляются новые методы неинвазивной нейромодуляции (стимуляция блуждающего нерва, тройничного нерва, транскраниальная магнитная стимуляция). Кроме этого выявляются новые мишени для терапии мигрени – орексины А и В и их рецепторы, АТФ-чувствительные калиевые и HCN-каналы [53].



