Введение
Эректильная дисфункция (ЭД) определяется как неспособность достигать и/или поддерживать эрекцию, достаточную для сексуальной активности. По разным оценкам, распространенность ЭД составляет от 16,2–20,7 до 31% [4, 5], при этом риск ее развития увеличивается с возрастом: чем старше пациент, тем больше шансов выявить у него тяжелую степень нарушений из-за наличия хронических васкулогенных и нейрогенных нарушений, а также возрастных гормональных, психогенных или смешанных причин, в т.ч. индуцированных постоянным приемом лекарственных средств [6]. ЭД негативно влияет на качество жизни, самооценку, взаимоотношения с сексуальным партнером [7, 8], может сопровождаться депрессией, хроническим стрессом, синдромом эмоционального выгорания [9].
Пациенты с ЭД часто требуют назначения терапии ингибиторами фосфодиэстеразы-5 типа (ФДЭ-5) на протяжении длительного времени. Учитывая полиэтиологичную природу ЭД, наличие психосоматического компонента и ряда других аспектов, появление новых препаратов для ее лечения заслуживает особого внимания. Необходимость запивать таблетку водой, проблемы, обусловленные продолжительностью действия и профилем безопасности препаратов, определяют поиск не только новых лекарственных средств для лечения ЭД, но и лекарственных форм, позволяющих маскировать эффект приема препарата, тем самым повышая качество жизни пациентов. На сегодняшний день ингибиторы ФДЭ-5 производятся в виде оральных диспергируемых таблеток, пленок, диспергируемых в полости рта, назальных спреев, дезодорантов и в некоторых других формах. Предполагается, что чем меньше качество интимной жизни пациента зависит от факта приема таблетки, тем выше возможный комплаенс пациента назначенной терапии и, соответственно, результат лечения.
С момента появления на российском рынке препаратов силденафила, т.е. в течение почти 20 лет, накоплен достаточный опыт его использования пациентами с ЭД. Препарат оказывает известный, прогнозируемый и управляемый клинический эффект, а также ряд хорошо изученных побочных эффектов. Клиническая эффективность и безопасность силденафила подтверждены значительным количеством многоцентровых контролируемых клинических исследований [10, 11], причем его эффективность показана в различных возрастных популяциях [12], а также на фоне лечения хронических заболеваний, провоцирующих развитие ЭД, например сахарного диабета [13].
Использование лекарственной формы в виде пленок заслуживает отдельного внимания, т.к. препарат растворяется в полости рта и представляет собой свободное основание силденафила, которое не имеет горького вкуса в отличие от его цитрата – действующего вещества таблетированных форм [14]. В более ранних исследованиях была показана биоэквивалентность препаратов силденафила в виде пленок таблетированной форме. Результаты этих исследований показали их сходную биодоступность [1, 2]. Поскольку фармакодинамическая кривая у таблетированной и оральной диспергируемой форм практически не отличаются, можно предположить, что количество транзитных потерь практически будет у них идентичным, причем для пленок не требуется дополнительного использования жидкости для попадания лекарственного препарата в организм.
Таким образом, Динамико Форвард (силденафил в виде пленок, диспергируемых в полости рта) является альтернативным препаратом по отношению к таблетированным формам силденафила. Динамико Форвард (Тева) зарегистрирован в ряде стран, в т.ч. и в Российской Федерации (РФ), для лечения ЭД, при этом данных в отношении его сравнительной с таблетированными препаратами терапевтической эффективности в российской популяции до настоящего момента получено не было, что и послужило причиной проведения нашего исследования.
Целью данного открытого многоцентрового рандомизированного исследования стала оценка эффективности и безопасности препарата Динамико Форвард в виде пленок, диспергируемых в полости рта, по сравнению с препаратами Виагра и Динамико в виде таблеток, покрытых пленочной оболочкой, при лечении пациентов с ЭД.
В качестве первичных конечных точек проведена оценка доли пациентов, у которых к концу лечения (12-я неделя) показатель индекса МИЭФ в первом домене составил ≥26 баллов или было отмечено увеличение этого показателя по сравнению с аналогичным показателем на визите скрининга на ≥50%.
Материал и методы
Дизайн исследования
В исследование были включены 120 амбулаторных пациентов мужского пола с ЭД в возрасте от 20 до 70 лет, из которых 114 завершили исследование в соответствии с протоколом. Пациенты были рандомизированы в 3 группы по 40 человек. Пациенты первой группы получали Динамико Форвард (силденафил, пленки, диспергируемые в полости рта, 100 мг, Тева), второй – Виагру (силденафил, таблетки, покрытые пленочной оболочкой, 100 мг, Пфайзер), третьей – Динамико (силденафил, таблетки, покрытые пленочной оболочкой, 100 мг, Тева) в режиме по требованию, 1 раз в сутки, рекомендуемая частота приема – 2–3 раза в неделю на протяжении 12 недель с последующим динамическим наблюдением за остаточными явлениями после приема препаратов в течение 2 недель. Пациентам 1-й группы было рекомендовано помещение препарата на язык до полного растворения с последующим проглатыванием, у пациентов остальных групп таблетированные препараты принимались стандартно. Исследование проведено в 6 клинических центрах РФ.
Для оценки клинической эффективности препаратов использовалось физикальное обследование, осмотр уролога; собирался сексуальный анамнез (в виде заполнения Опросника о качестве сексуальной жизни [ОКСЖ-М] и анкеты МИЭФ). В качестве параметров безопасности терапии оценивались жизненно важные показатели, лабораторные и инструментальные показатели, а также частота и тяжесть нежелательных явлений (НЯ), в т. ч. серьезных (СНЯ).
Сбор данных о пациентах на каждый из визитов
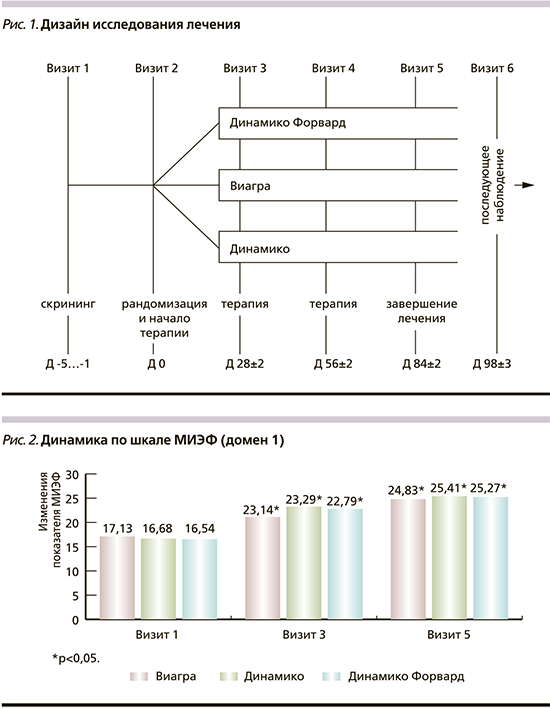
Исследование состояло из 3 этапов: периода скрининга, периода лечения и периода последующего наблюдения. За это время пациенты выполнили 6 визитов, период лечения составил 12 недель, период последующего наблюдения – 14 дней, максимальная продолжительность исследования – 15 недель (рис. 1).
После подписания информированного согласия проведены скрининговые мероприятия и оценка критериев включения, которыми являлись наличие документированного диагноза ЭД, поставленного не менее чем за 3 месяца до скрининга, и оценка в домене «эректильная функция» опросника МИЭФ от 11 до 25 баллов включительно (из 30 возможных) на момент скрининга. В рамках скрининговых мероприятий также проводились физикальный осмотр пациента, осмотр уролога, собирался сексуальный анамнез. После рандомизации пациентам назначалась соответствующая терапия ЭД.
С целью оценки безопасности терапии на визитах осуществлялся общий и биохимический анализы крови, общий анализ мочи, а также проводилось ЭКГ-исследование, регистрировалась сопутствующая терапия, оценивалась приверженность лечению, проводился учет исследуемых препаратов. На визитах 3 и 5 пациенты дополнительно заполняли опросники МИЭФ и ОКСЖ-М. Визит 6 проводился для контроля состояния пациентов и оценки безопасности терапии, после чего исследование для пациента считалось завершенным.

Статистика
Уровни статистической значимости различий и доверительные интервалы в исследовании рассчитывались как двусторонние с уровнем значимости 0,025 для доверительных интервалов соотношения терапевтического эффекта и 0,05 для остальных сравнений (если не указано дополнительно).
Этическая экспертиза
Исследование (номер протокола CS-DYN01-13) проведено с соблюдением принципов, заложенных в Хельсинкской декларации Всемирной медицинской ассоциации (1964 г. с последующими дополнениями), в соответствии с требованиями ГОСТ Р 52379–2005 «Надлежащая клиническая практика», правилами ICH GCP и действующими нормативными требованиями. Исследование было одобрено Советом по этике при Министерстве здравоохранения РФ.
Результаты
Исходные характеристики пациентов в трех группах значимо не различались (табл. 1).
Показатели индекса МИЭФ на момент включения в исследование в группе Виагры составили 17,13±2,88, Динамико – 16,68±2,75 и Динамико Форвард – 16,54±3,26. К моменту окончания исследования частота «положительных» ответов на терапию в исследуемых группах составила 55% (95% доверительный интервал [ДИ] – 39,82–69,30) в группе Виагры, 75% (95% ДИ – 62,30–85,54) в группе Динамико и 70% (95% ДИ – 54,47–82,03) в группе Динамико Форвард без достоверных различий между группами (p>0,05).
При сопоставлении эффективности Динамико Форвард и Виагры статистическая гипотеза «неменьшей эффективности» Динамико Форвард была подтверждена. При сопоставлении эффективности Динамико Форвард и Динамико были достигнуты сходные показатели клинической эффективности, однако вследствие недостаточной выборки пациентов опровергнуть нулевую гипотезу не удалось.
На рис. 2 показана динамика показателей по шкале МИЭФ. Статистически значимое увеличение этого показателя по сравнению со скрининговым было зафиксировано уже на визите 3 и сохранялось на визите 5 во всех группах пациентов. На рис. 3 представлен средний прирост баллов МИЭФ по сравнению с исходными показателями.
Динамика вторичных критериев эффективности также не имела достоверных различий между группами. Статистически значимый рост показателей определялся во всех трех группах на визите 3 (во всех доменах) и сохранялся до конца исследования.
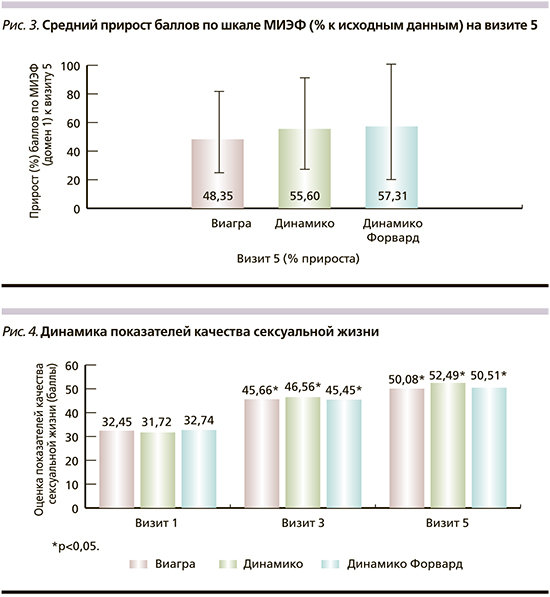
Рост показателей качества сексуальной жизни также фиксировался на визите 3 и сохранялся до окончания исследования во всех трех группах без существенных межгрупповых различий (рис. 4).
Приверженность терапии оценивалась по количеству возвращенных упаковок препарата. Если пациент принимал ≥4 таблеток/пленок препарата, данный показатель расценивался как 100%-ный комплаенс. У одного пациента комплаенс составил 69%, у всех остальных он достиг 100%.
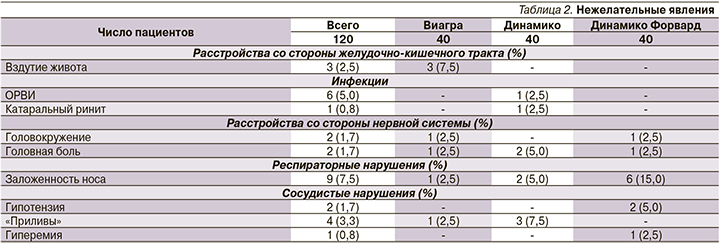
Вне зависимости от приема исследуемого препарата в исследовании было зарегистрировано 30 НЯ у 19 пациентов (табл. 2): 6 на фоне приема Виагры – у 4 пациентов, 9 на фоне приема Динамико – у 7 пациентов и 15 на фоне приема Динамико Форвард – у 8 пациентов. У одного пациента зарегистрировано одно СНЯ. Все случаи НЯ разрешились без последствий.
Желудочно-кишечных нарушений на фоне приема препарата Виагра, НЯ инфекционной природы на фоне приема Динамико и Динамико Форвард, а также гипотензии на фоне приема Динамико Форвард были расценены как непредвиденные. По выраженности все НЯ были отнесены исследователями к легкой степени тяжести и не требовали дополнительной медикаментозной коррекции, за исключением одного пациента в группе Динамико Форвард с ОРВИ средней степени тяжести. У одного пациента с развившейся на фоне приема Динамико Форвард артериальной гипотензией последующие дозировки исследуемого препарата были снижены на 50%, один пациент отозвал свое информированное согласие из-за выраженной заложенности носа, в связи с чем прием препарата был отменен. В остальных случаях доза исследуемых препаратов не менялась. В исследовании было зарегистрировано одно СНЯ – острый пансинусит, развившийся у пациента, принимавшего препарат Виагра. Заболевание потребовало госпитализации в ЛОР-стационар и разрешилось выздоровлением (было отнесено к СНЯ в связи с госпитализацией пациента). Данное СНЯ было расценено как средней тяжести, непредвиденное и не связанное с приемом препарата. Статистически значимых различий в НЯ между группами выявлено не было.
Обсуждение
Настоящее исследование представляет собой одно из первых исследований терапевтической эффективности генерической формы силденафила по сравнению с оригинальным препаратом.
В исследовании была подтверждена гипотеза «неменьшей эффективности» в отношении препаратов Динамико Форвард и Виагры; та же гипотеза по отношению ко второй паре препаратов, Динамико Форвард и Динамико, подтверждена не была. При этом схожие показатели терапевтической эффективности были продемонстрированы во всех группах наблюдения. Причиной того, что в рамках данного исследования нулевая гипотеза в отношении второй пары препаратов не была подтверждена, может быть недостаточная величина выборки пациентов. При анализе данных по окончанию исследования было рассчитано, что для доказательства первичной гипотезы в условиях выбора наиболее консервативной поправки Бонферрони понадобилось бы включение в каждую из групп не менее 74 пациентов.
Дополнительным объяснением является значительная вариабельность показателей первичной конечной точки, зафиксированная в данном исследовании. Практическим объяснением значительной вариабельности количества баллов по шкале МИЭФ может являться различная трактовка вопросов шкалы МИЭФ пациентами и как следствие – значительная вариабельность ответов.
Статистически значимых различий по влиянию на абсолютный показатель индекса МИЭФ в домене 1 между исследуемыми препаратами выявлено не было. Очевидно, что и с практической точки зрения минимальные абсолютные различия в показателях МИЭФ между группами не отражают клинически значимых эффектов.
Результаты этого исследования дополняют данные исследований биоэквивалентности, посвященных сравнению препаратов в таблетированной форме с препаратами в виде диспергируемых в ротовой полости пленок [1, 2]. В недавнем исследовании Е. Dadey было показано, что препараты в виде диспергируемых в ротовой полости пленок обеспечивают сходные показатели концентрации силденафила в плазме по сравнению с таблетированной формой [2].
Таким образом, в настоящее время имеются данные о биоэквивалентности указанных лекарственных форм, а результаты представленного нами исследования демонстрируют их схожую эффективность и безопасность. С учетом преимуществ силденафила в виде пленок (речь идет прежде всего об отсутствии необходимости запивать препарат водой), эти данные позволяют считать их возможной альтернативой таблетированной форме при терапии ряда пациентов с ЭД.
У пациентов всех трех групп установлены сходные, приемлемые показатели переносимости терапии. Количество НЯ в группах статистически значимо не различалось. Также не было выявлено влияния исследуемых препаратов на лабораторные показатели, основные жизненные функции организма и параметры электрокардиограммы. Данные, полученные в ходе исследования, соотносятся с аналогичными показателями переносимости терапии в более ранних работах [1, 2].
В исследовании М. Radicioni et al. было показано, что НЯ регистрировались с одинаковой частотой в группах пациентов, принимавших силденафил-препарат в виде пленок или таблеток [1]. Таким образом, полученные результаты подтверждают взаимозаменяемость исследуемых препаратов как в рамках показателей безопасности и переносимости, так и в отношении эффективности.
Пленки, диспергируемые в полости рта, – Динамико Форвард (Тева, Израиль), обладающие эквивалентными классическим таблеткам силденафила фармакокинетическими и фармакодинамическими свойствами, имеют перед ними ряд преимуществ. Их прием менее заметен для партнерши пациента, может быть «замаскирован» в виде приема «пастилки» для полости рта, не требует дополнительного приема жидкости, оказывая сравнимый с таблеткой клинический эффект.
При длительной терапии ингибиторами ФДЭ-5 незаметность приема препарата приобретает для пациента решающее значение. Прием препарата в режиме «по требованию» подразумевает некоторую свободу в выборе лекарственного средства для обеспечения адекватной эректильной функции. Если пациент имеет готовое решение в терапии ЭД, то после 30–40 приемов ингибиторов ФДЭ-5 в максимально удобном для него режиме «по требованию» он, как правило, перестает воспринимать ЭД как значительную проблему, зная, что может с ней успешно справиться.
Таким образом, пленки, диспергируемые в полости рта, – Динамико Форвард (Тева, Израиль) – обладают рядом преимуществ по сравнению с классической таблетированной формой силденафила при сравнимом клиническом эффекте и могут быть рекомендованы пациентам с эректильными расстройствами для приема в течение длительного времени.
Заключение
Применение препаратов Динамико Форвард и Динамико сопоставимо по терапевтической эффективности с препаратом Виагра. Исследование показало неменьшую терапевтическую эффективность препарата Динамико Форвард по сравнению с препаратом Виагра и сходную терапевтическую эффективность по сравнению с препаратом Динамико. Все три препарата продемонстрировали удовлетворительную переносимость и безопасность применения.



