Введение
Болезни системы кровообращения занимают лидирующее место в структуре заболеваемости и смертности по основным классам болезней. Сосудистая патология, в т.ч. и цереброваскулярные заболевания, во всем мире приобрели характер неинфекционной эпидемии. В Российской Федерации ежегодно регистрируется до полумиллиона первичных случаев инсульта. Заболеваемость инсультом в России составляет 3,36 случая на 1000 населения в год, стандартизованная заболеваемость – 2,39 на 1000 населения в год (у мужчин – 3,24 на 1000 населения, у женщин – 2,24 на 1000) [4, 5, 8].
По частоте инсульт выступает третьей причиной смертности населения в развитых странах, а также служит одной из основных причин стойкой утраты трудоспособности. Более четверти лиц, перенесших инсульт, умирают в течение 1-го месяца, 40% – в течение 1-го года, порядка трети пациентов, перенесших инсульт, – тяжелые инвалиды, зачастую требующие посторонней помощи в повседневном быту, а 20% не могут самостоятельно передвигаться. Лишь около пятой части пациентов, выживших после инсульта, способны вернуться к прежней трудовой деятельности и в состоянии полностью обслуживать себя самостоятельно. Вследствие колоссальных материальных затрат, связанных с проведением лечебных и реабилитационно-восстановительных мероприятий среди пациентов с инсультом, обеспечением ухода за больными, проблема цереброваскулярной патологии характеризуется не только медицинской, но и социальной значимостью [6, 7, 9].
В структуре инсультов от 67 до 80% имеют ишемическую природу.
Лечение острого инсульта направлено на сведение к минимуму повреждения мозга, снижение уровня инвалидизации и развития вторичных осложнений. Система лечения инсульта базируется на тех представлениях о механизмах развития заболевания, которые сложились в течение последних лет, и включает комплекс лечебных мероприятий помощи больным церебральным инсультом вне зависимости от его характера (т.н. базисная терапия) и дифференцированное лечение инсульта [12, 14, 15]. Дифференцированная терапия острого церебрального инсульта проводится в соответствии с характером нарушения мозгового кровообращения, локализацией и распространенностью очага поражения, а также зависит от патогенетических особенностей развития заболевания. Нейропротективная терапия в настоящее время остается одной из важнейших стратегических задач лечения пациентов с острым инсультом [1, 2].
В нашей клинике проведено сравнительное исследование по наблюдательной программе изучения эффективности препарата Целлекс в острейшем периоде ишемического инсульта. Препарат Целлекс (рег. № ЛП 0011393-201211, АО «Фарм-Синтез», Россия), представляющий собой комплекс средне- и высокомолекулярных белков и полипептидов, относящихся к факторам роста, дифференцировки нервной ткани, сигнальным молекулам цитоплазмы и межклеточного матрикса, выделенных из эмбриональной ткани головного мозга поросят [6, 8, 10, 11].
Препарат обладает выраженным нейропротективным действием, а также мощным нейрорепаративным потенциалом, не имеет аналогов среди лекарственных средств в современной фармакологии [13, 16]. Эффективность и безопасность применения Целлекса доказаны в многочисленных экспериментальных и клинических исследованиях на моделях острой фокальной ишемии и гипоксии мозга, у больных в остром периоде инсульта [3].
Ключевой целью данного исследования стала оценка эффективности применения Целлекса по отношению к выбранному препарату сравнения (по клиническим показателям). Переменными точками интереса являлись объем, динамика и сроки восстановления утраченных функций у больных острым ишемическим инсультом на фоне комплексной терапии.
Материал и методы
В исследовании приняли участие 60 пациентов, госпитализированных по поводу острого ишемического инсульта в системе внутренней сонной артерии. Наблюдавшиеся пациенты были распределены в две сопоставимые по размеру и основным клиническим и демографическим показателям группы: 1-ю (Целлекс) составили 30 больных, которые получали Целлекс по 1,0 мл подкожно 1 раз в сутки на протяжении 10 дней в дополнение к проводимой комплексной терапии, включившей как базисную, так и нейропротективную терапию (цитиколин); 2-ю группу (контроль) составили 30 больных, которые получали комплексную терапию, включившую как базисную, так и нейропротективную терапию (цитиколин), в дополнение к которой все пациенты группы получали этилметилгидроксипиридина сукцинат, который вводился, согласно действующей инструкции по 5,0 мл (500 мг), 2 раза в сутки внутривенно капельно первые 10 дней, затем по 2,0 мл (200 мг) внутримышечно до окончания клинического этапа исследования.
В качестве критериев эффективности были взяты:
- динамика общего балла по шкале инсульта (NIHSS – National Institutes of Health Stroke Scale) по каждой группе пациентов;
- динамика двигательных нарушений по шкале инсульта (NIHSS) по каждой группе пациентов;
- динамика речевых нарушений по шкале «Опросник речи» по каждой группе пациентов.
Оценку неврологического статуса и тестирование по шкале «Опросник речи» проводили до начала лечения, через 3 дня после начала лечения, через 6 дней после начала лечения и на 20-е сутки от начала лечения.
Статистическая обработка материала осуществлена стандартными статистическими методами с применением пакета SPSS 13.0. Результаты в зависимости от характера распределения представлены в виде медианы (Ме) и верхнего и нижнего квартилей или в виде средних значений (М) и стандартного отклонения (+SD). За достоверные принимались различия при p<0,05.
Результаты и обсуждение
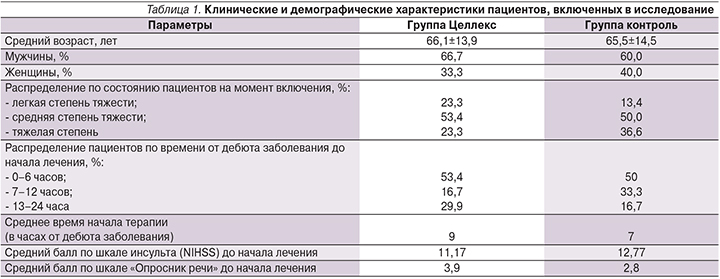
Обе группы оказались сопоставимыми по среднему возрасту, половому составу, тяжести инсульта, степени выраженности двигательных и речевых нарушений; данные представлены в табл. 1.
В группе Целлекс пяти пациентам был проведен внутривенный тромболизис (рТАП), в последующем из статистической обработки данные этих пяти пациентов исключены в связи с некорректностью сравнения различных технологий лечения и оказываемым искажением при сравнении групп. Весь последующий статистический анализ не учитывал результаты пациентов, получивших процедуру внутривенного тромболизиса, однако они завершили участие в исследовании согласно протоколу наблюдательной программы. Побочных эффектов на фоне терапии Целлексом у этих пяти пациентов не отмечено.
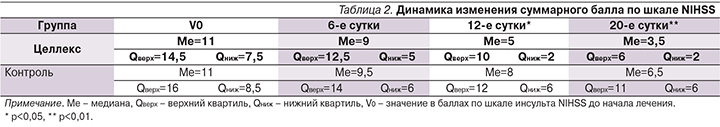
Динамика изменения суммарного балла по шкале инсульта NIHSS в сравниваемых подгруппах представлена в табл. 2.
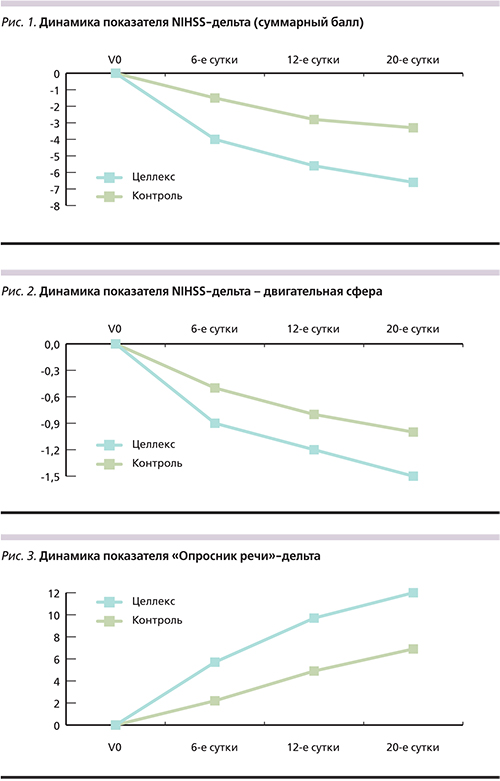
Динамика показателя NIHSS-дельта, демонстрировавшего уменьшение суммарного балла по шкале NIHSS от исходного состояния пациента (V0) к 6-м, 12-м и 20-м суткам лечения в сравниваемых подгруппах, представлена на рис. 1.
Снижение общего балла по шкале NIHSS в группе, получавшей в составе комбинированной терапии Целлекс, опережало контроль и носило достоверный характер (р=0,049; U-критерий Манна–Уитни) начиная с 12-х суток, достигнув к окончанию срока лечения разницы в 3 балла и более по сравнению с контролем.
Динамика изменения балла по шкале инсульта NIHSS (двигательная сфера в сравниваемых подгруппах) представлена в табл. 3.
Динамика показателя NIHSS-дельта (двигательная сфера, демонстрирующая уменьшение двигательного дефицита по шкале NIHSS от исходного состояния пациента (V0) к 6-м, 12-м и 20-м суткам лечения в сравниваемых подгруппах) представлена на рис. 2.
Таким образом, при оценке такого показателя, как NIHSS – двигательная сфера, достоверные различия (p<0,05) с группой контроля появились к 20-м суткам. Регресс баллов по шкале NIHSS – двигательная сфера в группе Целлекс – превосходил таковой в группе контроля в два раза.
При оценке динамики восстановления афатических нарушений использовалась шкала «Опросник речи», в которой 0 баллов соответствует тотальной афазии (мутизму), 19 – норме. По критериям отбора в наблюдательную программу включены пациенты с результатами тестирования по шкале «Опросник речи» не выше 10 баллов до распределения в одну из групп и, таким образом, до начала лечения, что соответствует выраженным речевым нарушениям.
Результаты тестирования по шкале «Опросник речи» в период от начала лечения к 20-м суткам в абсолютных значениях баллов представлены в табл. 4.
Динамика показателя «Опросник речи»-дельта, демонстрировавшего прирост в баллах по использованной шкале для оценки выраженности афатических нарушений в период от начала лечения к 20-м суткам, представлена на рис. 3.
Как следует из приведенных данных, достоверные различия в степени восстановления речевой функции в группах появляются уже к 6-м суткам (р<0,05) и в группе Целлекс превосходят показатели группы контроля в 2 раза. Указанные различия сохраняются в группах к окончанию периода клинического наблюдения (20-е сутки) с высокой степенью достоверности (p<0,001), несколько уменьшаясь в количественном соотношении по группам к 20-м суткам, что обусловлено довольно быстрым в группе Целлекс достижением максимального количества баллов (19) по используемой шкале «Опросник речи».

Заключение
В программе приняли участие 60 больных, рандомизированных в группы Целлекс и контроль, которые были сопоставимы по половозрастным характеристикам, тяжести состояния больных и по времени первого введения исследуемого препарата (либо препарата сравнения).
Анализ безопасности показал, что побочных эффектов у больных, включенных в программу, в течение всего срока наблюдения в рамках данного протокола отмечено не было.
Результаты исследования свидетельствуют о клинической эффективности применения исследуемого препарата в комплексном лечении инсульта, о чем свидетельствует более низкая по сравнению с группой сравнения доля больных, получавших Целлекс, с течением инсульта – без положительной динамики (снижение общего балла NIHSS менее чем на 3 балла за период наблюдения): в группе Целлекс – 1; в группе контроль – 5. А также с прогредиентным течением (прирост общего балла на 3 и более за период наблюдения): в группе Целлекс – 0, в группе контроль – 2.
Сравнение динамики средних значений теста «Опросник речи» у пациентов с выраженными речевыми нарушениями (от 0 до 10 баллов) показало значимое по сравнению с исходным уровнем его возрастание в обеих группах. При этом у пациентов, принимавших Целлекс, значение этого показателя начиная с 6-х суток было достоверно выше (p<0,05), а средний прирост в баллах составил 8 против 3,5 группы сравнения (более чем в 2 раза).
Сравнение динамики средних значений общего балла по шкале инсульта NIHSS также показало значимое по сравнению с исходным уровнем его снижение в обеих группах. При этом у пациентов группы Целлекс к 12-м суткам наблюдения различия с группой сравнения становились достоверными (p<0,05), а к 20-м суткам наблюдения среднее снижение общего балла по шкале NIHSS для группы Целлекс составило около 70% (MeV0=11→Me 20-е сутки=3,5) против 40% в группе контроль (MeV0=11→Me 20-е сутки=6,5).
Сравнение динамики средних значений показателя NIHSS (нарушения двигательной сферы) также показало значимое по сравнению с исходным уровнем его снижение в обеих группах. При этом у пациентов группы Целлекс достоверные различия с группой контроля (p<0,05) появились позже – только к 20-м суткам. Снижение суммы баллов в разделе шкалы NIHSS для двигательной сферы в группе Целлекс составило около 66% (MeV0=4,5→Me 20-е сутки=1,5), а в группе сравнения составило 40% (MeV0=5→Me 20-е сутки=3).
Таким образом, полученные данные свидетельствуют об эффективности исследуемого препарата Целлекс, при введении которого больным инсультом отмечено более выраженное улучшение состояния пациентов к концу срока наблюдения (20-е сутки), что подтверждено динамикой показателей шкалы инсульта NIHSS (общий балл; движение) и шкалы «Опросник речи».



