Введение
Бронхиальная астма (БА) – хроническое заболевание, которое имеет высокую распространенность среди всех возрастных групп и встречается, по данным эпидемиологических исследований, среди 1–18% лиц в зависимости от региона мира [1]. Распространенность БА в нашей стране не отличается от таковой в других европейских странах. По данным Российского респираторного общества (РРО), по результатам эпидемиологических исследований в России распространенность БА среди детей в нашей стране составляет от 5,6 до 12,1% [2], а среди взрослых – 5,6–7,3% [3]. По экспертной оценке академика А.Г. Чучалина, в России БА страдают около 7 млн человек, а результаты международного проекта GARD (Глобальный альянс по борьбе с хроническими респираторными заболеваниями), проведенного в России в 2010–2013 гг. по инициативе ВОЗ и под руководством НИИ пульмонологии, показали, что симптомы БА отмечают 25,7% респондентов, а спирометрические критерии БА встречаются среди 13,9% обследованных субъектов [4]. Анализ обширных эпидемиологических исследований БА у детей и взрослых, проведенных в период с 1990 по 2009 г., показал продолжающийся рост распространенности БА в большинстве регионов мира, особенно выраженный в странах с низким уровнем заболеваемости БА на период 1990-х гг. [5]. Наравне с ростом заболеваемости и распространенности БА за последние 15–20 лет повсеместно отмечается выраженное снижение частоты смертельных исходов вследствие БА [1, 6]. Существенный вклад в эту позитивную тенденцию внесли международные и национальные руководства по БА. Основной программный документ по БА – GINA (Global Initiative for Asthma, Глобальная инициатива по бронхиальной астме), который издается с 1995 г. и ежегодно пересматривается с 2002 г., публикуется на сайте www.ginasthma.org. В 2013 г. РРО созданы федеральные клинические рекомендации по диагностике и лечению БА, базирующиеся на основных принципах GINA [7]. Вместе с тем, несмотря на наличие современных руководств и довольно обширного выбора фармакологических препаратов для длительной терапии, БА по-прежнему остается заболеванием, приводящим к инвалидизации больных, незапланированным госпитализациям, обращениям за неотложной помощью и смертельным исходам. Кроме того, более половины больных БА, получающих лечение, не имеют контроля заболевания, а стало быть, имеют высокий риск развития обострений, низкое качество жизни, пропускают рабочие и учебные дни [8]. Настоящая статья посвящена основным принципам длительной контролирующей терапии БА и основывается на данных Федеральных клинических рекомендаций по диагностике и лечению БА РРО 2013 г. [3] и GINA-2014 [1].
Определение, диагностика и цели терапии БА
Бронхиальная астма является гетерогенным заболеванием и характеризуется хроническим воспалением дыхательных путей, приводящим к развитию респираторных симптомов, таких как свистящие хрипы, одышка, заложенность в груди и кашель, которые варьируются по времени и интенсивности и проявляются вместе с вариабельной обструкцией дыхательных путей, которая часто бывает обратимой спонтанно или под влиянием лечения. Диагноз БА сугубо клинический, устанавливается на основании жалоб и анамнестических данных пациента, клинико-функционального обследования с оценкой обратимости бронхиальной обструкции, специфического аллергологического обследования (кожные тесты с аллергенами и/или специфический IgЕ в сыворотке крови) и исключения других заболеваний.
На рис.1 представлен алгоритм диагноза впервые выявленной астмы по GINA-2014.
Бронхиальная астма – фенотипически гетерогенное заболевание, и впервые в GINA-2014 приводятся фенотипы БА, которые довольно легко могут быть идентифицированы:
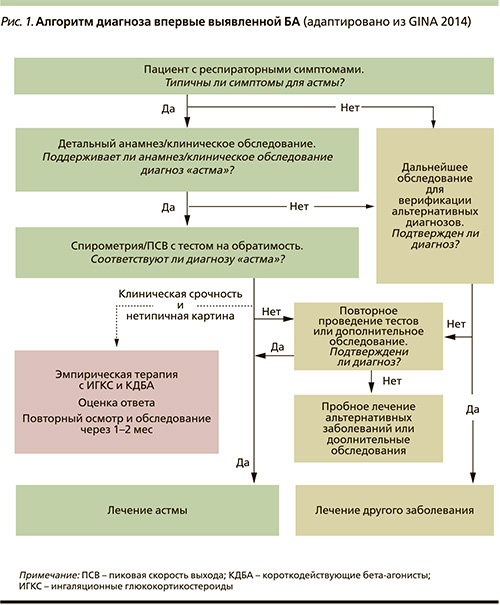
аллергическая БА: наиболее легко распознаваемый фенотип, который часто начинается в детстве, связан с наличием аллергических заболеваний (атопический дерматит, аллергический ринит, пищевая или лекарственная аллергия) в анамнезе или у родственников. Исследование индуцированной мокроты до лечения у пациентов с этим фенотипом БА часто выявляет эозинофильное воспаление дыхательных путей. Пациенты с фенотипом аллергической БА обычно хорошо отвечают на терапию ингаляционными кортикостероидами (ИГКС):
- неаллергическая БА: некоторые взрослые имеют БА, не связанную с аллергией. Профиль воспаления дыхательных путей у больных с данным фенотипом может быть нейтрофильным, эозинофильным или малогранулоцитарным. Эти пациенты часто отвечают не очень хорошо на ИГКС;
- БА с поздним дебютом: у некоторых пациентов, особенно у женщин, развивается астма впервые уже во взрослом состоянии. Эти больные чаще не имеют аллергии и требуют более высоких доз ИГКС или являются относительно рефрактерными к ГКС-терапии;
- БА с фиксированной обструкцией дыхательных путей: у ряда пациентов с длительным анамнезом БА развивается фиксированная обструкция дыхательных путей, которая, по-видимому, формируется вследствие ремоделирования бронхиальной стенки;
- БА у больных ожирением: некоторые пациенты с ожирением и БА имеют выраженные респираторные симптомы и незначительное эозинофильное воспаление.
Долгосрочные цели терапии БА:
- достижение хорошего контроля симптомов астмы и поддержание нормального уровня активности пациента;
- минимизация риска будущих обострений БА, фиксированной обструкции дыхательных путей и нежелательных побочных эффектов терапии [1, 7].
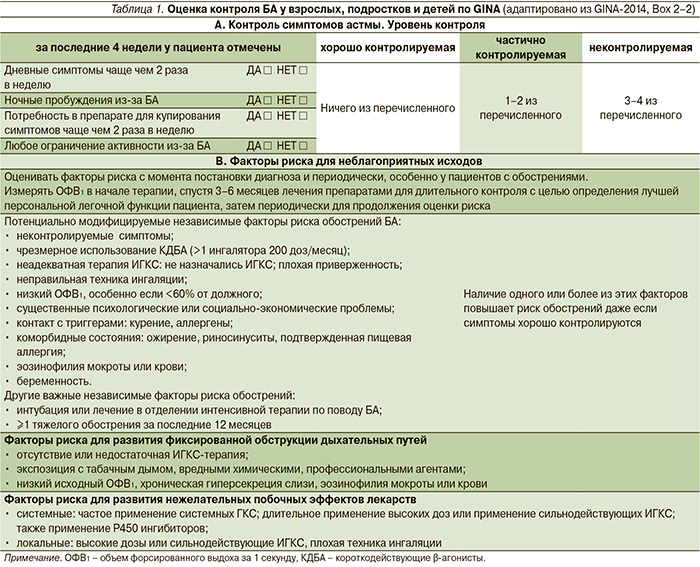
Оценка контроля симптомов астмы, безусловно, является важным предиктором риска обострения, но она недостаточна для полноценной оценки БА. Эксперты GINA-2014 рекомендуют классификацию контроля симптомов вместе с оценкой рисков обострений, развития фиксированной обструкции бронхов и побочных эффектов лекарственной терапии (табл. 1) с целью правильного выбора лечения, ибо наличие одного или более факторов риска обострения БА даже при хорошем контроле симптомов переводит пациента в группу риска по дальнейшему развитию обострения БА, влияет на тактику ведения и лечения больного.
Ступенчатая фармакотерапия БА
Лекарственные препараты для лечения БА делятся на три категории. Препараты для контроля симптомов: применяются для регулярного поддерживающего лечения. Они уменьшают воспаление дыхательных путей, контролируют симптомы и редуцируют будущие риски обострений и снижения функции легких. К этой группе относятся ИГКС; антилейкотриеновые препараты (АЛП); комбинированные препараты ИГКС и длительнодействующих β2-агонистов (ДДБА); пролонгированные теофиллины также в комбинации с ИГКС; кромоны. Ингаляционные ГКС являются самыми эффективными фармакологическими препаратами для длительного контроля БА и показаны для лечения персистирующих симптомов БА у всех пациентов. Практически все существующие молекулы ИГКС доступны и применяются в нашей стране: беклометазона дипропионат, будесонид, флутиказона пропионат, циклесонид и мометазона фуроат (табл. 2).
Два последних (циклесонид и мометазона фуроат) – наиболее современные ИГКС, обладающие высокой эффективностью при благоприятном профиле безопасности при персистирующей БА разной степени тяжести [9, 10]. Фармакологические и фармакокинетические свойства мометазона фуроата и циклесонида позволяют применять эти препараты однократно, особенно в диапазоне низких-средних доз, что повышает приверженность пациентов лечению и способствует достижению и поддержанию контроля [11].
Препараты, купирующие симптомы (скорой помощи): ими обеспечиваются все пациенты с БА с целью применения по необходимости, при возникновении симптомов затрудненного дыхания, включая периоды ухудшения и обострения БА. Они также рекомендуются для профилактического использования перед физической нагрузкой. Уменьшение потребности в этих препаратах, а в идеале полное ее отсутствие являются важной целью и мерой успеха лечения БА. К этой группе препаратов относятся КДБА; короткодействуйщий М-холинолитик (ипратропия бромид); комбинированный препарат беродуал; теофиллины короткого действия; из группы ДДБА только формотерол может применяться для купирования симптомов БА, т.к. развивает быстрый бронхолитический эффект, но регулярное или частое применение ДДБА без ИГКС категорически не рекомендуется вследствие риска обострений (категория доказательности А).
Дополнительная терапия для пациентов с тяжелой БА: эти препараты могут применяться, когда пациенты имеют персистирующие симптомы и/или обострения, несмотря на лечение высокими дозами препаратов для контроля симптомов (обычно высокие дозы ИГКС и ДДБА) и терапию модифицируемых факторов риска. К этой группе относятся препарат моноклональных антител против IgE (омализумаб), применяющийся при тяжелой аллергической IgE-обусловленной БА; системные ГКС (оральные и парентеральные) и длительнодействующий антихолинергический препарат тиотропия бромид, одобренный для лечения БА в РФ.
Основной принцип ступенчатого подхода к терапии БА заключается в следующем:
- текущий уровень контроля БА и объем получаемой пациентом терапии БА определяют выбор фармакологического лечения;
- если БА не контролируется на настоящей терапии, лечение должно быть увеличено на ступень вверх – step up;
- если контроль БА поддерживается по крайней мере в течение 3 месяцев, объем терапии может быть снижен на ступень вниз – step dawn – с целью сохранения контроля на минимально возможных дозах поддерживающей терапии (рис. 2).
Ступень 1: применение препаратов, купирующих симптомы по потребности. Предпочтительный выбор: КДБА по потребности, эта группа препаратов высокоэффективна для быстрого облегчения симптомов БА (категория доказательности А), однако этот вариант лечения может применяться только пациентами с очень редкими (<2 раз в месяц) дневными симптомами короткой продолжительностью (несколько часов); пациентами, не отмечающими ночных симптомов и имеющими нормальную функцию легких. Более частые симптомы БА или наличие факторов риска обострения, таких как сниженный ОФВ1 <80% от лучшего персонального или должного или обострение в предшествующие 12 месяцев, указывает на необходимость регулярной контролирующей терапии (категория доказательности В).
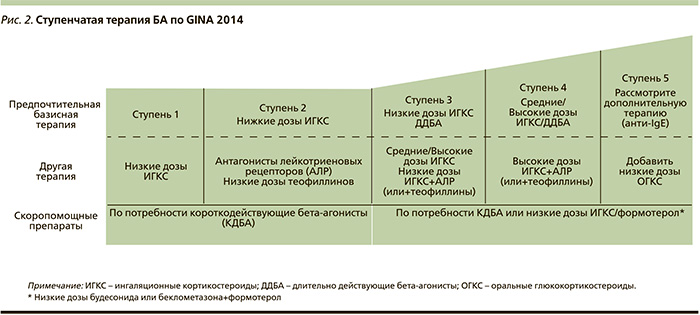
Другие варианты: регулярная терапия низкими дозами ИГКС в дополнение к КДБА по потребности должна быть рассмотрена для пациентов с риском обострений (категория доказательности В).
Ступень 2: низкие дозы препаратов для длительного контроля плюс препараты, купирующие симптомы по потребности. Предпочтительный выбор: регулярное применение низких доз ИГКС плюс КДБА по потребности. Лечение низкими дозами ИГКС редуцирует симптомы БА, повышает функцию легких, улучшает качество жизни, уменьшает риск обострений, госпитализаций и смертельных исходов из-за БА (категория доказательности А).
Другие варианты: АЛП менее эффективны, чем ИГКС (категория доказательности А). Они могут применяться в качестве начальной контролирующей терапии некоторых пациентов, которые не могут или не хотят применять ИГКС; пациентов, отмечающих выраженные побочные эффекты от ИГКС; или больных сопутствующим аллергическим ринитом (категория доказательности В). Для пациентов с изолированной сезонной аллергической астмой, например, обусловленной аллергией к пыльце березы, ИГКС должны начать применяться немедленно с момента появления симптомов и продолжать применяться в течение четырех недель после окончания сезона цветения (категория доказательности D).
Другие варианты, не рекомендованные для рутинного применения: теофиллины замедленного высвобождения имеют слабую эффективность при БА (категория доказательности В) и высокую частоту побочных эффектов, которые при применении высоких доз могут быть жизнеугрожающими. Кромоны (недокромил натрия и кромогликат натрия) имеют высокую безопасность, но низкую эффективность (категория доказательности А), кроме того, ингаляторы для этих лекарственных препаратов требуют ежедневного промывания, чтобы избежать их блокирования.
Ступень 3: один или два контролирующих препарата плюс препарат, купирующий симптомы по потребности. Предпочтительный выбор (взрослые/подростки): комбинация низких доз ИГКС/ДДБА как поддерживающая терапия плюс КДБА по потребности или комбинация низких доз ИГКС/формотерол (будесонид или беклометазон) в качестве поддерживающей терапии и для купирования симптомов по потребности. Предпочтительный выбор (дети 6–11 лет): средние дозы ИГКС плюс КДБА по потребности.
В нашей стране зарегистрировано абсолютное большинство комбинированных препаратов ИГКС/ДДБА: флутиказона пропионат/сальметерол; будесонид/формотерол; беклометазон/формотерол; мометазон/формотерол; флутиказона фуроат/вилантерол. Добавление ДДБА к той же дозе ИГКС обеспечивает дополнительное улучшение симптомов и легочной функции с редукцией риска обострений (категория доказательности А).
У пациентов, имеющих факторы риска развития обострений, ИГКС/формотерол в качестве единого ингалятора (для поддерживающей терапии и купирования симптомов по потребности) значительно редуцирует обострения и обеспечивает такой же уровень контроля БА на относительно низких дозах ИГКС по сравнению с фиксированными дозами ИГКС/ДДБА в качестве поддерживающей терапии+КДБА по потребности или по сравнению с высокими дозами ИГКС+КДБА по потребности (категория доказательности А).
Другие варианты: для взрослых и подростков другим вариантом может быть повышение ИГКС до средних доз, но эта стратегия менее эффективна, чем добавление ДДБА (категория доказательности А). Еще одним вариантом, тоже менее эффективным по сравнению с ИГКС/ДДБА, может быть комбинация низких доз ИГКС с АЛП (категория доказательности А) или комбинация низких доз ИГКС с теофиллинами замедленного высвобождения (категория доказательности В).
Ступень 4: два или больше препаратов контролирующей терапии плюс препарат, купирующий симптомы по потребности. Предпочтительный выбор (взрослые/подростки): комбинация низких доз ИГКС/формотерол в качестве единого ингалятора или комбинация средних доз ИГКС/ДДБА плюс КДБА по потребности. Предпочтительный вариант для детей 6–11 лет: направить к специалисту для экспертной оценки и совета. Выбор терапии на четвертой ступени зависит от выбора на третьей ступени, и следует прежде всего проверить технику ингаляции, приверженность лечению, контакт с триггерами и еще раз подтвердить диагноз БА, прежде чем увеличивать объем терапии. Для взрослых и подростков с БА, имеющих ≥1 обострения в предшествующий год, комбинация низких доз ИГКС/формотерол (будесонид/формотерол или беклометазон/формотерол) в качестве поддерживающей терапии и для купирования симптомов (режим единого ингалятора) более эффективна в уменьшении обострений, чем те же самые дозы ИГКС/ДДБА в качестве постоянной поддерживающей терапии фиксированными дозами или более высокие дозы ИГКС (категория доказательности А). Этот режим может быть назначен с низких доз ИГКС/формотерол на ступени 3, на ступени 4 поддерживающие дозы ИГКС могут быть увеличены до средних. Равно как для пациентов, получающих низкие дозы ИГКС/ДДБА в режиме фиксированного дозирования плюс КДБА по потребности и не имеющих адекватного контроля, доза ИГКС в комбинации ИГКС/ДДБА может быть также увеличена до средней (табл. 2).

Другие варианты: комбинация высоких доз ИГКС/ДДБА может быть рассмотрена для взрослых и подростков, но увеличение дозы ИГКС в основном дает небольшую дополнительную пользу (категория доказательности А) и увеличивает риск нежелательных побочных эффектов. Применение высоких доз ИГКС рекомендуется только на период 3–6 месяцев, когда контроль БА не может быть достигнут на средних дозах ИГКС плюс ДДБА и/или третий препарат для контроля симптомов (АЛП или теофиллины замедленного высвобождения, категория доказательности В). Для средних и высоких доз будесонида эффективность может быть улучшена увеличением кратности дозирования до четырех раз в день (категория доказательности В), но приверженность такому режиму может быть проблемой. Для других ИГКС подходит дозирование 2 раза в день (категория доказательности D). Другие варианты этой ступени лечения БА для взрослых и подростков, которые могут быть добавлены к средним или высоким дозам ИГКС, но менее эффективны, чем добавление ДДБА, это АЛП (категория доказательности А) или теофиллин замедленного высвобождения (категория доказательности В).
Ступень 5: Самый высокий уровень терапии и/или дополнительное лечение. Предпочтительный выбор: направить для обследования к специалисту и рассмотрения дополнительной терапии. Пациенты с персистирующими симптомами или обострениями БА, несмотря на правильную технику ингаляции и хорошую приверженность лечению, соответствующему ступени 4, должны быть направлены к специалисту, занимающемуся экспертизой и лечением тяжелой БА (категория доказательности D). Варианты лечения, которые могут быть рассмотрены на ступени 5, включают:
- анти-IgE-терапию (омализумаб): может быть предложен больным среднетяжелой и тяжелой аллергической БА, которая не контролируется лечением, соответствующим ступени 4 (категория доказательности А);
- терапия, основанная на анализе индуцированной мокроты: может быть рассмотрена для больных с персистирующими симптомами и/или обострениями, несмотря на высокие дозы ИГКС или ИГКС/ДДБА, лечение может подбираться на основании эозинофилии (>3%) индуцированной мокроты. Больных тяжелой БА эта стратегия ведет к редукции обострения и/или снижению дозы ИГКС (категория доказательности А);
- бронхиальная термопластика (в РФ не зарегистрирована): может быть рассмотрена для некоторых пациентов с тяжелой БА (категория доказательности В). Доказательства эффективности ограничиваются избранными пациентами, и не известен долгосрочный эффект;
- добавление низких доз оральных ГКС (≤7,5 мг/день по преднизолону): может быть эффективно для некоторых пациентов с тяжелой БА (категория доказательности D), но часто связано с существенными побочными эффектами (категория доказательности В). Поэтому этот вариант должен быть рассмотрен только для взрослых больных с плохим контролем симптомов и/или частыми обострениями, несмотря на правильную технику ингаляции и хорошую приверженность лечению, соответствующему ступени 4, и после исключения других усугубляющих факторов. Пациенты должны быть осведомлены о вероятных побочных эффектах и тщательно мониторироваться в отношении развития стероид-индуцированного остеопороза, им должно назначаться соответствующее профилактическое лечение;
- добавление тиотропия бромида к лечению, соответствующему 4–5-й ступеням терапии взрослых больных тяжелой БА, эффективно в отношении улучшения функции легких, уменьшения рисков развития обострений и ухудшения БА. При этом отмечен хороший профиль безопасности тиотропия [12]. Недостигнутый контроль БА у пациента, получающего терапию ступени 4 или 5, служит показанием к назначению тиотропия Респимат, одобренного в РФ для лечения БА у взрослых и подростков старше 18 лет (категория доказательности В).
Оценка ответа на проводимую терапию
Как часто пациенты с БА должны посещать врача
Частота визитов к врачу зависит от начального уровня контроля БА, отмеченного у пациента, его ответа на терапию, дисциплинированности и участия в лечении. Идеально пациент должен быть осмотрен врачом через 1–3 месяца от начала контролирующего лечения и затем каждые 3–12 месяцев. После обострения визит должен быть назначен через неделю для оценки состояния.
Увеличение объема терапии (step-up)
БА – вариабельное заболевание, поэтому периодически возникает потребность в корректировке терапии врачом или самим пациентом:
- step-up на продолжительный (по крайней мере на 2–3 месяца) период: некоторые пациенты могут не отвечать адекватно на начальное лечение, и в случае правильного диагноза, техники ингаляции, хорошей приверженности, элиминации триггерных факторов и контроля сопутствующих заболеваний должно быть назначено лечение, соответствующее более высокой ступени (рис. 2). Ответ на это усиленное лечение должен быть оценен через 2–3 месяца. В случае отсутствия эффекта следует спуститься на предыдущую ступень и рассмотреть альтернативные возможности лечения или обследования и консультации специалиста;
- step-up на короткий (до 1–2 недель) период: краткосрочное (на 1–2 недели) увеличение поддерживающей дозы ИГКС может возникнуть в период вирусных респираторных инфекций или сезонного цветения растений. Это увеличение пациент может проводить самостоятельно в соответствии с имеющимся у него индивидуальным планом действия при БА или по назначению врача;
- каждодневная корректировка: для пациентов, которым назначен ИГКС/формотерол в режиме единого ингалятора, применение дополнительных ингаляций ИГКС/формотерол осуществляется в зависимости от наличия симптомов на фоне постоянной поддерживающей терапии рекомендованными дозами ИГКС/формотерол.
Уменьшение объема терапии (step-down)
После того как контроль БА достигнут и поддерживается на протяжении трех месяцев, а функция легких достигла плато, объем терапии БА часто может быть успешно уменьшен без потери контроля над заболеванием. Снижение дозы ИГКС на 25–50% с 3-месячным интервалом, как правило, подходит и безопасно для большинства пациентов с контролируемой БА. Однако полное прекращение лечения ИГКС в отношении взрослых больных не рекомендуется, т.к. приводит к повышению риска развития обострений [1].
Помимо адекватной фармакотерапии необходимо образовывать пациента и обеспечивать его информацией (индивидуальный план действий при БА). Следует проводить лечение сопутствующих заболеваний и факторов риска (курение, ожирение, депрессия), советовать нефармакологические методы лечения и стратегии (физическая активность, снижение веса, меры по избеганию контактов с аллергенами и триггерами).
Таким образом, целью терапии БА служат достижение, поддержание контроля симптомов и минимизация рисков обострений, фиксированной обструкции дыхательных путей и нежелательных побочных эффектов лечения. Основным принципом лечения БА считается ступенчатый подход с увеличением объема фармакотерапии в отсутствие контроля и/или при наличии факторов риска обострений, снижении объема терапии при достижении и сохранении стабильного контроля, в отсутствие факторов риска. Применение современных фармакологических препаратов базисной терапии астмы, следование национальным и международным руководствам по диагностике и лечению БА позволят достигать контроля заболевания большему числу пациентов и снизят частоту обострений, госпитализаций, смертельных исходов из-за БА.



