Введение
Хроническая сердечная недостаточность (ХСН) – синдром, характеризующийся проявлением комплекса симптомов: одышка, повышенная утомляемость, симметричные отеки нижней части тела, связанные с неадекватной перфузией органов и тканей в покое или при нагрузке в связи с нарушением структуры и/или функции сердца, приводящим к снижению сердечного выброса и/или повышению давления наполнения сердца в покое или при нагрузке, что проявляется эпизодически вплоть до развития декомпенсации [1]. К основным этиологическим факторам ХСН следует отнести артериальную гипертензию (АГ) ишемическую болезнь сердца (ИБС), кардиомиопатию, миокардиты и пороки сердца [1].
Цели лечения ХСН включают устранение клинических проявлений ХСН, замедление прогрессирования болезни путем кардио- и нефропротекции, улучшение качества жизни больных, снижение смертности и числа госпитализаций [1].
У пациентов с систолической дисфункцией левого желудочка (ЛЖ) после миокардиального повреждения (например, инфаркта миокарда или миокардита) в кардиомиоцитах и экстрацеллюлярном матриксе инициируется патологическое ремоделирование желудочка с его дилатацией, изменением геометрии (ЛЖ становится более сферичным) и нарушением сократительной функции. В начале заболевания симптомы ХСН могут быть не выражены, но с течением времени прогрессируют и становятся заметными [1].
Примерно половина больных ХСН имеют сниженную фракцию выброса ЛЖ (ХСН-снФВ – ХСН со сниженной фракцией выброса ЛЖ менее 40%), меньшая часть – нормальную (ХСН-сФВ – ХСН с сохраненной фракцией выброса ≥50%) [2].
В прогрессировании ХСН принимают участие как минимум два патофизиологических механизма. Первый определяет новые события, приводящие к гибели кардиомиоцитов (например, повторный инфаркт миокарда). Однако дальнейшее ремоделирование сердца может происходить и в отсутствие явных повторных повреждений миокарда. Вторым механизмом является системный ответ на снижение систолической функции ЛЖ, ключевое значение в котором имеет активация оси «ренин–ангиотензин–альдостерон» и симпатической нервной системы, повышение активности других прессорных систем: эндотелина, вазопрессина и цитокинов. Эти нейрогуморальные факторы не только вызывают периферическую вазоконстрикцию, задержку натрия и жидкости, а следовательно, увеличение гемодинамической нагрузки на ЛЖ, но и оказывают прямое токсическое действие на миокард, стимулируя фиброз и апоптоз кариомиоцитов, приводящих к дальнейшему ремоделированию сердца и нарушению его функции. Кроме миокардиального повреждения активация нейрогуморальных систем оказывает неблагоприятное влияние и на другие органы – кровеносные сосуды, почки, мышцы, костный мозг, легкие и печень, формируя патофизиологический «порочный» круг и приводя к клиническим проявлениям ХСН [3–5].
Ключевая роль в развитии ХСН отводится олигопептидному гормону ангиотензину-II. Взаимодействие ангиотензина-II с рецепторами сосудов, включая коронарные, приводит к увеличению общего периферического сосудистого сопротивления и стимуляции сократительной функции миокарда на фоне вазоконстрикции. Это может приводить к развитию дисфункции желудочков, вызывать кислородный дисбаланс и провоцировать ишемию миокарда. Прямое воздействие ангиотензина-II на миокард проявляется в индукции процесса компенсации через увеличение его массы за счет гипертрофии кардиомиоцитов и накопления фиброзной ткани, расширения полостей и нарушения нормальной геометрии желудочков [6–8].
Масса исследований свидетельствует о существовании генетической предрасположенности к кардиоваскулярной патологии. Спектр однонуклеотидных полиморфизмов (SNP – single-nucleotide polymorphism), принимающих участие в реализации и прогрессировании АГ и сердечной недостаточности (СН), достаточно широк. В патогенезе сердечно-сосудистых заболеваний (ССЗ) задействованы группы генов, контролирующих системы нейрогуморальной регуляции, в частности ренин-ангиотензин-альдостероновой системы (РААС) [9].
Для терапии ССЗ наибольшее распространение получили β-адреноблокато-ры, ингибиторы ангиотензинпревращающего фермента (иАПФ) и блокаторы рецепторов ангиотензина-II (БРА). На данный момент интерес представляют именно БРА 1-го типа как перспективная для широкого применения группа лекарственных средств. Среди преимуществ данных препаратов по сравнению с более изученными иАПФ, β-адреноблокаторами – органо- и нефропротективное действия [1, 10]. Выдвинуто предположение о взаимосвязи определенных генетических полиморфизмов у пациентов с ССЗ и эффективностью применения БРА [11, 12].
Цель исследования: на основании анализа научной литературы выяснить наиболее значимые полиморфные варианты генов РААС, определяющие эффективность терапии ССЗ БРА 1-го типа.
Методы
Поиск статей проведен в базах данных PubMed в предметной рубрике (MeSH Term) и в указателе фраз унифицированной медицинской языковой системы (United Medical Language System) и Google Scholar путем тематического поиска с января по сентябрь 2023 г. Для поиска русскоязычных источников использованы следующие ключевые слова: сердечная недостаточность, антагонисты рецепторов к ангиотензину-II, антигипертензивные препараты, полиморфизмы генов РААС, ангиотензин-II, ангиотензиноген (АТГ), однонуклеотидный полиморфизм. В предметной рубрике MeSH Term поиск осуществлен по терминам arterial hypertension, angiotensin receptor antagonists, polymorphism, single nucleotide. Всего найдено 116 полнотекстовых публикаций после исключения дублирующих работ и несоответствующих целям исследований, к использованию в работе принято 45 источников, одобренных всеми соавторами. Стратегия поиска и отбора публикаций представлена в виде блок-схемы PRISMA (см. рисунок).
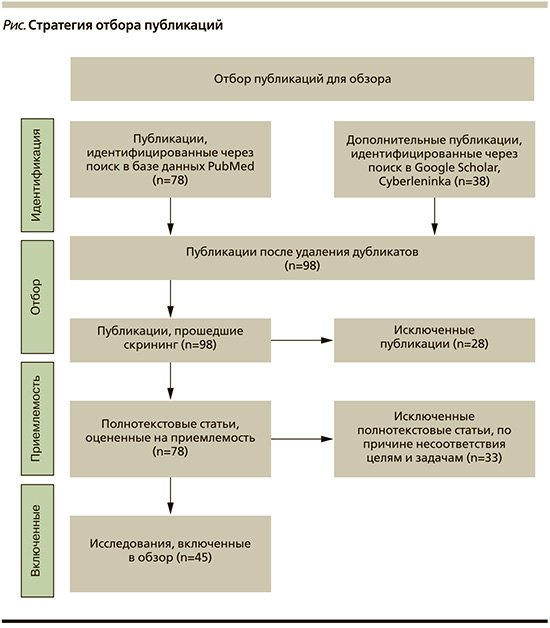
Результаты
Взаимосвязь однонуклеотидных полиморфизмов с развитием патологии сердечно-сосудистой системы. Влияние генов, кодирующих компоненты РААС, на патогенез ХСН осуществляется путем их участия в регуляции взаимодействия разных звеньев этой системы, эффектов эндотелиальных факторов, участия в мембранном ионном транспорте и передаче рецепторного сигнала в клетку. Клинически наиболее важными при оценке ССЗ считаются следующие гены-кандидаты: ACE, AGT, AGTR1, AGTR2, CYP11B2, ADD1, GNB3 [13–15].
ACE – ген АПФ. Концентрация АПФ в крови зависит от полиморфного варианта АСЕ типа I/D (insertion/deletion) в 16-м интроне (rs4646994): у носителей генотипа-II отмечается самый низкий уровень фермента, у лиц с генотипом DD содержание АПФ максимально. Наличие гомозиготного варианта DD считается фактором риска ССЗ [6, 14]. В мета-анализе 145 исследований полиморфизма генов, кодирующих белки РААС, с общим числом наблюдений 49 959 генотип DD АСЕ повышал риск развития ХСН на 45% [9, 16]. Кроме того, описана высокая частота встречаемости аллеля D только среди пациентов с тяжелыми формами ХСН [17].
С уровнем АТГ в крови ассоциированы полиморфные варианты T174M (rs4762) и M235T (rs699) гена ангиотензиногена (AGT). Наличие T-аллеля в 235-м положении AGT может быть ассоциировано с развитием АГ, т.к. приводит к повышенной экспрессии АТГ, существенному повышению содержания ангиотензина-II, обладающего вазоконстрикторным действием, повышающего общее периферическое сосудистое сопротивление и вызывающего быстрое повышение артериального давления (АД) [18, 19].
Белок АТГ также является важной частью РААС. Полиморфизмы гена AGT могут быть использованы в качестве генетических маркеров для атеросклероза, АГ и ИБС [20]. Изучено несколько полиморфных состояний гена AGT, однако особое внимание уделяется двум полиморфным вариантам: М235Т (rs699) и Т174М (rs4762), связанным с уровнем активности АТГ в плазме крови, содержанием ангиотензина-II, следовательно – с риском развития ССЗ [13, 15, 21–23]. Аллель T174М гена AGT гораздо чаще встречается у пациентов с ИБС [13, 23]. В ходе исследования полиморфизма М235Т обнаружено, что вариант 235Т представляет собой независимый фактор риска для развития ИБС, включая инфаркт миокарда. Увеличение риска развития эссенциальной АГ наблюдалось при наличии T-аллеля [21]. Наличие одного или двух Т-аллелей приводило к значительному увеличению уровня АТГ в плазме крови, что определяло повышение содержания ангиотензина-II и объясняло связь этого генетического полиморфизма с АГ [15]. Рецептор к ангиотензину-II 1-го типа играет ключевую роль в осуществлении нейрогуморальных реакций РААС. При рассмотрении полиморфизма A1166C гена (rs 5186) рецептора ангиотензина-II 1-го типа была выявлена трансверсия A→C в положении нуклеотида 1166 в 3’-нетранслируемой области гена рецептора ангиотензина II типа. Полученные результаты могут свидетельствовать о том, что данная генетическая вариация ассоциирована с АГ, гипертрофией ЛЖ, ИБС и прогрессированием диабетической нефропатии [24].
Ген рецептора 1-го типа к ангиотензину-II (АGТR1) локализован на длинном плече 3-й хромосомы и также относится к маркерам риска развития АГ. Среди однонуклеотидных полиморфизмов гена AGTR1 наиболее изучен полиморфизм А1166С, который может приводить не только к изменению регуляции сосудистого тонуса, но и к пролиферации элементов сосудистой стенки [12, 24–27].
Ген рецептора ангиотензина-II 2-го типа (AGTR2) является элементом РААС, участвующим в регуляции кровообращения и сосудистого тонуса, а также обладает широким спектром функций: от участия в регуляции апоптоза до вазодилатации с привлечением механизмов увеличения продукции оксида азота. Описано несколько полиморфных вариантов гена АGTR2, но наиболее изучены однонуклеотидные полиморфизмы G1675A и С3123А [28]. Полиморфизм G1675A снижает количество рецептора ангиотензина-II 2-го типа, для него описана взаимо-связь не только с сердечно-сосудистой патологией, но и с гипертензивными осложнениями беременности, в частности с преэклампсией [29, 30]. Вариант С3123А имеет несколько меньшее клиническое значение [29].
Ген CYP11B2 кодирует альдостеронсинтазу (АС). CYP11B2 катализирует последнюю стадию синтеза АС. Полиморфизм 344 C/T гена CYP11B2 обусловливает повышение уровня АС, следовательно – повышение уровня альдостерона в крови, что вызывает усиленную реабсорбцию Na+ в почечных канальцах, увеличение объема циркулирующей крови и повышение системного АД, что может приводить к развитию АГ и ХСН [31].
Гуанин-нуклеотид-связывающий белок β-3 (GNB3) опосредует передачу сигналов внутрь клеток, контролируя тонус сосудов и клеточную пролиферацию. Полиморфный вариант С825Т гена GNB3 обусловливает нарушение передачи сигналов внутрь клеток, что в результате приводит к сужению сосудов и существенно повышает риск АГ. Носительство аллеля T полиморфного маркера C825T гена GNB3 также ассоциировано с повышенной массой тела, которая также является фактором риска ССЗ [32].
Большинство данных, полученных в ходе исследования частот встречаемости описанных генотипов у пациентов с ССЗ, указывает на связь между ними и уровнем АД, а также риском развития АГ и СН. Также была обнаружена связь между аллелями риска генов АСЕ, AGT и AGTR1 и поражением органов-мишеней у пациентов с АГ, включая развитие гипертрофии ЛЖ [33].
Краткая характеристика БРА 1-го типа. Механизм действия препаратов из группы БРА 1-го типа препаратов заключается в воздействии на рецепторы ангиотензина-II 1-го типа (АТ1-рецепторы), блокируя которые, БРА способствуют повышению уровня АНГ-II в плазме крови, что ведет к стимуляции рецепторов 2-го типа (АТ2), ответственных за реализацию таких благоприятных для пациента эффектов, как стимуляция ангиогенеза, антиапоптоза, вазодилатации [16].
В настоящее время группа БРА представлена 4 подгруппами, различающимися по химической структуре:
- бифениловые производные тетразола (лозартан, ирбесартан, кандесартан);
- небифениловые производные тетразола (телмисартан);
- небифениловые нететразолы (эпросартан);
- негетероциклические соединения (валсартан) [34].
БРА различаются также по характеру связывания с рецепторами. Они могут связываться с рецептором обратимо и необратимо, что влияет на выраженность и длительность фармакологического эффекта. Так, лозартан, валсартан, ирбесартан, кандесартан, телмисартан выступают как неконкурентные антагонисты ангиотензиногена-II, а эпросартан, напротив, являются конкурентным антагонистом ангиотензиногена II [34].
К преимуществам терапии БРА относятся хорошая переносимость, метаболическая инертность (препараты не влияют на сердечный ритм, бронхиальную проходимость, эректильную функцию), меньшее по сравнению с иАПФ число наблюдаемых побочных эффектов: БРА реже провоцируют развитие кашля, гиперкалиемии и ангионевротического отека. БРА действуют вне зависимости от возра-ста, пола, расы при любом варианте гемодинамики. Благодаря всему вышеперечисленному отмечается высокая приверженность больных их приему [34, 35]. Однако у ряда пациентов снижение эффективности и увеличение частоты побочных эффектов при приеме БРА могут быть обусловлены генетическими особенностями индивида. Выявление ассоциаций генетических полиморфизмов с данными особенностями может способствовать таргетному назначению препаратов группы БРА именно тем пациентам, которым они наиболее показаны в соответствии с принципами персонифицированного назначения лекарственных препаратов.
Особенности терапии БРА на фоне генетических полиморфизмов РААС. Для подтверждения предположения о влиянии генетических полиморфизмов компонентов РААС на выраженность фармакологического ответа на препараты группы БРА (лозартана, ирбесартана, валсартана, кандесартана, телмисартана) проведен ряд исследований.
В исследовании влияния полиморфизма CYP11B2 rs1799998–344C>T на эффективность лечения валсартаном в китайской популяции генетические вариации CYP11B2 не только были ассоциированы с АГ, но и определяли фармакологический ответ. В группе 345 больных АГ частота встречаемости аллеля C была значительно выше, чем в группе 157 здоровых лиц. Сочетание мажорных аллелей СС+СT также превалировало у больных АГ. После 4 недель терапии валсартаном в выборке пациентов с гаплотипом CC+CT наблюдалось значимое снижение систолического, диастолического АД, среднего АД по сравнению с носителями аллелей TT. Таким образом, гомозиготный вариант CC CYP11B2 является определяющим для появления более активного антигипертензивного эффекта на терапию валсартаном вследствие изменения количества АС и повышения уровня альдостерона у пациентов в связи с индуцированием прерывания синтеза альдостерона на этапе разрывания комплекса ангиотензиноген-II–рецептор при той же дозе препарата, что у гетерозиготных пациентов (пациентов с Т-аллелем) [36].
В двойном слепом рандомизированном клиническом исследовании SILVHIA проанализирована зависимость выраженности антигипертензивного эффекта при терапии ирбесартаном и атенололом от наличия полиморфизма гена ACE I/D. При применении ирбесартана у гомозиготных по аллелю I антигипертензивный эффект выражен значительно сильнее, чем у носителей аллеля D. При этом результатов в пользу наличия корреляции между генотипом пациента и выраженностью фармакологического ответа при терапии атенололом выявлено не было[11].
В когортном исследовании 353 пациентов китайского происхождения (168 здоровых и 185 лиц с АГ) подтверждена связь наличия в генотипе вариантов гена ABCB1 с эффективностью терапии ирбесартаном. Первоначально результаты множественной линейной регрессии не показали каких-либо статистически значимых различий в изменении АД после применения ирбесартана пациентами с каждым из возможных генотипов. Однако метод сглаживания данных одномерными сплайнами показал, что терапия ирбесартаном при его концентрации в плазме крови более 300 нг/мл оказывает различное влияние на снижение АД у пациентов с разными вариантами генотипа ABCB1. Был сделан следующий вывод: разные реакции на ирбесартан среди носителей разных генотипов AGTR1 были обусловлены разнообразием конъюгированного с ирбесартаном белка, который отвечает за перекрестно-связанные внутриклеточные рецепторы, связанные с G-белком (GPCR) [37, 38].
В рандомизированном контролируемом заслепленном исследовании лиц европеоидной расы в малых группах был также проведен анализ влияния полиморфизма генов AGT, BDKRB2, ADD1, NOS3, T786C (rs 2070744), а также A1166C на эффективность лечения пациентов с ХСН кандесартаном. Гомозиготы по мажорному аллелю AGTR1 A1166 имели более выраженное снижение систолического и диастолического АД по сравнению с носителями аллеля C через 2 недели терапии при применении одинаковых доз препарата. При этом носители аллеля C1166 через 6 месяцев терапии демонстрировали более низкий уровень натрий-уретического пептида (NT-proBNP) по сравнению с пациентами с генотипом AA1166 [34, 39].
Существенные различия в антигипертензивном эффекте лозартана обнаружены у лиц с полиморфизмами генов REN (rs2368564) и AGTR1: носители АА-генотипа (G83A) гена REN имели значимо (p<0,05) более низкий фармакологический ответ на терапию лозартаном, чем лица с генотипами GG и GA [40, 41].
В испанском клиническом исследовании изучена связь между четырьмя полиморфизмами генов РААС и реакцией на снижение АД, а также развития микроальбуминурии как побочного эффекта у 206 пациентов с АГ, получавших телмисартан 80 мг/сут в течение 12 месяцев. Пациентов обследовали на наличие варианта A-6G гена ангиотензиногена, полиморфизма I/D ACE и вариантов A1166C и C573T (rs1045642) гена AGTR1. Не было обнаружено значимой связи между наличием полиморфизма какого-либо гена со снижением АД или развитием микроальбуминурии после лечения телмисартаном [42]. В то же время открытое несравнительное исследование группы пациентов, принимавших телмисартан в дозировке 40–80 мг/сут в течение 24 недель, продемонстрировало зависимость эффективности терапии от наличия у больного полиморфизма I/D ACE: пациенты с генотипом ID продемонстрировали более значительное уменьшение индекса массы ЛЖ, а также улучшение характеристик диастолической функции, чем пациенты с генотипами-II и DD [43].
В клиническом ретроспективном исследовании 281 пациента, принимавшего валсартан в течение 4 недель, проанализирована связь между антигипертензивным эффектом препарата и наличием полиморфного варианта A1166C гена AGTR1, а также полиморфизма CYP2C9*3 гена CYP2C9 цитохрома Р-450. В результате получена статистически значимая связь между наличием у пациента генотипа CC или AC AGTR1 и эффективностью антигипертензивной терапии валсартаном. Не было обнаружено связи между полиморфным вариантом гена CYP2C9 у пациентов и выраженностью антигипертензивного эффекта от данного препарата [44].
Фимасартан – БРА, выпущенный в марте 2011 г., в двойном слепом рандомизированном исследовании показал более высокую эффективность и профиль безопасности среди пациентов с АГ по сравнению с кандесартаном. Отмечается также высокая скорость фармакологического ответа, однако не было обнаружено исследований, посвященных изучению взаимосвязи наличия у пациентов определенных полиморфизмов генов РААС и выраженностью антигипертензивного эффекта при терапии фимасартаном [45].
Генетические исследования компонентов РААС показали, что полиморфизмы той генной сети, взятые по отдельности или в гаплотипе, могут выступать в качестве наследственных маркеров различных ССЗ.
Полиморфизм генов белков РААС вносит существенный вклад в формирование индивидуального фармакологического ответа и является особенностью пациентов, которую необходимо учитывать при подборе антигипертензивной терапии. Была выявлена взаимосвязь с эффективностью применения БРА 1-го типа у пациентов с различными генотипами. При терапии валсартаном более выраженный антигипертензивный эффект наблюдался у носителей аллеля CC гена, кодирующего АС. Применение ирбесартана пациентами с полиморфизмом (ACE) I/D, гомозиготными по аллелю-I, также показало наиболее выраженный эффект. Терапия кандесартаном наиболее эффективна у лиц, гомозиготных по мажорному аллелю AGTR1 A1166. Более выраженный фармакологический ответ на терапию лозартаном характерен для гомозигот по аллелю CC гена AGTR1 [37]. Но в то же время данные о связи между наличием полиморфизма генов и изменением фармакологического ответа на телмисартан противоречивы [42, 43].
На фармакологическом рынке появляются новые лекарственные препараты, например фимасартан. Однако данные о взаимосвязи эффективности терапии с определенным гаплотипом могут быть получены только после накопления достаточного опыта применения нового вещества.
Заключение
Несмотря на массу исследований влияния генов РААС на АГ, использование тестирования на генетические полиморфизмы при назначении терапии достаточно ограничено. В то же время молекулярно-генетическое исследование может повышать эффективность лечения и снижать число побочных эффектов. Имеющиеся данные позволяют предположить, что выявление аллельных вариантов генов, кодирующих компоненты РААС, может способствовать дифференцированному подходу к выбору отдельных БРА. Однако в настоящее время еще нет достаточной доказательной базы для выработки какой-либо стандартной панели полиморфизмов, оценка которых позволила бы разработать клинические рекомендации по персонифицированному выбору препаратов обсуждаемой группы.
Вклад авторов. Н.В. Изможерова, А.А. Попов, М.А. Шамбатов – идея исследования, поиск и отбор источников, обсуждение результатов, написание статьи, финальное редактирование текста. М.А. Гренадерова, М.Д. Шамилов – обсуждение результатов, написание статьи, редактирование текста. А.Е. Бортник, К.А. Вишнева – поиск и отбор источников, обсуждение результатов, написание статьи.
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы Гренадеровой М.А.: «Клинический профиль пациенток с хронической сердечной недостаточностью, полиморфизмом генов ренин-ангиотензин-альдостероновой системы и различной активностью нейрогуморальных факторов».



