Введение
Хроническая сердечная недостаточность (ХСН) является одной из наиболее значимых проблем современной кардиологии. Заболеваемость ХСН увеличивается с возрастом, причем доля женщин выше, чем мужчин во всех возрастных группах. Помимо высокой распространенности ХСН связана со значительным снижением качества жизни и повторной госпитализацией. По некоторым данным, заболеваемость ХСН составляет около 26 млн человек во всем мире [1].
В развитых странах распространенность этого заболевания составляет от 1 до 2% среди взрослого населения [2, 3]. Средняя распространенность ХСН у взрослых старше 60 лет составляет 11,8% [4], и по прогнозам на будущее, в ближайшие 20 лет этот показатель увеличится на 50% [5].
Распространенность ХСН I–IV функциональных классов (ФК) по классификации Нью-Йоркской кардиологической ассоциации (NYHA) за период с 1998 по 2017 г. увеличилась с 6,1до 8,2%, а ХСН III–IV ФК по NYHA – c 1,8 до 3,1% [6, 7]. Прогноз неблагоприятного исхода в виде госпитализации по поводу ХСН остается высоким в группе пациентов III–IV ФК. Кроме того, риск неблагоприятного исхода увеличивается, исходя из наличия сопутствующих патологий у пациента. Именно поражение органов-мишеней является предиктором неблагоприятного прогноза у пациентов данной категории.
Одним из таких заболеваний является сахарный диабет 2 типа (СД2). По данным Федерального регистра, больных СД2 насчитывается около 3% от всего населения страны. Коморбидность составляет около 44% [8, 9]. Среди женщин риск развития сердечной недостаточности (СН) в 5,0, а среди мужчин в 2,4 раза выше, чем у лиц без СД2 [10]. Причиной развития ХСН на фоне СД2 служат диабетическая кардиомиопатия и поражения коронарных артерий, что в свою очередь приводит к увеличению объема внеклеточной жидкости с течением времени. Адекватный контроль уровня гликемии с помощью ингибиторов натрий-глюкозного котранспортера 2-го типа (SGLT2) позволяет предотвращать вероятное развитие ХСН.
Ингибиторы SGLT2 – новый класс сахароснижающих средств, которые действуют путем ингибирования реабсорбции глюкозы в почках за счет подавления SGLT2. Клинический эффект достигается за счет глюкозурии. Представители данного класса – дапаглифлозин и эмпаглифлозин. Эта группа препаратов одобрена к применению в США (FDA), Европе (EMEA), в России с 2014 г. Ряд крупных рандомизированных клинических исследований (РКИ), таких как DAPA-HF, DELIVER, EMPA-REG OUTCOME, EMMY, демонстрируют, что ингибиторы SGLT2 значительно снижают частоту госпитализаций и смертность от сердечно-сосудистых заболеваний [11–14].
Цель обзора: оценка эффективности и безопасности применения ингибиторов SGLT2 у пациентов с ХСН на фоне СД2.
Материал и методы
Произведен поиск крупных завершенных рандомизированных плацебо-контролируемых исследований ингибиторов SGLT2 с помощью баз данных PubMed, Cochrane Library, направленных на оценку сердечно-сосудистых исходов у пациентов с ХСН на фоне СД2. Исследования были сопоставимыми по критериям включения и исключения.
Критерии включения в исследование: дизайн исследования (завершенные РКИ III фазы, оценка эффективности и безопасности ингибиторов SGLT2 у пациентов с ХСН на фоне СД2), популяция (возраст ≥18 лет, наличие структурных заболеваний сердца и проявление застойных явлений в кровотоке, фракция выброса [ФВ]≤50%), вмешательство (применение дапаглифлозина или эмпаглифлозина по сравнению с плацебо), госпитализация по поводу СН в течение предыдущих 12 месяцев.
Критерии невключения в исследование: обсервационные исследования, диагностические исследования и эксперименты на животных, СД 1 типа, расчетная скорость клубочковой фильтрации (рСКФ) <30 мл/мин/1,73 м2, систолическое артериальное давление (САД)<95 мм рт.ст., острый или предшествующий инфаркт миокарда (ИМ), печеночная и почечная дисфункции средней и тяжелой степеней.
Результаты
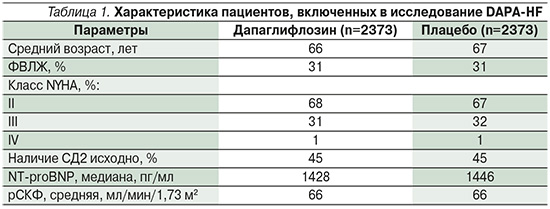
Одним из крупномасштабных и продолжительных РКИ является DAPA-HF. Это первое клиническое исследование, в котором дапаглифлозин, препарат группы SGLT2, назначался не с целью коррекции СД, а для лечения ХСН с ФВ<40%. В исследовании DAPA‐HF (NCT03036124) сравнивали эффективность и безопасность применения дапаглифлозина в дозе 10 мг и плацебо у пациентов со стабильным течением ХСН со сниженной ФВ левого желудочка (ФВЛЖ) в дополнение к стандартной терапии. В исследовании приняли участие 4744 пациента с ХСН. Медиана наблюдения составила 18,2 месяца. Пациенты были рандомизированы в две группы. Число больных СД2 было не менее 30% в каждой группе.
В первой группе пациенты получали дапаглифлозин в дозе 10 мг/сут. в дополнение к базовому лечению. Контрольная группа получала плацебо.
Критерии невключения: терапия ингибитором SGLT2 в течение 8 недель или его непереносимость, наличие СД1, гипотензия с симптоматикой, либо САД менее 95 мм рт.ст., острая декомпенсация СН в настоящее время либо госпитализация по поводу декомпенсации СН в течение 4 недель, коронарная реваскуляризация (чрескожное коронарное вмешательство или коронарное шунтирование), репаративные вмешательства/протезирование клапанов или установка устройства для сердечной ресинхронизирующей терапии в течение последних 12 недель, СН в связи с рестриктивной кардио-миопатией, активным миокардитом, констриктивным перикардитом, гипертрофической кардиомиопатией либо первичными клапанными пороками без репаративных вмешательств, рСКФ менее 30 мл/мин/1,73 м2.
Первичная конечная точка оценки эффективности: госпитализация по поводу СН, обращение за неотложной помощью по поводу СН, смерть по сердечно‐сосудистым причинам.
Вторичная конечная точка: время до первого наступления любого из компонентов комбинированной конечной точки, такие как сердечно-сосудистая смерть, либо госпитализация по поводу СН, изменение баллов по шкале общей оценки симптомов по KCCQ (Kansas City Cardiomyopathy Questionnaire – опросник для пациентов с кардиомиопатией клиники Канзас-Сити) за 8 месяцев, время до первого наступления любого из компонентов комбинированной конечной точки: стойкое снижение рСКФ на ≥50%, либо наступление терминальной ХПН, либо смерть от ХПН.
Критерии включения в исследование представлены в табл. 1.
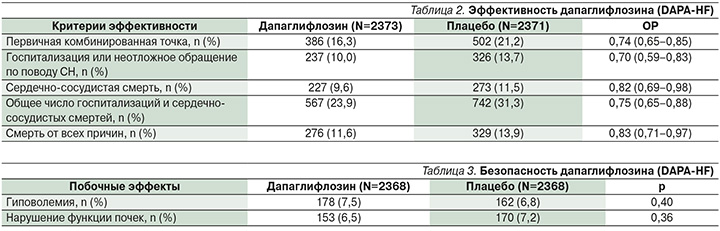
Результаты исследования DAPA-HF (табл. 2) демонстрируют снижение как первичных, так и комбинированных конечных точек (см. рисунок): снижение частоты госпитализаций по поводу СН или сердечно-сосудистой смерти на 25% (отношение рисков [ОР]=0,75, 95% доверительный интервал [ДИ]: 0,65–0,85; p=0,00002). За 8 месяцев применения дапаглифлозина улучшились общие показатели симптоматики по KCCQ (+6,1±18,6 балла) по сравнению с плацебо (+3,3±19,2 балла). Ухудшение показателей со стороны функции почек имели место у 1,2% пациентов в группе дапаглифлозина и у 1,6% пациентов в группе плацебо (ОР=0,71, 95% ДИ: 0,44–1,16; p=0,17).
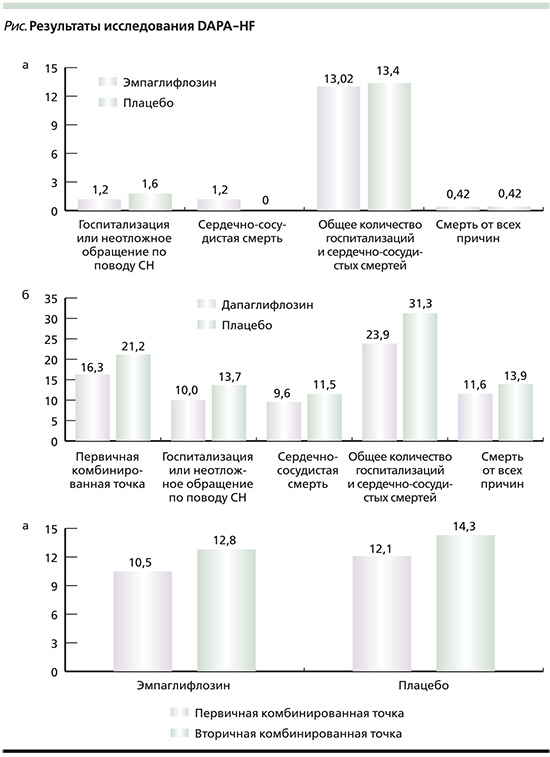
Эффективность дапаглифлозина была сопоставимой в группах и не зависела от возраста участников, степени снижения ФВ, уровня NT‐proBNP, наличия или отсутствия СД2, индекса массы тела, а также уровня рСКФ.
Оценка безопасности применения дапаглифлозина свидетельствует о том, что различий в побочных эффектах между дапаглифлозином и плацебо в целом или по категориям оценки риска не было (табл. 3).
В дополнение к DAPA-HF было инициировано исследование DELIVER для оценки применения дапаглифлозина у пациентов с ХСН и сохраненной ФВ [15–17]. DELIVER – международное рандомизированное двойное слепое плацебо-контролируемое сравнительное исследование III фазы, проводимое в параллельных группах и разработанное для оценки эффективности применения дапаглифлозина по сравнению с плацебо при лечении пациентов с СН с ФВ более 40% и сопутствующим СД2 или без него. В исследовании пациенты получали дапаглифлозин 10 мг 1 раз в сутки в дополнение к стандартной терапии. DELIVER – крупнейшее на сегодняшний день клиническое исследование, в которое включены пациенты с СН и ФВЛЖ более 40% (6263 пациента).
В исследование не включались пациенты, принимавшие ингибиторы SGLT2 в течение 4 недель до рандомизации, непереносимостью ингибиторов SGLT2, с наличием СД1, рСКФ<25 мл/мин/1,73 м2 при скрининге, САД≥160 мм рт.ст., если не было антигипертензивной терапии тремя и более препаратами, илиСАД≥180 мм рт.ст. независимо от количества препаратов.
Для объективности результатов первичные конечные точки оценивались как во всей популяции, так и у пациентов с ФВЛЖ<60% [18–20]. Согласно результатам исследования DELIVER, дапаглифлозин продемонстрировал снижение риска сердечно-сосудистой смерти или ухудшения течения СН, которое определялось как госпитализация или неотложное обращение по поводу СН, на 18% (ОР=0,82, 95% ДИ: 0,73–0,92; р<0,001 при медиане наблюдения в 2,3 года). Продемонстрирована устойчивая эффективность дапаглифлозина во всех подгруппах пациентов. Снижение риска сердечно-сосудистой смерти и ухудшения течения СН было отмечено у пациентов вне зависимости от ФВ. Результаты исследования также продемонстрировали улучшение общей оценки пациентами симптомов по итогам заполнения KCCQ. Согласно данным объединенного мета-анализа, в котором приняли участие 11 007 пациентов, включенных в исследования DAPA-HF и DELIVER, подтверждено достоверное снижение частоты госпитализаций по поводу ухудшения течения СН на фоне терапии дапаглифлозином, а также сердечно-сосудистой смерти и смерти от всех причин вне зависимости от значения ФВ [21].
Еще одним представителем ингибиторов SGLT2, показавшим эффективность у пациентов с ХСН на фоне СД2, является эмпаглифлозин. Исследование EMMY было направленно на оценку эффективности применения эмпаглифлозина у пациентов с острым ИМ независимо от диабетического статуса [22]. В исследование были включены 476 пациентов с острым ИМ, значительным повышением уровня креатинкиназы (более 800 МЕ/л) через 72 часа после чрескожного коронарного вмешательства. Участники исследования были рандомизированы в 2 равные группы, первая получала эмпаглифлозин в дозировке 10 мг/сут., контрольная – плацебо.
Первичная конечная точка: изменение уровня NT-proBNP от рандомизации до 26-й недели.
Вторичная конечная точка: изменение уровня NT-proBNP от рандомизации до 6-й недели, изменение ФВЛЖ от рандомизации до 6-й и 26-й недель, ЭхоКГпараметры диастолической дисфункции, конечные систолический и диастолический объемы, изменение уровня кетоновых тел, изменение уровня гликированного гемоглобина, изменение массы тела.
За дополнительные конечные точки были приняты число госпитализаций и их продолжительность по поводу СН или других причин, а также смертность от всех причин. В ходе исследования 26 (5,5%) пациентов преждевременно прекратили прием исследуемого препарата, 12 (2,5%) участников отозвали информированное согласие. За 26 недель наблюдения среднее значение NT-proBNP было на 15% (95% ДИ от -4,4 до -23,6%) ниже в группе эмпаглифлозина. По результатам ЭхоКГ отмечена положительная динамика в группе эмпаглифлозина по сравнению с плацебо. У пациентов с ХСН повышенная потребность миокарда в кислороде может обеспечиваться кетоновыми телами. По концентрации кетоновых тел группа эмпаглифлозина превзошла группу плацебо более чем на 75% (ОР=23,4%, 95% ДИ: 5,9–42,4%; р=0,0066). По частоте серьезных побочных эффектов различий не было. За весь период наблюдения госпитализированы 63 участника, 7 из них были госпитализированы по поводу ХСН.
EMPA-REG OUTCOME – многоцентровое плацебо-контролируемое РКИ пациентов с СД2 и высоким кардиоваскулярным риском. В исследовании приняли участие 7020 пациентов, из них 2333 получали плацебо, 4687 – эмпаглифлозин в дополнение к стандартной сахароснижающей терапии, из них 2345 – эмпаглифлозин 10 мг/сут, 2342 – эмпаглифлозин 25 мг/сут.
В исследовании приняли участие пациенты с высоким риском развития сердечно-сосудистых событий. Медиана длительности лечения составила 2,6, медиана наблюдения – 3,1 года.
Первичная конечная точка (комбинированная): смерть от сердечно-сосудистых заболеваний, нефатальные ИМ и острое нарушение мозгового крово-обращения (ОНМК).
Вторичные конечные точки: сердечно-сосудистая смерть (включая фатальный инсульт и фатальный ИМ), нефатальные ИМ и ОНМК, госпитализация по поводу нестабильной стенокардии.
Различие между сравниваемыми группами достигнуто за счет снижения сердечно-сосудистой смертности на 38% (ОР=0,62, 95% ДИ от 0,49 до 0,77; р<0,001), смерти от любых причин на 32% (ОР=0,68, 95% ДИ от 0,57 до 0,82; р<0,001) и госпитализации по поводу СН на 35% (ОР=0,65, 95% ДИ от 0,50 до 0,85; р=0,002).

Таким образом, у пациентов с СД2 с высоким риском сердечно-сосудистых осложнений, получавших эмпаглифлозин, частота основного комбинированного сердечно-сосудистого исхода и смертности от любой причины была значительно ниже (табл. 5), чем у пациентов в группе плацебо, когда исследуемые препараты были добавлены к стандартной терапии [23].
Серия исследований EMPEROR последовательно продемонстрировала улучшение исходов ХСН при применении эмпаглифлозина независимо от ФВ и наличия СД2. Исследование EMPEROR-Preserved – многоцентровое плацебо-контролируемое РКИ. Цель данного исследования заключалась в оценке влияния эмпаглифлозина на прогноз и качество жизни пациентов с ХСН со сниженной ФВЛЖ. В исследование были включены 5988 пациентов с ХСН со сниженной ФВЛЖ и ФВ>40% независимо от наличия СД2. Результаты показали, что применение эмпаглифлозина способствует снижению риска смерти от коронарных событий на 21% (ОР=0,79, 95% ДИ: 0,69–0,90; р<0,001) и общее число госпитализаций в связи с ухудшением течения ХСН в группе эмпаглифлозина по сравнению с плацебо меньше на 27% (ОР=0,73, 95% ДИ: 0,61–0,88; р<0,001).
Таким образом, по результатам исследования DELIVER, дапаглифлозин продемонстрировал снижение риска сердечно-сосудистой смерти.
По данным международного рандомизированного плацебо‐контролируемого исследования DAPA‐HF с участием пациентов с ХСН со сниженной ФВЛЖ, риск событий комбинированной конечной точки был ниже в группе дапаглифлозина на 30% (ОР=0,70, 95% ДИ: 0,59–0,83).
Результаты оценки безопасности свидетельствуют о том, что большинство показателей были сопоставимыми в обеих группах. С учетом благоприятного профиля безопасности дапаглифлозин может быть рассмотрен в качестве дополнения к стандартной терапии ХСН со сниженной ФВ левого желудочка с целью улучшения прогноза выживаемости и снижения числа госпитализаций в связи с ухудшением течения ХСН.
По результатам исследования EMPEROR-Reduced, эмпаглифлозин продемонстрировал положительное влияние на риск сердечно‑сосудистой смерти или госпитализации по причине ХСН, риск снижения функции почек и число госпитализаций независимо от наличия СД. Субанализ исследования EMPEROR‑Reduced показал, что у больных ХСН эмпаглифлозин снижал риск первой и повторной госпитализаций по поводу СН на 30%. Результаты в подгруппах не зависели от наличия или отсутствия СД.
По данным исследования EMPA-REG OUTCOME, при добавлении эмпаглифлозина к стандартной терапии в дозировке как 10, так и 25 мг смертность от сердечно-сосудистых причин, нефатальный ИМ или нефатальный инсульт наступали у 10,5% пациентов по сравнению с плацебо, где процент нефатальных осложнений составил 12,1%. Пациентов со сниженной ФВ лечение эмпаглифлозином привело к снижению риска обострения СН в стационарных и амбулаторных условиях на 30%. При применении эмпаглифлозина не наблюдалось повышенного риска гипогликемии, однако в ряде случаев у пациентов отмечалась гипогликемия, но возникшая гипогликемия не уменьшала кардиопротекторного эффекта.
Заключение
Таким образом, класс ингибиторов иНГЛТ-2 улучшает как прогноз, так и качество жизни пациентов с ХСН со сниженной ФВЛЖ. Результаты завершенных исследований наглядно демонстрируют эффективность и безопасность применения ингибиторов SGLT2 в кардиологической практике, что позволяет с уверенностью говорить о дальнейшем их внедрении в практику независимо от наличия или отсутствия СД. В настоящее время ингибиторы SGLT2 вошли в клинические рекомендации Европейского общества кардиологов с уровнем доказательности IA [24].
Вклад авторов. В.И. Петров, О.В. Шаталова – концепция и дизайн исследования. М.С. Клыкова – сбор и обработка материала. М.С. Клыкова, Н.П. Стецкий – написание текста. О.В. Шаталова – редактирование.



