Хроническая абдоминальная боль – одна из основных проблем гастроэнтерологии, абдоминальной хирургии, также достаточно часто она встречается в практике врачей скорой помощи и участковых терапевтов. В настоящее время подходы к терапии хронической абдоминальной боли разнообразны, спектр препаратов, представленных на фармакологическом рынке, довольно широк. Вместе с тем выбор лекарственного средства для купирования абдоминальной боли подчас является затруднительным в связи с многообразием причин и механизмов ее развития.
Особую сложность представляет трактовка механизмов формирования абдоминального болевого синдрома при функциональных расстройствах пищеварительной системы, т. е. хронической абдоминальной боли функционального характера. В настоящее время в практике используется третий пересмотр положений о функциональных расстройствах пищеварительного тракта – Римские критерии III (2006) [1, 2]. В качестве возможных причин и механизмов развития функциональных расстройств были определены нарушения моторики, висцеральная гиперчувствительность внутренних органов, показана роль воспаления, а также влияния психосоциальных факторов и нарушения регуляции основных функций желудочно-кишечного тракта (ЖКТ) (центральной, периферической, гуморальной).
Классификация функциональных гастроинтестинальных расстройств (Римские критерии III):
А. Пищеводные расстройства:
А1. Комок в горле.
А2. Регургитация, срыгивание.
А3. Функциональная боль за грудиной преимущественно пищеводного генеза.
А4. Функциональное жжение за грудиной.
А5. Функциональная дисфагия.
А6. Неспецифические (неопределенные) пищеводные дисфункции.
В. Гастродуоденальные расстройства (функциональная диспепсия, аэрофагия, функциональная тошнота и рвота, постпрандиальный дистресс-синдром, эпигастральный болевой синдром).
C. Кишечные расстройства:
C1. Синдром раздраженного кишечника (СРК).
C2. Функциональное вздутие живота.
C3. Функциональный запор.
C4. Функциональная диарея.
C5. Неспецифические (неопределенные) функциональные расстройства кишечника.
D. Функциональная абдоминальная боль:
D1. Синдром функциональной абдоминальной боли.
D2. Неспецифическая (неопределенная) абдоминальная боль.
Е. Билиарные расстройства:
Е1. Дисфункция желчного пузыря.
Е2. Дисфункция сфинктера Одди (по билиарному типу, по панкреатическому типу).
F. Аноректальные расстройства.
G. Функциональные расстройства у детей.
Гастроинтестинальный тракт находится под влиянием многих регуляторных систем, таких как центральная нервная система, периферическая нервная система (симпатическая и парасимпатическая), энтеральная нервная система, а также нейротрансмиттеров. Сбой в процессе взаимодействия органов ЖКТ и регуляторных систем приводит к моторным нарушениям как гипертонического, так и гипо- и атонического характера; кроме того, могут иметь место сочeтанные варианты нарушения моторики; как следствие – у пациента появляются жалобы на абдоминальную боль [3, 4].
Подход к лечению функциональных расстройств, в частности абдоминальной боли как одного из проявлений функциональных нарушений, достаточно сложен. Основными препаратами, используемыми в клинической практике с целью купирования болевого синдрома, являются спазмолитики [5, 6] (см. таблицу).
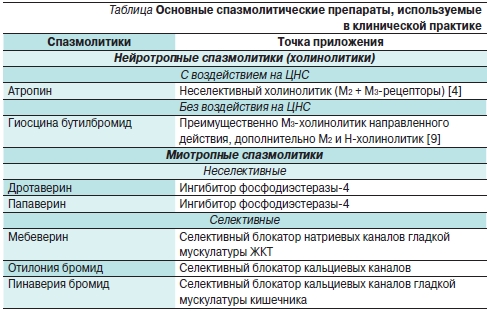
Наряду со спазмолитиками в клиничоеской практике для купирования синдрома абдоминальной боли используются препараты с другими точками и уровнями воздействия на регуляцию гладкомышечных сокращений ЖКТ: аналоги соматостатина, антагонисты холецистокинина, антагонисты 5-гидрокситриптамина-3, антидепрессанты, а также агонист опиоидных рецепторов тримебутин.
Развитие современной медицины напрямую связано с внедрением в клиническую практику новых высокотехнологичных методов обследования и лечения. В настоящее время для адекватного подбора корригирующей терапии с учетом преобладающего у пациента типа нарушений моторики целесообразно использовать метод периферической электрогастроэнтерографии (ЭГЭГ), который в настоящее время становится все более популярным, о чем свидетельствуют многочисленные исследовательские работы в данной области. В основе метода лежит учение о сензитивности гладкомышечной ткани, вследствие которой определенные зоны ЖКТ действуют как электрические водители ритма – пейсмейкеры, от них волна деполяризации распространяется на другие отделы кишечной трубки, и именно это свойство гладкомышечной ткани определяет моторно-эвакуаторную функцию ЖКТ.
Электрофизиологические методы исследования моторно-эвакуаторной функции гастроинтестинального тракта можно разделить на две группы: прямая ЭГЭГ-регистрация электрических потенциалов с помощью вживленных в стенку органа электродов или со стороны слизистой оболочки с помощью электродов зонда; периферическая ЭГЭГ-регистрация электрической активности с поверхности тела – брюшной стенки или конечностей. Необходимость имплантировать электроды в стенку органа и невозможность оценить биоэлектрическую активность всех отделов ЖКТ ограничивают использование прямой ЭГЭГ в повседневной клинической практике. При проведении непрямой (периферической) ЭГЭГ возможна регистрация электрической активности органов ЖКТ как в целом, так и в конкретном отделе (желудке, двенадцатиперстной, тощей, подвздошной и толстой кишке), а также определение соотношений изменений электрической активности рядом лежащих отделов, что отражает скоординированность работы различных отделов. Учитывая неинвазивный характер и простоту данной методики, можно повторять исследование необходимое число раз, не влияя на психику пациента отрицательно. Благодаря этому существует возможность длительного беззондового исследования моторной деятельности различных отделов ЖКТ как натощак, так и после пищевой стимуляции стандартным завтраком, а также после приема различных лекарственных препаратов, что особенно важно для диагностики функциональной патологии. Возможность проведения многократных исследований позволяет также оценивать моторную функцию как до, так и в процессе лечения, при необходимости индивидуально корригировать терапию. К методике периферической ЭГЭГ отсутствуют противопоказания. Кроме того, метод позволяет проводить мониторинг моторно-эвакуаторной функции ЖКТ в течение длительного времени (от 2 до 48 часов) [7, 8].
Для проведения периферической ЭГЭГ в нашей клинике используется прибор гастроэнтеромонитор ГЭМ-01 “Гастроскан-ГЭМ” (рис. 1), созданный НПП “Исток-Система”, Фрязино. Оцениваемый сигнал электрической активности ЖКТ обрабатывается оригинальной программой с использованием алгоритмов быстрого преобразования Фурье и Вейвлет. Аппарат обеспечивает прием и регистрацию сигнала с накожных электродов, а также хранение, обработку и документальное представление получаемой информации.

При анализе сигнала по мощности используются следующие показатели:
• уровень электрической активности суммарный (PS);
• уровень электрической активности по каждому из обследуемых отделов ЖКТ (Pi);
• Р(i)/PS – относительная электрическая активность каждого отдела ЖКТ, представляет собой отношение абсолютных значений электрической активности в каждом отделе ЖКТ Р(i) к суммарной активности PS, рассчитывается отдельно для каждого отдела ЖКТ;
• коэффициент ритмичности Kritm – отражает ритмичность сокращений, с его помощью можно оценить характер пропульсивных сокращений каждого отдела ЖКТ;
• коэффициент соотношения P(i)/P(i+1), представляет собой отношение электрической активности вышележащего отдела к нижележащему.
Стандартное исследование электрической активности ЖКТ включает два этапа: первый – тощаковое исследование продолжительностью 40 минут, второй этап – исследование после стандартного завтрака продолжительностью 40 минут. При необходимости вместо регистрации ЭГЭГ на фоне пищевой стимуляции во время второго этапа исследования можно проводить запись электрической активности на фоне приема лекарственного средства для адекватного подбора корригирующей терапии конкретному пациенту, а также оценки ее эффективности.
Нами были проанализированы данные ЭГЭГ пациентов, получавших лечение в клинике гастроэнтерологии кафедры пропедевтики внутренних болезней СЗГМУ им. И.И. Мечникова по поводу СРК. Клинически все пациенты предъявляли жалобу на наличие хронической абдоминальной боли. В схемы терапии были включены следующие спазмолитические препараты: дротаверин, мебеверин, гиосцина бутилбромид (Бускопан).
Периферическая ЭГЭГ проводилась по следующей схеме:
• до начала терапии;
• после первого приема спазмолитического препарата;
• через 10 дней на фоне курсового приема спазмолитика.
Изначально у всех пациентов имели место изменения ЭГЭГ. Отмечено повышение показателей Р(i)/PS, Kritm, P(i)/P(i+1) натощак и после пищевой стимуляции на частотах желудка, двенадцатиперстной, тонкой и толстой кишки, а также избыточное нарастание Р(i) после пищевой стимуляции. Усиление двигательной активности органов ЖКТ вызывало развитие гипермоторной дискинезии, клинически проявлявшейся абдоминальной болью спастического характера. Именно это обстоятельство определило выбор препаратов группы спазмолитиков в качестве терапии купирования симптомов СРК у этих больных.
В результате сравнительного анализа были получены следующие данные. На фоне курсового приема различных спазмолитиков отмечено снижение таких показателей, как суммарная мощность (PS) и мощность по каждому из отделов Р(i) натощак, а также после пищевой стимуляции, отсутствие избыточного нарастания Р(i) в верхних отделах на фоне пищевой стимуляции, нормализация (в данном случае – снижение) таких показателей, как Kritm, P(i)/P(i+1) натощак и после пищевой стимуляции на частотах желудка, двенадцатиперстной, тонкой и толстой кишки (рис. 2).
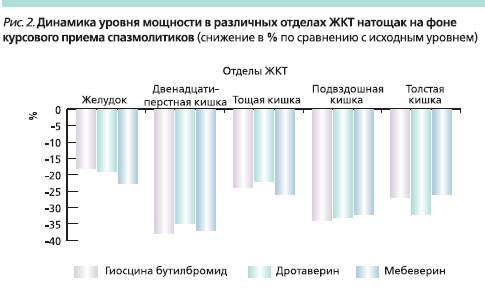
Таким образом, все препараты оказались эффективными, достоверных различий между используемыми спазмолитиками при проведении ЭГЭГ на фоне курсового приема выявлено не было.
Несколько иная картина имеет место при анализе данных ЭГЭГ, проведенных пациентам в течение 40 минут на фоне однократного (первого) приема сравниваемых препаратов (рис. 3). Было отмечено, что прием гиосцина бутилбромида приводит к более быстрому проявлению спазмолитических свойств по сравнению с другими препаратами этой группы, что проявляется в более выраженном снижении моторной активности по таким показателям, как суммарная мощность (PS) и мощность по каждому из отделов Р(i), как следствие – более быстрое купирование абдоминальной боли при однократном приеме.
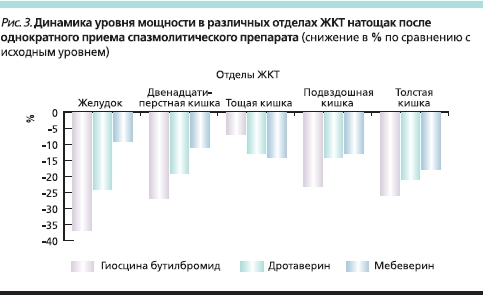
При анализе данных ЭГЭГ пациентов с СРК на фоне курсового приема не отмечено статистически достоверных различий между спазмолитическими препаратами различных групп. При разовом приеме наибольшей спазмолитической активностью в короткий промежуток времени обладает гиосцина бутилбромид. Вероятнее всего это объясняется его двойным спазмолитическим действием путем селективного связывания с мускариновыми рецепторами, расположенными на висцеральных гладких мышцах ЖКТ, и параллельным ганглиоблокирующим действием, что обусловливает быстрое наступление клинического эффекта [9]. Спазмолитик гиосцина бутилбромид (Бускопан) показал себя как эффективное средство терапии “по требованию”, что позволяет рекомендовать его использование в этих целях.



