Запором считают хроническую задержку опорожнения кишечника более чем на 48 часов, что сопровождается чувством неполного опорожнения с отхождением малого количества кала повышенной твердости. Запоры представляют собой серьезную медико-социальную проблему из-за широкой распространенности данного состояния. Так, в Великобритании запорами страдают более 50 % населения, в Германии – более 30 %, во Франции – более 25 %; в России подобная статистика отсутствует, но средние цифры не уступают представленным.
Существует много подходов к классификации запоров. С практической точки зрения важно учитывать длительность запоров (острый – до 3 месяцев, хронический – больше 3 месяцев).
Различают следующие механизмы формирования запоров:
- органический, вызванный механической обструкцией толстой кишки (опухоли, стриктуры, аномалии развития);
- функциональный, вызванный расстройствами функции кишечника;
- проктогенный, обусловленный расстройствами (снижением, утратой) рефлекса на дефекацию.
В данной статье мы рассматриваем функциональные запоры.
Функциональным называется хронический запор, патогенез которого не связан с известными генетическими, структурными, органическими изменениями кишечника, при этом, по критериям международных экспертов (Римские критерии III, 2006), присутствуют два или более из числа следующих признаков:
- редкая эвакуация содержимого кишечника (менее трех дефекаций в неделю);
- отхождение при дефекации малого количества кала (< 35 г/сут);
- отхождение плотного, сухого кала, фрагментированного по типу “овечьего”, травмирующего область заднепроходного отверстия (при этом признак встречается чаще, чем в четверти актов дефекации);
- отсутствие чувства полного опорожнения кишечника (признак встречается чаще, чем в четверти актов дефекации);
- ощущение чувства блокирования содержимого в прямой кишке при потугах (аноректальная обструкция);
- не менее 25 % времени акта дефекации сопровождается натуживанием, иногда возникает необходимость удаления содержимого из прямой кишки при помощи пальца, поддержки пальцами тазового дна (чаще чем в четверти актов дефекации).
Запор считается функциональным в тех случаях, если его симптомы появились по меньшей мере за 6 месяцев до момента диагностики и сохраняются на протяжении по меньшей мере трех последних месяцев до момента диагностики, не обязательно непрерывных; отсутствуют достаточные критерии для диагностики синдрома раздраженного кишечника; самостоятельный стул редко возникает без использования слабительных средств.
Выделяют следующие причины развития функционального запора:
- алиментарные (недостаток балластных веществ и жидкости в рационе, малый объем пищи);
- эндокринные (гипотиреоз, сахарный диабет, гиперпаратиреоз, менопауза);
- лекарственные (прием холинолитиков, опиатов, антидепрессантов, нейролептиков, мочегонных препаратов и др.);
- психогенные (как симптом психических заболеваний, реакция на неблагоприятные условия для опорожнения кишечника);
- неврогенные (паркинсонизм, рассеянный склероз, спинальные расстройства);
- токсические (воздействие свинца, ртути, таллия и других токсических веществ);
- “старческие” (абдоминальная ишемия, гипоксия, снижение репарации тканей, гиподинамия);
- заболевания внутренних органов (хронические заболевания легких, нарушение кровоснабжения, хронические болезни печени).
По типу моторных нарушений толстой шкики функциональные запоры разделяют на следующие типы:
- гиперсегментарный, гиперкинетический;
- гипо- и атонический.
Главными механизмами функционального запора следует считать нарушение синтеза регуляторных интестинальных пептидов, отвечающих за моторику желудочно-кишечного тракта (ЖКТ), деградацию энтеральных нервных сплетений, снижение кровотока в малом тазу, прогрессирующую слабость мышц тазового дна, снижение чувствительности анального сфинктера, нарушение ВИПергической и серотонинеэргической регуляции.
Разнообразие причин развития запора порождает желание упростить подход к диагностике этого состояния. Алгоритм диагностики при первом появлении запора должен быть поэтапным:
1-й этап. Оценка клинических данных (соответствие жалоб пациента принятым критериям запора). Рентгенологическое исследование кишечника, позволяющее оценить анатомическое состояние толстой кишки (ее нормальное строение при функциональных расстройствах, аномалии положения, идиопатический мегаколон, опухоли, стриктуры, болезнь Гиршпрунга, спаечная болезнь).
2-й этап. Колоноскопия с биопсией слизистой оболочки кишки для исключения структурных нарушений. Оценка функций других органов и отделов ЖКТ, эндокринного аппарата, позволяющая установить первичный или вторичный характер запоров. Для женщин обязателен осмотр гинеколога с целью определения положения матки.
3-й этап. Специальные методы исследования, позволяющие оценить моторно-эвакуаторную функцию толстой кишки, состояние запирательного аппарата прямой кишки (электромиография, изотопные методы, дефекография, анальная манометрия, исследования микробного спектра, короткоцепочечных жирных кислот в кале).
Выполненная программа обследования позволит ответить на основной вопрос: вызван ли запор заболеванием, или является функциональным расстройством? Таким образом, диагноз функционального запора – диагноз исключения. И только после того, как диагностика осуществлена, определены формы, подлежащие хирургическому лечению, привлечены к лечению эндокринологи, гинекологи, психотерапевты, проводится длительное лечение у терапевта или гастроэнтеролога.
Основные принципы лечения запоров:
- диетические рекомендации (коррекция рациона питания и водного баланса);
- рекомендации по изменению образа жизни в соответствии с возрастом;
- лечение основного заболевания, вызвавшего запор;
- коррекция негативных медикаментозных влияний;
- физиотерапевтические процедуры (в отсутствие противопоказаний);
- нормализация моторной функции толстой кишки (прокинетики при гипокинезии или спазмолитики при гиперкинезии толстой кишки);
- применение слабительных средств.
Диетические рекомендации пациенту с запорами строятся в зависимости от моторной функции толстой кишки. При гипомоторной дискинезии рацион формируется по типу шлаковой нагрузки. Освобождению кишечника способствуют овощи и фрукты, ягоды, преимущественно сырые, не менее 200 г/сут, чернослив или курага (8–12 ягод), бананы и яблоки, масло растительное (оливковое, кукурузное), 1–2 столовые ложки натощак (лучше размешать в кефире и принимать на ночь), гречневая, овсяная, ячневая, перловая каши, мед (1 столовая ложка 2–3 раза в сутки), пшеничные отруби 20–30 г в сутки (добавлять практически в любые блюда). Отруби включены в специальные сорта хлеба: “Здоровье”, “Барвихинский”, “Докторский”. Количество жидкости следует увеличить (не менее 1,5–2,0 литров в сутки). Целесообразно выпивать 1–2 стакана холодной воды (или фруктового сока) с утра натощак с добавлением 1 столовой ложки меда или ксилита. Из рациона исключают рисовую, манную каши, макароны и вермишель, картофельное пюре, кисели, поскольку эти продукты тормозят опорожнение кишечника. Следует также исключить репу, редьку, щавель, молоко, кофе, крепкий чай, шоколад.
В рационе питания используются пищевые волокна (отруби, микрокристаллическая целлюлоза, Мукофальк – подорожника семенная кожура; псилиум – подорожник, морская капуста; биологически активные добавки с высоким содержанием растворимых и нерастворимых волокон). Обязательным условием применения пищевых волокон является соблюдение водного баланса. Отруби адсорбируют воду, увеличивают число бактерий в толстой кишке, повышают массу фекалий и изменяют миоэлектрическую активность кишечника, приводят в равновесие пропульсивные и тонические сокращения мускулатуры толстой кишки.
Важную роль в регуляции энергетического метаболизма в слизистой оболочке играют жирные кислоты с короткой цепью (ацетат, пропионат, бутират), образующиеся при разрушении пищевых волокон. Пожилым пациентам и больным сердечнососудистыми заболеваниями пищевые волокна следует назначать с большой осторожностью в связи с невозможностью в ряде случаев соблюдения ими водного режима.
Диета при гипермоторной дискинезии толстой кишки более щадящая. Овощи дают в отварном виде, большое внимание уделяют растительным жирам. Пшеничные отруби назначают в постепенно повышающихся дозах (с 2 чайных до 3–6 столовых ложек), то уменьшая, то увеличивая их количество до установления оптимальной дозы, которая будет поддерживать терапевтический эффект.
В лечении запоров помимо диеты важное значение имеет образ жизни: отсутствие утренней спешки, прием “объемного” завтрака, комфортабельный удобный туалет в доме, удобная поза в туалете (с подтянутыми коленями, ноги на маленькой скамеечке), утренняя гимнастика (движение Вальсальвы, имитация езды на велосипеде, самомассаж живота).
Не менее важной задачей представляется воздействие на моторную функцию толстой кишки. При гипомоторной дискинезии может быть использован отечественный препаратТримедат (тримебутин), действующий на опиоидные рецепторы и восстанавливающий физиологический контроль над моторикой. При гипермоторной дискинезии оправданно назначение селективных миотропных спазмолитиков: мебеверина (Дюспаталина) и пинаверия бромида (Дицетела).
Пунктуальное соблюдение рассмотренных рекомендаций часто оказывается достаточным для нормализации стула. Если же стул не нормализуется, приходится прибегать к слабительным средствам, к которым предъявляются следующие требования: появление регулярного оформленного стула, отсутствие осложнений, привыкания, побочных эффектов, предсказуемое время дефекации. Большинство специалистов дифференцируют выбор слабительных средств в зависимости от характера запоров.
Все слабительные средства разделяют на три основные группы:
1. Увеличивающие объем кишечного содержимого:
- пищевые волокна;
- гидрофильные коллоиды (макроголи);
- осмотические: олигосахара (лактулоза – Дюфалак), спирты (сорбитол, маннитол, глицерин), солевые слабительные (магнезия, глауберова соль и др.).
2. Стимулирующие:
- антрагликозиды (препараты сенны, крушины, ревеня);
- производные дифенилметана (бисакодил – Дульколакс);
- пикосульфат натрия (Гутталакс).
3. Размягчающие фекалии: вазелиновое и другие минеральные масла.
У каждой из указанных групп есть свои достоинства и недостатки, и для каждой группы препаратов должна быть своя ниша, определяемая характеристиками запора. К гидрофильным коллоидам относятся многоатомные спирты-макроголи, обладающие умеренно выраженным осмотическим действием и увеличивающим объем кишечного содержимого. Недостатком этих слабительных средств следует считать медленно развивающийся эффект, и у лиц с выраженной гипотонией кишечника эти средства малоэффективны. Кроме того, слабительные этой подгруппы не показаны пациентам с проктогенными запорами.
Осмотические слабительные отличаются друг от друга зоной действия. Так, спирты с короткой углеродной цепью (сорбитол, маннитол, глицерин) и солевые слабительные действуют на уровне тонкой кишки, способствуют выделению в ее просвет больших количеств жидкости. Существенным недостатком этой группы слабительных при систематическом приеме является неконтролируемая диарея с гиповолемией, что может привести к дегидратации и электролитным нарушениям. В настоящее время эти слабительные используются в комплексной подготовке кишечника к исследованиям.
Олигосахара (лактулоза) действуют только в толстой кишке. Обладают двойным механизмом действия – восстанавливают толстокишечный биоценоз, являясь бифидогенным и лактогенным пребиотиком, и увеличивают объем кишечного содержимого за счет осмотического действия и стимуляции бактериального роста.
Размягчающие фекалии средства – вазелиновое и другие масла – действуют на всем протяжении кишечника. Их применяют в случаях, когда нужно достичь быстрого эффекта, например, при отравлениях и у больных в послеоперационном периоде.
У группы стимулирующих слабительных есть существенное достоинство – быстрое достижение послабляющего эффекта. Показания к применению именно стимулирующих слабительных имеют определенные группы пациентов, у которых необходимо получить быстрый результат и которым противопоказано повышение внутрибрюшного давления, а также натуживание. К ним относятся пациенты с сердечно-сосудистыми заболеваниями (инфаркт миокарда, тяжелая артериальная гипертензия, аневризма, тромбозы), отслойкой сетчатки, грыжами.
В порядке самолечения больными особенно широко используются препараты, содержащие антрагликозиды, которые действуют непосредственно на уровне энтеральных сплетений и вызывают выделение веществ, усиливающих пропульсивную активность кишечника. Препараты сены (анрагликозиды) имеют дозозависимый эффект. Доказано, что при длительном применении метаболиты этих препаратов накапливаются в слизистой оболочке кишечника, нейронах ганглионарных сплетений, что ведет к дегенеративным изменениям гладкой мускулатуры и нервных сплетений, а также развитию “инертной толстой кишки”. Метаболиты антрагликозидов гепатои нефротоксичны, обладают мутагенным действием. В связи с этим они не предназначены для длительного, тем более постоянного, применения.
Среди стимулирующих слабительных с учетом недостатков и побочных эффектов антрагликозидов следует отдать предпочтение производным дифенилметана. Представителем этой группы является бисакодил (Дульколакс). Активное вещество бисакодил является контактным слабительным средством, увеличивающим секрецию слизи в толстой кишке. Взаимодействуя с эпителиальными структурами кишечника, это бифенольное соединение вызывает активную секрецию жидкости в его просвет, одновременно уменьшая всасывание воды. Вследствие прямой стимуляции нервных окончаний в слизистой оболочке толстой кишки активный дифенол повышает ее моторику, уменьшая время прохождения кала. Бисакодил подвергается гидролизу (а именно деацетилированию) тонкокишечными ферментами во время всасывания. После глюкоронизации в печени он секретируется обратно в тонкую кишку с желчью. Далее неабсорбируемый глюкоронид поступает в толстую кишку, где происходит его деконъюгация посредством бактериальных ферментов, и в толстой кишке препарат действует как дифеноловое слабительное.
Дульколакс (Берингер Ингельхайм, Германия) имеет кишечнорастворимую оболочку, растворяющуюся лишь при рН = 8,1. Благодаря этой оболочке действующее вещество препарата высвобождается и действует непосредственно в толстой кишке, не абсорбируясь в тонкой кишке. Поскольку отсутствует возврат в энтерогепатическую циркуляцию, Дульколакс действует более быстро по сравнению с ацетилобогащенным бисакодилом.
Бисакодил хорошо изучен, его эффективность подтверждена в рандомизированных клинических испытаниях. Проводились сравнительные исследования эффективности и безопасности Дульколакса и пикосульфата натрия (Гутталакс, Берингер Ингельхайм) при длительном сроке их использования большим числом пациентов, показавшие высокий профиль безопасности обоих препаратов при ежедневном 28-дневном применении. В имеющихся научных источниках даются рекомендации избегать длительного ежедневного приема бисакодилов из-за возможной секреторной диареи, которая может привести к излишней потере жидкости и электролитным нарушениям (прежде всего гипокалиемии). К тому же при ежедневном приеме не удается достичь должного объема кишечного содержимого. При неизбежности регулярного применения этих препаратов следует использовать их минимально короткими курсами по 5–7 дней или 1 раз в 3–4 дня в минимально эффективной дозе, что позволяет в течение длительного времени сохранить к ним чувствительность и избежать негативных последствий. Ректальные суппозитории, содержащие Дульколакс, эффективны при функциональных проктогенных запорах. Скорость развития эффекта Дульколакса в свечах составляет 15–60 минут.
Материал и методы
На кафедре гастроэнтерологии УНМЦ проведено сравнительное изучение эффективности Дульколакса (Берингер Ингельхайм) и Бисакодила (Хемофарм) у 110 пациентов с хроническими функциональными запорами, из которых 55 человек получали Дульколакс (1-я группа) и 55 – Бисакодил (2-я группа). Средний возраст больных в группе Дульколакса составил 64,0 ± 12,8, в группе Бисакодила – 62,5 ± 2,6 года. Длительность болезни составила от 1 года до 35 лет, продолжительность запоров – от 3 до 5–7 дней. До включения в исследование 98 пациентов регулярно пользовались слабительными средствами; чаще всего это были препараты сенны, пикосульфат натрия, лактулоза. Клинические симптомы запора полностью соответствовали Римским критериям III. Для исключения органических изменений в кишечнике у всех больных была выполнена колоноили ирригоскопия в период от месяца до 3 лет до настоящего исследования.
Дульколакс и Бисакодил назначали в дозе 10 мг (или 2 таблетки) 1 раз в сутки на ночь в течение 10 дней, и последующие 10 дней наблюдали за пациентами с целью оценки эффекта последействия. Больные ежедневно заполняли дневник наблюдения. Оценку клинических симптомов пациенты проводили самостоятельно в баллах: 0 – отсутствие симптома; 1 – слабо выражен; 2 – умеренно выражен; 3 – значительно выражен.
Эффективность препаратов оценивали по следующим критериям:
- динамика клинических симптомов в процессе лечения;
- карболеновая проба – время пассажа активированного угля по ЖКТ до и после лечения;
- оценка электромоторной активности толстой кишки по показателям электроколографии до и после применения препаратов;
- уровень летучих жирных кислот в кале до и после курса лечения;
- оценка возможных побочных эффектов препарата или индивидуальной переносимости.
По окончании курса оценивалась общая эффективность лечения по следующей градации: отличным считался эффект купирования всех клинических симптомов; хорошим – значительное уменьшение симптомов; удовлетворительным – ослабление отдельных симптомов; неудовлетворительным – сохранение или нарастание симптоматики.
Результаты
Все пациенты начинали прием сравниваемых препаратов с 2 таблеток, в процессе лечения 42 пациента уменьшили дозу до 1 таблетки (20 человек – на Дульколаксе, 22 – на Бисакодиле), что, соответственно, уменьшило частоту опорожнения в течение последующих дней лечения. Результаты лечения представлены в таблице.
Таблица.Динамика клинических симптомов до и после 10-дневного приема Дульколакса и Бисакодила.
За период лечения в обеих группах форма стула менялась от твердой до мягкой, нормально оформленной и жидкой.
Среднее число дефекаций в день и консистенция стула показали различия в пользу группы Дульколакса. Одновременно уменьшился метеоризм, исчезло ощущение неполного опорожнения кишечника (последнее было менее выражено на фоне Бисакодила). У 35 пациентов перед актом дефекации и непродолжительное время после него появлялись небольшие схваткообразные боли в животе, купирующиеся самостоятельно.
Время карболеновой пробы сократилось с 74 и 72 до 24 и 36 часов соответственно в 1-й и 2-й группах. Таким образом, общее время транзита на фоне приема исследуемых слабительных значительно (в 2–3 раза) сократилось. Время наступления эффекта составило в среднем 6–10 часов у Дульколакса и 10–12 часов у Бисакодила, что дает возможность индивидуализировать прием препаратов с предсказанием ожидаемого эффекта.
Появление неуправляемой выраженной диареи и усиление болей в животе, сопровождающих дефекацию, наблюдались у 4 пациентов (по 2 человека в каждой из групп), что заставило пациентов прекратить исследование на 4–7-е сутки.
Оценка переносимости препаратов в обеих группах соответствовала очень хорошей и хорошей в 80 % случаев на фоне Дульколакса и в 72 % случаев на фоне Бисакодила. В последующие 10 дней самостоятельное опорожнение кишечника наблюдалось в 20 % случаев (у 15 человек в группе Дульколакса и у 7 в группе Бисакодила).
 Электрическая активность на частотах толстой кишки в двух группах пациентов до лечения была значительно ниже нормы. Коэффициент ритмических сокращений в 3–4 раза превышал нормальные показатели, что свидетельствовало о непропульсивных сокращениях толстой кишки. После 10-дневного приема препаратов моторная активность толстой кишки у больных улучшилась. Показатели электромоторной активности заметно возросли на фоне Дульколакса (41,4 ± 21,2 % исходно и 53,39 ± 17,6 % в динамике), в группе Бисакодила эти показатели составляли 55,16 ± 12,6 и 53,4 ± 18,6 % соответственно при норме 64,04 ± 32,01 %. Эти данные свидетельствовали о мягком стимулирующем эффекте Дульколакса на моторику кишечника. Таким образом, преимущество Дульколакса перед Бисакодилом заключалось в более мягком изменении частоты и консистенции стула, достижении полноты опорожнения, более быстром и предсказуемом времени наступления эффекта, более значимом повышении электромоторной активности толстой кишки.
Электрическая активность на частотах толстой кишки в двух группах пациентов до лечения была значительно ниже нормы. Коэффициент ритмических сокращений в 3–4 раза превышал нормальные показатели, что свидетельствовало о непропульсивных сокращениях толстой кишки. После 10-дневного приема препаратов моторная активность толстой кишки у больных улучшилась. Показатели электромоторной активности заметно возросли на фоне Дульколакса (41,4 ± 21,2 % исходно и 53,39 ± 17,6 % в динамике), в группе Бисакодила эти показатели составляли 55,16 ± 12,6 и 53,4 ± 18,6 % соответственно при норме 64,04 ± 32,01 %. Эти данные свидетельствовали о мягком стимулирующем эффекте Дульколакса на моторику кишечника. Таким образом, преимущество Дульколакса перед Бисакодилом заключалось в более мягком изменении частоты и консистенции стула, достижении полноты опорожнения, более быстром и предсказуемом времени наступления эффекта, более значимом повышении электромоторной активности толстой кишки.
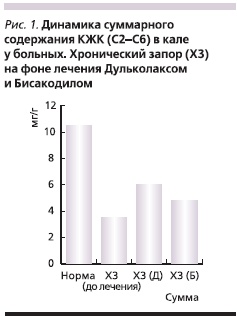
Результаты изучения абсолютного содержания короткоцепочечных летучих жирных кислот (КЖК) в кале больных исходно демонстрировали снижение их абсолютной концентрации по сравнению с нормой, что может свидетельствовать как о нарушении утилизации данных кислот колоноцитами вследствие изменений моторноэвакуационной функции кишечника, так и об изменении активности, а также численности различных популяций микроорганизмов эндогенной толстокишечной микрофлоры. Повышение абсолютной концентрации КЖК после приема препаратов говорило о тенденции к восстановлению функциональной активности и численности толстокишечной микрофлоры, причем данные изменения были более выраженными у пациентов, принимавших Дульколакс. Результаты лечения представлены на рис. 1, 2.
У больных хроническими запорами исходно отмечается достоверное повышение относительно содержания пропионовой и масляной кислот при снижении доли уксусной кислоты по сравнению с группой здоровых лиц, что свидетельствует о выраженном дисбалансе аэробных и анаэробных популяций микроорганизмов и активизации анаэробов, в частности родов бактероидов, пропиони-, фузобактерий, клостридий и др. После применения Дульколакса и Бисакодила выявилась тенденция к формированию нормального профиля кислот, свидетельствующая о восстановлении качественного состава микроорганизмов. Аналогичная, но менее выраженная динамика отмечена и у больных, получавших Бисакодил.

Исходно у пациентов с хроническими запорами наблюдается смещение значений аэробного индекса, отражающего окислительно-восстановительный потенциал внутрипросветной среды в область отрицательных значений, что способствует активизации анаэробных популяций микроорганизмов. После применения Дульколакса выявилась тенденция к смещению аэробного индекса в область нормальных значений, что обеспечивает условия для нормальной и эффективной жизнедеятельности облигатной микрофлоры. На фоне Бисакодила наблюдалась менее выраженная динамика изменения аэробного индекса. Результаты лечения представлены на рис. 3.

Выводы:
- Препараты Дульколакс и Бисакодил эффективны в терапии медленнотранзитных запоров, протекающих на фоне гипомоторной дискинезии толстой кишки.
- Отличный и хороший эффекты отмечены в 85 % случаев на фоне приема Дульколакса и в 75 % на фоне Бисакодила.
- Дульколакс выгодно отличается от других бисакодилов в плане изменения частоты, консистенции стула и полноты опорожнения.
- Исследуемые препараты обладают предсказуемым временем наступления эффекта с тенденцией к более быстрому ожидаемому действию у Дульколакса.
- После 10-дневного применения исследуемых препаратов значительно сократилось общее время транзита по ЖКТ. На фоне приема Дульколакса улучшились показатели электромоторной активности толстой кишки.
- Динамика суммарного и относительного содержания КЖК в кале в обеих группах больных свидетельствовала о тенденции к восстановлению функциональной активности и качественного состава толстокишечной микрофлоры, более выражена у пациентов, принимавших Дульколакс. Изменения значений аэробного индекса свидетельствовали в пользу улучшения условий для нормальной и эффективной жизнедеятельности облигатной микрофлоры.
- Переносимость Дульколакса и Бисакодила была очень хорошей и хорошей в 80 и 72 % случаев соответственно.
- В 20 % случаев наблюдался эффект последействия препаратов в сроки от 3 до 7 дней.
- Препараты Дульколакс и Бисакодил рекомендованы как эффективные средства при функциональных запорах, особенно у пожилых пациентов.
Таким образом, терапия хронического функционального запора требует индивидуального подхода, тщательной этапной диагностики его причин, обоснованного выбора слабительного препарата с учетом возраста больного и всех факторов развития запора.
Информация об авторах:
Минушкин Олег Николаевич – доктор медицинских наук, профессор, главный гастроэнтеролог Медицинского Центра
Управления делами Президента РФ, заведующий кафедрой гастроэнтерологии
Учебно-научного центра МЦ УД Президента РФ
Тел. 8 (499) 146-80-25
Елизаветина Галина Алексеевна – доцент кафедры гастроэнтерологии, ФГУ “НИ Медицинский Центр при Правительстве РФ”.
Тел. 8 (499) 146-80-25
Ардатская Мария Дмитриевна – доктор медицинских наук, профессор кафедры гастроэнтерологии
Учебно-научного медицинского центра Управления делами Президента РФ.
Тел. 8 (495) 140-20-7



