Введение
В 2009 г. на сайте Всемирной организации здравоохранения (ВОЗ) появилось первое сообщение о вспышке в Мексике и США нового варианта вируса гриппа, А(H1N1) pdm09, с которым была связана более высокая смертность, чем при ранее циркулировавших вирусах гриппа A(H1N1), A(H3N2) и В [1].
Традиционно для лечения и профилактики осложнений при вирусных и бактериальных инфекциях, облегчения клинической симптоматики применяют препараты разных лекарственных групп, вводимые «во входные ворота» возбудителей, например орально или интраназально. Бензидамина гидрохлорид (БГ), его лекарственные формы Тантум Роза и Тантум Верде – лекарственные средства, обладающие сразу несколькими фармакодинамическими свойствами: антибактериальным, фунгицидным, обезболивающим и противовоспалительным [2]. Антисептический эффект БГ изучался в исследованиях in vitro с использованием нескольких типов культурных сред и множества микроорганизмов [3, 4]. БГ ингибировал различные бактерии (грамположительные и грамотрицательные кокки, грамотрицательные бациллы), дрожжевые и другие грибы в культурных средах, инфицированных изучаемыми микроорганизмами. До настоящего времени действие БГ на вирусы гриппа человека не изучали.
Исходя из вышесказанного, актуальность исследования активности БГ и его лекарственных форм в отношении вируса гриппа очевидна с точки зрения возможности расширения рекомендаций по их практическому применению.
Методы
Субстанция и лекарственные препараты
Субстанция БГ и готовое лекарственное средство Тантум Верде (содержит 0,15% БГ) производства Angelini S.p.a. (Италия) были предоставлены российским представительством компании ООО «Анджелини Фарма Рус». Субстанцию БГ и Тантум Верде растворяли в дистиллированной воде до конечной концентрации 1,0 мг/мл (сток). Перед постановкой опытов готовили разведение стоков средой Игла МЕМ с двойным набором аминокислот. В работе использовали концентрации соединения 0,5; 1,0; 2,5; 5,0; 7,5 и 10,0 мкг/мл. В качестве контроля использовали среду Игла МЕМ с двойным набором аминокислот.
Вирусы, применяемые в опытах in vitro
В исследования был включен пандемический штамм вируса гриппа человека, вызвавший тяжелую форму гриппозной инфекции с летальным исходом – A/IIV-Orenburg/29-L/2016 (H1N1) pdm09 – в эпидемическом сезоне 2015–2016 гг. Вирус был выделен из аутопсийного материала (легкие – L) на культуре клеток MDCK в лаборатории этиологии и эпидемиологии гриппа ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России. Штамм депонирован в Государственную коллекцию вирусов Центра экологии и эпидемиологии гриппа Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России; номер депонирования – 2827.
Данный вирус гриппа резистентен к ремантадину. По данным частичного секвенирования гемагглютинина, определена мутация в рецептор-связывающем сайте (D222N), что определяет более широкую специфичность вируса по отношению к рецепторам респираторного тракта человека (не только верхних, но и нижних дыхательных путей).
Характеристика клеточной культуры, использованной в опытах in vitro
Для изучения активности препаратов БГ и Тантум Верде использовали клетки культуры ткани MDCK (Madin and Darby Canine Kidney), перевиваемую линию клеток почки собаки породы «спаниель», которую применяют во всех лабораториях мира для выделения эпидемических штаммов вирусов гриппа из клинических материалов, а также проведения опытов in vitro.
Изучение токсичности субстанций для клеток культуры ткани MDCK
Клетки MDCK выращивали в 96-луночных культуральных плоскодонных планшетах до полного монослоя. Затем среду удаляли и в планшеты вносили разные концентрации Тантум Верде: 10,0–1000,0 мкг/мл.
После инкубации клеток с препаратом в течение 48 часов при 37oС в атмосфере 5% СО2 визуально под микроскопом оценивали состояние клеточного монослоя. После этого клетки отмывали средой Игла МЕМ и добавляли фосфатно-солевой буфер, содержащий краситель XTT (2,3-бис(2-метокси-4-нитро-5-сульфофенил)-2Н-тетразолий-5-карбоксианимид) и 5-мМ раствора PMS (фенозинметасульфат; Sigma, США). После инкубации в течение 3 часов при 37oС результаты просчитывали на спектрофотометре фирмы «Biotek, Synergy HT» при длине волны 450 нм.
Концентрацию соединения, уменьшающую значение оптической плотности ОП450 на 50% по сравнению с контролем клеток, принимали за 50%-ную тканевую цитотоксическую дозу (ТЦД50). Максимальную концентрацию соединения, не изменяющую значения ОП450 по сравнению с контролем клеток, принимали за его максимально переносимую концентрацию (МПК).
Изучение специфической активности препаратов в отношении вирусов гриппа
Подавление экспрессии вирусных антигенов под влиянием БГ и Тантум Верде изучали при внесении препаратов в разных концентрациях (0,5; 1,0; 2,5; 5,0; 7,5 и 10,0 мкг/мл) и режимах (профилактический и лечебный) по отношению ко времени инфицирования культуры клеток MDCK (одновременно с заражением и через 2 часа после заражения соответственно) с последующим учетом результатов постановкой иммуноферментного анализа ИФА, как описано ранее [6]. Реакция учитывалась по оптической плотности (ОП) при 450 нМ на спектрофотометре фирмы «Biotek, Synergy HT». Каждое разведение вируса исследовано в 6 повторах, для чего вычисляли среднее значение оптической плотности. Процент ингибирования определяли как отношение между разницей ОП опыта и ОП клеточного контроля, разделенное на разницу ОП вирусного контроля и ОП клеточного контроля, умноженное на 100%, по формуле:
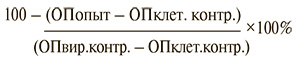
Также рассчитана минимальная концентрация соединения, подавляющая активность вируса на 50,0% (IC50).
Кроме того, исследовали способность Тантум Верде инактивировать инфекционные свойства вируса гриппа. Готовили восемь десятикратных разведений вируса гриппа, и в каждое его разведение вносили разные концентрации Тантум Верде (от 0,5 до 10,0 мкг/мл). Затем на монослой клеток культуры ткани MDCK 96-луночных панелей последовательно наносили
8 десятикратных разведений вируса гриппа в 3 лунки повтора с разными концентрациями исследуемого вещества, часть клеток инфицировали только вирусом (контроль вирусной репродукции), в другую часть клеток вносили только поддерживающую клетки среду Игла МЕМ (клеточный контроль). Панели инкубировали в термостате в течение 48 часов при температуре 37oС. Затем из каждой лунки производили отбор вируссодержащей жидкости с последующей постановкой реакции гемагглютинации (РГА) по общепринятой методике с использованием 0,75%-ной взвеси эритроцитов человека 0(I) группы крови. Расчет инфекционных титров для каждой концентрации исследуемого вещества и разведения вируса проводили по методу Рида и Менча. Титр выражали в lg ТЦИД50/мл. По разнице инфекционных титров в контрольных и опытных лунках оценивали вирулицидную активность Тантум Верде. Препарат считали активным при разнице инфекционного титра вируса в опыте и контроле на 2 lg и более.
Результаты
Токсичность субстанции Тантум Верде была изучена при нанесении разных концентраций препарата (от 10,0 до 1000,0 мкг/мл) на клетки культуры ткани MDCK по вышеописанной методике. ТЦИД50 субстанции составила 20,0 мкг/мл, а максимально переносимая концентрация – 15,0 мкг/мл.
Изучение специфической активности БГ и Тантум Верде по подавлению репродукции пандемического штамма вируса А(H1N1) pdm09 в культуре клеток MDCK проведено согласно ранее представленной методике с учетом результатов ИФА, рассчитанных по данным трех одинаковых опытов, для достижения средних показателей активности препаратов в разных режимах инфицирования клеток двумя дозами вируса, которые составили 100–1000 ТЦИД50 (тканевая цитопатическая инфекционная доза, вызывающая гибель 50% клеток монослоя).
Согласно средним данным серии опытов, представленных в таблице, препараты проявили различную подавляющую активность на репродукцию вируса гриппа A(H1N1) pdm09, зависяшую от их концентрации и режимов внесения.
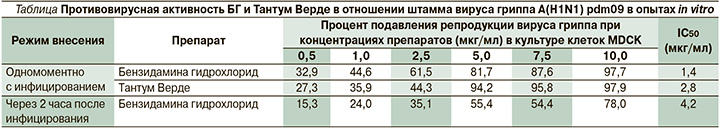
Активность БГ была дозозависимой, т.е. увеличение концентрации препарата приводило к возрастанию процента подавления вирусной репродукции. Причем в режиме внесения препарата через 2 часа после инфицирования активность его при тех же концентрациях была несколько ниже по сравнению с режимом одномоментного внесения препарата и вируса. Исходя из вышесказанного, IC50 БГ составила 1,4 и 4,2 мкг/мл в профилактическом и лечебном режиме соответственно.
Результаты исследования активности Тантум Верде также подтвердили его активность в отношении вируса гриппа человека A(H1N1) pdm09 в не токсичных для клеток культуры ткани MDCK концентрациях. Причем возрастание его активности зависело от увеличения концентрации препарата, а показатель IC50 для Тантум Верде составил 2,8 мкг/мл при одномоментном внесении с вирусом гриппа.
В целом результаты изучения специфической активности БГ и его лекарственной формы Тантум Верде по подавлению репродукции пандемического штамма вируса гриппа человека А(H1N1) pdm09 сравнимы друг с другом. При возрастании концентраций препаратов от 0,5 до 10,0 мкг/мл процент ингибирования вирусной репродукции постепенно увеличивался от ~30,0 до ~98,0%. Рассчитанная концентрация, подавляющая вирусную активность на 50,0%, была в 2 раза выше для лекарственной формы Тантум Верде, содержащей 0,15% БГ, при профилактическом режиме внесения препаратов.
В серии последующих опытов изучена вирулицидная активность препарата Тантум Верде, согласно представленным ранее методикам с учетом результатов в РГА.
Тантум Верде обнаружил высокую вирулицидную активность в отношении пандемического штамма вируса гриппа человека A(H1N1) pdm09. При концентрации препарата 1,0 мкг/мл наблюдали снижение инфекционного титра вируса на 4,0 lg. При концентрациях препарата 2,5; 5,0; 7,5 и 10,0 мкг/мл отмечали подавление вирусной репродукции на 6,0 lg, что служит достоверным показателем по сравнению с вирусным контролем.
Таким образом, результаты проведенных исследований принципиально отличают БГ от других аналогичных средств с заявленными антимикробными свойствами, применяемых в клинике при схожих показаниях. Также следует отметить, что БГ влияет на уровень медиаторов воспаления, что останавливает воспалительный процесс, снижая риск развития опасных осложнений, например абсцессов, паратонзиллитов, одновременно оказывая местное обезболивание [5]. В итоге вместо нескольких средств можно использовать одно.
Примером других средств, применяемых для профилактики осложнений при инфекционных заболеваниях ЛОР-органов, служат гексэтидин, бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрат и прочие антисептики [6]. Однако их применение сопряжено с рядом недостатков: в частности, они обладают лишь антисептическим действием в отношении вирусов и бактерий, но собственным противовоспалительным и обезболивающим действиями не обладают, что требует добавления к терапии анестетика. Следует отметить, что молекула БГ имеет серьезные фармакокинетические преимущества, в частности, она лучше проникает в очаг воспаления по сравнению с вышеуказанными средствами [7–9]. Это отражается и на профиле безопасности препарата, т.к. иные противомикробные средства приходится комбинировать с симптоматическими препаратами, имеющими свои побочные эффекты, что сопряжено с бόльшими рисками по сравнению с БГ.
Противовирусное действие вышеперечисленных средств также имеет ряд важных особенностей [10]. В частности, ранее было показано противовирусное действие гексэтидина in vitro, но данное средство нейтрализовало вирус простого герпеса, лишь пока он был на поверхности клетки. При этом, как правило, клиническая симптоматика и распространение вирусной инфекции связаны с проникновением вируса внутрь клетки для осуществления процесса репликации. В ходе упомянутого исследования показано, что гексэтидин не влияет на репликацию вируса простого герпеса, а значит, не останавливает процесса размножения и распространения его копий.
Другое средство, применяемое при множестве инфекционно-воспалительных процессов, но обладающее только антисептическими свойствами, – это бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрат [11]. По результатам исследований in vitro авторы заявляют о его противовирусных свойствах в отношении вирусов гриппа А(H3N2) и А(H5N1). Однако введение препарата в монослой клеток через 12 часов после их инфицирования не защищало эти клетки от действия вируса гриппа.
Обсуждение
Исходя из результатов указанных исследований, становится очевидным, что возможности вышеперечисленных лекарственных средств имеют ряд важных ограничений для широкого клинического применения с целью снижения локальной вирусной активности. Исходя из этого, БГ имеет клинические преимущества, давая возможность врачу использовать его как в профилактической схеме аналогично другим местным препаратам от боли в горле, так в лечебной схеме уже при появлении симптомов вирусной инфекции, что на основании современных данных не актуально для описанных выше препаратов.
Таким образом, клиническая значимость результатов настоящего исследования состоит в подтверждении способности БГ и его готовой лекарственной формы Тантум Верде ингибировать вирус гриппа как при профилактической, так и при лечебной схеме применения. Лечебная схема особенно важна для практикующего врача, т.к. пациент обращается за помощью, как правило, при появлении у него ОРЗ-ассоциированных симптомов.
Заключение
На основании проведенных исследований показано, что как субстанция БГ, так и готовая лекарственная форма на ее основе – 0,15%-ный раствор в виде спрея под торговым наименованием «Тантум Верде», обладают специфическим действием в отношении пандемического штамма вируса гриппа человека A/IIV-Orenburg/29-L/2016 (H1N1) pdm09 в не токсичных для клеток культуры ткани MDCK концентрациях (ТЦД50=20,0 мкг/мл, МПК=15,0 мкг/мл). Следует отметить, что выявленный противовирусный эффект имеет дозозависмый характер, т.е. увеличение концентрации препаратов приводило к возрастанию их противогриппозной активности.
Минимальные IC50 для БГ составили 1,4 и 4,2 мкг/мл в профилактическом и лечебном режимах соответственно, а для Тантум Верде – 2,8 мкг/мл в профилактическом режиме.
Также отмечено наличие у Тантум Верде вирулицидного действия. При концентрациях препарата 1,0–10,0 мкг/мл наблюдали подавление вирусной репродукции на 4,0–6,0 lg.
Таким образом, БГ является активным и перспективным препаратом в отношении вирусов гриппа человека, что расширяет рекомендации его в области клинического применения.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов. Исследование проводилось при научном сотрудничестве с ООО «Анджелини Фарма Рус».



