Эпилепсия является одним из распространенных неврологических заболеваний, которым страдают от 1 до 1,5% населения земли и диагностируется чаще у детей, чем у взрослых [1]. Распространенность эпилепсии среди детского и подросткового населения европейских стран составляет от 2,8 до 9,2 на 1000 [1].
При лечении детей с эпилепсией необходим индивидуальный подход с учетом не только специфики течения заболевания, но и возраста ребенка, соматического и иммунного статусов, метаболических процессов, роли наследственных факторов, аллергических реакций и некоторых других особенностей [2]. Основной принцип лечения эпилепсии: максимум терапевтической эффективности при минимуме побочных эффектов [2].
В процессе диагностики эпилепсии требуются тщательная оценка анамнеза и описания пароксизмального (судорожного) состояния, выявление и по возможности устранение эпилептогенных факторов (например, опухоли), исключение провоцирующих приступы ситуаций. После подтверждения диагноза перед врачом встает вопрос о выборе антиэпилептического препарата (АЭП).
Современные АЭП должны отвечать следующим требованиям:
- высокая эффективность в лечении;
- широкий спектр терапевтического воздействия на приступы;
- отсутствие аггравации приступов;
- хорошая переносимость;
- доступность для населения.
Подбор АЭП не должен быть эмпирическим! Препараты назначают строго в соответствии с формой эпилепсии и характером и приступов.
S. Shorvon в 2010 г. [3] сформулировал основные факторы, которые надо учитывать при назначении противосудорожной терапии:
- Факторы, относящиеся к пациенту: пол и возраст; коморбидность и эмоциональный настрой; социальные факторы (работа, семья, учеба); отношение к риску приступов и необходимости лечения.
- Факторы, относящиеся к эпилепсии: форма эпилепсии и тип приступов; тяжесть эпилепсии и приступов, этиология.
- Факторы, относящиеся к препаратам: механизм действия; лекарственные взаимодействия и сила эффекта; терапевтическая широта и сила эффекта; доступность и стоимость.
В детском возрасте особенно важно учитывать такие моменты, как форма эпилепсии и характер приступов, возраст и пол пациента, приверженность лечению (лекарственная форма, схема дозирования, обеспечивающие простоту использования, психологические аспекты, особенно у подростков), влияние болезни на качество жизни, социальное функционирование, учебу, а также затраты на терапию (как прямые, так и дополнительные) и доступность препарата.
На современном этапе большое внимание уделяется лечению пациентов с хроническими заболеваниями (к которым относится эпилепсия) в амбулаторных условиях, сокращению количества необоснованных госпитализаций. В связи с этим большое значение приобретает выбор АЭП. Лекарственное средство должно быть высокоэффективным и одновременно иметь минимальный риск возникновения побочных эффектов, быть удобным в применении, не требовать частого контроля в процессе лечения лабораторных показателей крови и мочи, многократного проведения ультразвукового исследования органов брюшной полости.
Одним из современных АЭП, применяемых детскими эпилептологами и удовлетворяющих перечисленным требованиям, является леветирацетам. Он обладает широким спектром терапевтического действия: эффективен при большинстве эпилептических приступов (генерализованных и парциальных), применяется как в составе комбинированного лечения, так и в монотерапии эпилепсии [4–6].
Леветирацетам обладает уникальным механизмом действия, отличным от других АЭП: связывается с транспортным белком (SV2A) синаптических везикул в пресинаптических терминалях, тем самым ингибируя выход кальция из нейрона. Кроме того, леветирацетам ингибирует калиевые каналы N-типа в гиппокампе, снижает активность негативных модуляторов ГАМК(γ-аминомасляная кислота)- и глициновых рецепторов, подавляет избыточную синхронизацию нейронов [4]. Для амбулаторной практики особенно важны благоприятный фармакокинетический профиль с линейной кинетикой (концентрация в крови нарастает пропорционально дозе препарата), стабильностью концентрации в крови (достигается через 2 дня после начала приема препарата дважды в сутки), отсутствием клинически значимого взаимодействия с другими лекарственными препаратами, что отличает его от традиционных АЭП.
 Целью исследования стала оценка применения леветирацетама в условиях амбулаторной нейропедиатрической практики.
Целью исследования стала оценка применения леветирацетама в условиях амбулаторной нейропедиатрической практики.
Материал и методы
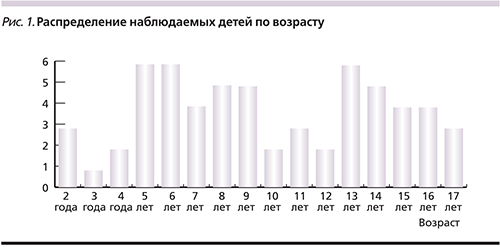
На базе неврологического отделения консультативного центра Морозовской детской городской клинической больницы ДЗ г. Москвы наблюдаются дети с различными формами эпилепсии. Нами проанализированы данные из историй болезни детей с эпилепсией, у которых при лечении применялся леветирацетам. Всего был обследован 61 пациент (31 девочка и 30 мальчиков в возрасте от 2 до 17 лет: детей от 2 до 6 лет – 18, от 7 до 11 лет – 19, от 12 до 17–24 человека) [рис. 1].
Диагностика эпилепсии осуществлялась на основании результатов клинического обследования, видео-электроэнцефалография (ЭЭГ)-мониторирования, нейровизуализации (компьютерная томография, магнитно-резонансная томография – МРТ). Формы эпилепсии, с которыми наблюдались пациенты, представлены в табл. 1.
У пациентов отмечались различные типы приступов: типичные и атипичные абсансы, миоклонические, вторично-генерализованные, генерализованные тонико-клонические (ГТКП), сложнопарциальные (гемиклонические, гемифациальные, версивные, фациобрахиальные, диалептические), миоклонии век с абсансами, вегетативные. Диагностированы разные формы эпилепсии: фокальные (идиопатические, криптогенные и симптоматические), идиопатические генерализованные (детская абсансная эпилепсия и юношеская абсансная эпилепсия, юношеская миоклоническая – ЮМЭ, с изолированными генерализованными приступами), синдром Драве, синдром Леннокса–Гасто, синдром Дживонса, атипичная роландическая эпилепсия, синдром Дузе. Чаще всего в наблюдавшейся группе пациентов отмечались симптоматическая (22,9%) и криптогенная (19,6%) фокальные эпилепсии, ЮМЭ (13%). Треть пациентов (n=21, 34,4%) имели только один тип приступов, чаще всего это были абсансы, миоклонии или ГТКП.
Изменения на МРТ головного мозга были выявлены у 13 (21,3%) наблюдавшихся пациентов и были представлены следующими патологическими процессами: субатрофия корковая – 5, резидуальная лейкопатия – 2, арахноидальные кисты – 4, кистозно-глиозные изменения – 2.
Результаты исследования
На момент начала приема леветирацетама длительность течения эпилепсии составляла от 2 месяцев до 10 лет. Препарат назначали в терапевтической дозе от 30 до 70 мг/кг/сут.
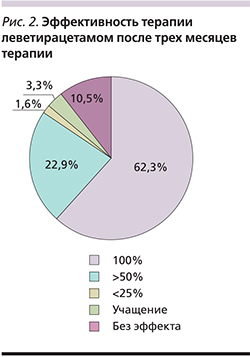
На монотерапии леветирацетамом находились 23 (37,7%) ребенка. В 6 случаях леветирацетам был первым препаратом, с которого стартовала терапия эпилепсии. Формами эпилепсии, при которых леветирацетам использовался в качестве стартовой монотерапии, были идиопатическая генерализованная с изолированными генерализованными судорожными приступами, юношеская миоклоническая, детская абсансная, синдром Дживонса, роландическая эпилепсия, идиопатическая затылочная (синдром Панайотопулоса). У 17 пациентов из 23 на монотерапии леветирацетам стал вторым АЭП, замена производилась после неуспешности терапии первым АЭП (недостаточная эффективность, побочные эффекты, ухудшение на ЭЭГ) [рис. 2].
В 33 (54%) случаях применялась дуотерапия, в 5 (8,1%) – 3 препарата. На трех препаратах находились дети с атипичной роландической эпилепсией и детским церебральным параличом.
Перевод на монотерапию леветирацетамом с других АЭП осуществлялся чаще всего при идиопатических формах (идиопатической фокальной, атипичной роландической эпилепсии, детская абсансная эпилепсия, юношеская абсансная эпилепсия, ЮМЭ) при возникновении побочных эффектов первого/второго назначенного АЭП и, что немаловажно, из-за негативного отношения родителей к «старым» АЭП.
Наиболее часто леветирацетам при комбинированной терапии сочетался со следующими АЭП: вальпроевой кислотой – 19, карбамазепином – 5, окскарбазепином – 2, топираматом – 2, фризиумом – 2, ламотриджином – 1, сабрилом – 1, стирипентолом – 1.

Чаще всего необходимость в комбинированной противоэпилептической терапии возникала при недостаточной эффективности монотерапии и возникновении побочных эффектов первого (второго) препарата: вальпроевая кислота – изменение показателей крови, выпадение волос, боли в животе, данные фармакомониторинга, прибавка массы тела; топирамат – появление солей в моче, заторможенность; ламотриджин – аллергическая сыпь; окскарбазепин – головокружение; карбамазепин – изменения биохимических показателей крови (аланинаминотрансфераза, аспартатаминотрансфераза, щелочная фосфотаза).
Отсутствие клинического эффекта (сохранение приступов) через 3–6 месяцев терапии леветирацетамом было зафиксировано только у 5 (8,1%), а у 2 детей с симптоматическими фокальными эпилепсими и обширными кистозно-глиозными изменениями на МРТ наблюдалось учащение приступов. Все эти пациенты страдали тяжелыми формами эпилепсии: симптоматическими фокальными, атипичной роландической, синдромом Леннокса–Гасто, синдромом Драве.
Из пациентов на стартовой монотерапии леветирацетамом (n=6) достигли клинической ремиссии четверо: с ЮМЭ и идиопатической генерализованной эпилепсией с генерализованными судорожными припадками. У 17 пациентов на монотерапии леветирацетамом (после смены монотерапии) достигнута клиническая ремиссия в 9 случаях, остальным через 3–6 месяцев к лечению был добавлен второй АЭП (вальпроевая кислота, окскарбазепин, ламотриджин).
В двух случаях препарат был отменен через 3 месяца приема из-за неэффективности (учащения приступов), у пятерых пациентов – через 6 месяцев приема и наращивания дозы до достижения терапевтического эффекта (рис. 3).
Большинство (78,7%) пациентов хорошо переносили терапию леветирацетамом, и она не сопровождалась побочными эффектами. Побочные эффекты за время приема препарата возникли у 13 (21,3%) пациентов и были представлены нарушением сна (прерывистостью) у 6, усилением тиков – у 1, раздражительностью, агрессивностью – у 5, аллергической сыпью – у 1. Важно отметить, что ни в одном из случаев побочные эффекты не были настолько значительными, чтобы потребовалась отмена препарата. Обращал на себя внимание тот факт, что дети с данными побочными эффектами и до начала приема леветирацетама имели проблемы со сном, невротические реакции.
При динамической оценке ЭЭГ на фоне приема леветирацетама (проведена у 39 пациентов) только в 4 случаях (после 6 месяцев лечения) отмечено исчезновение и значительное снижение индекса эпилептиформной активности (преимущественно диффузной пик- и полипик-волновой активности). При изначально зарегистрированной фокальной эпилептиформной активности, особенно на фоне регионального замедления, наличии доброкачественных эпилептиформных разрядов детства влияние препарата на картину ЭЭГ было слабовыраженным (отсутствовало через 3–6 месяцев).
К числу важных факторов, определяющих выбор АЭП, помимо типа приступов, формы эпилепсии, возраста относятся коморбидные нарушения.
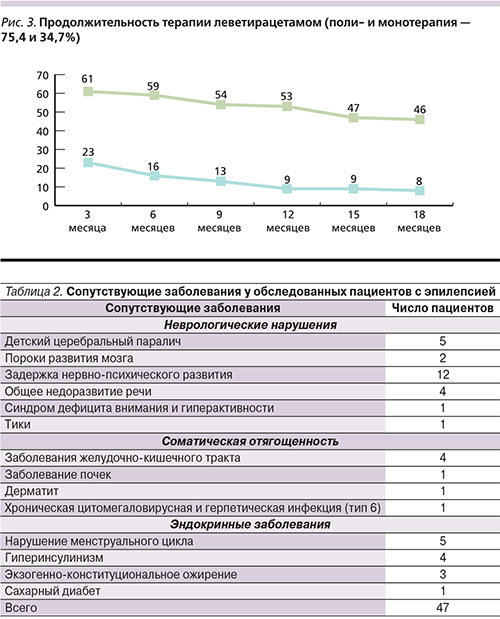
В табл. 2 перечислены сопутствующие заболевания, которые из 61 обследованного пациента с эпилепсией отмечались у 47, что потребовало при выборе АЭП особенно осторожного подхода. В частности, сопутствующие неврологические нарушения отмечались у 25 пациентов. Они были представлены детским церебральным параличом (5 пациентов), пороками развития головного мозга (1 – аномалия Арнольда– Киари, 1 – гипоплазия мозолистого тела). Задержка нервно-психического развития наблюдалась у 12 пациентов, общее недоразвитие речи – у 4, синдром дефицита внимания и гиперактивности – у 1, тики – у 1. В ходе динамического наблюдения обращало на себя внимание отсутствие негативного влияния леветирацетама на состояние высших психических функций как во всей группе обследованных, так и у пациентов с коморбидными неврологическими нарушениями.
Соматическая отягощенность имела место в 6 случаях и была представлена заболеваниями желудочно-кишечного тракта (4 пациента), заболеванием почек (1), дерматитом (1), хронической вирусной инфекцией (1). Эндокринными заболеваниями страдали 13 пациентов, их них нарушениями менструального цикла – 5, гиперинсулинизмом – 4, экзогенно-конституциональным ожирением – 3, сахарным диабетом – 1. Следует подчеркнуть, что ни у одного из пациентов с соматической отягощенностью и эндокринными расстройствами лечение леветирацетамом не сопровождалось нарастанием указанных нарушений.
Отдельно хотелось бы поделиться опытом использования леветирацетама у детей с эпилептическими приступами после трансплантации печени. Мы наблюдали троих детей (9, 11 и 15 лет) после данной операции, у которых в раннем послеоперационном периоде развились повторные вторично-генерализованные судорожные приступы. С учетом данных неврологического осмотра, ЭЭГ, МРТ головного мозга было принято решение о начале противосудорожной терапии. Во всех случаях одним из важных факторов выбора антиконвульсанта был безопасный профиль препарата. Все дети переносили препарат хорошо, и он был отменен через 6 и 9 месяцев под динамическим контролем невролога и ЭЭГ.
Обсуждение
К настоящему времени в нейропедиатрической практике накоплены данные о том, что леветирацетам в качестве дополнительной терапии обладает высокой эффективностью при разных типах эпилептических приступов (как парциальных, так и генерализованных), а при ряде форм эпилепсии может успешно применяться в качестве монотерапии [4–8]. При этом для него характерны довольно быстрое достижение терапевтического эффекта и хорошая переносимость у детей и подростков.
Леветирацетам имеет благоприятный профиль безопасности – невысокую частоту побочных эффектов, отсутствие негативного влияния на когнитивные функции. Одновременно препарат обладает противосудорожным синергизмом со многими АЭП, не проявляя синергизма по нейротоксическим эффектам. Отсутствуют клинически значимые фармакокинетические взаимодействия как с АЭП, так и с другими лекарственными средствами. Поэтому он может считаться оптимальным препаратом для комбинированного лечения эпилепсии.
Перечисленные характеристики приводят к улучшению приверженности лечению со стороны пациентов и родителей, что имеет большое значение в амбулаторной практике. Этому способствуют также простота и удобство его применения – простая схема титрования дозы, прием 2 раза в сутки независимо от еды. Кроме того, применение препарата не требует определения его концентрации в сыворотке крови и лабораторного мониторинга (анализов крови, мочи, определения активности печеночных ферментов).
Хорошо известно, что бремя эпилепсии усиливается при наличии сопутствующих заболеваний [10]. Длительное лечение леветирацетамом, проводимое в амбулаторных условиях, хорошо переносится и не сопровождается клинически значимыми лекарственными взаимодействиями. Это имеет особое значение для пациентов с эпилепсией, получающих политерапию, а также имеющих сопутствующие заболевания, по поводу которых помимо АЭП они принимают препараты других групп. Лекарственные взаимодействия могут ухудшать как эффективность, так и переносимость противоэпилептической терапии. Леветирацетам – АЭП нового поколения, имеющий линейный фармакокинетический профиль, обладает явным преимуществом перед другими АЭП в лечении детей и подростков с эпилепсией и сопутствующей патологией.
Среди детей с эпилепсией умственная отсталость и регресс психического развития отмечаются лишь при ограниченном числе форм заболевания. Большинство пациентов с эпилепсией имеют сохранный интеллект и могут обучаться по программе общеобразовательной школы. Однако не менее чем у 50% из них наблюдаются поведенческие и эмоциональные нарушения, трудности в обучении [5].
В основе познавательных трудностей лежат повреждение мозговых структур, локализация эпилептического очага, характер, тяжесть и частота приступов, наличие субклинической эпилептиформной активности на ЭЭГ, перенесенный эпилептический статус, недостаточная эффективность либо побочные эффекты АЭП. Как показали многолетние катамнестические исследования, последствия эпилепсии с началом в детстве часто сохраняются вплоть до взрослого возраста и определяются рано проявившимися сопутствующими когнитивными, поведенческими и эмоциональными расстройствами [6]. Учитывая это, процесс лечения эпилепсии у детей должен включать специальные меры, направленные на своевременное и наиболее полное преодоление когнитивных, поведенческих и эмоциональных нарушений.
Наличие задержки нервно-психического развития определяет тактику врача при ведении ребенка с эпилепсией. Если эта задержка возникла в результате текущего эпилептического процесса, то основные усилия должны быть направлены на купирование эпилептических приступов и подавление эпилептиформной активности на ЭЭГ. Если же ребенок имел нормальный интеллект до начала приступов, то приоритет отдается препарату, эффективному при имеющемся типе приступов и минимально влияющему на когнитивные функции. Преимущество леветирацетама в таких случаях связано с тем, что он не только не оказывает негативного влияния на состояние высших психических функций, но при длительном применении оказывает на них положительное действие. Как показали исследования, терапия леветирацетамом способствует улучшению показателей памяти, внимания, времени реакции, организации и контроля психических и моторных процессов [11].
При выборе препарата как для стартовой терапии эпилепсии, так и политерапии, помимо типа эпилептических приступов и формы эпилепсии у детей и подростков важно учитывать особенности соматического статуса пациента. В нашей группе обследованных выбор леветирацетама пациентами с нарушениями углеводного обмена (сахарный диабет, врожденный гиперинсулинизм) определялся преимуществами фармакокинетики препарата, отсутствием негативного влияния на обменные процессы. Не менее важным было отсутствие взаимодействия леветирацетама с другими препаратами, что имело значение при его выборе для назначения пациентам с сопутствующими хроническими соматическими заболеваниями.
Заключение
Леветирацетам продемонстрировал высокую терапевтическую эффективность, в т.ч. в достижении ремиссии у детей и подростков как с генерализованными, так и с фокальными формами эпилепсии. Наибольший клинический эффект был отмечен при идиопатических формах. Леветирацетам показал высокий уровень безопасности и хорошую переносимость, что позволяет применять его в составе политерапии эпилепсии, в т.ч. у детей и подростков с сопутствующими неврологическими, соматическими и эндокринными заболеваниями, требующими особенно осторожного подхода при выборе АЭП.
Безопасность препарата позволяет использовать его в амбулаторных условиях и избегать дополнительных исследований. Леветирацетам – современный стандарт качества лечения эпилепсии, имеющий преимущество перед другими АЭП для применения в амбулаторной нейропедиатрической практике.



