Распространенность заболеваний толстой кишки в Российской Федерации, как и в других индустриальных регионах мира, имеют в последние десятилетия объективную тенденцию к росту. Наиболее остро стоит проблема колоректального рака (КРР), который в настоящее время переместился на третье место в структуре онкологической заболеваемости, а также прогрессивного увеличения числа больных с неспецифическими аутоиммунными заболеваниями толстой кишки (язвенный колит, энтероколит Крона и др.) [2, 5].
В рамках оказания помощи этим больным большое значение имеет своевременная диагностика [11]. В частности, при раннем выявлении КРР современные хирургические технологии позволяют излечивать большинство пациентов малоинвазивными эндоскопическими методами [8].
Одним из препятствий на пути ранней диагностики в колопроктологии стоят трудности подготовки пациента к исследованию, необходимость полной эвакуации кишечного содержимого с последующим поиском патологического очага. Сложность и отрицательная эмоциональная окраска процедуры очистки толстой кишки, особенно в случаях нарушения эвакуаторной функции, служат поводом к отказу от исследования со стороны как врача, так и пациента. Кроме того, выполненная рутинными методами (слабительное, очистительные клизмы) подготовка кишечника к колоноскопии в 10–35 % случаев является неэффективной ввиду сохранения в кишке содержимого [3, 9].
История проблемы
Современный спектр слабительных препаратов, в т. ч. средств подготовки толстой кишки к обследованиям, достаточно широк: это препараты на основе лактулозы, фосфорнокислых солей натрия, высокомолекулярного полиэтиленгликоля (ПЭГ, макрогол), электролитов [1, 10]. Существуют комбинированные методики, сочетающие применение нескольких из указанных средств [4]. К сожалению, препараты ведущих мировых брендов имеют относительно высокую стоимость, поэтому в большинстве отечественных бюджетных лечебно-профилактических учреждениях для подготовки толстой кишки используется традиционная методика с очистительными клизмами.
Вместе с тем большинство авторов сходятся во мнении, что сочетание эффективности и безопасности наилучшим образом обеспечивается при применении препаратов на основе макрогола [6, 7]. Пероральные препараты практически не адсорбируются в желудочно-кишечном тракте, стимулируют перистальтику, способствуют растворению содержимого кишечника и в течение 4–6 часов обеспечивают полную эвакуацию кишечного содержимого без нарушений систем гомеостаза пациента.
Разработка и внедрение эффективных, безопасных и экономически доступных методов подготовки толстой кишки к обследованию и операциям являются одними из приоритетных научно-практических направлений ГНЦ колопроктологии Росмедтехнологий. В последние годы наиболее перспективными для разработки были признаны препараты для подготовки толстой кишки на основе водно-электролитных растворов ПЭГ.
Группой авторов проведены необходимые этапы разработки оптимального запатентованного химического состава препарата, доклиническое изучение токсичности, а затем многоцентровое клиническое испытание. Зарегистрированы две лекарственные формы: раствор и порошок, получившие товарный знак “Лавакол®”. С 2004 г. начат серийный выпуск данного препарата на Московской фармацевтической фабрике (ЗАО “Мосфарма”). К настоящему времени накоплен обширный клинический опыт использования Левакола, позволяющий оценивать перспективы его применения и продолжать разработку новой улучшенной рецептуры лекарственного средства.
Изучение токсичности Лавакола
Экспериментальное исследование токсичности Левакола проводилось на беспородных белых крысах. Препарат вводили животным ежедневно в течение 10 дней внутрижелудочно из расчета 1,7; 8,5 и 17 г сухого вещества; 1-я доза соответствовала клинической, 2-я и 3-я – в 5 и 10 раз превышали ее. Морфологическое исследование внутренних органов животных проводили по окончании 10-дневного введения препарата и спустя месяц с момента последнего его введения.
Для оценки местнораздражающего действия у крыс, получавших Лавакол, в сравнении с контрольными животными визуально и гистологически обследованы желудок, тонкая и толстая кишки. Патологических изменений обнаружено не было. В других внутренних органах гистологические исследования также не были обнаружены, в т. ч. при применении Лавакола в максимальной дозе.
Клиническое изучение безопасности Лавакола
В рамках клинических испытаний проведена оценка влияния препарата на системы гомеостаза пациентов, в т. ч. проведен анализ электролитного баланса, гематологических показателей, биохимических проб, характеризующих функции печени и почек, показателей кислотно-основного состояния (КОС), объема циркулирующей крови (ОЦК), изучено состояние сердечно-сосудистой системы (ЭКГ с суточным мониторированием). У пациентов оценивали соотношение введенной и выведенной жидкости в процессе кишечного лаважа. Большое значение придавали динамике микрофлоры кишечника, т. к. любая методика подготовки толстой кишки влияет на микробный ценоз и может приводить к дисбиозу.
Изучены две группы больных, которым проводилась подготовка к диагностической колоноскопии методом кишечного лаважа с Лаваколом (n = 87; основная группа) и традиционным методом очистительных клизм (n = 87; группа сравнения). Показанием к колоноскопии были плановые случаи онкологического поиска и контроля перед выполнением вмешательств на аноректальной зоне. Пациенты со стенозирующим КРР, воспалительными заболеваниями толстой кишки и мегаколон были исключены из исследования.
Пациенты основной группы получали 15 саше с порошком (1 упаковку препарата), которые они самостоятельно последовательно растворяли по 1 саше в стакане воды и принимали внутрь с интервалами в 20 минут. Дополнительный прием жидкости ограничен не был. Время приема препарата: с 18.00 до 21.00, время исследования: с 8.00 до 10.00 следующего дня. Общая доза препарата составляла 210 г сухого вещества, или 3000 мл водного раствора. Эвакуация кишечного содержимого начиналась через 45–75 минут после начала приема Лавакола и заканчивалась через 2,0–2,5 часа после приема последней его порции. В группе сравнения больных готовили посредством солевого слабительного (магния сульфат 25 % в 14.00 накануне исследования), а также 4 очистительных клизм вечером и утром перед колоноскопией.
При приеме внутрь 3 литров лаваж-раствора больные основной группы в течение дня дополнительно потребляли в среднем 1250 ± 140 мл жидкости; при этом потери из прямой кишки составляли 3430 ± 182 г. Суточный диурез больных при подготовке методом общего промывания составил 1140 ± 211 мл. Это дало основание считать, что практически весь принятый внутрь раствор эвакуировался естественным путем через прямую кишку. В целом масса больных контрольной группы за период подготовки уменьшилась на 0,85 ± 0,07, а основной – на 0,45 ± 0,05 кг (р < 0,05).
В лабораторных анализах изменялись показатели гематокрита, нараставшего в группе сравнения (с 43,4 ± 1,2 до 48,2 ± 1,1 %) более интенсивно, чем в основной группе (с 42,2 ± 1,1 до 45,2 ± 0,9 %). При исследовании ОЦК было показано, что его исходный дефицит в течение подготовки нарастал в большей степени в контрольной группе, где составлял в среднем 349 ± 5,1 мл (в основной группе – 215 ± 4,3 мл). Это свидетельствовало о более выраженной гиповолемии, развивавшейся при подготовке с помощью очистительных клизм. Электролиты плазмы у больных основной группы не подверглись значительным изменениям: уровень калия, в частности, составил 4,15 ± 0,08 ммоль/л в начале подготовки и 4,22 ± 0,06 – в конце. В группе сравнения наблюдалось достоверное снижение уровня калия – с 4,09 ± 0,08 до 3,81 ± 0,07 ммоль/л. Изменений других показателей клинического анализа крови, коагулограммы и КОС в группах зарегистрировано не было. Наблюдавшееся снижение уровней общего белка и альбумина носило достоверный характер только в контрольной группе.
Таким образом, в процессе подготовки к колоноскопии у пациентов не было выявлено значимых нарушений гомеостаза, а изменения электролитного баланса и ОЦК были более выраженными в группе сравнения, чем при применении кишечного лаважа.
Известно, что изменения водно-электролитного баланса, введение больших объемов жидкости могут отражаться на показателях гемодинамики и характеристиках ЭКГ (удлинение зубцов, нарушение сердечной проводимости). В связи с этим у пациентов обеих групп контролировали показатели гемодинамики и ЭКГ, включая суточное мониторирование. В частности, холтеровский мониторинг был направлен на выявление скрытых нарушений сердечного ритма до, в течение и после кишечного лаважа. Сердечный ритм фиксировали в течение 8 часов до начала процедуры, в период ее проведения, а также в течение ночи и утра, включая непосредственно процедуру колоноскопии.
Было установлено, что кишечный лаваж не приводил к появлению или усугублению уже имевшихся нарушений сердечного ритма. У двух пациентов с мерцательной аритмией нарушения ритма фиксировались независимо от времени приема препарата. У 8 пациентов основной группы и 5 из группы сравнения с сопутствующей артериальной гипертензией отмечено повышение артериального давления, которое было купировано и не потребовало отмены подготовки.
Микробиологическое исследование
Изучение микробного ценоза толстой кишки пациентов, получавших лаваж-раствор, было проведено при поступлении в стационар, перед колоноскопией или операцией и через 5 дней после вмешательства. Было установлено, что при приеме лаваж-раствора с полиэтиленгликолем не наступает значительного “вымывания” кишечной микрофлоры, хотя снижение всех изучавшихся групп микроорганизмов (кишечная палочка, бактероиды и энтерококки) перед колоноскопией носило достоверный характер, К 5-м суткам ценоз практически полностью восстанавливался без появления в просвете толстой кишки патогенной микрофлоры.
Сцинтиграфия кишечника
Изучение сроков опорожнения толстой кишки проводилось на основании динамической сцинтиграфии кишечника с Тх99т на пентатехе (200 мБк внутрь), который был введен с первой порцией препарата 34 пациентам в процессе подготовки к колоноскопии.
Обработка данных динамической сцинтиграфии проведена по системе Daewoo CMC1418S, при этом оценивали процентное накопление перорально введенного изотопа в проекции толстой кишки. Выявлено ускорение транзита изотопа в процессе общего промывания: через 2 часа принятый радиофармпрепарат (РФП) покинул зону проекции тонкой кишки, в течение последующих 3 часов проходила эвакуация изотопа из толстой кишки, через 5 часов от дозы введенного РПФ в кишечнике оставалось только 2–4 %. Полученные данные позволили разработать способ применения и установить сроки приема Лавакола, исходя из времени проведения назначенного исследования или операции. Рекомендованное время приема – не позднее чем за 6 часов перед манипуляцией.
Эффективность подготовки к колоноскопии (сравнение методик)
Эффективность подготовки к колоноскопии изучили на основании опыта 527 исследований, выполненных после применения различных методов подготовки (табл. 1). Группы были сравнимы по полу, возрасту, показаниям к исследованию (исключались случаи стенозирующего КРР, воспалительных заболеваний кишечника и мегаколон).
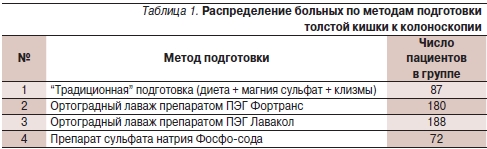
Субъективная оценка переносимости подготовки проведена на основании целенаправленного опроса пациентов о степени комфортности процедуры. Меньше всего побочных явлений отмечено у пациентов, которые готовились “традиционным” методом, и больше всего в группе принимавших Фосфо-соду (тошнота и рвота). Следует отметить, что абсолютное большинство пациентов (84 %), проходивших подготовку различными способами, включая Лавакол, указали на свое предпочтение этому препарату перед другими методиками. Симптомов, потребовавших полностью прервать подготовку, ни в одной группе зарегистрировано не было.
В анкете, заполнявшейся специалистом по эндоскопической диагностике, оценивалась эффективность подготовки во время колоноскопии: количество, характер и локализация остаточной жидкости либо каловых масс (табл. 2).
Каждое эндоскопическое исследование в целом после суммации баллов по каждому анатомическому отделу получало общую оценку степени визуализации стенки кишки: “отличная” при сумме 0–2 балла, “хорошая” – 3–5 баллов, “удовлетворительная” – 6–8 баллов, “плохая” – 9 баллов и более. Приемлемой считали “отличную” и “хорошую” визуализацию, неприемлемой – “удовлетворительную” и “плохую”.
“Проблемной” зоной при подготовке к колоноскопии являлись правые отделы ободочной кишки, полная эвакуация содержимого из которых наиболее затруднена. У 40–50 % пациентов в правых отделах толстой кишки имелись фрагменты каловых масс и темная остаточная жидкость, затрудняющие проведение исследования, в 5 % случаев (очистительные клизмы) делающие его невозможным.
В целом наибольшее количество отличных результатов подготовки (40 %) отмечено у пациентов, готовившихся с использованием натрия фосфата, однако в этой группе отмечено и наибольшее число пациентов с плохой подготовкой (10 %). Число пациентов с отличными результатами подготовки в остальных группах было приблизительно одинаковым (около 25 %), с хорошими – наибольшее при подготовке Лаваколом – 63 %.
В общей сложности доля пациентов с отличными и хорошими результатами при различных способах подготовки составила: Лавакол – 85 %, Фортранс – 80 %, “традиционная” подготовка – 70 %, Фосфо-сода – 70 %.
Мы не выявили достоверного различия в качестве подготовки указанными методами у пациентов, страдающих запорами, и у лиц с регулярной дефекацией. При этом следует учитывать, что больные хроническим толстокишечным стазом и мегаколон были исключены из исследования. Кроме того, не было выявлено зависимости времени проведения колоноскопии от количества остаточной жидкости в просвете толстой кишки. Таким образом, стабильно хорошие результаты подготовки были достигнуты преимущественно при подготовке препаратами ПЭГ (макрогола).
Фармакоэкономические аспекты
Включение препарата в стандарты оказания помощи больным с заболеваниями толстой кишки требует оценки соотношения стоимости и эффективности применяемых методик. Стоимость Лавакола, необходимого для подготовки одного больного, составляет по списку жизненно необходимых и важнейших лекарственных средств 109 рублей. По тому же списку можно оценить стоимость ближайшего по эффективности конкурента Лавакола – препарата Фортранс: 409 рублей. Розничная цена на Фосфо-соду составляет около 800 рублей на подготовку одного пациента. Еще одним потенциальным “конкурентом” является традиционная методика “бесплатной” подготовки очистительными клизмами. Однако следует учесть трудозатраты персонала в течение 40–60 минут на подготовку каждого больного, а также достаточно высокую частоту неэффективного обследования, когда у 16–28 % пациентов после подготовки клизмами приходится повторять колоноскопию ввиду недостаточной подготовки и невозможности адекватной визуализации стенки кишки.
Заключение
Методика перорального кишечного лаважа комплексными растворами макрогола и электролитов является методом выбора по сочетанию безопасности, эффективности и комфортности для пациента при подготовке толстой кишки к обследованию и операциям. Применение препарата Лавакол® дополнительно обеспечивает и экономический эффект.
В настоящее время актуально дальнейшее совершенствование методики ортоградного кишечного лаважа растворами полиэтиленгликоля путем улучшения органолептических свойств препарата, уменьшения необходимого объема раствора для приема внутрь, оптимизации электролитного состава и введение функциональных ингредиентов.



