Сахарный диабет (CД) относится к группе социально значимых заболеваний, характеризуется высокой распространенностью, постоянной тенденцией к росту заболеваемости, хроническим течением, высокой частотой развития осложнений и инвалидизации.
В соответствии с определением ВОЗ CД – это группа метаболических (обменных) заболеваний, характеризующихся гипергликемией, которая является результатом дефектов секреции инсулина, действия инсулина или обоих этих факторов.
В России, как и в других странах мира, ежегодно увеличивается число больных СД. По данным экспертов ВОЗ, общее количество больных к 2025 г. превысит 350 млн человек [11]. При этом в общей структуре диабета на долю СД типа 1 (СД1) приходится 3–6 %.
Известно, что при СД риск развития микро- и макрососудистых осложнений ассоциируется с возрастом пациента, длительностью заболевания и степенью компенсации углеводного обмена. Достижение оптимального контроля углеводного обмена на протяжении всей жизни больного является важнейшим фактором профилактики поздних осложнений СД.
Применяемые в настоящее время в России терапевтические цели контроля заболевания у взрослых больных СД1 отражены в алгоритмах специализированной медицинской помощи при СД [2] и представлены в таблице.
Примечание. HbA1c – гликированный гемоглобин.
Достижение таких показателей углеводного обмена реально у обученных пациентов с высоким уровнем мотивации, обеспеченных инновационными препаратами инсулина и средствами его введения, при регулярном проведении самоконтроля гликемии и адекватной коррекции доз вводимого инсулина.
Необходимость поддержания показателей гликемии у пациентов с СД1, особенно молодого возраста, близких к физиологическим значениям, подтверждена данными одного из фундаментальных клинических исследований (DCCT). В исследовании рассматривалось влияние различных режимов лечения СД1 на частоту развития и степень тяжести поздних осложнений диабета. Оценка конечных результатов осуществлялась в двух группах пациентов. Первая группа включала 726 человек без признаков осложнений, характерных для СД, в частности ретинопатии (группа первичной профилактики). Во вторую группу входили 715 пациентов с признаками ретинопатии (группа вторичной профилактики). В каждой группе одним пациентам назначалась традиционная терапия, другим – интенсивная терапия. Средняя продолжительность наблюдения за больными составила 6,5 лет.
У пациентов без диабетической ретинопатии (группа первичной профилактики) интенсивная терапия при частом измерении содержания глюкозы в крови снижала риск развития данного осложнения минимум на 34 %, а максимально – на 76 % в зависимости от способов выявления исходной тяжести CД.
Интенсивная терапия оказывала благоприятное воздействие и на пациентов с признаками ретинопатии. На начальном этапе наблюдения у пациентов, находящихся на интенсивной терапии, прогрессирование ретинопатии выявлялось на 54 % реже, чем у больных, получавших традиционную терапию.
У пациентов, находившихся на интенсивной терапии, на 35 % сократилась частота поражения почек, которое оценивалось по уровню микроальбуминурии. Использование интенсивной терапии привело к уменьшению клинически значимой микроальбуминурии в целом по группе на 56 %. Интенсивное лечение сокращало риск развития клинически значимой нейропатии на 60 % (в группе в целом). В группе первичной профилактики этот риск уменьшался на 70 % [7, 18].
Поскольку в основе патогенеза СД1 лежит абсолютный дефицит инсулина в результате поражения β-клеток поджелудочной железы, единственным способом его лечения является заместительная терапия в виде интенсифицированной инсулинотерапии (ИИТ).
Цель заместительной инсулинотерапии больных СД – это достижение компенсации заболевания путем имитации нормальной физиологической секреции инсулина. В соответствии с международными и российскими рекомендациями в целях больных СД желательно использовать человеческий генно-инженерный инсулин и его аналоги. В физиологических условиях высвобождение инсулина складывается из базальной (постоянной) секреции для поддержания основного обмена и болюсной (пищевой) секреции, представляющей собой усиленную секрецию в ответ на прием пищи или гипергликемию (рис. 1).
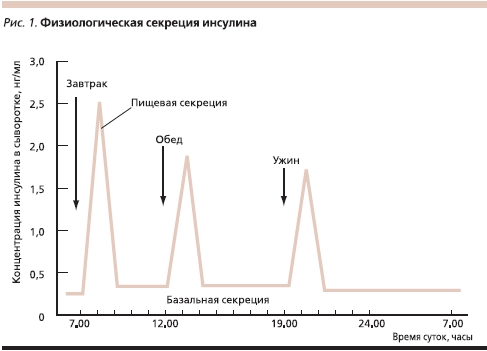
При проведении заместительной терапии инсулином схемы его введения должны быть максимально приближенными к режиму физиологической секреции инсулина β-клетками поджелудочной железы. Исторически введение инсулина осуществлялось с помощью шприцов. Первый в мире шприц для введения инсулина был выпущен в 1924 г. В настоящее время для этой цели все чаще используют многоразовые шприц-ручки со сменными картриджами или заправленные инсулином одноразовые шприц-ручки (флекспены). С помощью как шприцов, так и шприц-ручек введение инсулина осуществляется в основном в базис-болюсном режиме: инсулин короткого или ультракороткого действия вводится перед основными приемами пищи 3 раза в день (имитация болюсной секреции), а инсулин продленного действия – 1 или 2 раза в день (имитация базальной секреции; рис. 2). При таком режиме введения инсулинов наблюдается флюктуация гликемии. Влияние на гликемию оказывают такие факторы, как уровень инсулина в крови в данный момент времени, физическая нагрузка, энергетические потребности организма, прием пищи. При применении ИИТ, когда одновременно используются два типа инсулина, а введение осуществляется с помощью многократных ежедневных инъекций, учесть влияние всех факторов и полностью воспроизвести нормальную секрецию инсулина не всегда удается.
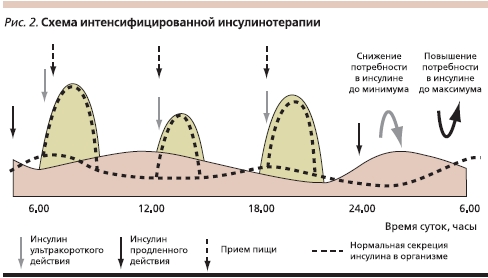
Вследствие этого остаются нерешенными многие проблемы. У части больных возникают ночные гипогликемии, когда уровень базального инсулина в промежутке между 0 и 3 часами ночи выше, чем обычная потребность в нем. Управлять таким состоянием крайне сложно. При уменьшении дозы пролонгированного инсулина, вводимого перед сном, снижается вероятность возникновения ночной гипогликемии, однако часто наблюдается утренняя гипергликемия. Это связано с тем, что в ранние утренние часы потребность в инсулине возрастает (феномен “утренней зари”) и одновременно уменьшается концентрация гормона. Нивелировать повышение гликемии в утренние часы можно за счет дополнительного введения короткого или ультракороткого инсулина в 4–5 часов утра. Это приводит к неудобству в повседневной жизни, нарушению ночного сна, необходимости ежедневно делать до 6–7 инъекций. При введении инсулина, особенно продленного действия, в подкожно-жировой клетчатке формируется его “депо”. Это приводит к неравномерному всасыванию и непредсказуемым колебаниям в действии введенного инсулина. Следовательно, повседневная жизнь больного СД на инсулинотерапии должна находиться в определенных рамках: физическую активность, спорт, секс, посещения кафе, ресторанов, прием алкоголя необходимо тщательно планировать.
ИИТ в виде болюсного инсулина с использованием быстродействующих аналогов позволила повысить соответствие этого режима физиологическим потребностям. Внедрение в практику безпиковых аналогов базального инсулина также обеспечило ряд клинических преимуществ по сравнению с традиционными пролонгированными препаратами. Поэтому ИИТ в настоящее время остается наиболее доступным методом, позволяющим стабилизировать клинико-метаболические показатели, снижать риск осложнений, повышать качество жизни и улучшать прогноз течения диабета.
Манифестация заболевания в раннем возрасте и угроза развития остры, а также хронических осложнений уже в молодости в условиях плохой компенсации СД1 не только привела к появлению новых видов инсулинов, но и обусловила поиск наиболее оптимальных методов его введения, дающих возможность достигать лучшего контроля углеводного обмена.
Современным, эффективным подходом, позволяющим решать проблему более полной имитации физиологической инсулинемии, стало использование метода постоянной подкожной инфузии инсулина (ППИИ) с помощью портативного устройства – инсулинового дозатора (помпы). В основе работы инсулиновой помпы лежит также базисно-болюсный принцип подачи инсулина (рис. 3). Это единственное на сегодняшний день устройство, обеспечивающее постоянное подкожное введение инсулина малыми дозами. Схема и принцип введения инсулина помпой максимально соответствуют ритму работы здоровой поджелудочной железы, что позволяет обеспечивать оптимальный контроль уровня сахара в течение 24 часов. В помпе используется только один вид инсулина: аналог инсулина ультракороткого действия или инсулин короткого действия. Использование аналогов инсулина при ППИИ позволяет вводить их непосредственно перед едой в отличие от обычных инсулинов короткого действия, которые вводят за 30 минут до еды. Использование ППИИ дает возможность отказаться от введения продленного инсулина и оптимизировать базальную инсулинемию за счет ежечасного введения малых доз ультракороткого инсулина (0,1 ЕД или более), которые точно соответствуют индивидуальным особенностям организма больного СД1. Базальный уровень инсулина программируют в зависимости от уровня глюкозы в ночные часы вне приема пищи, физической нагрузки, времени суток и изменяется в зависимости от индивидуальных особенностей углеводного обмена и режима дня. Инсулиновая помпа позволяет программировать сразу несколько режимов введения базального инсулина. Это снижает риск развития гипогликемии в ночные часы или в отсутствие приема пищи, а также позволяет избегать резкого повышения гликемии в ранние утренние часы. В любое время в зависимости от потребности организма в инсулине пациент самостоятельно может уменьшить или увеличить введение инсулина в базальном режиме: например, в период занятия физическими упражнениями или при необходимости отключить помпу на короткий период времени (до 30 минут). Обеспечение физиологической потребности в базальном инсулине в течение суток позволяет избегать развития гипогликемических состояний, необходимости в дополнительных приемах пищи, прибавки массы тела.
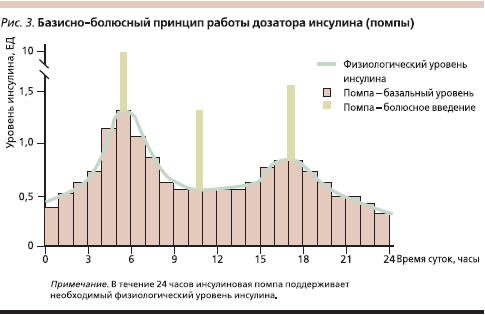
В течении 24 часов инсулиновая помпа поддерживает необходимый физиологический уровень инсулина.
Во время приема пищи потребность организма в инсулине повышается. В связи с этим требуется дополнительное введение инсулина путем нажатия соответствующей кнопки на помпе – болюсное введение. Необходимую дозу инсулина определяет сам пациент в зависимости от количества принимаемых углеводов. В отличие от инъекций шприцами или шприц-ручками при применении помпы существует уникальная возможность использовать различные варианты болюсного введения, например “растянутый” или “многопериодный” болюсы. “Стандартный” болюс вводится на прием пищи или при гипергликемии для снижения ее уровня. “Пролонгированный” болюс вводится в течение заданного периода времени: от 15 минут до 12 часов. “Многоволновой” болюс состоит из “стандартного” и “пролонгированного” болюсов. Он применяется при приеме пищи, богатой белком и жиром, и при гастропарезе. “Многоволновой” режим удобен при продолжительном приеме пищи во время длительных обедов, встреч или при приеме пищи, медленноусвояемой. Использование разных типов болюса обеспечивает пациенту большую свободу в повседневной жизни и способствует улучшению постпрандиальной гликемиии.
Таким образом, введение инсулина с помощью дозатора осуществляется в двух режимах: непрерывная подача инсулина в микродозах (базальный режим) и введение инсулина на прием пищи или при высоком уровне гликемии (болюсный режим).
На фоне ППИИ необходимо стремиться к достижению показателей гликемии, аналогичных у здорового человека:
• натощак – 4,4–6,0 ммоль/л;
• через 2 часа после еды – < 8,0 ммоль/л;
• перед сном – 6,0–7,0 ммоль/л;
• в 3 часа ночи – > 5,0 ммоль/л.
В настоящее время в России зарегистрированы следующие инсулиновые дозаторы; Accu-Chek D-TRONplus, Accu-Chek Spirit (Рош, Германия), Medtronic Paradigm 722 (Медтроник, США), Sooil Dana Diabecare II (SOOIL Development Сompany Ltd, Южная Кoрея).
В данной статье в качестве примера мы хотели бы подробнее остановиться на инсулиновых помпах “Акку-Чек”. Данное устройство представляет собой компактный электронный прибор, в герметичном корпусе которого располагается картридж с инсулином (рис. 4). Бесшумный мотор, управляемый двумя микропроцессорами, каждые три минуты двигает поршень внутри этого картриджа. Инсулин в свою очередь через инфузионный комплект, состоящий из длинного гибкого катетера и канюли, введенной под кожу, поступает в организм. Введение инсулина осуществляется в двух режимах: постоянная подача в малых дозах (базальный уровень с шагом введения 0,005 ЕД, т. е. 20 раз в течение минуты) и болюсный режим при приеме пищи или при высоком уровне гликемии (скорость подачи болюсного инсулина 1 ЕД в 5 секунд).

Инсулиновая помпа “Акку-Чек” собирается вручную и на каждом этапе сборки многократно тестируется. В помпе есть функция поворота экрана на 180 градусов для удобства считывания информации. В приборе возможно программирование сразу 5 базальных уровней. Помпа может работать как от аккумулятора, так и от батареек. Возможна работа с дополнительным программным обеспечением, таким как “болюсный калькулятор”. Дозатор совместим с глюкометрами “Акку-Чек”. Два микропроцессора контролируют работу друг друга. Этот двупроцессорный комплекс совершает более 9 млн проверок в сутки и своевременно сообщает пользователю всю необходимую информацию. Герметичный корпус защищает помпы от попадания пыли и влаги. Помпы имеют блокировку кнопок, исключающую случайное нажатие, а также аудио/виброподдержку сигналов предупреждения. Отключить вибросигнал невозможно. Если в резервуаре помпы остается от 0 до 20 ЕД инсулина, подается сигнал предупреждения: “инсулин в картридже заканчивается”.
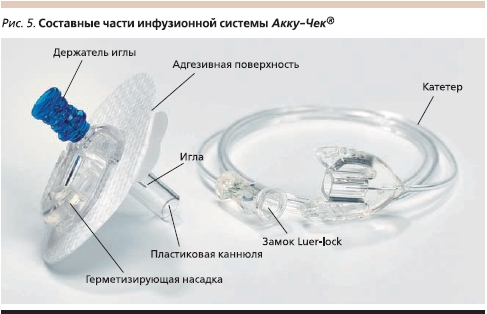
Установка дозатора на теле больного диабетом осуществляется в строго определенных местах. Канюля фиксируется на коже пациента гипоаллергенным водостойким пластырем, а гибкая трубочка вводится под кожу с помощью иглы проводника (рис. 5). Инфузионную систему необходимо менять 1 раз в 3 дня.
Проведение постоянного самоконтроля – неотъемлемая часть комплексного лечения пациента на инсулиновой помпе. При использовании ППИИ следует проводить самоконтроль гликемии не менее 4 раз в сутки. Даже при идеально отработанном базальном режиме любое дополнительное введение болюсного инсулина должно осуществляться только после исследования гликемии.
Показания к ППИИ:
• желание пациента иметь более высокое качество жизни с диабетом;
• феномен “утренней зари”;
• частые гипогликемии;
• бессимптомные гипогликемии;
• лабильное течение СД;
• беременность и планирование беременности;
• перенесенная трансплантация почек;
• гастропарез;
• высокая чувствительность к инсулину, если требуются малые дозы инсулина;
• отсутствие адекватной компенсации углеводного обмена на фоне многократных инъекций инсулина [17].
Противопоказания к ППИИ:
• низкий уровень комплаентности пациентов в отношении к проводимой терапии (пациенты, не соблюдающие режим введения инсулина, не проводящие подсчет углеводов в питании, не проводящие самоконтроль гликемии);
• психические нарушения [1].
Использование ППИИ имеет ряд преимуществ перед режимом многократных инъекций инсулина.
Введение инсулина с помощью ППИИ позволяет:
• добиваться лучших показателей гликемии [5];
• максимально приближать режим введения инсулина к профилю физиологической секреции;
• более гибко регулировать содержание глюкозы в крови при изменении режима питания, физической нагрузки и т. д.;
• уменьшать общее количество инъекций, т. к. в течение нескольких дней поступление инсулина осуществляется через катетер, что сравнимо с одной инъекцией инсулина;
• достигать точности дозирования с маленьким шагом введения инсулина – 0,1 ЕД;
• уменьшать периферическую гиперинсулинемию, что позволяет избегать передозировки инсулина;
• вести более активный образ жизни, обеспеченный за счет изменения скорости подачи инсулина;
• улучшить социальную адаптацию пациента.
К преимуществам ППИИ можно также отнести высокую предсказуемость действия инсулина, достигаемую использованием аналогов короткого действия (Хумалог, Новорапид), всасывание которых более стабильно по отношению к продленному инсулину. Если вариабельность всасывания продленного инсулина составляет около 50 %, использование коротких или ультракоротких инсулиновых препаратов позволяет снижать ее до 3 %. Кроме того, индивидуально подобранный режим введения инсулина позволяет снижать диапазон колебания уровня глюкозы крови, уменьшать количество случаев гипогликемический состояний и их тяжесть.
В 1978 г. Пикап Дж. и соавт. [15] впервые описали метод ППИИ с использованием инсулиновой помпы у больных СД1. Наблюдения последующих лет показали эффективность данного способа введения инсулина в плане достижения компенсации углеводного обмена и профилактики развития поздних осложнений СД [16]. Совершенствование инсулиновых помп повлекло за собой более активное их использовании пациентами с СД1.
Число пользователей ППИИ постоянно увеличивается. Например, в Дании в 2003 г. насчитывалось около 25 тыс. больных СД1, из них 142 человека (0,5 %) пользовались ППИИ [14], в Англии и Уэльсе 800 человек использовали помпу [17]. В США только в 2000 г. помпу применяла приблизительно 81 тыс. пациентов с СД1 [20].
В настоящее время в мире накоплен большой опыт применения инсулиновых помп. Клиническую эффективность помповой терапии оценивают по следующим критериям:
1) динамика метаболических параметров (устранение феномена “утренней зари”; изменение суточной вариабельности глюкозы крови, уровня гликированного гемоглобина, потребности в инсулине; снижение частоты развития гипогликемий и кетоацидоза);
2) влияние на массу тела;
3) частота возникновения технических проблем с оборудованием;
4) количество эпизодов инфицирования в местах постановки катетера;
5) изменение качества жизни пациента.
Феномен “утренней зари” является одной из ведущих причин повышения утренней гликемии. При использовании инсулиновых аналогов длительного действия можно в ряде случаев улучшать показатели гликемии натощак, однако полностью устранить феномен “утренней зари” невозможно. Только с помощью инсулиновой помпы удается полнее имитировать физиологическую секрецию инсулина за счет создания различной скорости подачи базального инсулина в ночные и особенно ранние утренние часы, когда необходимы значительные дозы инсулина. Это позволяет нормализовать показатели гликемии натощак.
Одним из важных факторов, препятствующих достижению компенсации углеводного обмена на фоне многократных инъекций инсулина (МИИ), является высокая вариабельность гликемии в течение суток.
Так, Bruttomesso D. показал, что у пациентов с СД1 (38 пациентов, длительность заболевания –16,6 ± 8,2 года, НbА1с – 7,6 ± 0,8 %) вариабельность уровня глюкозы в группе ППИИ была на 5–12 % ниже, чем в группе МИИ. С помощью метода постоянного мониторинга глюкозы (СGMS) было установлено, что при использовании ППИИ пациенты большее количество времени имеют нормальные и субнормальные показатели гликемии по сравнению с МИИ при одинаковых значениях НbА1с [6].
Bode B.W. и соавт. оценивали эффективность ППИИ по динамике НbА1с и частоте развития тяжелых гипогликемий в двугодичном исследовании у пациентов с СД1 (225 человек). В группе пациентов на ППИИ было зарегистрировано 22 тяжелые гипогликемии на 100 пациенто-лет, в группе на МИИ – 138 на 100 пациенто-лет. При этом достоверной динамики по уровню НbА1с в обеих группах не наблюдалось. Однако в подгруппе пациентов, исходно имеющих уровень НbА1с ≥ 8,0 %, наблюдалось снижение данного показателя с 8,9 ± 0,8 до 8,1 ± 1,0 % (p = 0,0004) [4].
Мета-анализ 21 исследования показал существенное снижение гликемии с 9,8 ± 0,5 до 6,5 ± 0,2 ммоль/л (р < 0,001) при использовании инсулиновой помпы [20].
Изменение потребности в инсулине на фоне помповой инсулинотерапии оценивалось в 22 клинических исследованиях. В 10 публикациях учитывали динамику изменения суточной дозы инсулина, а в 12 сообщениях приводили данные об изменении дозы инсулина. На фоне помповой терапии наблюдалось снижение как средней суточной дозы инсулина с 53,69 ± 0,1 до 44,19 ± 0,1 ЕД (р < 0,001), так и количества единиц инсулина на 1 кг массы тела с 0,74 ± 0,04 до 0,62 ± 0,02 (р <0,001) [20].
Изменение массы тела на фоне ППИИ оценивалось по результатам 10 исследований. Большинство авторов (7 публикаций) отметили увеличение массы тела с 68,2 ± 0,3 до 71,2 ± 0,3 кг (р < 0,001). Однако ряд исследователей выявили снижение массы тела [20].
По данным мета-анализа 29 исследований повышения риска развития гипогликемии на фоне помповой терапии не выявлено. В 4 исследованиях было отмечено снижение числа гипогликемий средней степени тяжести, а в 7 – тяжелых. В 4 исследованиях не было выявлено динамики по частоте средних, а в 10 – тяжелых эпизодов гипогликемии [20]. По данным мета-анализа 11 исследований не было отмечено существенного различия в количестве эпизодов кетоацидоза на фоне помповой терапии по отношению к ИИТ [20]. В то же время имеются сообщения, подтверждающие значительное уменьшение частота кетоацидоза на фоне применения инсулиновой помпы [14, 19].
При анализе технических проблем, возникающих при применении инсулиновой помпы, отмечены наиболее частые ситуации, с которыми сталкивались пользователи: отключение помпы, разрядка батареи, повреждение помпы самими пациентами, нарушение подачи инсулина через инфузионную систему. Инфицирование кожи в местах прикрепления катетера встречалось редко [20].
Оценка количества гипогликемий, случаев кетоацидоза, качества жизни, степени гликемического контроля была проведена Linkeschova R. в двугодичном исследовании у пациентов с СД1, использовавших ППИИ, в сравнении с группой пациентов, получавших ИИТ. В исследование были включены больные с тяжелыми гипогликемиями в анамнезе. На фоне терапии НbА1с снизился до 7,2 % в обеих группах. Частота тяжелых гипогликемических состояний при ППИИ составила 0,29 случая на 1 пациента в год по сравнению с 1,23 случая при ИИТ. В группе пациентов на помповой терапии было зарегистрировано развитие абсцессов в местах постановки катетера и кетоацидоза: 0,11 и 0,01 случая на 1 пациента в год соответственно. Все больные отметили улучшение качества жизни на помповой терапии [12, 13].
Убедительные данные о преимуществе ППИИ перед МИИ при использовании аналогов инсулина были получены в недавно завершившемся английском исследовании [3]. В группе пациентов, получавших ППИИ, наблюдалось достоверное снижение уровня НbА1с на 0,8 ± 0,8 %, а в группе пациентов на МИИ – на 0,2 ± 0,9 % (р < 0,001). Исходно все пациенты имели уровень НbА1с > 8 %. Доля пациентов на помповой терапии, достигших НbА1с < 7 %, составила 27 %, в группе пациентов на МИИ – 10 % (р < 0,001). При этом достоверных различий в количестве тяжелых гипогликемий и динамике массы тела между группами не отмечено.
Современные инсулиновые дозаторы имеют дополнительные сигнальные опции (вибрация, звуковой сигнал), информирующие пользователя о введении инсулина. Использование этих функций позволяет улучшать компенсацию углеводного обмена [3, 9].
У ряда пациентов в первые 6 месяцев на фоне ППИИ возникают психосоциальные проблемы в виде дискомфорта при ношении дозатора, ухудшаются показатели углеводного обмена, возникают трудности при физической активности, особенно при занятиях водными видами спорта [10]. Однако большинство пациентов на фоне ППИИ отмечали большую свободу в плане питания, физической нагрузки и уменьшение чувства психологической ограниченности [20].
Эффективность заместительной терапии инсулином во многом зависит от таких факторов как:
• тщательное соблюдение баланса между поступлением пищи, физической нагрузкой, дозами инсулина;
• ежедневный самоконтроль гликемии;
• самостоятельная коррекция дозы инсулина в соответствии с показателями гликемии и режимом дня;
• мотивация и желание добиться хороших показателей метаболического контроля;
• обучение и психосоциальная поддержка [1].
Следует отметить, что не у всех пациентов удается добиться улучшения показателей углеводного обмена при ППИИ. Существуют корригируемые и некорригируемые факторы, поддерживающие хроническую декомпенсацию СД. Неправильная настройка помпы, проблемы с инфузионным набором для подкожного введения инсулина, нарушение подачи инсулина помпой, пропуск или введение неправильно подобранной дозы болюсного инсулина перед едой, отсутствие коррекции дозы вводимого инсулина при приеме препаратов, повышающих гликемию (стероиды, гормоны щитовидной железы), развитие сопутствующего заболевания, физическая нагрузка – наиболее распространенные корригируемые факторы, поддерживающие хроническую декомпенсацию. К некорригируемым относятся факторы, связанные с фармакокинетикой инсулина, индивидуальные особенности адсорбции инсулина из подкожно-жировой клетчатки в местах введения инсулина с помощью катетера, снижение чувствительности к инсулину, гастропарез.
Таким образом, ППИИ являются эффективным методом введения инсулина при СД1, обеспечивающим лучший контроль заболевания без увеличения числа гипогликемий. ППИИ позволяет пациенту гибко регулировать режим инсулинотерапии в соответствии с особенностями питания, уровнем физической нагрузки, образом жизни.



