Введение
Хроническая цереброваскулярная недостаточность – один из наиболее распространенных синдромов в клинической неврологии, в т.ч. среди лиц трудоспособного возраста. Терминология ангиоцеребральной патологии дискутабельна, имеет место признание правомочности понятия «дисциркуляторная энцефалопатия», являющегося более общим определением патогенетических процессов, лежащих в основе повреждения мозга сосудистой природы, в т.ч. и ишемию, и микрогеморрагию, и нарушения ликвородинамики, и нейрогенную регуляцию микроциркуляторного русла. В то же время в существующей классификации болезней системы кровообращения остается устойчивым термин «хроническая ишемия мозга» (ХИМ), являющийся «зонтичным» диагнозом, объединяющим этиологически и патогенетически разнородную группу клинических состояний, которые развиваются в результате сосудистого поражения головного мозга (ГМ), не связанного с перенесенными инсультами [1–3].
Этиологические факторы развития ХИМ можно разделить на генетические (наличие аллели эпсилон-4 гена АРОЕ, церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией – CADASIL), социально-демографические (возраст старше 60 лет, монголоидная или негроидная раса, мужской пол, низкий образовательный уровень), общие факторы риска развития сосудистых заболеваний (артериальная гипертензия [АГ], ишемическая болезнь сердца, ортостатическая гипотензия, сахарный диабет, гиперхолестеринемия, гипергомоцистеинемия, ожирение), прочие (курение, алкоголизм, сонные апноэ) [4–6].
Как показывают результаты многих исследований, именно когнитивные нарушения (КН) представляют собой наиболее раннее и объективное проявление хронической сосудистой патологии ГМ, поэтому примерную оценку распространенности ХИМ можно сделать на основании проведенных в западных странах исследований распространенности сосудистых КН. По данным различных исследователей, цереброваскулярные КН выявляются у 5–22% пожилых лиц [1]. При аутопсии те или иные сосудистые изменения, чаще всего микроваскулярной природы, обнаруживают примерно у трети пожилых людей. Таким образом, общая распространенность хронической цереброваскулярной патологии может составлять около трети пожилых лиц.
Важнейшие в развитии ХИМ – по-прежнему сосудистые факторы риска [7]: АГ, дислипидемия, сахарный диабет, фибрилляция предсердий, избыточная масса тела/ожирение. Наблюдается взаимосвязь этих факторов, их одновременное наличие значительно увеличивает риск появления и прогрессирования КН [8]. Безусловно, немаловажную роль в развитии и прогрессировании ХИМ играют ишемическая болезнь сердца, сопровождающаяся хронической сердечной недостаточностью, гемостатические нарушения, венозная дисциркуляция, артериальная гипотония, курение, злоупотребление алкоголем [8]. При этом может формироваться поражение как мелких артерий, так и крупных артериальных стволов либо их сочетание. При преимущественном поражении артерий мелкого калибра развивается либо фокальное поражение, либо диффузное повреждение мозговой ткани в виде формирования микроинфарктов и лейкоареоза. Изменения крупных артерий приводят к формированию территориальных и «водораздельных» инфарктов мозга. Перечисленные факторы риска, имеющиеся у пациентов, способствуют развитию гемодинамических и гемореологических нарушений [9].
Основные патогенетические механизмы ишемии ГМ составляют «ишемический каскад», включающий снижение мозгового кровотока, нарастание глутаматной эксайтотоксичности, накопление кальция и лактатацидоз, активацию внутриклеточных ферментов, местного и системного протеолиза, возникновение и прогрессирование антиоксидантного стресса, экспрессию генов раннего реагирования с развитием депрессии пластических белковых и снижением энергетических процессов, отдаленные последствия ишемии (локальная воспалительная реакция, микроциркуляторные нарушения, повреждения гематоэнцефалического барьера).
Характер и выраженность клинических нарушений при ХИМ зависят от локализации, объема пораженной ткани и количества очагов, при этом мнестические расстройства, как правило, не доминируют в клинической картине [10]. В подобной ситуации становится актуальным ранжирование стадий ХИМ в зависимости от выраженности патоморфологических изменений ГМ.
Для диагностики ХИМ целесообразно использовать соответствующие критерии [5]: 1) объективно выявляемые нейропсихологические и/или неврологические симптомы; 2) признаки цереброваскулярного заболевания, включающие факторы риска и/или инструментально подтвержденные признаки поражения мозговых сосудов (например, данные дуплексного сканирования), и/или вещества ГМ (данные КТ/МРТ); 3) наличие причинно-следственной связи между сосудистым поражением мозга и клинической картиной заболевания; 4) отсутствие признаков других заболеваний, способных объяснить клиническую картину.
Патогенетическая терапия ХИМ должна быть направлена на оптимизацию мозгового кровотока и создание нейрометаболической защиты ГМ от ишемии и гипоксии. Лечение пациентов с ХИМ в первую очередь предполагает контроль сосудистых факторов риска, профилактику инсульта и прогрессирования хронической цереброваскулярной патологии и, следовательно, на улучшение когнитивных функций. Профилактика инсульта основывается на коррекции факторов его риска (курение, злоупотребление алкоголем, низкая физическая активность, ожирение), лечении АГ и сахарного диабета [11]. Рекомендуется регулярная физическая активность в виде прогулок и лечебной гимнастики, интенсивность и длительность которых зависят от функционального состояния пациента, наличия сопутствующих заболеваний; во многих случаях может быть полезным плавание. В рацион питания рекомендуется включать большое количество фруктов и овощей, обладающих антиоксидантными свойствами [12].
Комплексная терапия ХИМ включает назначения антиоксидантов, антиагрегантов, препаратов, оптимизирующих метаболизм ГМ, вазоактивных препаратов. Антидепрессанты назначаются при выраженных астенодепрессивных проявлениях заболевания. Аналогичным образом назначаются антиастенические препараты.
Важным компонентом лечения ХИМ является назначение препаратов, обладающих антиоксидантной активностью. В настоящее время в клинической практике используются следующие препараты данного ряда: мексидол, троллокс, токоферола ацетат, токоферола сукцинат, эксифон, тирилазад, меклофеноксат, атеровит, эбселен, тиотриазолин, эмоксипин, цитофлавин, глутоксим [13].
Клинические исследования [14] выявили перспективность использования этилметилгидроксипиридина сукцината для ослабления проявлений астенического синдрома, психоэмоциональных расстройств и кохлеовестибулярных нарушений у пациентов с ХИМ. Препапат способствовал уменьшению инсулинорезистентности, гипертриглицеридемии, гипергликемии у пациентов с цереброваскулярными заболеваниями и метаболическим синдромом [15].
Цель исследования: изучение эффективности и безопасности терапии антиоксидантным препаратом этилметилгидроксипиридина сукцинат в дозе 250 мг 3 раза день в течение 60 дней для пациентов с ХИМ на фоне АГ и атеросклероза.
Задачи исследования: 1) оценить эффективность этилметилгидроксипиридина сукцината 250 мг в составе комплексной терапии пациентов с ХИМ на фоне стандартной терапии в течение 60 дней при пероральном введении по сравнению с контролем; 2) оценить безопасность этилметилгидроксипиридина сукцината 250 мг в составе комплексной терапии пациентов с ХИМ на фоне стандартной терапии в течение 60 дней при пероральном введении по сравнению с контролем; 3) изучить влияние курсового парентерального и перорального приемов этилметилгидроксипиридина сукцината 250 мг на динамику неврологических и психоневрологических проявлений ХИМ в сравнении с контролем.
Методы
В исследование были включены 40 пациентов в возрасте 45–75 лет, имевших диагноз ХИМ, верифицированный методами нейровизуализации (КТ или МРТ ГМ), с признаками стабильного течения заболевания не менее месяца до скрининга, при наличии АГ, атеросклероза, отсутствии лекарственной терапии препаратами вазоактивного, ноотропного, нейротрофического, нейрорегенерационного и антиоксидантного действий, в т.ч. с действующим веществом этилметилгидроксипиридина сукцинат, за 3 месяца до включения в исследование. Критерии исключения: возраст менее 45 и более 75 лет, наличие развития инсульта за 6 месяцев до включения в исследование, наличие развития инфаркта миокарда за 6 месяцев до включения в исследование, плохо контролируемая АГ с цифрами артериального давления более 200/100 мм рт.ст., наличие деменции, сахарного диабета, застойной сердечной недостаточности функционального класса II и более, выраженной печеночной и почечной недостаточности, онкологических заболеваний; прием вазоактивных, ноотропных, нейротрофических, нейрорегенерационных и антиоксидантных препаратов за 3 месяца до включения в исследование, беременность и лактация, установленная гиперчувствительность к этилметилгидроксипиридина сукцинату, злоупотребление алкоголем, участие в других клинических исследованиях, наличие других симптомов/заболеваний, по мнению исследователя, способных препятствовать участию пациента в исследовании или влиять на результаты тестов.
Всем пациентам, включенным в исследование, помимо объективных методов обследования (артериальное давление, частота сердечных сокращений и др.), подробного неврологического исследования проводилась оценка динамики субъективных жалоб пациентов с использованием шкалы Общего клинического впечатления клинициста (Clinical Global Impression; CGI, W. Guy, 1976), монреальской шкалы оценки когнитивых функций (МоСа, Z. Nasreddine, 2004), субъективной шкалы оценки астении (MFI 20, E.M. Smets et al., 1994), шкалы Гамильтона для оценки тревоги (HARS, M. Hamilton, 1959) и шкалы депрессии Гамильтона, а также оценки двигательной активности пожилых (шкала Тинетти, M. Tinetti,1986).
Пациенты, включенные в исследование, были рандомизированы в две группы методом конвертов. Пациентам 1-й (основной) группы (20 человек) назначался этилметилгидроксипиридина сукцинат перорально в дозе 250 мг 3 раза сутки в течение 60 дней от начала включения в исследование; пациентам 2-й (контрольной) группы проводилась коррекция имевшихся факторов риска (гипотензивная, гиполипидемическая, антиагрегантная или антикоагулянтная терапия, коррекция эмоционального статуса) в соответствии с принятыми клиническми рекомендациями, проколами ведения АГ, атеросклероза, ХИМ.
Все пациенты подписали информированное согласие на включение в исследование.
Статистическая обработка его результатов проводилась с использованием пакета прикладных программ Статистика 8.0. Степень статистической значимости различий несвязанных групп оценивалась с использованием непараметрического критерия Манна–Уитни. Степень статистической значимости различий между связанными группами оценивалась с использованием непараметрического критерия Вилкоксона. Различия считались значимыми при уровне р<0,05.
Результаты исследования
Исследование проводилось на базе кафедры нервных болезней с курсом медицинской реабилитации Красноярского государственного медицинского университета им. профессора В.Ф. Войно-Ясенецкого с 01.04.2019 по 01.07.2019. Исследование прошло этическую экспертизу в локальном этическом комитете КрасГМУ.
При обследовании пациентов на момент включения в исследование получены следующие результаты: включены 40 пациентов, из них 29 (72,5%) женщин и 11 (27,5%) мужчин в возрасте от 52 до 72 лет, медиана возраста составила в первой группе 59,1 [56; 71] года, во второй – 58,9 [57; 70]. Группы не различались по половозрастному составу, выраженности сосудистых факторов риска.
Пациенты 1-й и 2-й групп предъявляли жалобы на головную боль в 72 и 66% случаев соответственно, головокружение – в 38 и 32%, на шаткость – в 12 и 16%, на изменения настроения в 56 и 34%, снижение памяти, концентрации внимания – в 23 и 30% случаев.
По оценке состояния на момент включения в исследования по клиническим шкалам получены данные, представленные в табл. 1.

Как видно из представленных данных, группы были однородными по степени выраженности жалоб, а также вестибуло-атактических, астенических, когнитивных, эмоционально-волевых нарушений. Степень выраженности астении в обеих группах соответствовала клинически выраженной, у пациентов основной и контрольной групп эмоционально-волевые нарушения соответствовали симптоматической тревоге, легкой степени депрессии, уровень КН – умеренным расстройствам в обоих группах, двигательная активность по шкале Тинетти соответствовала на момент включения в обоих группах ее умеренному снижению.
Повторное обследование пациентов через 2 недели лечения обнаружило удовлетворительную переносимость терапии, случаев отмены приема тестируемого препарата из-за непереносимости в основной группе не отмечено, у 3 человек основной группы и 1 – контрольной появилась умеренная головная боль, не требовавшая приема дополнительной терапии, изменения схемы лечения. При этом у ряда пациентов жалобы уменьшились: так, на 2-й неделе лечения пациенты 1-й и 2-й групп предъявляли жалобы на головную боль в 68 и 65% случаев соответственно, на головокружение – в 28 и 33%, на шаткость – в 12 и 16%, на изменения настроения – в 30 и 24%, на снижение когнитивных функций – в 24 и 30% случаев.
При повторном тестировании по набору используемых шкал были получены показатели, представленные в табл. 2.
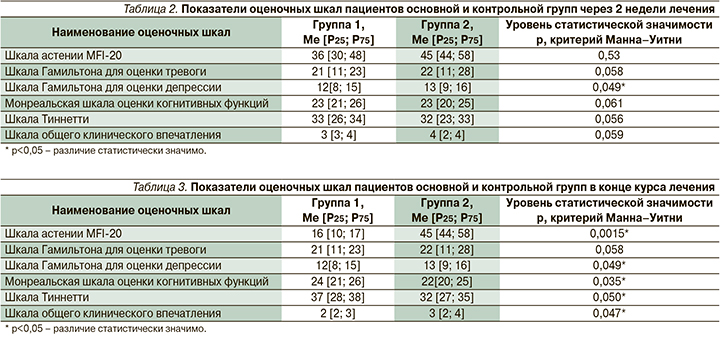
Повторная оценка по шкалам свидетельствует о тенденции к улучшению по шкале равновесия Тиннети, шкале Гамильтона для оценки тревоги и депрессии, шкале общего клинического впечатления. Комплаентность пациентов в обеих группах была высокой, рекомендовано продолжение терапии.
При повторной оценке состояния пациентов в конце курса лечения (через 2 месяца терапии) произошли его следующие изменения: в 1-й и 2-й группах число больных, жаловавшихся на головную боль, уменьшилось на 60 и 5% соответственно, на головокружение – на 50 и 15% соответственно, на шаткость – на 70 и 10%, изменения настроения – на 80 и 27%, КН – на 50 и 12%.
При использовании набора валидизированных шкал получены данные, представленные в табл. 3.
Как следует из представленных данных, в результате лечения препаратом этилметилгидроксипиридина сукцинат 250 мг в основной группе значительно снизилась выраженность симптомов астении по субъективной шкале ее оценки MFI-20 от исходной выраженной астении с медианой 48 [47; 57] до нормальных показателей – 16 [10; 17] (р<0,0001, критерий Вилкоксона), при этом антиастенический эффект препарата проявлялся уже на ранних этапах лечения. Оценка когнитивных функций в конце лечения показала усиление психической работоспособности и темпа выполнения заданий, при этом показатели Монреальской шкалы оценки когнитивных функций имели позитивную динамику в основой группе заболевания с медианой при включении в исследование – 22 [20; 25], в конце курса лечения – 24 [21; 26] (р=0,026, критерий Вилкоксона).
Регресс жалоб на головокружение и шаткость в конце лечения сопровождались повышением оценки двигательной активности пожилых по шкале Тинетти от умеренной степени нарушения при включении в исследование (32 [23; 33]) до легкой степени в конце курса терапии: 37 [28; 38] (р<0,001, критерий Вилкоксона).
Оценка обследуемых пациентов обеих групп по шкале общего впечатления обнаружило преимущество в основной группе больных (р=0,047, критерий Манна–Уитни), прошедших лечение с использованием препарата этилметилгидроксипиридина сукцинат 250 мг по сравнению с пациентами, получавшими лечение в рамках коррекции факторов риска в соответствии с общепринятыми стандартами ведения АГ и атеросклероза.
Обсуждение
Хронические цереброваскулярные заболевания – состояния, с которыми наиболее часто приходится сталкиваться врачам различных специальностей в повседневной практике, поэтому научные исследования данной проблемы не теряют своей актуальности. Разнообразные патологические состояния, лежащие в основе развития ХИМ, предопределяют формирование ангиоэнцефалопатии, которая проявляется различными нервно-психическими расстройствами, в зарубежной литературе нередко выделяемыми в качестве самостоятельных нозологических форм, например мультиинфарктная лейкоэнцефалопатия, болезнь Бинсвангера и др. Патогенетическая терапия ХИМ должна быть направлена на оптимизацию мозгового кровотока и создание нейрометаболической защиты ГМ от ишемии и гипоксии. Вот почему наряду с коррекцией сосудистых факторов риска внимание исследователей привлекают препараты антиоксидантного действия.
Этилметилгидроксипиридина сукцинат, изучен и разработан в НИИ фармакологии РАМН и Всесоюзном научном центре по безопасности биологически активных веществ [16]. Препарат обладает широким спектром фармакологических эффектов, оказывает антиоксидантное, антигипоксантное, анксиолитическое, антистрессорное, противоалкогольное, противосудорожное, нейропротективное, ноотропное, антимнестическое, нейропсихотропное, кардиопротективное, антиатеросклеротическое, антиагрегантное, противопаркинсоническое, вегетотропное действия. Клинические исследования [17–19] продемонстрировали достоверные терапевтические эффекты препарта при лечении неврологических, психических и сердечно-сосудистых заболеваний.
Так, этилметилгидроксипиридина сукцинат проявил эффективность при лечении невротических и неврозоподобных расстройств, различных состояний при алкоголизме, в т.ч. абстинентного синдрома, а также острых и хронических нарушений мозгового кровообращения (инсульт, дисциркуляторная энцефалопатия, вегетососудистая дистония), нарушений функций ГМ при старении и атеросклерозе.
Существенным преимуществом препарта являются широкий спектр его фармакологических эффектов, низкая токсичность, практическое отсутствие побочных эффектов (типичных, например, для некоторых «стандартных» нейропсихотропных препаратов), седативного, миорелаксантного, возбуждающего и эйфоризирующего действий [18].
Заключение
В настоящей работе представлены результаты применения этилметилгидроксипиридина сукцината в дозировке 250 мг 3 раза в день в течение 2 месяцев пациентами с ХИМ, вызванной АГ и атеросклерозом. Результаты применения препарата свидетельствуют об эффективности лечения основных неврологических, нейропсихиатрических симптомов ХИМ, таких как головокружение, атаксия, КН, тревога и астения. В результате лечения препаратом этилметилгидроксипиридина сукцинат 250 мг в основной группе имело место значительное снижение выраженности симптомов астении по субъективной шкале оценки MFI-20, при этом антиастенический эффект проявлялся уже на ранних этапах лечения. Оценка когнитивных функций в конце лечения показала усиление психической работоспособности и темпа выполнения заданий по данным Монреальской шкалы оценки когнитивных функций, регресс жалоб на головокружение и шаткость в конце лечения сопровождался повышением оценки двигательной активности у пожилых по шкале Тинетти. На протяжении 2 месяцев препарат демонстрировал безопасность при использовании в указанной дозировке. Выявленные побочные эффекты были кратковременными и незначительными.



