Введение
Несмотря на всевозрастающее освещение проблемы и социальной значимости инфекций, передаваемых половым путем (ИППП), в популярных средствах массовой информации ежегодно в мире регистрируется сотни миллионов случаев подобных заболеваний, среди которых до 100 млн обусловлено именно хламидийной инфекцией (ХИ) урогенитальной локализации. Хламидиоз по праву считается «тихой», или «спящей», инфекцией, т.к. начальные неосложненные его формы в виде уретрита у мужчин и слизисто-гнойного цервицита у женщин более чем в половине случаев протекают со стертой симптоматикой или вовсе бессимптомно. Последнее обстоятельство служит и главным фактором эпидемио-логического распространения ИППП негонококковой природы. При этом абсолютно точно установлены крайне негативные последствия длительного прогрессирования хламидиоза на мужскую и женскую фертильность к моменту изменения приоритетов в жизни молодых людей, когда на первый план выходит не поиск полового партнера, а желание создания семьи и возможность продолжения рода.
В связи с этим представляется крайне важным ранняя точная диагностика заболевания и безотлагательное начало эффективного антибактериального лечения до начала необратимых изменений в тканях репродуктивной системы.
Характеристика возбудителя
Хламидии – уникальный облигатный внутриклеточный грамотрицательный бактериальный патоген, способный вызывать заболевания у человека и животных. Из 19 известных серотипов Chlamydia trachomatis 8 способны поражать урогенитальный тракт (другие становятся причиной трахомы, венерической лимфогранулемы, инфекций лимфатической системы) [1, 2]. Бактерия характеризуется наличием бифазного жизненного цикла в виде элементарных телец, находящихся внеклеточно, и ретикулярных телец с внутриклеточной локализацией. Заражение происходит при контакте элементарных телец с эпителием урогенитального тракта, после чего наблюдаются процесс эндоцитоза (проникновения внутрь клетки) и трансформация метаболически неактивных элементарных телец в более крупные и метаболически активные ретикулярные тельца, способные размножаться. После завершения жизненного цикла хламидии вновь трансформируются в элементарные тельца, которые, разрушая мембрану, выходят наружу (экзоцитоз) и инфицируют соседние интактные клетки, распространяя инфекционный процесс. Важнейшим звеном патогенеза является внутриклеточная локализация возбудителя, что препятствует развитию нормального иммунного ответа и эрадикации, способствуя персистенции инфекции [3]. Внутриклеточная локализация возбудителя в данном случае – исторически верное обоснование выбора эффективных антимикробных препаратов (АМП) для лечения, характеризующихся большим объемом распределения и способных создавать высокие тканевые концентрации.
Эпидемиология и социальное значение ХИ
Вопреки широкой доступности барьерной контрацепции, повышенному вниманию к проблеме ИППП медицинской общественности и сексуально активных лиц молодого возраста сегодня отмечается общемировая тенденция стабильного роста заболеваемости хламидиозом. Согласно данным ежегодного отчета по венерическим заболеваниям от Центров по контролю и профилактике заболеваний (CDC – Centers for Disease Control and Prevention), в 2015 г. заболеваемость хламидиозом в США составила более 400 случаев на 100 тыс. населения.
И основное число зарегистрированных случаев приходилось на женщин в возрасте 19–24 лет [4].
В Европе показатели заболеваемости хламидиозом несколько ниже – 173 случая на 100 тыс. населения в 2015 г. [5]. При этом стоит отметить, что заболеваемость в отдельных странах Евросоюза сильно различается, что связано скорее не с реальными отличиями в распространенности ХИ, а различной степенью выявляемости. Относительно низкие показатели заболеваемости ХИ в России (менее 50 на 100 тыс. населения) также могут быть связаны с неполным выявлением больных ХИ в связи с широким использованием низкочувствительных методов диагностики (ПИФ – прямая иммунофлуоресценция, ИФА – иммуноферментный анализ) и отсутствием программ скрининга групп риска [6, 7].
В среднем в 25–50% случаев ХИ протекает бессимптомно. Тем не менее клиническая картина инфекции у женщин помимо цервицита может включать проявления уретрита, бартолинита и поражения верхних отделов генитального тракта (эндометрит, сальпингоофорит) и даже брюшины (выражающиеся в перигепатите и перисплените), а также реактивного артрита. Нелеченая инфекция известна своими последствиями, касающимися репродуктивной функции: бесплодие, эктопическая беременность, невынашивание и осложнения беременности (преждевременные роды, низкая масса плода и высокая неонатальная смертность, послеродовый эндометрит) [8–12]. По некоторым наблюдениям, у 20% женщин со слизисто-гнойным цервицитом развивается воспалительное заболевание органов малого таза, приблизительно у 4% – синдром хронической тазовой боли, у 3 и 2% – бесплодие и невынашивание соответственно [13, 14].
Особую проблему представляет и риск инфицирования новорожденного в случае ХИ половых путей матери. Так, риск развития конъюнктивита и пневмонии у таких детей при физиологических родах может составлять 20–50% и 10–20% соответственно [15].
На этом более чем серьезном фоне складывается ситуация недостаточно внимательного отношения к последствиям хламидийного поражения мужских половых органов. На сегодняшний момент несомненна этиологическая роль хламидий для уретрита, эпидидимита и орхоэпидидимита. Также не исключена роль патогена в возникновении простатита и везикулита [16–18].
C. trachomatis служит самой частой причиной уретритов у мужчин вообще и самой частой причиной т.н. негонококковых уретритов (НГУ) в частности. Так, в среднем, по данным различных исследователей, хламидии выделяют в 30% случаев всех уретритов и в более чем 42% случаев НГУ [19]. По другим данным, у четверти пациентов с НГУ заболевание протекает бессимптомно, а хламидии выделяют примерно в половине всех случаев уретритов с клиническими проявлениями и без [20–23]. У 70% мужчин заболевание сопровождается выделениями из уретры и раздражением ее наружного отверстия, дизурией, симптомами эпидидимита, орхита или простатита, что обычно наблюдается через 1–3 недели после инфицирования [24].
При наличии 150 млн популяции мужчин в США там ежегодно регистрируют до 600 тыс. случаев эпидидимита, к основным симптомам которого относятся боль, отек мошонки, изменение структуры придатка яичка, лихорадка, расстройства мочеиспускания, выделения из уретры [17, 25]. В прогрессирующее инфекционное воспаление может быть вовлечено и яичко, в результате чего развивается орхоэпидидимит. Важным последствием перенесенного заболевания является уменьшение числа сперматозоидов в семенной жидкости и снижение их подвижности, что и становится в большинстве случаев причиной мужского бесплодия [26–28]. Помимо орхита и эпидидимита к осложнениям негонококкового уретрита относят синдром Рейтера (реактивный артрит и конъюнктивит) и поражения аноректальной области.
Отрицательная роль и степень влияния ХИ на мужскую фертильность еще окончательно не определены, однако ряд весьма доказательных экспериментальных и клинических данных все-таки свидетельствует в ее пользу. Например, исследования с применением электронной микроскопии продемонстрировали возможности взаимодействия хламидий со сперматозоидами [29, 30]. Более того, элементарные тельца хламидий могут вести к апоптозу мужских половых клеток [31]. Множество исследований выявили корреляцию между ХИ количественными и качественными характеристиками спермы [32–34]. Наконец, клинические наблюдения также свидетельствуют о взаимосвязи патогена с мужским бесплодием [13, 35–37]. Перспективным считается направление раскрытия аутоиммунных механизмов в нарушении фертильности вследствие перенесенного инфекционного заболевания. Парадоксальный иммунный ответ при этом направлен на потенцирование хронического воспаления, что в итоге ведет к пролиферации клеток, перестройке тканей, рубцеванию и аутоиммунному ответу у предрасположенных индивидуумов [38, 39]. К «промежуточным» проблемам на пути потери репродуктивного здоровья относятся существенно ухудшающие качество жизни синдром хронической тазовой боли (у мужчин и женщин), а также воспалительные заболевания органов малого таза.
Принимая во внимание не только сиюминутную необходимость лечения острого НГУ и слизисто-гонойного цервицита, но и серьезные социальные последствия ХИ, особую актуальность представляют своевременная диагностика и адекватный выбор АМП с учетом принципов рационального использования последних.
Диагностика
Диагноз заболевания устанавливается на основании клинической картины и выявления возбудителя в результате лабораторных исследований клинического материала.
Молекулярно-биологическое исследование направлено на выявление нуклеиновых кислот C. trachomatis методом полимеразной цепной реакции в режиме реального времени (ПЦР-РВ). Данный вид исследования имеет самую высокую чувствительность и специфичность, позволяя обнаружить возбудителя в концентрациях, много меньших, чем предел обнаружения хламидий другими лабораторными методами, включая ПИФ или культуральный метод. Чувствительность и специфичность исследования составляют 95–98% и 99–100% соответственно. ПЦР может быть использована для выявления генетического материала хламидий в любом клиническом образце, в т.ч. полученном неинвазивным способом (первая порция мочи). Отличительной особенностью ПЦР-РВ является возможность одновременной диагностики нескольких этиологически значимых возбудителей, а для пациентов с подозрением на ИППП это особенно актуально.
Культуральный метод является «золотым» стандартом по специфичности (100%), однако вследствие низкой чувствительности (40–60%), трудоемкости, длительности и дороговизны процесса культивирования хламидий его использование в рутинной практике имеет существенные ограничения. ПИФ отличается высокой степенью субъективности оценки результатов и низкой воспроизводимостью, а серологические методы, основанные на определении антихламидийных антител в сыворотке крови, для диагностики локализованной ХИ не применяются. В связи с этим в учреждениях практического здравоохранения необходимо отдавать предпочтение современным молекулярным методам диагностики [41].
Для получения наиболее достоверных результатов лабораторных исследований необходимо соблюдение следующих условий:
- пациент не принимал системных или местных АМП в течение 7–8 суток до обследования;
- пациент воздерживался от мочеиспускания не менее 2 часов до обследования;
- пациент воздерживался от незащищенных половых контактов в течение суток до обследования;
- клинический материал получен с учетом субъективных и объективных проявлений заболевания (материал из локуса, где имеются клинические проявления, т.е. из уретры и цервикального канала для мужчин и женщин соответственно).
Считаем необходимым отметить, что в настоящий момент коммерчески широко доступными являются комплексные тест-системы, позволяющие быстро (в течение нескольких часов) определять генетический материал трех наиболее важных возбудителей ИППП – гонококков, хламидий и микоплазм (Mycoplasma genitalium) – в клиническом материале одновременно. Точное выделение возбудителя/лей в конкретной клинической ситуации представляется совершенно необходимым для исключения необоснованного назначения тех или иных антибиотиков и в то же время – для расширения возможностей терапевтического выбора препаратов (или их комбинации) в целях незамедлительного начала лечения [42, 43].
Лечение
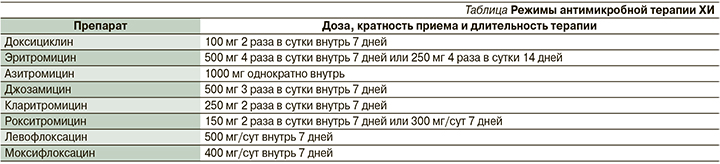
К основным задачам лечения относятся элиминация возбудителя, разрешение клинических проявлений болезни, предупреждение развития осложнений и распространения инфекции. С целью лечения ХИ традиционно используются препараты различных фармакологических групп: макролиды, тетрациклины и фторхинолоны (см. таблицу). Определение чувствительности хламидий к АМП в рутинной практике не проводится в связи с тем, что стандартизированные методы тестирования антибиотикорезистентности патогена к настоящему времени не разработаны. В то же время отдельные наблюдения свидетельствуют об отсутствии роста резистентности хламидий к АМП вообще и макролидам в частности [40]. Кроме того, высокая клиническая эффективность антибиотиков не всегда коррелирует с показателями активности препаратов in vitro [41, 44].
Пациентам следует разъяснить необходимость обследования их половых партнеров на ХИ и другие ИППП. Следует убедить пациента использовать барьерные средства контрацепции при половых контактах (или вовсе воздерживаться от них) до полного излечения. Установление клинико-микробиологических критериев излеченности ХИ проводится не ранее чем через 3 недели после начала терапии.
Исторически эритромицин и доксициклин были первыми АМП, использовавшимися для терапии ХИ генитальной локализации. Появление современных макролидов (азитро-, кларитро-, рокситромицин) с лучшими фармакокинетическими характеристиками и более выгодным профилем безопасности наряду с доступностью «новых» фторхинолонов (лево- и моксифлоксацин) существенно расширило армаментариум врача-уролога и дерматовенеролога в лечении хламидиоза.
С середины 1990-х гг. предпочтение в лечении генитального хламидиоза отдавалось именно современным макролидам. На фоне гораздо лучшей переносимости и более высокой приверженности лечению (по сравнению с эритромицином и доксициклином) кларитромицин, например, демонстрировал еще и в 8 раз бóльшую активность в отношении хламидий по сравнению с эритромицином [45–47]. Последнее обстоятельство нашло свое подтверждение в весьма оптимистичных результатах первых клинических сравнительных исследований терапии пациентов с хламидиозом урогенитальной локализации [48–51].
Современная доказательная база обоснованности использования кларитромицина основана на актуальных данных сохраняющейся высокой активности препарата (в т.ч. по сравнению с другими современными макролидами), результатах качественных клинических исследований и наличии препарата в схемах лечения, приведенных в авторитетных руководствах [40, 44]. Так, частота эрадикации C. trachomatis цервикальной локализации у работниц коммерческого секса и в общей популяции женщин после 7-дневного курса терапии кларитромицином составила 100%, тем не менее для достижения подобных показателей для эрадикации возбудителя фарингеальной локализации понадобились более длительные (14-дневные) курсы. Авторы исследования особенно отмечают, что в связи с высочайшей чувствительностью метода ПЦР-РВ окончательное суждение об эффективности терапии следует формировать по прошествии не менее 3 недель после ее окончания [52].
Необходимо заметить, что далеко нередким феноменом является уретрит, при котором молекулярные методы выявления возбудителей показывают отрицательный результат в отношении как распространенных гонококков и хламидий, так и реже встречающихся мико- и уреаплазм. При этом патогенность последних точно не определена. Считается, что уреаплазмы могут быть целью терапии только при наличии клинических проявлений в случае, когда другие возбудители не выявлены высокоточными методами диагностики. Продолжающиеся симптомы уретрита в отсутствие возбудителя связывают со сложностью воспалительного ответа при ИППП, обусловливающего длительную воспалительную реакцию даже после элиминации патогенов [43]. Интересным фактом служит демонстрация высокой частоты (90,7%) нормализации уретрального мазка в таких клинических случаях после курса терапии кларитромицином [53].
Заслуживает внимания точка зрения, согласно которой азитромицин, до недавнего времени широко рекомендовавшийся для стартовой терапии НГУ в режиме 1 г (реже 2 г) однократно, может потенцировать рост резистентности микоплазм к макролидам [42]. В связи с этим последнее Европейское руководство по лечению НГУ рекомендует вернуться к 4-дневной схеме приема препарата, что в значительной мере нивелирует преимущество приверженности приему азитромицина по сравнению с другими современными макролидами [43]. Последнее обстоятельство, как известно, сыграло не последнюю роль в вытеснении других современных макролидов из схем лечения НГУ в ведущих руководствах, несмотря на то что кларитромицин, например, обладает высокой in vitro-активностью в отношении других возбудителей заболевания (M. genitalium) и характеризуется высокой эффективностью в лечении таких пациентов [54, 55].
Заключение
Таким образом, ХИ урогенитальной локализации представляет собой сложную медицинскую и социальную проблему, касающуюся не только аспектов дальнейшего распространения инфекции вследствие возможного бессимптомного течения заболевания и проблем, связанных с возможными неудобствами, сопровождающими уретрит и цервицит, но и нарушениями фертильности мужчин и женщин.
С учетом вышесказанного оперативная достоверная неинвазивная диагностика с использованием молекулярных методов определения генетического материала (ПЦР-РВ) хламидий в клиническом материале (моча, отделяемое из уретры и цервикального канала) остается условием своевременного начала лечения заболевания до развития осложнений и необратимых последствий, серьезно снижающих качество жизни.
Современные схемы лечения хламидиоза предполагают использование широкого круга АМП из группы макролидов, тетрациклинов и фторхинолонов со сравнимо высокой эффективностью и безопасностью. На этом фоне доступность того или иного антибиотика на рынке, репутация производителя вкупе с индивидуальными особенностями переносимости и характеристиками, влияющими на приверженность лечению (например, возможность приема 1–2 раз в сутки и высокая безопасность для современных макролидов), являются сегодня фактором, определяющим рациональный выбор терапии в каждом конкретном случае.
Популярное освещение проблемы ИППП в развитых странах обычно сопровождается повышением сознательности и социальной ответственности молодых и сексуально активных мужчин и женщин [56]. Добавим, что пропаганда здорового образа жизни и семейных ценностей наряду с данным подходом считается важным моментом предупреждения распространения и профилактики развития известных негативных последствий ИППП.



