Введение
Возможным путем повышения эффективности эрадикации Helicobacter pylori и оптимизации лечения H. pylori-ассоциированных заболеваний является применение пробиотиков. Препараты с пробиотическим действием кроме коррекции дисбиотических изменений кишечной микрофлоры обеспечивают ряд дополнительных положительных эффектов, например иммунологических (улучшение показателей гуморального и клеточного иммунитета, снижение аллергизации организма), а также оказывают воздействие на H. pylori в желудке за счет прямого антагонистического влияния и стимуляции местной иммунологической защиты (укрепление слизистого защитного барьера и снижение выраженности воспаления слизистой оболочки желудка, выработка бактериоцинов) [1–3].
В ряде работ показано, что применение пробиотиков (на основе бифидобактерий, лактобацилл, культуры сенной палочки и др.) в отношении больных заболеваниями, ассоциированными с H. pylori, способствует улучшению состояния микрофлоры кишечника, снижению риска развития побочных эффектов антибактериальной терапии, в т.ч. антибиотикоассоциированной диареи, способствует наступлению более быстрой клинико-эндоскопической ремиссии заболевания и повышению эффективности эрадикации H. pylori [4–8].
В постулатах IV и V Маастрихтских консенсусов упоминается о возможной эффективности некоторых пробиотиков в качестве дополнения к стандартной эрадикационной терапии [9, 10].
Исследования, посвященные роли пробиотиков в эрадикации H. pylori, движутся по двум направлениям.
В первом случае пробиотики включают в состав стандартной эрадикационной терапии [11–13]. Второе направление изучает влияние монотерапии пробиотиками на эффективность антихеликобактерной терапии [14–18]. Важным аспектом является также подтверждение антагонистических свойств пробиотиков in vitro для более четкого понимания процессов взаимодействия пробиотических штаммов с H. pylori. Предлагается схема основных механизмов положительного влияния пробиотиков (средств коррекции нарушений микробиоценоза кишечника) на эффективность эрадикации Helicobacter pylori (рис. 1) [19–21].
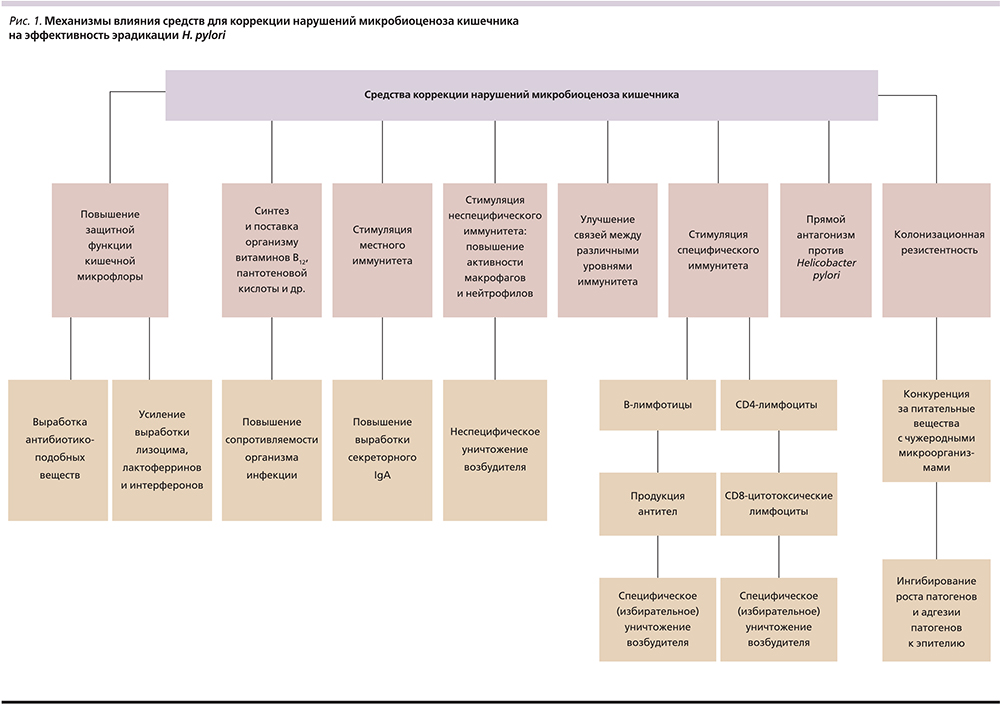
Цель работы: изучить влияние некоторых пробиотиков на рост инфекции H. pylori in vitro, оценка эффективности эрадикации при использовании монотерапии пробиотиками in vivo.
Материал и методы
Исследование in vitro
Были успешно культивированы 14 штаммов H. pylori. Штаммы микроорганизма были получены при проведении бактериологического анализа биоптатов слизистой оболочки антрального отдела желудка пациентов с клиническими проявлениями диспепсии. Инкубирование проведено в стандартных условиях для роста H. pylori. Оценивалось действие трех различных пробиотиков: 1-й – на основе Enterococcus faecium strain L-3, 2-й – на основе лиофилизированной культуральной жидкости Bacillus subtilis, 3-й – на основе комбинации Bifidobacterium longum и E. faecium. Исследуемые пробиотики разводились в дистиллированной воде в соотношении 1:100 и затем добавлялись в чашку с агаром, на который высевался штамм H. pylori. Учет роста осуществлен на 6–7-е сутки.
Исследование in vivo
Под наблюдением находились 55 больных хроническим гастродуоденитом, ассоциированным с H. pylori.
В зависимости от получаемой терапии пациенты были разделены на 3 группы. 1-я группа (18 больных) получала пробиотик на основе B. subtilis, 2 капсулы 2 раза в сутки во время еды 20 дней (согласно схеме назначения в инструкции); 2-я группа (17 пациентов) – пробиотик на основе E. faecium, 3 драже 3 раза в сутки во время еды в течение 1 месяца (согласно схеме назначения в инструкции), 3-я группа (20 больных – группа сравнения) – стандартную тройную эрадикационную терапию (омепразол 20 мг 2 раза в сутки, амоксициллин 1000 мг 2 раза в сутки, кларитромицин 500 мг 2 раза в сутки 7 дней). В 1-ю и 2-ю группы вошли пациенты, у которых имела место аллергическая реакция на кларитромицин или амоксициллин и/или которые отказались от проведения тройной эрадикационной терапии. До и после лечения (через 1,5–2,0 месяца) проведен стандартизированный опрос всех больных для оценки характера жалоб, фиброэзофагогастродуоденоскопия с взятием двух биоптатов из антрального отдела желудка для верификации инфекции H. pylori (проведены быстрый уреазный тест, гистологическое исследование биоптатов, полимеразная цепная реакция с детекцией гена ureC). Статистическая обработка данных осуществлена с помощью программы Excel для Windows.
Результаты и обсуждение
Исследование in vitro
Ингибирование роста H. pylori имело место в 50% случаев при контакте культуры микроорганизма с пробиотиком на основе B. subtilis, в 78,6% случаев при контакте с пробиотиком на основе E. faecium strain L-3 и в 64% случаев при контакте с пробиотиком на основе B. longum и E. faecium (см. таблицу).
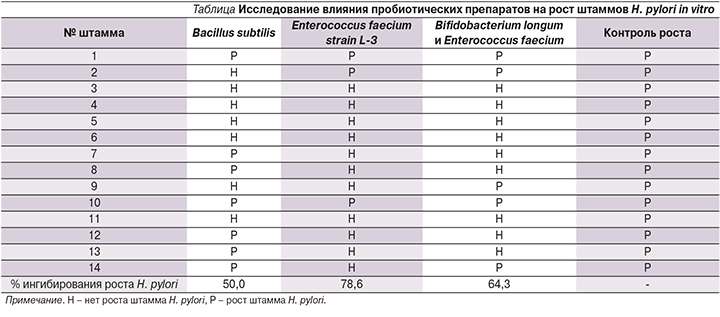
Из представленной таблицы видно, что ингибирование роста H. pylori при контакте со всеми тремя выбранными пробиотиками произошло лишь у 35,7% штаммов данного микроорганизма. Ингибирование роста 35,7% штаммов микроорганизма было отмечено в присутствии каких-либо двух из трех пробиотиков. В 14,3% случаев ингибирование роста H. pylori определено в присутствии только какого-то одного пробиотика. Это может говорить о различной реакции штаммов возбудителя на разные пробиотики и требует дальнейшего изучения.
Исследование in vivo
Пробиотики в качестве монотерапии H. pylori-ассоциированного гастрита показали свою эффективность (рис. 2) и безопасность. Пациенты отмечали хорошую переносимость пробиотических препаратов, побочных эффектов на фоне их приема выявлено не было.
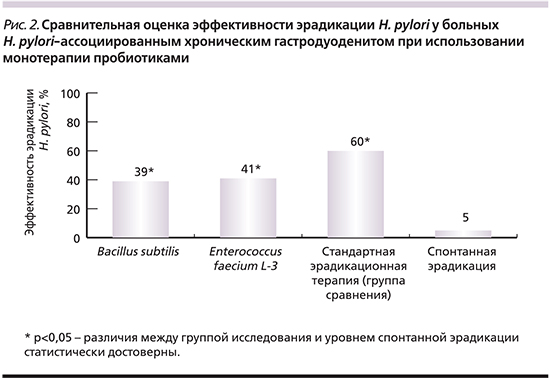
Заключение
Результаты, полученные in vitro, могут быть следствием прямого ингибирующего (антагонистического) действия пробиотиков (возможно, за счет синтеза бактериоцинов) в отношении H. pylori. Однако данная гипотеза нуждается в дальнейшем углубленном изучении. Использование монотерапии пробиотиками обеспечивает достижение уровня успешной эрадикации H. pylori (39 и 41%), достоверно превышающего процент спонтанной эрадикации (3–5%). Лучшие показатели ингибирования H. pylori продемонстрировал пробиотический штамм E. faecium strain L-3 in vitro и in vivo. Следовательно, возможно проведение дальнейших исследований именно с этим пробиотиком. В целом монотерапия пробиотиками может быть рекомендована как альтернативный способ лечения хронического гастродуоденита, ассоциированного с H. pylori, в особенности при непереносимости компонентов стандартной антихеликобактерной терапии.



