Успешное решение проблем, связанных с диагностикой и лечением бесплодия, привело к постановке новых задач, поскольку целью лечения бесплодия является не только наступление беременности, но и в первую очередь сохранение здоровья женщины и рождение здоровых детей. В настоящее время наиболее актуальна проблема влияния методов, используемых для достижения беременности у женщин с бесплодием, на состояние их здоровья.
Mолочные железы – органы репродуктивной системы, которые являются «мишенью» для стероидных гормонов, гормонов коры надпочечников, щитовидной железы, гипофиза и различных биологически активных соединений. Поэтому патологические стимулы, возникающие в результате нарушений в сложной цепи гормональных взаимоотношений, могут приводить к развитию как гипер-, так и гипопластических изменений.
Для всех гиперпластических процессов характерно сильнейшее влияние стероидных гормонов. Так, в женской репродуктивной системе ключевыми гормонами являются эстрогены: эстрон, эстрадиол, эстриол. При лечении бесплодия применяют препараты, стимулирующие функцию яичников, при этом наблюдается значительное повышение уровня эндогенных гормонов, в первую очередь эстрогенов. Поэтому дисбаланс нормального функционирования гипоталамо-гипофизарной системы может приводить к нарушению физиологических преобразований в молочной железе (МЖ) и развитию в ней патологической пролиферации.
Поскольку большинство факторов риска развития патологии МЖ, в частности бесплодия, связано с длительным воздействием эндогенных половых стероидов, возможность ассоциации применения индукторов овуляции с риском рака МЖ (РМЖ) представляет серьезный научный и клинический интерес. Следовательно, данную группу женщин можно отнести к группе риска по заболеваниям МЖ.
Учитывая интенсивный рост заболеваемости РМЖ и широкую распространенность фиброзно-кистозной болезни, возникает крайняя необходимость интегрировать в сферу задач акушерско-гинекологической помощи проблемы профилактики, ранней диагностики и лечения целого ряда доброкачественных патологических процессов, являющихся фоном развития РМЖ.
Все вышеизложенное заставляет относиться к гормональной терапии при бесплодии с осторожностью и создает необходимость комплексного обследования МЖ у женщин с различными факторами бесплодия в рамках подготовки к проведению программ вспомогательных репродуктивных технологий (ВРТ) и профилактических мероприятий для уменьшения отрицательных влияний гормональной терапии ввиду высокой частоты доброкачественных изменений МЖ у данного контингента женщин.
Первым этапом является комплексное обследование МЖ перед проведением репродуктивных технологий. Ранняя диагностика дисгормональных и опухолевых заболеваний МЖ необходима перед проведением протоколов, связанных с репродуктивными методами лечения.
Кажущаяся простота и доступность МЖ для обследования нередко приводят к ошибочной постановке диагноза и неправильной трактовке результатов осмотра и исследований. Это часто приводит не только к недооценке степени выраженности заболевания, но и к гипердиагностике, результатом которой является тяжелая психическая травма, приводящая к эндогенной депрессии. Еще более непоправимый вред приносит пропуск онкологической патологии.
Соответственно, данные консультации в клиниках репродуктивной медицины должны осуществляться онкологом или акушером-гинекологом, прошедшим соответствующие курсы тематического усовершенствования.
Самым первым этапом является осмотр МЖ врачом-онкологом. При сборе анамнеза необходимо выяснить сроки появления первых признаков заболевания и темп их развития, выявить факторы риска маммологических заболеваний (травмы МЖ, послеродовые маститы, раннее менархе, поздние первые роды, отсутствие лактации в послеродовом периоде, позднее наступление менопаузы, нарушение менструальной функции, бесплодие, нерегулярность и позднее начало половой жизни, характер профессиональной деятельности, гинекологические заболевания, заболевания гипоталамо-гипофизарно-яичниковой оси, ожирение, сахарный диабет, патология щитовидной железы, отягощенная наследственность, гинекологические заболевания).
Для удобства описания МЖ делят вертикальной и горизонтальной линиями, проведенными через сосок на 4 квадранта.
При осмотре МЖ следует обратить внимание на следующее:
- цвет кожных покровов;
- размер и симметричность МЖ (некоторая асимметричность МЖ может наблюдаться и в отсутствие какой-либо патологии);
- форму МЖ;
- размер и форму ареолы и соска, его направление, наличие сыпи, изъязвлений и выделений из соска. Сосок обычно направлен наружу и вниз. Иногда инверсия соска может наблюдаться и без наличия какой-либо патологии;
- оценить степень развития МЖ, возрастные особенности;
- попросить женщину отвести руки в сторону и затем поднять руки вверх и еще раз внимательно осмотреть МЖ.
Наличие втяжения соска, его деформации, мацерация или эрозия ареолы и соска, кровянистые выделения из него, деформация МЖ, втяжение кожи на различных участках МЖ (симптом «умбиликации»), частичный или тотальный отек кожи (симптом «лимонной» или «апельсинной корки»), ее гиперемия, уплотнение ткани МЖ (инфильтрация) являются причиной дальнейшего углубленного обследования на предмет выявления злокачественной опухоли МЖ.
Пальпация МЖ производится в положении женщины стоя и лежа на спине. Пальпировать следует одинаково тщательно обе МЖ, а не только железу с выявленными при осмотре изменениями, т.к. нередки случаи двустороннего поражения МЖ раком. Вначале ощупывают МЖ в положении стоя. Изучают состояние сосков и ареол, их утолщение или уплотнение, наличие или отсутствие выделений из сосков, их характер. Осмотр МЖ следует повторно проводить в первую фазу следующего менструального цикла. После исследования в вертикальном положении больную следует уложить на кушетку и повторить осмотр в положении на спине и на боку в той же последовательности.
После тщательного исследования МЖ производятся осмотр и пальпация регионарных зон (подмышечных, надключичных и подключичных областей) с обеих сторон с целью выявления возможно существующих метастазов в лимфатические узлы. В связи с этим любое мануальное обследование должно быть дополнено комплексным ультразвуковым исследованием (УЗИ).
Согласно приказу Минздрава России от 01.11.2012 N 572н «Об утверждении порядка оказания медицинской помощи по профилю ‘‘акушерство и гинекология’’», медицинская помощь женщинам с целью выявления заболеваний молочных желез оказывается врачом-акушером-гинекологом, прошедшим тематическое усовершенствование по патологии молочной железы. УЗИ МЖ проводится 1 раз в год, далее по показаниям; маммография впервые в 35–36 лет, далее в возрастной группе 35–50 лет 1 раз в 2 года, старше 50 лет 1 раз в год.
Женщины с выявленными кистозными и узловыми изменениями молочных желез направляются в онкологический диспансер для верификации диагноза. После исключения злокачественных новообразований женщины с доброкачественными заболеваниями молочных желез находятся под диспансерным наблюдением врача-акушера-гинеколога, который оказывает медицинскую помощь по диагностике доброкачественной патологии молочных желез и лечению доброкачественных диффузных изменений с учетом сопутствующей гинекологической патологии.
Ультразвуковой метод диагностики – абсолютно безвредный вид исследования, что позволяет применять его многократно в процессе мониторинга и скрининга. УЗИ, так же как и маммография, проводится в первую фазу менструального цикла.
Данный метод позволяет с высокой точностью распознавать узловые образования, кисты, оценивать диффузные изменения. Однако диагностическая эффективность при диагностике опухолей менее 1 см составляет 58%, непальпируемых образований – 80%.
Преимущества УЗИ МЖ:
- безопасность в плане дозовой нагрузки (обследование беременных и кормящих женщин);
- высокая разрешающая способность, что важно при плотном фоне МЖ у молодых женщин (возможность визуализации рентгенонегативных опухолей, образований, расположенных вблизи грудной стенки);
- дифференциальная диагностика сóлидного и полостного образования (практически 100%-ная диагностика кист любого размера);
- оценка состояния силиконовых имплантатов МЖ, особенно при их разрывах и утечке содержимого;
- обследование МЖ в острый период травмы или воспаления;
- визуализация регионарных лимфатических узлов;
- проведение прицельных пункционных биопсий под объективным визуальным контролем пальпируемых и непальпируемых образований в МЖ, многократное динамическое исследование в процессе лечения.
Недостатки УЗИ:
- отсутствие визуализации органа в целом (только томографический срез);
- малая информативность при жировой инволюции (ультразвуковая контрастность между опухолевой и жировой тканями слабая);
- субъективность интерпретации полученного изображения (зависит от уровня квалификации врача и технических параметров используемого УЗ-сканера и УЗ-датчиков);
- нецелесообразность использования для скрининга РМЖ (не удается визуализировать неинвазивные внутрипротоковые опухоли в виде микрокальцинатов без опухолевой массы).
Все это позволяет использовать УЗИ лишь как дополнительный метод в сочетании с рентгенологическим. Совместное их применение позволяет повышать точность диагностики заболеваний МЖ до 97%. Таким образом, ультразвуковую и рентгенологическую маммографию целесообразно считать не альтернативными, а взаимодополняющими методиками, которые должны широко использоваться в диагностическом алгоритме заболеваний МЖ.
При обследовании более чем у половины женщин с различными факторами бесплодия отмечаются доброкачественные заболевания МЖ, среди которых преобладает диффузная фиброзно-кистозная мастопатия; три четверти выявленной патологии приходится на эндокринный фактор.
В группе женщин после 35 лет основным методом объективной оценки состояния МЖ является рентгеномаммография, которая позволяет своевременно диагностировать патологические изменения в МЖ в 85% случаев. Поэтому в отличие от других методов диагностики маммография является основным методом скрининга заболеваний МЖ. Особенно велика роль данного метода в обнаружении непальпируемых опухолей в доклинической фазе их развития, в выявлении злокачественных опухолей на фоне диффузных и узловых форм мастопатии.
Маммографию проводят в двух проекциях (прямой – кранио-каудальной и боковой) на 5–12-й день менструального цикла, когда паренхима МЖ менее отечна и болезненна, а в отсутствие менструаций – в любой день.
Рентгеновское маммографическое обследование является наиболее точным методом, позволяющим распознавать заболевание на самых ранних стадиях. Рентгеновская маммография используется в качестве скрининга, т.е. метода быстрого обследования больших групп пациенток, задача которого – выявление заболевания до появления симптомов или признаков, по поводу которых больные впоследствии обратились бы за медицинской помощью. Этот метод позволяет не только определить наличие изменений в тканях МЖ на ранних стадиях, но и оценить их размеры, характер, распространенность. Ценность раннего выявления заболевания заключается в том, что становится возможным обнаружить рак на стадии, когда он носит локальный характер и может быть излечен.
Таким образом, основными преимуществами маммографии являются:
- возможность полипозиционного изображения МЖ;
- самая высокая информативность (чувствительность до 95%, специфичность до 97%);
- возможность визуализации непальпируемых образований (в виде узла, локальной тяжистой структуры, скопления микрокальцинатов);
- возможность выполнения широкого спектра инвазивных и неинвазивных методик, используемых как для диагностики, так и для лечения ряда заболеваний (аспирационная биопсия, склерозирование кист, дуктография, внутритканевая маркировка опухоли и пр.);
- возможность объективного сравнительного анализа изображения МЖ на маммограмме в динамике.
Недостатками рентгеновской маммографии являются:
- дозовая нагрузка (0,15–0,2 м3В на снимок);
- снижение информативности метода при плотном фоне МЖ, в т.ч. при рентгеннегативном РМЖ до 6%.
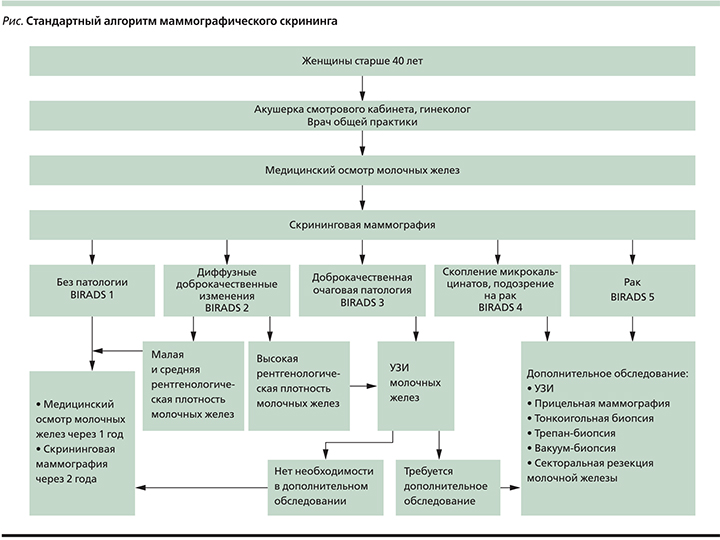
Стандартный процесс проведения маммографического скрининга представлен на рисунке.
В схеме использована классификация состояния ткани МЖ, основанная на эхографических и маммографических характеристиках, применяемая в экономически развитых странах уже несколько лет. BIRADS – классификация (Breast Imaging Reporting and Data System) создана для того, чтобы привести к общему знаменателю данные, полученные с помощью инструментальных неинвазивных методик обследования МЖ.
Согласно классификации, состояние ткани МЖ можно разделить на 5 категорий.
- BIRADS, 1-я категория – нормальная ткань МЖ;
- BIRADS, 2-я категория – доброкачественные изменения образование;
- BIRADS, 3-я категория – вероятнее, доброкачественное образование; противопоказания к экстракорпоральному оплодотворению (ЭКО);
- BIRADS, 4-я категория – подозрительное на рак образование; противопоказания к ЭКО;
- BIRADS, 5-я категория – высокая вероятность злокачественного образования, противопоказания к ЭКО.
В последние годы к пяти категориям BIRADS была добавлена еще одна категория: 0 – образование МЖ, которое нуждается в дополнительных диагностических мероприятиях.
По международным стандартам, маммографические снимки каждой женщины должны оцениваться двумя независимыми специалистами, каждый из которых дает свое личное заключение. Следует отметить, что женщины любого возраста (в т.ч. моложе 40 лет) при наличии клинически определяемой патологии в МЖ, также должны направляться как на УЗИ МЖ, так и на маммографию.
Дисплазия МЖ (фиброзно-кистозная мастопатия) представляет собой группу гетерогенных заболеваний, характеризующихся широким спектром пролиферативных и регрессивных изменений ткани МЖ с нарушенным соотношением эпителиального и соединительнотканного компонен-тов.
Фиброзно-кистозная болезнь, по данным различных исследователей, выявляется примерно у 50–60 % женщин, как правило, в возрасте от 30 до 50 лет и гораздо реже – у женщин в постменопаузе. Факторы, приводящие к развитию мастопатии, разнообразны и недостаточно изучены: неблагоприятные факторы репродуктивного анамнеза (раннее менархе – до 12 лет и поздняя менопауза – позднее 55 лет; поздние роды – после 35 лет; прерывание беременности; отсутствие или неполноценная лактация – до 1 года или более 2 лет); неблагоприятные факторы гинекологического анамнеза (нарушение менструального цикла, ановуляторное бесплодие, миома матки, эндометриоз, гиперпластические процессы эндометрия – в основе всех этих процессов лежат прогестерондефицитные состояния); нейроэндокринные нарушения (гипотиреоз, сахарный диабет 2 типа и ожирение как составляющие метаболического синдрома, синдром поликистозных яичников, гиперпролактинемия).
Важной причиной возникновения диспластических заболеваний МЖ считается нарушение баланса половых стероидов (эстрогены и прогестерон) в организме женщины, в результате которого развивается относительная гиперэстрогения, что приводит к пролиферации эпителия альвеол, протоков, усилению активности фибробластов и вызывает пролиферацию соединительной ткани МЖ.
У пациенток в программах ВРТ отмечается достоверное увеличение диаметра млечных протоков, а также повышение среднего уровня температуры в тканях МЖ, прямо коррелирующее с числом попыток ЭКО, дозой гонадотропинов, наличием синдрома гиперстимуляции яичников.
Профилактическое применение препаратов, влияющих на МЖ, благоприятно воздействует на состояние МЖ у женщин с диффузной фиброзно-кистозной мастопатией.
Учитывая большое число способов лечения мастопатии, целесообразно проводить оценку эффективности данной терапии. На сегодня это возможно сделать методом радиотермометрии (патент «Способ оценки эффективности лечения диффузной мастопатии» РФ № 2449724, дата публикации 10.05.2012), когда измеряют внутреннюю температуру ткани в области МЖ и всех сегментов МЖ. Повышение уровня средней температуры в тканях МЖ свидетельствует о повышении пролиферативной активности. Проведено повторное обследование через 6 месяцев и у 9 женщин через 12 месяцев после проведения программы ЭКО. Установлено, что через 6 месяцев после проведения программы ЭКО уровень средней температуры в тканях МЖ снизился наполовину, а через 12 месяцев – практически достиг исходного. Таким образом, длительность интервала между проведением программ ВРТ должна составлять не менее шести месяцев.
Консультативные приемы онкологов-маммологов в составе отделений и центров репродукции позволяют эффективно использовать рабочее время персонала, организовывать диагностику УЗИ квалифицированным специалистом.



