Алопеции представляют группу хронических дерматологических заболеваний, в основе которых лежит поражение волосяного фолликула. Как правило, за исключением тяжелых форм алопеций, рубцовых или гнездной, одним из ключевых элементов патофизиологического процесса выпадения волос при алопециях являются изменения цикла волосяного фолликула. Клинически алопеции характеризуются частичной или полной потерей волос на волосистой части головы, а иногда и на теле. Наиболее распространенными в этой группе заболеваний являются андрогенная алопеция и телогенное выпадение волос [1–4].
Телогенное выпадение волос (telogen effluvium) впервые было описано A.M. Kligman в 1961 г. В настоящее время телогенное выпадение волос, согласно Международной классификации болезней 10-го пересмотра, классифицируется по коду L65.0 и отнесено к разделу «алопеции – L65. Другая нерубцующая потеря волос». Телогенное выпадение волос характеризуется диффузным выпадением телогеновых волос на волосистой части головы, которое, как правило, происходит через 2–3 месяца после инициирующего воздействия [5, 6]. Перечень триггерных факторов включает гипо- и гипертиреоз, хронические системные заболевания, аутоиммунные, инфекционные заболевания, нарушения микроциркуляции кожи волосистой части головы, дефицит ряда микроэлементов, ряд лекарственных препаратов [7–12].
Потеря телогеновых волос является как самостоятельным заболеванием, так и симптомом андрогенной алопеции [13]. В основе данного симптома лежит сокращение продолжительности фазы роста (анагена) и длительное пребывание фолликулов в латентной фазе – кеногене, что клинически проявляется появлением коротких волос, которые не достигают достаточной длины. Истончение волос при андрогенной алопеции происходит вследствие трансформации фолликулов терминальных (длинных) волос в миниатюризированные волосяные фолликулы, соответствующие диаметром размерам веллусных (пушковых) волос [5, 14].
В настоящее время доказано, что андрогенная алопеция у мужчин имеет наследственную предрасположенность, является андрогензависимым заболеванием и ассоциируется с полиморфизмом гена андрогенового рецептора [15–17]. Однако остаются неясными вопросы генетической предрасположенности и андрогензависимого характера андрогенной алопеции у женщин [18].
Учитывая недостаточную изученность патогенеза и хронический характер алопеций, для достижения положительного эффекта лечение необходимо начинать на ранних стадиях заболевания, которое предполагает длительные курсы с последующей поддерживающей терапией.
Основываясь на патогенезе телогенного выпадения волос, потенциальные терапевтические возможности включают ингибирование стадии катагена, для того чтобы продлить стадию анагена; индукцию анагена в телогеновых фолликулах и подавление стадии экзогена с целью уменьшения выпадения волос. Применяемые в настоящее время препараты для лечения выпадения волос не являются высокоэффективными в отношении ингибирования стадии катагена или индукции стадии анагена [19].
Современные методы лечения андрогенной алопеции включают наружные и системные препараты. К средствам для наружного применения относятся препараты, содержащие миноксидил [20–22]. Механизм действия миноксидила до конца не изучен, имеются данные о его стимулирующем влиянии и пролонгировании стадии анагена путем активации калиевых каналов. Однако миноксидил эффективен в 30–35% случаев андрогенной алопеции у мужчин и женщин, а лечение необходимо проводить постоянно на протяжении жизни [23]. Исследования показали, что 5%-ный раствор миноксидила более эффективен, чем 2%-ный раствор, однако его применение имеет ряд побочных эффектов, таких как аллергический контактный дерматит, сухость, зуд кожи головы, а прекращение использования приводит к развитию синдрома отмены [24].
К системным препаратам, используемым в практике, относят финастерид и ципротерона ацетат. Финастерид являясь ингибитором 5α-редуктазы II типа, снижает конверсию тестостерона в дигидротестостерон. Финастерид является высокоэффективным средством для лечения андрогенной алопеции у мужчин. Однако он обладает рядом побочных эффектов, к которым относятся снижение либидо, импотенция, расстройства эякуляции и депрессия. Отмена препарата приводит к дальнейшему прогрессированию заболевания [24, 25]. Ципротерона ацетат является средством лечения андрогенной алопеции у женщин, обладает антинандрогенным действием. Исследование P. Vexiau показало, что применение ципротерона ацетата более эффективно при наличии симптомов гиперандрогении у женщин, тогда как у пациенток без симптомов гиперандрогении не было получено достоверного увеличения общего количества волос. Побочные эффекты дозозависимы и включают нарушения менструального цикла, увеличение массы тела, болезненность молочных желез, тошноту, депрессию [26, 27].
Таким образом, применяемые средства терапии алопеций имеют ограничения в применении и не позволяют добиваться стойкого эффекта. В связи с этим требуется поиск новых эффективных и безопасных методов лечения выпадения волос.
Исследования последних лет свидетельствуют об эффективности гомеопатических препаратов в лечении различных видов алопеций [36]. Благодаря регулирующему и стимулирующему действию на весь организм гомеопатические препараты включают аутогенные механизмы регуляции физиологической смены волос. Комплексное гомеопатическое лекарственное средство Селенцин разработано для лечения различных видов алопеций с учетом совместимости компонентов таким образом, что каждый ингредиент воздействует на определенный этиопатогенетический фактор с учетом положений о совместимости гомеопатических лекарств и безопасности действия комплексного лекарственного средства. Лекарственное средство содержит компоненты натурального природного происхождения и оказывает регулирующее воздействие на обменные процессы. Особо отмечается отсутствие побочного действия препарата на организм человека.
В исследовании N. Lengg и соавт. (2007) была показана эффективность применения L-цистеина у пациенток с телогенным выпадением волос, отмечено увеличение роста волос в стадии анагена [28]. Известно, что разнообразные семейства факторов роста являются стимуляторами, ингибиторами роста и дифференцировки в волосяном фолликуле. Экспериментальные работы на животной модели доказали, что факторы роста способны вызывать пролиферацию клеток эндотелия сосудов и дермальных фибробластов, продлевать стадию анагена и задерживать наступление стадии катагена волосяного фолликула [29–31]. Следовательно, с помощью факторов роста можно увеличить продолжительность стадии анагена и таким образом стимулировать рост волос [22, 32, 33]. С учетом того что на физиологические процессы оказывают влияние не целые молекулы факторов роста, а их небольшие фрагменты – олигопептиды, большое внимание привлекло применение биомиметических пептидов в лечении алопеций [34, 35].
Целью настоящей работы было оценить терапевтическую эффективность препарата Селенцин в комплексной терапии телогенного выпадения волос и андрогенной алопеции.
Материал и методы
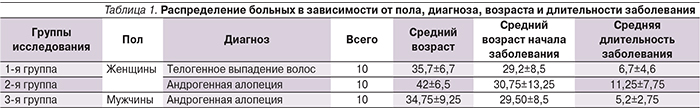
Под наблюдением находились 30 пациентов с диагнозом «телогенное выпадение волос» (10 женщин) и «андрогенная алопеция» (10 женщин и 10 мужчин) (табл. 1). Во всех наблюдениях диагноз был установлен на основании данных клинического осмотра, трихоскопии и фототрихографии.
Критериями невключения в исследование стали заболевания щитовидной железы, заболевания кожи в стадии обострения, инфекционные заболевания, гиперандрогения, сопутствующая тяжелая соматическая патология.
Выраженность проявлений андрогенной алопеции у мужчин оценивалась по шкале Норвуда–Гамильтона (1975) с определением cтадии андрогенной алопеции: у 2 мужчин диагностирована андрогенная алопеция II стадии, у 5 мужчин – III, у 3 мужчин – IIIa стадии. Для оценки выраженности клинических проявлений облысения у женщин была применена шкала Sinclair (2004). С учетом пяти степеней тяжести поредения волос по срединной линии у 7 женщин диагностирована 3-я стадия, у 7 женщин – 2-я, у 6 женщин – 1-я стадия.
Трихоскопию и фототрихографию проводили с использованием специальной микрокамеры «Aramo SG» (компания «Aram HUVIS Co., Ltd.», Республика Корея) и двух объективов (×60 – для исследования внешней поверхности кожи и волос, ×200 – для исследования состояния волосяных фолликулов и кожи головы) в сочетании со специализированной диагностической компьютерной программой «Программа для профессиональной диагностики в трихологии Трихосаенс/Trichoscience v.1.7 (RUS)» (Россия) в фиксированных зонах с нанесением несмываемой метки до и после лечения.
Для оценки клинической картины в динамике проводили обзорное фотографирование волосистой части головы до лечения и при последующих визитах.
После проведения диагностики всем пациентам назначали комплексную терапию, которая включала медикаментозное лечение: пероральный прием гомеопатического препарата Селенцин по 1 таблетке 3 раза в сутки за 30 минут до или через час после еды сублингвально в течение 2 месяцев; пероральный прием препарата, содержащего L-цистеин по 1 капсуле 3 раза в сутки во время еды в течение 3 месяцев; и дополнительно местное применение лосьона на основе биомиметических пептидов на кожу волосистой части головы с применением мезороллера (всего 16 процедур). Комплекс биомиметических пептидов включал декапептид-18, олигопептид-54, декапептид-10, октапептид-2, декапептид-19, олигопептид-71, декапептид-28.
Период наблюдения больных после лечения составил 6 месяцев и включил оценку клинической эффективности лечения и контрольное проведение трихоскопии и фототрихографии через 2 и 6 месяцев.
Статистическая обработка полученных данных была проведена с помощью программы Statistica 10. Применялся параметрический t-критерий Стьюдента. Различия считали достоверными при уровне статистической значимости p≤0,05.
Результаты исследования
При анализе анамнестических данных пациентов было выявлено, что причины выпадения и поредения волос могут назвать только женщины из 1-й и 2-й групп, которые указывали на психологический стресс, роды. Все мужчины 3-й группы не могли связать возникновение первых проявлений заболевания с конкретным фактором.
Наследственность была отягощена по отцовской линии у 5 (50%) пациенток 1-й группы, у 4 (40 %) пациенток 2-й, у 6 (60%) пациентов 3-й группы. Заболевание имело внесезонный характер течения у 5 (50%) пациенток 1-й группы, у 6 (60%) – 2-й, в 100% у пациентов 3-й группы. В 1-й группе преобладал хронический рецидивирующий характер выпадения волос (n=6, 60%), во 2-й и 3-й – хронический персистирующий (n=6; 60% и n=10; 100% соответственно). Большинство пациентов проводили самостоятельное лечение с применением наружных средств для ухода за волосами: (n=8; 80% в 1-й группе, n=10; 100% во 2-й группе, n=7; 70% в 3-й группе) без значительного улучшения.
Таким образом, согласно данным анамнеза, у больных андрогенной алопецией отмечено хронически-персистирующее течение, у пациентов с телогенным выпадением волос – хронически-рецидивирующее течение заболевания. Телогенное выпадение волос преобладало у женщин молодого возраста, при этом наиболее частой причиной выпадения волос оказались психологический стресс, интенсивный ритм жизни и роды. Наружные средства терапии обоих видов алопеций не оказывали выраженного терапевтического эффекта.
Оценка эффективности терапии у пациенток с телогенным выпадением волос (1-я группа). По данным трихоскопии и фототрихографии, у пациенток 1-й группы до начала терапии выявлено нарушение соотношения анагеновых и телогеновых волос в сторону увеличения волос, находящихся в телогене (процентное соотношение анагеновых волос к телогеновым в теменной области – 61,9:38,1, в затылочной области – 76,65:23,35). При этом общее количество волос на см2, соотношение терминальных и веллусных волос в теменной и затылочной областях соответствовали норме.
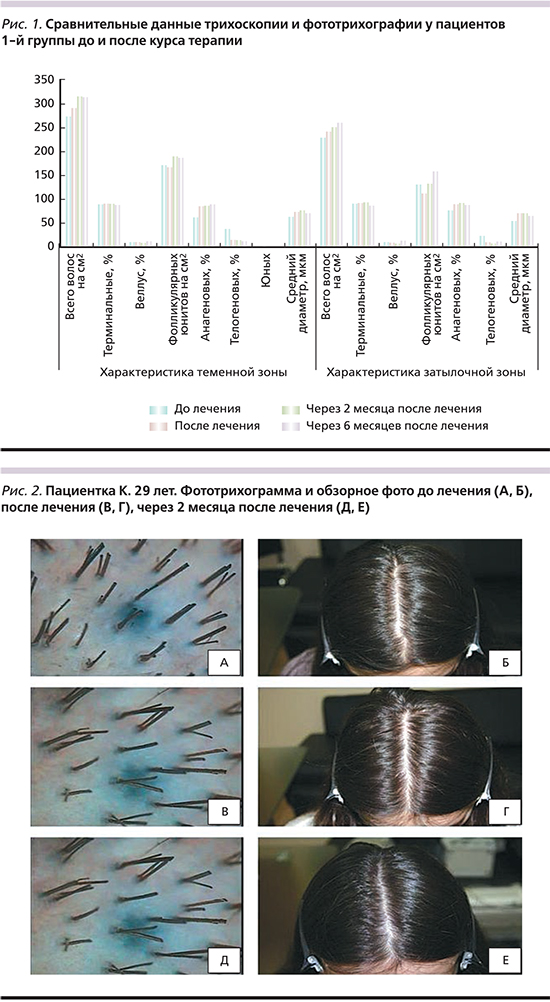
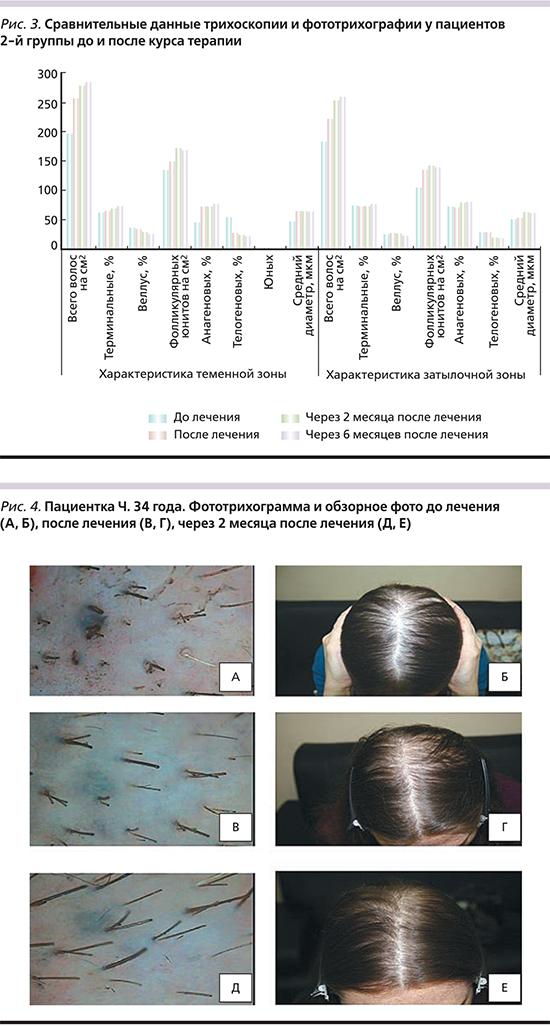
После проведенной комплексной терапии процентное соотношение анагеновых волос к телогеновым составило 84,5:14,8 в теменной области, 90,05:9,95 – в затылочной, а также отмечено появление юных волос (0,6%) в теменной области. Лучший результат отмечен через 2 месяца после окончания лечения (рис. 2). По данным фототрихограммы, соотношение анагеновых волос к телогеновым в теменной области составило 88,6:11,4, в затылочной – 97,15:2,85. Через 6 месяцев после лечения наблюдалось сохранение положительной динамики (рис. 1).

Таким образом, при сравнении результатов трихоскопии и фототрихографии у пациенток 1-й группы до и после проведенного лечения было выявлено статистически достоверное уменьшение волос, находившихся в стадии телогена (р<0,05). При сравнении общего количества волос на см2, диаметра волос до и после лечения достоверных различий не выявлено, однако наблюдалась тенденция к их увеличению.
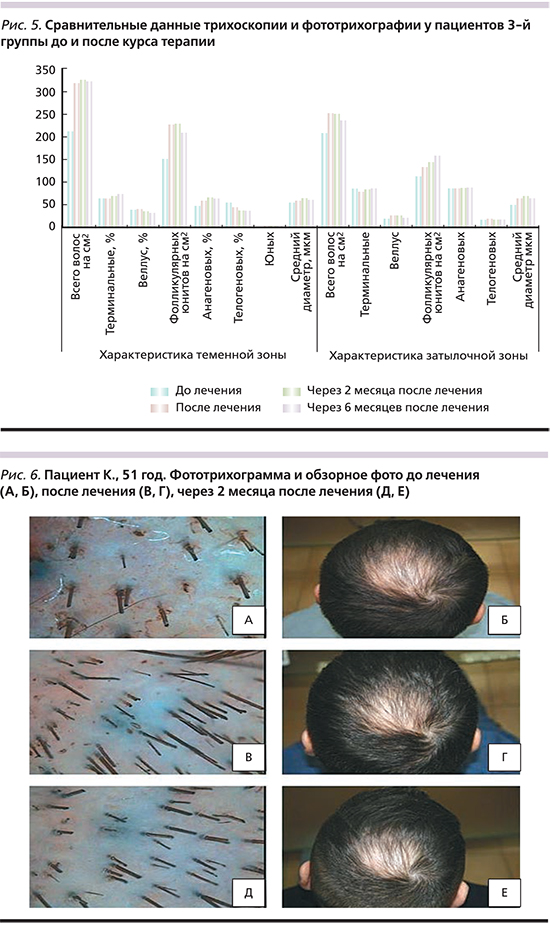
Оценка эффективности терапии у пациенток с андрогенной алопецией (2-я группа). По данным трихоскопии и фототрихогафии, у пациенток 2-й группы до лечения выявлено снижение общего количества волос на см2 в теменной области (196,1±60,35), изменение нормального соотношения терминальных и веллусных волос в теменной и затылочной областях в сторону увеличения веллусных волос (36,8±9,0% в теменной области, 26,38±4,5% в затылочной области), нарушение нормального соотношения анагеновых и телогеновых волос (процентное соотношение анагеновых волос к телогеновым в теменной области – 45,35:54,65, в затылочной области – 73,1:28,1).
После проведенной комплексной терапии общее число волос на см2 в теменной области составило 255,9±80,8. Соотношение анагеновых волос к телогеновым составило 72,5:27,5 в теменной области, 71,75:28,25 – в затылочной, а также появление юных волос (0,35%) в теменной области (рис. 4). Через 2 месяца после окончания лечения общее число волос на см2 в теменной области составило 278,4±60,9. Таким образом, общее количество волос на см2 в теменной области увеличилось на 41,9%. Соотношение анагеновых волос к телогеновым составило 73,3:24,9, а также появление юных волос (1,8%) в теменной области, 80,17:19,83 – в затылочной области. Через 6 месяцев после лечения наблюдалось сохранение положительной динамики (рис. 3).
Таким образом, при сравнении результатов трихоскопии и фототрихографии у пациенток 2-й группы до и после проведенного лечения было выявлено статистически достоверное увеличение общего числа волос на см2 в теменной и затылочной областях, уменьшение волос, находившихся в стадии телогена (р<0,05). Достоверных различий в соотношении терминальных и веллусных волос в теменной и затылочной областях, диаметре волос до и после проведенной терапии выявлено не было, однако наблюдалась тенденция к увеличению диаметра, уменьшению количества веллусных волос в теменной и затылочной областях.
Оценка эффективности терапии у мужчин с андрогенной алопецией (3-я группа). По данным трихоскопии и фототрихографии, у пациентов 3-й группы было выявлено снижение общего количества волос на см2 в теменной области (211,1±64,85), изменение нормального соотношения терминальных и веллусных волос в теменной области в сторону увеличения веллусных волос (37,5±5,0%), нарушение нормального соотношения анагеновых и телогеновых волос (процентное соотношение анагеновых волос к телогеновым в теменной области 47,1:52,9). Соотношение терминальных и веллусных волос, а также анагеновых и телогеновых волос в затылочной зоне не имело значительных отклонений от нормы и у большинства пациентов соответствовало норме.
После проведенной комплексной терапии общее количество волос на см2 в теменной области составило 319,3±69,95. Соотношение анагеновых волос к телогеновым в теменной области составило 56,75:41,68, а также появились юные волосы, которые увеличили общее количество волос на 1,57%. Через 2 месяца после окончания лечения общее количество волос на см2 в теменной области составило 325,7±33,5. Таким образом, общее количество волос на см2 в теменной области увеличилось на 54,3%. Соотношение анагеновых волос к телогеновым в теменной области составило 63,55:35,6, а также появились юные волосы (0,85%). Через 6 месяцев после лечения наблюдалось сохранение положительной динамики (рис. 5, 6).
При статистической обработке результатов трихоскопии и фототрихографии у пациентов 3-й группы до и после проведенного лечения выявлено достоверное увеличение общего количества волос на см2 в теменной области, уменьшение волос, находившихся в стадии телогена (р<0,05). Корреляционный анализ не показал значимых достоверных изменений соотношения терминальных и веллусных волос в теменной области, диаметра волос до и после проведенной терапии, однако наблюдалась тенденция к увеличению диаметра, уменьшению количества веллусных волос в теменной области.
Достоверных изменений показателей трихоскопии и фототрихограммы в затылочной области после проведенного лечения у пациентов 3-й группы не выявлено.

Все пациенты, получившие комплексное лечение (пероральный прием гомеопатического препарата Селенцин; препарата, содержащего L-цистеин и местное применение лосьона на основе биомиметических пептидов на кожу волосистой части головы с применением мезороллера) отметили уменьшение количества ежедневной потери волос, улучшение структуры, повышение плотности стержня волос и уменьшение количества седых волос. Побочных эффектов, требующих отмены терапии, выявлено не было. После завершения лечения синдрома отмены пациентами отмечено не было.
Обсуждение
Сравнительный анализ показал, что в результате терапии у пациенток 1-й группы с телогенным выпадением волос количество анагеновых волос увеличилось на 22,6% в теменной и на 13,4% в затылочной областях. Кроме того, терапия имела пролонгированный эффект, который сохранился через 2 месяца терапии. За этот период времени количество волос в стадии роста увеличилось еще на 4,1% в теменной и на 7,1% в затылочной областях (табл. 2).
Необходимо отметить, что только в этой группе данные трихограммы достигли показателей нормы. Анализ показателей фототрихограммы позволил сделать следующий вывод: у больных телогенным выпадением волос уменьшается выпадение волос за счет стимуляции и удлинения фазы анагена и, следовательно, сокращения стадии телогена. Инициацию стадии анагена подтверждает объективный факт появления юных волос (0,6%), а увеличение количества юнитов за период лечения указывает на удлинение периода анагена (табл. 3).
У женщин с андрогенной алопецией также отмечался положительный эффект. Поскольку патологической зоной выпадения волос является теменная область, наиболее положительный эффект терапии отмечался именно в этой области волосистой части головы. Так же как и в 1-й группе увеличилось количество волос в стадии роста в теменной (на 27,15%) и на 1,35% в затылочной областях. Таким образом, по окончании курса терапии общее количество волос увеличилось на 30,5%. Положительный эффект терапии отмечался и через 2 месяца после окончания лечения (табл. 2). В отличие от пациенток с телогенным выпадением волос у больных андрогенной алопецией регистрировалось больше юных волос (1,8%) и общее количество волос увеличилось на 41,9%. В этой группе также отмечалось нарастающее количество фолликулярных юнитов, что демонстрирует удлинение фазы анагена (табл. 3).
Однако необходимо отметить, что достоверных различий коэффициента соотношения терминальных и веллусных волос у больных андрогенной алопецией не имелось. Это может констатировать факт наличия большого количества миниатюризированных фолликулов. У данных больных увеличение количества волос достигается за счет сокращения стадии кеногена, телогена и за счет инициации фазы анагена. Вследствие этого можно сделать вывод о высоком стимулирующем эффекте препарата Селенцин в комплексной терапии с препаратом, содержащим L-цистеин, и биомиметических пептидов на рост волос, однако при наличии большого количества веллусных волос недостаточно одного курса терапии.
Как известно, наибольшие трудности в лечении андрогенной алопеции возникают у мужчин, однако в нашем исследовании максимальный эффект терапии отмечен именно у пациентов 3-й группы. Именно в этой группе общее количество волос увеличилось на 54,3%. Только в этой группе на первых этапах лечения появились юные волосы, которые увеличили количество волос на 1,57%, через 2 месяца их количество увеличилось еще на 0,85%. Хотя количество волос, находившихся в стадии анагена, не достигло показателей нормы, их количество в процессе лечения возросло на 16,45% (табл. 2). По сравнению с другими группами у больных 3-й группы имели место наибольшие положительные показатели в количестве юнитов на 1 см2, что указывает на удлинение фазы анагена и сокращение фаз телогена и кеногена (табл. 3).
Однако у мужчин с андрогенной алопецией, так же как и у женщин с андрогенной алопецией, достоверных различий соотношения терминальных и веллусных волос в теменной области до и после лечения не установлено. Это еще раз подтверждает факт, что количество волос у больных андрогенной алопецией увеличивается за счет сокращения периодов кеногена и телогена и стимуляции начала анагена.
Заключение
Таким образом, проведенное исследование показало высокую терапевтическую эффективность применения препарата Селенцин в комплексной терапии телогенного выпадения волос и андрогенной алопеции. Комплексное лечение инициирует фазу анагена и стимулирует продолжительность этой фазы, вследствие чего сокращаются периоды кеногена и телогена. Клиническая картина после проведенного комплексного лечения больных телогенным выпадением волос и андрогенной алопецией характеризуется ростом юных волос, увеличением общего количества волос и волос в стадии анагена. Положительный эффект сохраняется в течение 6 месяцев. У больных телогенным выпадением волос, получивших комплексное лечение, показатели трихоскопии и фототрихограммы достигли нормы, что позволяет констатировать высокую эффективность данного лечения за счет воздействия на патогенетические звенья заболевания.



