Введение
Острые нарушения мозгового кровообращения (ОНМК) представляют собой важнейшую медико-социальную проблему, что обусловлено их высокой долей в структуре заболеваемости и смертности населения, значительными показателями временных трудовых потерь и первичной инвалидности. Постинсультная инвалидизация занимает первое место среди всех ее причин и составляет 3,2 на 10 тыс. населения, при этом треть заболевающих инсультом – люди трудоспособного возраста [1–3]. После инсульта 70–80% больных становятся инвалидами, примерно 20–30% из них нуждаются в постоянном постороннем уходе. Ограничения в повседневной жизни и трудовой сфере у больных инсультом возникают вследствие развившегося неврологического дефицита: гемипарез в остром периоде инсульта выявляется у 80–90% больных, в 40–50% случаев отмечаются сенсорные расстройства, у 7–15% пациентов – эпилептические припадки [5, 6].
Частота когнитивных нарушений у больных, перенесших церебральный инсульт, достигает 68%, из них трансформация в деменцию в последующем происходит в 26% случаев. Нарушения высших мозговых функций достаточно часто проявляются афазией, которая наблюдается у 20–38% больных [4, 7–9]. В резидуальном периоде инсульта после длительного (до 2 лет) восстановления в 17,5% случаев наблюдаются в различной степени выраженные моторная, сенсорная, реже сенсомоторная и другие виды афазий, которые могут быть изолированными (у 4% больных), но чаще (в 24% случаев) сочетаются с двигательным дефицитом [9]. Речевые расстройства, возникающие при очаговом поражении головного мозга, оказывают негативное влияние на восстановление двигательных функций у пациентов с ОНМК [9–12]. Любые формы когнитивных нарушений, в частности речевые расстройства, ведут к изменению личности, меняется поведение больного, его эмоциональное состояние, качество жизни. Афатические нарушения, как правило, затрагивают разные уровни организации речи, снижают или полностью ограничивают коммуникативную функцию, тем самым приводя к дезинтеграции всей психической сферы человека, нарушению его трудоспособности и социальной депривации.
В связи с этим крайне важным аспектом в лечении пациентов с инсультом служит ранняя нейропротективная терапия, а также коррекция приобретенных вследствие заболевания речевых расстройств [2, 4].
 Поскольку ишемические инсульты (ИИ) составляют подавляющее большинство в структуре ОНМК, приоритетным направлением исследований в современной ангионеврологии стало изучение процессов нейропластичности как основы компенсации нарушенных функций [6]. Полученные данные были положены в основу разработки и применения препаратов, обладающих нейропротективным, нейрорепаративным действиями, поддерживающих, стимулирующих саногенез, способствующих защите мозга от очаговой ишемии, уменьшению зоны инфаркта мозга и улучшению исхода инсульта [5, 13].
Поскольку ишемические инсульты (ИИ) составляют подавляющее большинство в структуре ОНМК, приоритетным направлением исследований в современной ангионеврологии стало изучение процессов нейропластичности как основы компенсации нарушенных функций [6]. Полученные данные были положены в основу разработки и применения препаратов, обладающих нейропротективным, нейрорепаративным действиями, поддерживающих, стимулирующих саногенез, способствующих защите мозга от очаговой ишемии, уменьшению зоны инфаркта мозга и улучшению исхода инсульта [5, 13].
В связи с этим особый интерес представляют пептидные препараты, обладающие нейропротективными и репаративными свойствами. Эти соединения оказывают многостороннее воздействие на головной мозг, что обеспечивает их высокую эффективность в условиях малой концентрации в организме [6, 10–12].
Одним из перспективных представителей данного класса лекарственных препаратов является Целлекс – тканеспецифичный белково-пептидный комплекс, который получают из эмбриональной ткани головного мозга свиней. Целлекс оказывает репаративное действие на нейрональную ткань, о чем свидетельствуют доклинические исследования препарата. Индуцируя процессы нейропластичности при ишемии головного мозга, препарат способствует уменьшению зоны инфаркта и регрессу неврологического дефицита [4, 13, 14]. Результаты, полученные экспериментальным путем, стали основанием для проведения ряда клинических исследований, уточняющих особенности действия препарата, его терапевтическую «нишу», поскольку в медицинской практике единственным критерием, позволяющим аргументировать назначение препаратов, остаются данные клинических исследований, проведенных с учетом принципов доказательной медицины.
С этой целью было проведено двойное слепое плацебо-контролируемое рандомизированное мультицентровое клиническое исследование эффективности Целлекса в лечении больных ОНМК по ишемическому типу (завершено в 2015 г.), в котором, в частности, оценивалось влияние препарата на динамику и сроки восстановления когнитивных, в т.ч. речевых, функций.
Материал и методы
Исследование проведено в соответствии с действующими регуляторными нормами Российской Федерации, Правилами надлежащей клинической практики (GCP) и этическими принципами Хельсинкской декларации (1964, в последней редакции). В нем приняли участие 8 российских клинических центров.
Дизайн и участники исследования
В исследование были включены 480 пациентов (мужчины в возрасте 35–80 лет, женщины 45–80 лет) с установленным диагнозом ИИ в соответствии с критериями МКБ-10, подтвержденным результатами компьютерной или магнитно-резонансной томографии головного мозга, госпитализированных в течение первых 48 часов с момента развития заболевания. Уровень сознания был не ниже поверхностной комы по отечественной классификации (по суммарной Шкале Комы Глазго ≥9 баллов; индекс по шкале Карновского ≥20 баллов; по шкале инсульта NIHSS в разделах 1a+1b+1c в сумме ≤4 балла). Результаты тестирования по шкалам оценки высших корковых функций (Тест–Память–Концентрация внимания и Опросник речи, Монреальская шкала оценки когнитивных функций или Мока-тест и краткая шкала оценки психического статуса – Mini-Mental State Examination) не влияли на включение или невключение пациента в исследование.
Критерии исключения: крайняя тяжесть состояния пациента с уровнем сознания <9 баллов по суммарной Шкале Комы Глазго и/или индекс по шкале Карновского <20 баллов, и/или по шкале инсульта NIHSS в разделах 1a+1b+1c в сумме >4 баллов (пациенты с уровнем сознания – поверхностная кома и ниже по отечественной классификации); регресс неврологической симптоматики в период до первого введения исследуемого препарата или препарата контроля (плацебо); наличие у пациента заболеваний или состояний, указанных в противопоказаниях к назначению препарата Целлекс: эпилепсия, маниакальный психоз, продуктивный бред, делирий; наличие в анамнезе анафилактических реакций на препараты белковой природы (альбумин, плазма крови, иммуноглобулины, сыворотки); индекс массы тела: ИМТ≤19 или ≥30; злокачественные новообразования; острые и/или хронические заболевания в стадии обострения или декомпенсации.
Все больные, отвечающие критериям включения, были рандомизированы в группы Целлекс (n=240) и Контроль (n=240) в соответствии с назначаемым препаратом, кроме того, все больные пациенты получали стандартную базовую терапию.
Препарат Целлекс (либо плацебо) вводился на фоне стандартной терапии по 0,1 мг (1 мл) подкожно один раз в сутки (утром или днем) в течение 10 дней начиная с первого дня госпитализации.
Оценка речевой функции пациентов была проведена в течение первых суток от момента госпитализации (исходный визит); на 3-и, 6, 15-е сутки (плановые визиты) и 21-е сутки (заключительный визит) госпитализации с помощью шкалы Инсульта (NIHSS) и Опросника речи.
Результаты исследования оценивались при помощи стандартных методов описательной статистики. Для сравнения результатов исследования с исходными значениями в каждой группе был использован парный критерий Вилкоксона, для сравнения исходных данных в группах и сравнения конечных точек в группах применен критерий Манна–Уитни.
Результаты
Включенные в исследование 480 больных были рандомизированы в группы Целлекс и Контроль, которые не различались по численности пациентов, половозрастным характеристикам, тяжести состояния и по времени первого введения исследуемого препарата (либо плацебо). Доля мужчин составила 57,1%, женщин – 42,9%.
Разделение по тяжести состояния проводилось в соответствии со шкалой инсульта NIHSS. Максимальной была доля больных ИИ легкой степени тяжести – 48,3%, минимальной – тяжелым инсультом – 8,2 %, пациентов с ИИ средней тяжести было 43,5%. В контрольной группе доля больных со средней тяжестью инсульта была несколько выше, чем в группе Целлекс, а соответственно, в группе Контроль было меньше пациентов со средней и тяжелой степенями ИИ, хотя значимых межгрупповых отличий отмечено не было.
Оценка речевых расстройств проводилась с использованием Опросника речи и шкалы Инсульта (NIHSS). Указанные шкалы применялись с целью получения ответа на следующие вопросы: какова эффективность Целлекса при разной степени тяжести речевых расстройств, какова динамика регресса афатических нарушений в случае назначения Целлекса и без него, каковы оптимальные сроки назначения препарата больным ИИ?
Для этого были изучены особенности восстановления речевых функций у больных с различной степенью выраженности афазии под влиянием назначенной терапии.
Сравнение динамики средних значений теста «Опросник речи» у больных с легкими речевыми нарушениями и без таковых показало значимое по сравнению с исходным уровнем (p<0,01) увеличение уровня данного показателя у пациентов обеих групп на визите 4 (21-е сутки). При этом у пациентов группы Целлекс среднее значение данного теста увеличилось с 13,7 до 17,0 баллов, в контрольной группе – с 14,2 до 16,7, не достигнув степени достоверности по межгрупповым различиям (рис. 1).
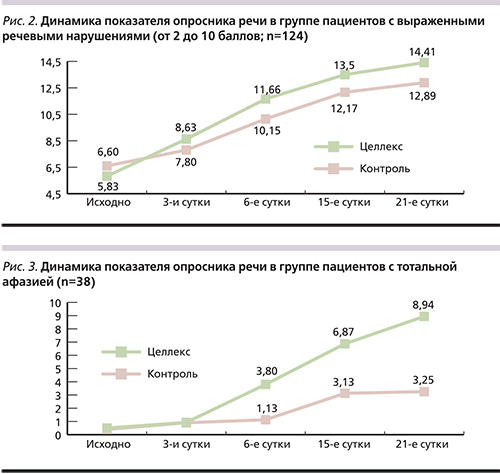
Оценка динамики средних значений данного теста у 124 больных с выраженными речевыми нарушениями (от 2 до 10 баллов) выявила значимое по сравнению с исходным уровнем его возрастание в обеих группах. При этом у пациентов, принимавших Целлекс, значение этого показателя начиная с 3-х суток было выше, чем в контрольной группе. На визите 4 (21-е сутки) величина показателя опросника речи у пациентов группы Целлекс была на 20% выше, чем в группе Контроль (рис. 2).
Анализ динамики средних значений данного теста у больных с тотальной афазией (мутизмом, 0–1 балл до лечения) показал увеличение этого параметра по сравнению с исходным уровнем в обеих группах (рис. 3). При этом у пациентов, получавших Целлекс, значение данного показателя уже на 2-м визите (6-е сутки) в 3,5 раза превышало соответствующий уровень в группе контроля. На визите 3 уровень этого показателя также был существенно выше (p<0,01) в группе Целлекс по сравнению с Контролем, а на визите 4 (21-е сутки) среднее значение показателя «Опросник речи» составило 8,94 балла, тогда как в контрольной группе – лишь 3,25 (p<0,01).
Представленные данные убедительно демонстрируют возрастающую эффективность препарата в случае более тяжелого проявления неврологического дефицита.
Весьма интересны результаты оценки динамики изучаемых параметров в течение 21 суток наблюдения. Сравнение степени изменений показателей (дельта) групп больных инсультом выявило, что к 21-м суткам в группе Целлекс (во всей выборке) была более выражена, чем в группе Контроль, динамика ряда показателей, в т.ч. показателя речи по шкале инсульта: -0,69±0,80 и -0,53±0,68 соответственно, что подтверждалось выявленными статистически значимыми межгрупповыми различиями (р<0,05).
При этом анализ выраженности изменений показателя Речь шкалы NIHSS у больных ИИ тяжелой степени выявил, что на визите 4 в группе Целлекс динамика была более существенной, чем в группе Контроль, о чем свидетельствовало наличие статистически значимых различий: -1,59±1,01 и -0,81±0,83 соответственно (р<0,05).
С целью определения оптимальных сроков назначения Целлекса для достижения более значимого регресса речевых расстройств были сопоставлены данные, полученные при исследовании больных, которым Целлекс вводился в первые 6 часов по сравнению с общей выборкой больных, получавших препарат.
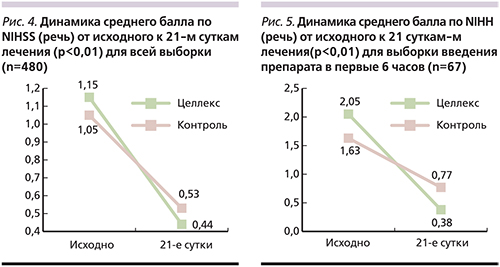
Оценка степени изменений показателей в группах больных ИИ со сроком введения препарата 0–6 часов выявила, что на визите 4 в группе Целлекс была более выражена, чем в группе Контроль, динамика показателя Речь шкалы инсульта, что подтверждалось наличием статистически достоверных различий полученных данных (рис. 4). Изменение данного показателя для всей выборки составило 12%, тогда как у пациентов с ранним началом введения препарата (0–6 часов) оно достигло 26% (рис. 4, 5). Полученные данные, безусловно, свидетельствуют в пользу целесообразности раннего назначения препарата.
В результате проведенного многоцентрового исследования получены убедительные данные в отношении эффективности препарата Целлекс при афатических расстройствах в остром периоде ИИ. Сравнение динамики средних значений теста «Опросник речи» у больных с выраженными речевыми нарушениями (от 2 до 10 баллов) показало значимое по сравнению с исходным уровнем его возрастание в обеих группах. При этом у пациентов, принимавших Целлекс, значение показателей начиная с 3-х суток заболевания было выше, чем в контрольной группе, а на 21-е сутки значение показателей Опросника речи у пациентов группы Целлекс было на 20% выше, чем в группе Контроль.
Оценка средних значений данного теста у больных тотальной афазией (мутизмом, 0–1 балл до лечения) выявила, что у пациентов, принимавших Целлекс, значение данного показателя уже на 2-м визите (6-е сутки) в 3,5 раза превышало соответствующий уровень в группе контроля. К 21-м суткам наблюдения значение этого показателя в группе Целлекс было в 3 раза выше по сравнению с контролем. Лучшие результаты лечения достигнуты при более раннем назначении препарата. Проведенное клиническое исследование подтвердило нейропротективное действие препарата Целлекс в комплексной терапии больных в остром периоде ИИ.
В ходе исследования не было отмечено серьезных нежелательных явлений, связанных с применением препарата Целлекс, не было побочных эффектов ни у одного пациента, что свидетельствует о его безопасности. Пациенты и врачи отметили хорошую переносимость данного препарата.
Таким образом, согласно полученным результатам исследования, подкожное введение оригинального препарата Целлекс в остром периоде ИИ у больных со среднетяжелым и тяжелым течением заболевания с речевыми нарушениями позволяет компенсировать возникший неврологический дефицит, что в целом улучшает когнитивные функции и увеличивает реабилитационный потенциал пациентов.



