Монополярное депрессивное расстройство (ДР) – одна из самых часто встречаемых форм психической патологии [27]. Распространенность ДР составляет от 3,1 до 10,4% среди взрослого населения, и их значительный рост, отмечаемый за последнее время, во многом обусловлен увеличением удельного веса непсихотических форм депрессий [4, 24]. Как показали многочисленные исследования, при ДР часто выявляются разнообразные когнитивные нарушения [7, 12, 23, 28], характеризующиеся различной степенью специфичности, выраженности и стойкости [22]. Когнитивные нарушения при депрессиях чаще всего проявляются в снижении памяти, внимания и исполнительных функций [16]. В недавних исследованиях было выявлено, что некоторые когнитивные нарушения сохраняются, даже когда основные симптомы депрессии уменьшаются [8]. В связи с этим когнитивную дисфункцию предлагается рассматривать как отдельную группу симптомов, свойственных депрессии, но в то же время имеющих собственные патогенетические механизмы [9]. Следует отметить, что социальные, психологические и биологические факторы играют существенную роль в формировании когнитивного профиля больных депрессией, однако этиология этих нарушений, несмотря на проведенные исследования, пока остается неясной [10].
С учетом того места, которое когнитивные нарушения занимают среди клинических проявлений депрессии, можно полагать, что эти симптомы заслуживают особого лечения. Однако до настоящего времени основные способы терапевтического воздействия на депрессию были направлены исключительно на лечение собственно аффективного компонента депрессивной триады. На настоящий момент существует мало исследований, посвященных методам терапии, которая могла бы улучшить когнитивное, психосоциальное и общее функционирование. Основным терапевтическим методом лечения ДР, как известно, служит применение антидепрессантов [1, 5]. При этом предварительный анализ клинических исследований выявил противоречие в оценках влияния тимоаналептиков на когнитивные функции больных непсихотическими ДР. По данным одних авторов, несмотря на высокую эффективность и хорошую в целом переносимость, спектр фармакологической активности антидепрессантов включает эффекты, проявляющиеся замедлением психомоторных реакций и нарушением когнитивных функций [13, 19]. Другие авторы приводят свидетельства отсутствия значимого влияния тимоаналептиков на когнитивные дисфункции [15, 22, 25]. Существует и противоположная точка зрения, согласно которой под влиянием терапии антидепрессантами происходит редукция ДР и наблюдается «вторичное» улучшение памяти, внимания, моторных реакций [3, 14]. Однако для довольно большого числа пациентов недостаточно применения одной лишь монотерапии антидепрессантами [26].
Исследования обнаруживают, что среди многочисленной категории больных наблюдается неполная редукция депрессивной симптоматики и, соответственно, остаточная когнитивная дисфункция. В связи с этим целесообразно изучать способность других групп препаратов помимо антидепрессантов воздействовать на остаточную симптоматику. Патогенетически обоснованной терапией когнитивных нарушений является применение ноотропных препаратов [2, 6]. При этом ноотропы характеризуются более широким спектром фармакологического действия, что позволяет использовать их при терапии непсихотических ДР. Существующие единичные исследования применения ноотропных препаратов на пациентах с непсихотическими ДР свидетельствуют о целесообразности дальнейшего изучения их применения в комплексе с антидепрессивной терапией.
Помимо фармакологических методов лечения когнитивных нарушений при депрессии существуют и психотерапевтические методики. В первую очередь речь идет о когнитивно-поведенческой терапии (КПТ) [17]. КПТ является эффективным методом лечения ДР, демонстрируя сопоставимые с психофармакотерапией результаты при депрессиях легкой, умеренной и даже тяжелой степеней. Когнитивное реструктурирование подразумевает применение анализа, систематического обучения и корректировки ошибочных концептуализаций и дисфункциональных убеждений (схем) с целью улучшения количества и качества когнитивной переработки. Было показано, что у депрессивных пациентов с резидуальной симптоматикой на фоне проведения КПТ имело место улучшение исполнительных функций, психосоциального взаимодействия и уменьшение остаточной аффективной симптоматики [11]. Согласно существующим данным, лечение депрессии с помощью КПТ и в комбинации с антидепрессантами более эффективно и показывает результат, наиболее устойчивый, чем использование только фармакотерапии [20].
Таким образом, изучение структуры когнитивных нарушений на больных непсихотическими ДР, анализ влияния психофармакотерапии антидепрессантами на когнитивную сферу, а также поиск методов коррекции когнитивных нарушений с целью оптимизации комплексной терапии больных депрессией остаются актуальной проблемой для изучения.
Целью настоящего исследования стало сопоставление влияния разных видов антидепрессивной терапии на когнитивные нарушения у больных непсихотическими ДР.
Материал и методы
Исследование было выполнено в отделе пограничной психиатрии ФГБУ «Федеральный медицинский исследовательский центр психиатрии и наркологии» Минздрава России на базе ГБУЗ «Психиатрическая клиническая больница № 12» ДЗ Москвы. В исследование были включены амбулаторные и стационарные пациенты, давшие свое информированное согласие на участие в нем. Критерии включения: наличие первичного или рекуррентного депрессивного эпизода, или дистимии, определенных на основании критериев Международной классификации болезней 10-го пересмотра (МКБ-10); возраст участников – от 18 до 55 лет; общее число баллов по шкале MADRS (Montgomery–Åsberg Depression Rating Scale) – не менее 15. В исследование не включали пациентов с тяжелыми неврологическими и соматическими заболеваниями; выраженными органическими и дегенеративными заболеваниями головного мозга; шизофренией, шизотипическими и бредовыми расстройствами; с психическими и поведенческими расстройствами, связанными с употреблением психоактивных веществ; беременные и кормящие грудью женщины.

Для решения поставленной цели исследования наряду с клинико-психопатологическим методом применялась психометрическая шкала MADRS. Оценка психофизиологических параметров проведена с помощью аппаратно-программного психодиагностического комплекса «Мультипсихометр», включившая следующие тесты: память на лица (кратковременная память), арифметический счет (оперативная память), корректурную пробу с кольцами Ландольта (внимание), простую зрительно-моторную реакцию (время реакции), позиционный цветовой выбор (динамичность), реакцию на движущиеся объекты (регуляторно-исполнительные функции), теппинг-тест (сила нервных процессов), стресс-тест (стрессустойчивость). Абсолютные величины показателей тестов стандартизировались программой «Мультипсихометр» относительно средних величин, полученных при тестировании 2000 относительно здоровых лиц, и выражались в виде баллов от 1 до 10. Средняя величина для популяции составила 5,5±1,0 балл. Значение показателя от 4,5 до 3,5 баллов соответствовало уровню ниже среднего, от 3,5 до 2,5 – низкому, а меньше 2,5 баллов – очень низкому уровню. Аналогичным образом величины от 6,6 до 7,5 баллов соответствовали уровню показателя выше среднего, от 7,5 до 8,5 – высокому и свыше 8,5 баллов – очень высокому уровню. Математико-статистическая обработка результатов исследования проведена с помощью программ Statistica и SPSS.
По своему дизайну исследование было проспективным нерандомизированным. После проведения фонового обследования всем пациентам назначена монотерапия антидепрессантами группы СИОЗС (селективные ингибиторы обратного захвата серотонина) – флуоксетином, пароксетином, эсциталопрамом, сертралином – в соответствии с принятыми клиническими рекомендациями и стандартами лечения. В течение первых двух недель терапии произведена оценка динамики состояния пациентов и в зависимости от характера и степени редукции депрессивной симптоматики могла происходить коррекция терапевтического воздействия путем либо замены препаратов группы СИОЗС на трициклические антидепрессанты (ТЦА; амитриптилин, кломипрамин), либо присоединения к лечению СИОЗС когнитивно-поведенческой терапии, или ноотропного препарата группы рацетамов (фенотропил, пирацетам). Жестких критериев замены или усиления терапии СИОЗС не было. Тем не менее основными показаниями к отмене СИОЗС и назначению ТЦА стали выраженность депрессивной симптоматики и отсутствие значимого терапевтического ответа в первые две недели терапии. КПТ преимущественно назначалась пациентам с преобладанием руминативного депрессивного мышления. Основанием к назначению ноотропных препаратов служили жалобы больных на снижение памяти и внимания, а также наличие выраженных астенических симптомов.
 В результате сформировались четыре терапевтические группы, включившие: 1) 29 (56,9%) пациентов, принимавших СИОЗС весь период исследования; 2) 7 (13,7%) больных, получавших со второй недели ТЦА взамен СИОЗС; 3) 10 (19,6%) пациентов, прошедших КПТ на фоне приема СИОЗС; 4) 5 (9,8%) больных, принимавших комбинацию СИОЗС и ноотропного средства.
В результате сформировались четыре терапевтические группы, включившие: 1) 29 (56,9%) пациентов, принимавших СИОЗС весь период исследования; 2) 7 (13,7%) больных, получавших со второй недели ТЦА взамен СИОЗС; 3) 10 (19,6%) пациентов, прошедших КПТ на фоне приема СИОЗС; 4) 5 (9,8%) больных, принимавших комбинацию СИОЗС и ноотропного средства.
Оценка исходного состояния больных включала клинико-психопатологическое обследование, определение показателей психометрических шкал, психофизиологическое исследование. В дальнейшем обследование проводилось на 7-й, 14, 21, 28, 42, 56-й дни терапии. В течение первых двух недель исследования пациенты проходили клинико-психологическое обследование. В дальнейшем планируется катамнестическое наблюдение пациентов, достигших стойкой ремиссии.
Результаты исследования
В строгом соответствии с критериями включения/исключения из исследования был включен 51 пациент. Изученная группа больных состояла из 11 (21,6%) мужчин и 40 (71,4%) женщин. Средний возраст исследуемых составил 30,6±10,01 года. Большинство (54,9%) пациентов имели высшее образование или числились студентами высших учебных заведений. В браке состояли 25,5% больных. На момент обращения профессионально были заняты 39,2% пациентов. В исследуемую выборку вошли 24 пациента с первичным депрессивным эпизодом, что составило 47,0% от общего числа больных, 20 (39,2%) больных с диагнозом рекуррентного ДР и 7 (13,7%) – с дистимией в соответствии с диагностическими критериями МКБ-10. Средняя длительность заболевания у пациентов с первичным депрессивным эпизодом составила 5,2±2,4 месяца, у больных рекуррентным ДР – 107,8±111,8; 27±11,4 месяца – в группе больных дистимией соответственно. Синдромальная оценка депрессии позволила выделить тоскливый (23,5% больных), тревожный (35,3%), астено-адинамический (21,6%), истерический (11,8%) и ипохондрический (7,8% больных) типы. Средний общий показатель по шкале MADRS в изучаемой выборке пациентов составил 25,4±7,3 балла.
Поскольку основной задачей исследования стало изучение когнитивного функционирования у больных непсихотической депрессией, оценивали их краткосрочную и оперативную память, показатели внимания, времени реакции и нейродинамической активности с помощью аппаратно-программного психодиагностического комплекса «Мультипсихометр».
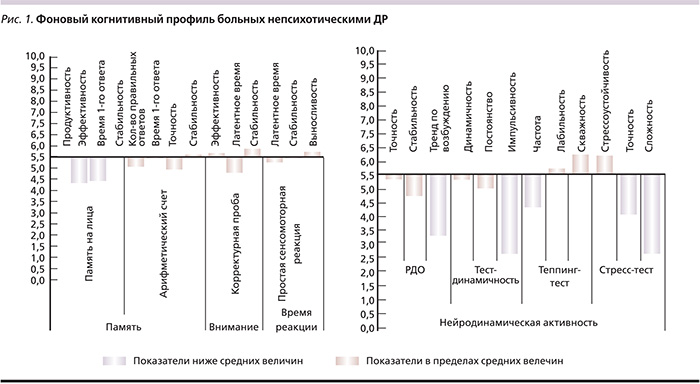
Анализ фоновых показателей когнитивных функций во всей изучаемой выборке показал, что для пациентов с непсихотическими ДР был характерен уровень ниже среднего для показателей эффективности и латентности кратковременной памяти (тест «память на лица»), в то время как продуктивность и стабильность сохранялись в пределах средних значений (рис. 1). Показатели оперативной памяти (в тесте на арифметический счет), внимания (в тесте корректурной пробы) и простой зрительно-моторной реакции в изучаемой выборке также не отличались от средних популяционных величин (5,5±1,0). Однако во всех более сложных тестовых методиках, оценивавших нейродинамическую активность, регуляторные (исполнительные) функции, стрессоустойчивость и силу нервной системы, выявлены показатели ниже среднего и низкого уровней. Снижение некоторых из них, таких как «тренд по возбуждению» в реакции на движущийся объект (РДО), «импульсивность» в тесте на динамичность и «частота касания» в теппинг-тесте, свидетельствуют в целом о более выраженной психомоторной заторможенности пациентов с ДР. Кроме того, была снижена способность изучаемых больных к антиципации (предвосхищению) положения динамических объектов в пространстве (в стресс-тесте).
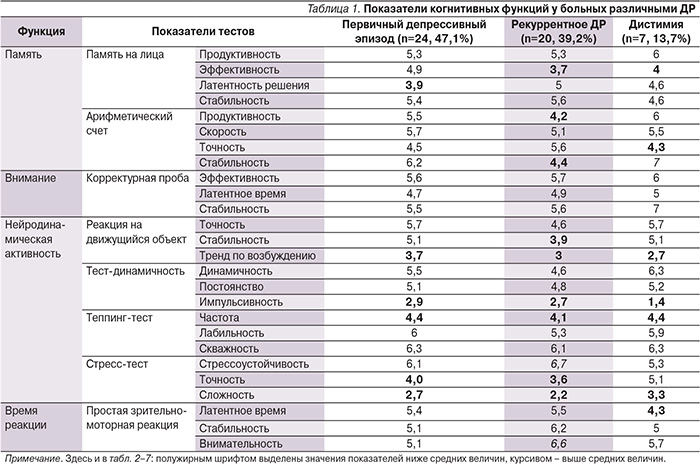
Была проведена сравнительная оценка когнитивного профиля больных, отнесенных к разным диагностическим категориям ДР (согласно МКБ-10). Общей для пациентов с впервые возникшим рекуррентным депрессивным эпизодом и с дистимией оказалась тенденция к более выраженной психомоторной заторможенности, проявившаяся во всех нейродинамических тестах, а также отсутствие какого-либо снижения показателей внимания (табл. 1). Тем не менее выявлен и целый ряд различий между больными, отнесенными к разным диагностическим рубрикам. Так, для пациентов с рекуррентным депрессивным эпизодом были характерны самые низкие значения большинства сниженных во всех трех группах параметров. Кроме того, по числу сниженных показателей пациенты с повторными эпизодами превосходили (10 параметров) больных дистимией (8 параметров), в свою очередь опередивших по этому критерию пациентов с первичным эпизодом (7 параметров). Поскольку средняя продолжительность заболевания уменьшилась в ряду рекуррентный эпизод–дистимия–первичный эпизод, можно предположить значение длительности ДР и числа в развитии когнитивных нарушений.
Проведен сравнительный анализ когнитивных нарушений у пациентов с разной степенью выраженности депрессивных симптомов.
В качестве критерия тяжести депрессии был выбран общий показатель шкалы MADRS, равный 30 баллам и более. В соответствии с выбранным критерием изучаемая выборка пациентов разделилась на больных с более тяжелой (11 человек – 21,6%) и менее выраженной (40 человек – 78,4%) депрессией. Группа больных нетяжелым ДР помимо существенно большей численности характеризовалась таким же профилем когнитивного функционирования, что и вся выборка в целом (табл. 2). Вместе с тем пациенты с более выраженной депрессивной симптоматикой отличались большим числом показателей ниже среднего и низкого уровней, в т.ч. касательно таких когнитивных функций, как оперативная память, внимание и простая зрительно-моторная реакция, которые не затрагивались при менее выраженных депрессиях. Следовательно, у больных ДР есть основание для когнитивных нарушений.
Диагностика клинических особенностей ДР в изучаемой выборке пациентов позволила выделить несколько синдромальных вариантов депрессии. Наиболее распространенным оказался тревожно-депрессивный синдром – он встречался среди 35,3% пациентов. Вслед за ним по распространенности следовал тоскливый (меланхолический) вариант депрессивного синдрома – среди 23,5%, затем астено-адинамический – у 21,6% пациентов. Истерическая депрессия имела место у 11,8%, а ипохондрическая – у 7,8% больных.
Сравнительный анализ когнитивных показателей при разных синдромальных вариантах депрессии подтвердил наличие общих тенденций в отношении снижения величин кратковременной памяти, а также нейродинамической активности, регуляторных (исполнительных) функций, силы и стрессоустойчивости нервных процессов (табл. 3).
Кроме того, определены некоторые особенности когнитивных нарушений, характеризующие каждый из диагностированных вариантов. В частности, тоскливый, тревожный и ипохондрический типы депрессивного синдрома имели в среднем большее число сниженных показателей (по 9 параметров) по сравнению с астеноадинамическим и истерическим вариантами (по 7 параметров). В то же время оперативная память была затронута в наибольшей степени при тревожном и истерическом типах, а простая зрительно-моторная реакция сильнее страдала при тоскливой депрессии. Итак, в исследуемой выборке удалось выявить ряд когнитивных параметров, снижение которых характерно для большинства больных, страдающих ДР. В то же время некоторые когнитивные нарушения в большей степени зависят от клинических особенностей депрессивного синдрома.

Основным исследовательским критерием эффективности антидепрессивной терапии в настоящей работе была редукция общего балла шкалы депрессии Мантгомери–Асберг.
В течение первых двух недель все пациенты получали монотерапию СИОЗС и в отношении большинства (56,9%) больных имел место достаточный терапевтический ответ для того, чтобы они продолжили прием первоначально назначенного антидепрессанта как минимум еще 6 недель. Семи (13,7%) пациентам проведена последующая замена СИОЗС на ТЦА, прежде всего в результате недостаточной эффективности исходного препарата. КПТ дополнительно была назначена 10 (19,6%) больным, продолжавшим принимать СИОЗС, а 5 (9,8%) пациентам в дополнение к СИОЗС – ноотропные препараты группы рацетамов. По завершении 8-недельного периода исследования пациенты могли продолжить начатую антидепрессивную терапию в соответствии с показаниями.
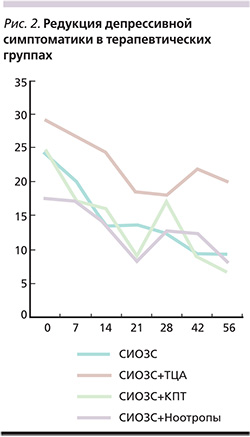
Сравнительный анализ динамики показателя шкалы MADRS в сформировавшихся терапевтических группах показал, что исходный средний балл у больных, оставшихся на монотерапии СИОЗС (24,3 балла), был близким к среднему в выборке (25,4±7,3 балла), а его редукция за первые две недели составила 44,5% (рис. 2).
У пациентов, которым пришлось менять антидепрессант, фоновый показатель шкалы MADRS был выше среднего (29,1 балла), а 2-недельная монотерапия СИОЗС привела к его редукции лишь на 15,5%, что существенно меньше 25%-ного критерия частичного терапевтического ответа. Это подтверждает обоснованность замены СИОЗС на ТЦА. В группе пациентов, которым с третьей недели комбинировали СИОЗС и КПТ, исходный показатель шкалы MADRS (24,6) был также близок к средней для всей выборки величине и в целом его редукция через две недели (на 35,6%) соответствовала критериям частичного терапевтического отклика. Однако она существенно замедлилась на второй неделе по сравнению с первой, что наряду с преобладанием депрессивных руминаций послужило причиной назначения КПТ, значительно ускорившей дальнейшее снижение общего балла MADRS. Назначению ноотропов четвертой группе пациентов предшествовала относительно медленная двухнедельная (21,9%) редукция исходно более низкого по сравнению со средним значением показателя MADRS, а также преобладание у больных астеноадинамических симптомов и жалоб на снижение памяти и трудности сосредоточения. В результате применения рацетамов удалось резко понизить общий балл MADRS и, несмотря на последующие его флуктуации, добиться хорошей степени редукции депрессии.
В результате к концу 8-й недели терапии максимальная величина редукции общего балла MADRS отмечена при сочетании СИОЗС и КПТ (72,9%). В среднем более чем на 50% редуцировался общий балл MADRS в группе больных, получавших монотерапию СИОЗС (на 61,7%), и в группе комбинированной фармакотерапии СИОЗС+ноотроп (на 54,3%). Замена СИОЗС на ТЦА не привела к значительной редукции MADRS (только на 31,3%) за период наблюдения, однако это может быть объяснено тем, что пациенты с исходно более выраженной депрессией требуют большего времени для достижения терапевтического ответа.
Анализ влияния антидепрессивной терапии на когнитивные нарушения у исследуемых больных ДР показал, что в среднем антидепрессанты слабо влияют на сниженные при депрессии показатели кратковременной памяти, не улучшая, но и не ухудшая их при курсовом применении. Данная тенденция справедлива и в отношении ТЦА. Положительное влияние на кратковременную память возникало преимущественно при присоединении к терапии ноотропных препаратов. Параметры оперативной памяти были снижены только при более выраженных депрессивных состояниях, слабо реагировали на терапию СИОЗС, но в то же время активно возрастали на фоне приема ТЦА и в случае присоединения КПТ (табл. 4).
Характеристики внимания исследуемых больных в целом соответствовали среднему уровню в популяции и изредка были нарушены при более тяжелых состояниях. Применение ТЦА значительно нарушало способность сосредоточения. Использование СИОЗС, особенно в комбинации с ноотропами, оказывало положительный эффект на сниженные параметры внимания (табл. 5).
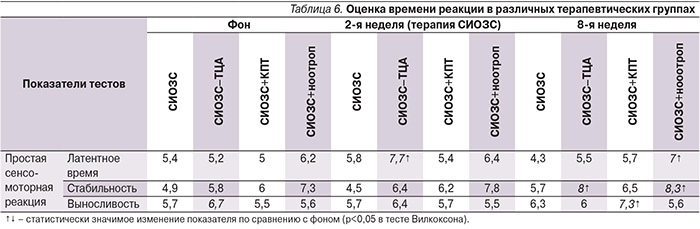
Показатели времени реакции больных непсихотическими ДР практически не были нарушены, а по отдельным параметрам в некоторых группах были даже выше средних значений. Антидепрессивная терапия также не оказывала какого-либо закономерного воздействия на эту когнитивную функцию (табл. 6).
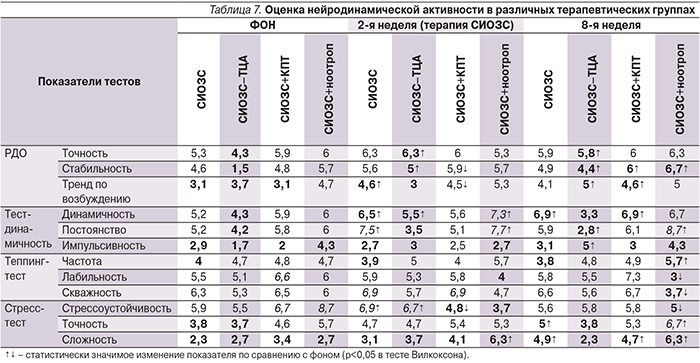
Характеристики нейродинамической активности, регуляторных (исполнительных) функций, силы и стрессоустойчивости нервной системы были в наибольшей степени нарушены в изучаемой выборке пациентов. Важно отметить, что терапия СИОЗС в значительной степени нормализовала сниженные показатели, а применение ТЦА оказывало разнонаправленные влияния, улучшая, например, регуляторные функции (по всей видимости, за счет антидепрессивного эффекта), но ухудшая показатели динамичности. Отчетливым положительным воздействием практически на все параметры отличалось и присоединение КПТ к основному курсу. Дополнительная ноотропная терапия также давала положительный прирост величин во многих тестах (табл. 7). Таким образом, на основании полученных результатов можно сделать следующий вывод: когнитивные нарушения у больных непсихотическими ДР характеризуются более низкими по сравнению со средними популяционными значениями показателями кратковременной памяти, нейродинамической активности, регуляторных (исполнительных) функций, стрессоустойчивости и силы нервных процессов. Выраженность и широта спектра когнитивных нарушений положительно коррелируют с длительностью ДР, числом повторных эпизодов и тяжестью депрессии. Различные антидепрессанты по-разному влияют на отдельные показатели когнитивного функционирования у больных непсихотическими ДР.
В целом антидепрессанты группы СИОЗС оказывают незначительное воздействие на сниженные показатели кратковременной памяти, но существенно улучшают параметры нейродинамической активности. Действие ТЦА на когнитивные функции характеризуются значительным снижением способности к сосредоточению и ухудшением показателей динамичности, тем не менее оказывая положительное влияние на регуляторные функции (по всей видимости, за счет антидепрессивного эффекта). Присоединение к терапии антидепрессантами ноотропных препаратов оказывает положительный эффект на сниженные параметры внимания и кратковременной памяти. Присоединение КПТ к основному курсу терапии ведет к отчетливым положительным воздействиям на многие параметры когнитивного функционирования.



